| Issue |
Med Sci (Paris)
Volume 35, Number 12, Décembre 2019
Anticorps monoclonaux en thérapeutique
|
|
|---|---|---|
| Page(s) | 1034 - 1042 | |
| Section | Les anticorps armés | |
| DOI | https://doi.org/10.1051/medsci/2019227 | |
| Published online | 06 January 2020 | |
Les immuno-conjugués en oncologie
Les raisons du succès récent d’une approche ancienne
Antibody-drug conjugates in oncology. Recent success of an ancient concept
1
Institut de Recherche Pierre Fabre, Centre d’Immunologie Pierre Fabre, 5 Avenue Napoléon III, 74160 Saint-Julien-en-Genevois, France
2
Cancer Research Center of Lyon (CRCL), Inserm 1052/CNRS, 69000 Lyon, France
3
Université de Lyon, 69000 Lyon, France
4
Hospices Civils de Lyon, 69000 Lyon, France
5
GICC EA7501, Université de Tours, équipe IMT, 31 avenue Monge, 37200 Tours, France
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Un anticorps armé (antibody-drug conjugate en anglais) est une chimiothérapie vectorisée qui résulte du greffage d’un agent cytotoxique sur un anticorps monoclonal par l’intermédiaire d’un bras espaceur judicieusement construit. Les anticorps armés ont fait des progrès considérables en 10 ans. En 2009, seul le gemtuzumab ozogamicine (Mylotarg®) était utilisé en clinique. En 2019, 4 autres ADC ont été approuvés par la Food and drug administration et plus de 80 autres sont en études cliniques actives. La première partie de cette revue sera focalisée sur les anticorps armés approuvés, leurs limitations, ainsi que leur toxicité et mécanismes de résistances associés.
Abstract
An Antibody-Drug Conjugate (armed antibody) is a vectorized chemotherapy that results from the grafting of a cytotoxic agent on a monoclonal antibody thanks to a judiciously designed spacer arm. ADCs have made considerable progress in 10 years. In 2009, only gemtuzumab ozogamicin (Mylotarg®) was used clinically. In 2019, 4 other ADCs have been approved and more than 80 others are in active clinical trials. The first part of this review will focus on Food and Drug Administration-approved Antibody-Drug Conjugates, their limitations as well as their associated toxicity and resistance mechanisms.
© 2019 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Les immunoconjugués (antibody-drug conjugates ou ADC en anglais) ont fait des progrès considérables en 10 ans. Un ADC est une chimiothérapie vectorisée, permettant la délivrance sélective d’un agent cytotoxique puissant au sein d’une tumeur. Un ADC résulte du greffage généralement stochastique d’un agent cytotoxique sur un anticorps monoclonal (AcM) par l’intermédiaire d’un bras espaceur judicieusement construit (linker, en anglais), et se présente sous la forme d’un mélange complexe d’immunoconjugués où varient la distribution DLD (drug loading and distribution) et le DAR (drug-to-antibody ratio, correspondant au nombre de molécules cytotoxiques greffées sur l’anticorps) [1, 2]. En 2009, le gemtuzumab ozogamicine (Mylotarg®) était le seul ADC approuvé par la FDA (food and drug administration) et 12 autres candidats étaient en études cliniques [3] (→).
(→) Voir la Synthèse de J.F. Haeuw et al., m/s n° 12, décembre 2009, page 1046
À l’heure actuelle, quatre autres ADC ont été approuvés (Figure 1) et plus de 80 autres sont en études cliniques actives dont 8 en phase III ou phase II pivotales (Tableau I). Plus de 50 candidats ont par ailleurs été abandonnés en clinique pour des raisons toxicologiques, de manque d’efficacité ou de priorisation de portefeuilles. Si on peut constater que, parmi les cinq ADC approuvés aujourd’hui, quatre visent des cancers hématologiques (« tumeurs liquides » réputées plus facile à cibler pour des ADC) contre un seul dirigé contre des tumeurs solides, les ADC en phase clinique avancée sont au contraire principalement dirigés vers les tumeurs solides (six contre des tumeurs solides ; deux dirigés contre des myélomes ou des lymphomes).
 |
Figure 1. Représentation des 5 ADC approuvés par la FDA: Mylotarg®, Adcetris®, Kadcyla®, Besponsa® et Polivy®. |
ADC approuvés ou en phases cliniques avancées (III ou II pivotale).
Six ADC ont reçu par la FDA les statuts de percée thérapeutique ou désignation accélérée ou examen prioritaire: examen prioritaire du sacituzumab govitécan dans le cancer du sein triple négatif métastatique (23 juillet 2018) ; désignation de traitement de pointe pour le trastuzumab déruxtécan contre le cancer du sein métastatique HER2-positif (30 août 2017) ; désignation accélérée pour le trastuzumab duocarmazine contre le cancer du sein métastatique HER2-positif (28 janvier 2018) ; désignation accélérée pour le mirvétuximab soravtansine contre le cancer de l’ovaire résistant au traitement par les dérivés du platine (18 juin 2018) ; désignation de traitement de pointe pour l’enfortumab védotine pour le cancer métastatique urothélial (28 mars 2018). Désignation de percée thérapeutique pour le bélantamab mafodotine pour le myélome multiple (2 novembre 2017).
Cette revue, en deux parties, sera focalisée sur les ADC approuvés et en phase de développement tardif, leur limitation, ainsi que leur toxicité et mécanismes de résistances associés, les nouvelles stratégies émergentes pour y faire face, dont les constructions moléculaires de 3e génération, le choix de vecteurs alternatifs, les systèmes de libération innovants et les combinaisons ADC avec la chimiothérapie conventionnelle ou des inhibiteurs de point de contrôle immunitaire.
En 2009, les calichéamycines, les auristatines et les maytansinoïdes étaient les classes principales de cytotoxiques utilisés. Dix ans plus tard, ces mêmes molécules sont toujours utilisées avec des structures et agents de liaison optimisés pour une meilleure stabilité et hydrophilie. De nouvelles classes de molécules cytotoxiques sont apparues: pyrrolobenzodiazépines (PBD), duocarmycines, dérivés de camptothécine. En 10 ans, des progrès considérables ont été réalisés en ingénierie d’anticorps pour permettre des conjugaisons plus site-spécifique, améliorer l’homogénéité et la stabilité des constructions et amener en clinique des ADC de 2e et de 3e génération dans l’espoir d’élargir la fenêtre thérapeutique (delta entre la dose maximale tolérée [DMT] et la dose minimale efficace [DME]) [4]. Plusieurs dizaines de technologie de bioconjugaison ont été proposées en préclinique, fondées sur l’utilisation de résidus cystéines, d’acides aminés non-naturels ou de motifs introduits par ingénierie moléculaire au niveau des chaînes légères ou lourdes, ou bien des techniques de re-pontage des résidus cystéines. Enfin, les ADC ont également été améliorés grâce à des cibles antigéniques mieux choisies et en optimisant des mécanismes de libération de l’agent cytotoxique au sein de la tumeur [5].
Conception et mécanisme d’action des ADC approuvés en clinique
Le développement des immunoconjugués en oncologie a permis l’émergence de deux éléments clés nécessaires pour assurer le succès d’un ADC. Le premier concerne la nature et la nécessité d’un espaceur en tant qu’intermédiaire entre l’anticorps (Ac) et la molécule cytotoxique que nous désignerons désormais par « le cytotoxique ». Ce système Ac-espaceur-cytotoxique a d’abord été conçu avec un espaceur clivable (Figure 2) supposé stable dans les conditions physiologiques dans la circulation plasmatique, puis clivé rapidement après endocytose dans la cellule tumorale, afin d’y libérer sélectivement le cytotoxique et limiter l’apparition d’effets secondaires indésirables. Ce type d’espaceur est sensible aux conditions lysosomales (protéases, acidité, milieu réducteur). Le second est corrélé à la nécessité d’avoir un agent cytotoxique puissant greffé à l’anticorps. Les premiers ADC étaient caractérisés par un faible indice thérapeutique en raison de la faible puissance du cytotoxique (e.g. anthracycline), entraînant un effet thérapeutique très limité à la DMT (DMT et DME confondues à 100 mg/kg). Ce phénomène peut être expliqué conjointement par la densité antigénique à la surface des cellules cancéreuses et par la quantité d’ADC arrivant à la surface des cellules tumorales par rapport à celle injectée (ne dépassant guère 0,1 %) [6].
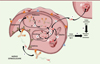 |
Figure 2. Représentation schématique d’un ADC ou anticorps armé. |
Mylotarg®, Besponsa® et l’espaceur clivable de première génération
Le Mylotarg® (gemtuzumab ozogamicine) a été approuvé par la FDA avec une indication de traitement de la leucémie myéloïde aiguë (LMA) [7,8]. En effet, le Mylotarg® est le résultat de la conjugaison de la calichéamycine, un puissant agent alkylant de l’ADN [9] possédant une activité subnanomolaire, au gemtuzumab, un AcM anti-CD33, via une liaison hydrazone labile en milieu acide (Figure 1). Après l’internalisation de l’ADC, la liaison hydrazone de cet espaceur peut être hydrolysée dans les lysosomes pour libérer un précurseur de la calichéamycine, qui subit ensuite une réduction par le glutathion, suivie d’une cyclisation de Bergman pour libérer la calichéamycine active (Figure 3).
 |
Figure 3. Mécanisme d’action du Mylotarg® ou du Besponsa®. Les différentes étapes sont: (1) liaison à un antigène (Ag) spécifique, suivie de l’internalisation du complexe ADC-Ag selon un mécanisme dépendant de la clathrine ; (2) transfert dans les endosomes ; (3) le clivage du linker dans les lysosomes s’effectue au niveau de l’hydrazone acido-sensible ; (4) transfert de la pro-calichéamycine dans le lysosome ; (5) clivage du pont disulfure pour donner la calichéamycine puis (6) transfert de la calichéamycine dans le cytoplasme ; (7) transfert de la calichéamycine dans le noyau. (8) Alternativement à 7, transfert de la calichéamycine dans le cytoplasme puis: (9) diffusion de la calichéamycine dans les cellules cancéreuses voisines pour obtenir un effet bystander cytotoxique ; (10) toutes les étapes précédentes conduisent à la mort cellulaire. |
Théoriquement, les hydrazones devaient être stables dans la circulation sanguine à pH neutre et subir une hydrolyse après internalisation dans un environnement cellulaire qui possède un pH plus acide (respectivement un pH de 5,0 à 6,5 pour les endosomes et de 4,5 à 5,0 pour les lysosomes). Cependant, l’espaceur du Mylotarg® présente une certaine instabilité, entraînant la libération prématurée du cytotoxique dans la circulation plasmatique [10], ce qui explique son retrait volontaire en 2010. Le Mylotarg® a bénéficié du savoir accumulé en clinique ces dernières années pour être réapprouvé par la FDA en 2017, utilisé à une dose plus faible, avec un schéma d’administration modifié et pour une population différente de patients. En parallèle, un espaceur semblable a été développé et utilisé pour greffer la calichéamycine sur l’inotuzumab anti-CD22, conduisant au Besponsa® (inotuzumab ozogamicine, Figure 1 ), approuvé par la FDA en 2017 contre la leucémie aiguë lymphoblastique (LAL) et la leucémie lymphoïde chronique (LLC) [11].
Kadcyla® et la notion d’espaceur non clivable
Devant ces constats, des stratégies alternatives pour la conception d’un espaceur étaient nécessaires pour continuer le développement des ADC. Ainsi, une attention particulière a été portée sur l’utilisation d’espaceurs permettant la conjugaison de dérivés de maytansines et incorporant un système de libération utilisant une liaison disulfure sensible au glutathion [12]. Ces espaceurs innovants chimiquement labiles devaient permettre une libération contrôlée grâce au glutathion (GSH)1 dont la concentration cytoplasmique dans les cellules cancéreuses est environ 1 000 fois plus élevée que dans le plasma. En complément, un choix réfléchi des groupements (méthyles) voisins de la liaison disulfure a permis un contrôle de la cinétique de libération [13]. Ainsi, la concentration élevée des molécules réductrices dans la tumeur aurait dû garantir une libération sélective du cytotoxique dans les cellules cancéreuses par rapport au plasma. Ce type d’espaceur n’a pas encore permis de fabriquer un ADC qui soit approuvé sur le marché2.
Cependant, une découverte fortuite a permis d’identifier un ADC d’une efficacité inattendue. La conjugaison de la DM1 (derivative maytansine 1, un inhibiteur des microtubules) aux résidus lysine du trastuzumab anti-HER2/neu via un espaceur non clivable thioéther hétérobifonctionnel contenant un ester de NHS (succinimidyl-4-(N-maléimidométhyl) cyclohexane-1-carboxylate ou SMCC) a permis d’aboutir au Kadcyla® (T-DM1 ou ado-trastuzumab emtansine, Figure 1 ), qui a été approuvé par la FDA en 2013 [14]. Étonnamment, lors de son développement, il a été observé in vitro que cet ADC original était très puissant dans un modèle de cancer du sein HER2/neu-positif, la structure n’étant active qu’après internalisation et digestion enzymatique complète de l’ADC dans le lysosome, conduisant à la formation du métabolite actif, le lysine-MCC-DM1 (Figure 4). Suite à cette découverte, plusieurs remarques peuvent être faites: (1) le métabolite lysine-MCC-DM1 conserve le potentiel cytotoxique de la DM1 libre, permettant à l’ADC d’atteindre une activité in vitro de l’ordre du picomolaire ; (2) cet ADC ne présente aucun effet collatéral de cytotoxicité (bystander killing effect) en raison du caractère chargé de son métabolite actif à pH physiologique ; (3) l’ADC avec l’espaceur clivable ne peut cibler que les cellules Ag-positives ; (4) un ADC avec l’espaceur non-clivable présente une toxicité limitée sur les tissus normaux et se révèle plus stable qu’un ADC avec espaceur clivable.
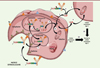 |
Figure 4. Mécanisme d’action du Kadcyla®. Les différentes étapes sont: (1) fixation du Kadcyla® sur son antigène (Ag) spécifique HER2/neu, suivie d’une internalisation du complexe T-DM1-HER2/neu par un mécanisme dépendant de la clathrine ; (2) transfert dans l’endosome puis (3) dans le lysosome ; (4) digestion complète du trastuzumab pour libérer le métabolite actif, l’acide LYS-NCL-DM1 ; (5) transfert dans le cytoplasme. (6) Pas d’effet bystander cytotoxique, et transfert vers la tubuline. (7) Toutes les étapes précédentes conduisent à la mort cellulaire de la cellule cancéreuse HER2-positive. |
Adcetris® et Polivy® et l’espaceur clivable de seconde génération
Par ailleurs, une technologie d’espaceur permettant la bioconjugaison de dérivés de la dolastatine (telle que la monométhyl auristatine E ou MMAE) aux résidus cystéine d’un AcM anti-CD30 a été mise au point. Après réduction ménagée, l’anticorps a été bioconjugué à un espaceur hétérobifonctionnel maléimide clivable possédant une gâchette peptidique valine-citrulline (ValCit) sensible à la cathepsine B lysosomale et un alcool para-aminobenzylique (PAB) en tant qu’espaceur auto-immolable permettant la libération de la MMAE après internalisation dans la cellule tumorale CD30-positive (maléimidocaproyl-valine-citrulline-p-aminobenzyloxycarbonyle), pour produire l’Adcetris® (SGN-35 ou brentuximab védotin, Figure 1) [15-17].
L’Adcetris® a été approuvé par la FDA en 2011 et cible le lymphome à grandes cellules anaplasiques et le lymphome de Hodgkin. Après l’internalisation de l’ADC avec CD30, suivie de la dégradation de l’espaceur clivable, la MMAE libérée est capable de détruire la cellule ciblée et de diffuser dans la tumeur pour atteindre et tuer les cellules cancéreuses voisines. Ce phénomène est responsable du phénomène dit du bystander killing effect [18, 19], permettant à la MMAE libérée de tuer les cellules cancéreuses CD30+ et CD30- à l’intérieur de la tumeur (Figure 5) [20], et de l’efficacité particulière de l’Adcetris® dans des lymphomes hétérogènes in vivo. Récemment, Neri et son équipe ont démontré que l’espaceur utilisé dans cet ADC peut également être clivé avant internalisation [21], participant à faire tomber le dogme stipulant qu’un ADC devait cibler un antigène internalisant [22] pour être sélectif et actif3. De manière similaire, le même espaceur a permis de conjuguer la MMAE au polatuzumab anti-CD79b, conduisant au Polivy® (polatuzumab védotine-piiq, Figure 1), approuvé par la FDA en 2019 en association avec la chimiothérapie à base de bendamustine et de rituximab, pour traiter les patients adultes atteints de lymphome diffus à grandes cellules B (DLBCL) [23, 24].
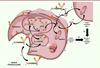 |
Figure 5. Mécanisme d’action de l’Adcetris® ou du Polivy®. Les différentes étapes sont: (1) liaison à un antigène (Ag) spécifique, suivie de l’internalisation du complexe ADC-Ag selon un mécanisme dépendant de la clathrine ; (2) transfert dans les endosomes puis (3) dans les lysosomes ; (4) le clivage du linker dans les lysosomes s’effectue entre la séquence peptidique (ValCit) et l’espaceur auto-immolable (PAB) ; (5) transfert de la MMAE dans le cytoplasme. (6) La MMAE peut également être libérée avant internalisation, puis (7) entrer dans la cellule ciblée (ou une cellule proche voisine). (8) Dans tous les cas, la MMAE libérée peut ensuite agir sur la tubuline. Alternativement à (8), (9) diffusion de la MMAE dans les cellules cancéreuses voisines non ciblées par l’ADC conduisant à un effet bystander cytotoxique. Toutes les étapes précédentes conduisent à la mort cellulaire. |
La conception structurale de l’Adcetris® ou du Polivy® possède néanmoins deux limitations: la première est liée à l’instabilité du maléimide utilisé pour la bioconjugaison, capable de réaliser une réaction de rétro-Michael4 dans le plasma, entraînant une déconjugaison partielle puis un transfert lent vers l’albumine, éventuellement corrélé à une toxicité non ciblée [25] ; la seconde est liée à la gâchette « ValCit » dans l’Adcetris®, décrite comme substrat de la carboxylestérase 1C plasmatique et de certaines protéases sécrétées par des neutrophiles (par exemple, l’élastase), ce qui pourrait expliquer en partie les effets indésirables hématologiques liés à l’Adcetris® (par exemple, la neutropénie) [26-28].
Toxicité et conditions d’utilisation
L’utilisation d’un conjugué fortement toxique a modifié le paradigme d’une immunothérapie dirigée contre les antigènes tumoraux et possédant des effets secondaires relativement limités en relation avec l’expression de la cible. Les deux anticorps de cette famille les plus utilisés, le rituximab dirigé contre CD20 et le trastuzumab dirigé contre HER2/neu, ont tous deux un profil de toxicité leur permettant d’être combinés à des agents de chimiothérapie conventionnels sans toxicité redondante avec celle de ces derniers. Dans le cas des ADC, la situation est différente dans la mesure où certains effets secondaires sont similaires à ceux des agents cytotoxiques classiques alors que d’autres sont spécifiques aux conjugués utilisés. La survenue de ces effets secondaires, parfois sévères, est en partie expliquée par le fait que seule une faible fraction de la dose totale injectée atteint la tumeur, le reste pouvant se fixer de façon non spécifique, avec une libération non contrôlée au moins partielle du conjugué ou de ses métabolites. Le développement de ces agents, que ce soit en monothérapie ou en combinaison, s’est donc avéré complexe, comme en témoigne le cas du gemtuzumab ozogamicine.
Le gemtuzumab ozogamicine ou les montagnes russes du premier ADC approuvé chez l’homme
Le gemtuzumab ozogamicine (Mylotarg®) est un AcM humanisé ayant une région Fc d’IgG4 humaine, anti-CD33, approuvé en 2000 par la FDA pour le traitement de certains patients atteints de leucémie aiguë myéloblastique (LAM). Dès 2001, la FDA émettait une alerte en raison de l’observation de cas de maladie veino-occlusive. En 2004, une étude randomisée comparant un traitement classique avec un bras associant le Mylotarg® fut interrompue prématurément en raison d’un taux de mortalité augmenté dans ce dernier. En 2010, le Mylotarg® fut retiré de la plupart des marchés, à l’exception du Japon. L’étude 0701 de l’association française Acute Leukemia French Association (ALFA) devait ensuite montrer que le fractionnement de l’administration en trois doses permettait une amélioration à la fois de la survie sans évènement et de la survie globale, sans toxicité significative supplémentaire, en particulier sur le plan hépatique [29].
Le cas du Mylotarg® est intéressant à de multiples titres. En raison des méthodes analytiques limitées disponibles lors des premières études cliniques, le Mylotarg® n’était notamment pas un produit homogène en termes de DAR. Alors que le DAR théorique était de l’ordre de 2, plus de 50 % des anticorps contenus dans les préparations pharmaceutiques n’étaient pas conjugués alors que d’autres avaient un DAR de 4 ou 5. Les difficultés de développement du Mylotarg® montrent également la difficulté d’identifier un schéma posologique permettant d’obtenir un index thérapeutique satisfaisant et la nécessité de ne pas abandonner le développement d’un ADC après l’exploration d’un seul schéma posologique.
Le brentuximab védotine dans le traitement de la maladie de Hodgkin
Le brentuximab védotine (Adcetris®) est un anticorps dirigé contre CD30, approuvé dans certaines formes de syndromes lymphoprolifératifs exprimant CD30 dont la maladie de Hodgkin. Le conjugué védotine (MMAE) est un puissant anti-tubuline. Cet ADC possède une forte activité antitumorale en monothérapie, à la fois dans certaines formes de lymphomes T tels que les lymphomes anaplasiques à grandes cellules (ALCL) et la maladie de Hodgkin réfractaire (NCT00848926) [30, 31]. L’Adcetris® en monothérapie a été associé à des neuropathies périphériques pouvant être sévères, des neutropénies et des thrombopénies, des effets secondaires classiques des agents anti-tubuline. Des cas rares, mais graves, de leucoencéphalopathies multifocale progressive (LMP), ont été observés, ainsi que, de façon plus inattendue, une augmentation de la toxicité pulmonaire en cas de combinaison avec la bléomycine, un agent connu pour induire des fibroses pulmonaires [32].
Les toxicités classiques ou inattendues des ADC
Certaines toxicités observées avec les immunoconjugués sont attendues dans la mesure où les conjugués ciblent soit la tubuline et le fuseau mitotique (auristatines, maytansinoïdes), soit l’ADN (calichéamycine, PBD). Ceux-ci comportent notamment une toxicité médullaire pouvant atteindre des grades 4, des toxicités neurologiques sensitives et végétatives. En revanche, plusieurs effets secondaires, qui ne sont pas observés avec les agents cytotoxiques standards, ont été rapportés. Ceux-ci comportent notamment des toxicités oculaires à type de kératites ou de dépôts cornéens avec les ADC comportant de la MMAF ou DM4, pouvant constituer une toxicité limitante pour ces composés [26]. Le Kadcyla® peut augmenter le risque de radionécrose [33]. Une meilleure compréhension et prise en charge de ces toxicités inattendues seront essentielles pour une utilisation optimale de ces agents.
Mécanismes de résistance aux ADC
Le mécanisme d’action des ADC au niveau de la cellule cible tumorale comporte plusieurs étapes: liaison à l’antigène, internalisation, libération du conjugué, relargage du conjugué dans le cytoplasme, puis liaison à la cible moléculaire du conjugué induisant la mort cellulaire par apoptose. Chacune de ces étapes peut être impliquée dans des phénotypes de résistance comme le suggèrent plusieurs travaux précliniques utilisant des lignées cellulaires ou dans des modèles animaux: expression réduite de l’antigène cible [34, 35], modification des pompes de transport lysosomales [36], du cytosquelette microtubulaire ou des voies des prostaglandines [37]. D’autres mécanismes tels que la surexpression de pompes d’efflux ont également été invoqués [38, 39], bien que certains conjugués ne soient pas de bons substrats pour les pompes de type ABC.
La pertinence clinique de ces différents mécanismes potentiels de résistance reste à démontrer. Cela n’a rien de surprenant dans la mesure où la détermination des mécanismes cliniques de résistance à des composés présents depuis plusieurs décennies dans la pharmacopée restent encore mal connus. De plus, il est complexe d’avoir accès à des échantillons tumoraux immédiatement avant la mise en place d’un traitement par ADC puis lors de la rechute qui suit un tel traitement. Enfin, dans le cadre de combinaisons thérapeutiques, il peut être difficile de discerner les mécanismes de résistance aux ADC de ceux des autres composés administrés. Malgré cela, les observations réalisées dans des modèles précliniques soulèvent des pistes intéressantes pour l’analyse de la résistance aux ADC chez l’homme.
Limites des approches actuelles
De nombreux ADC, en développement clinique ou utilisés en clinique, reposent sur un format d’immunoglobuline G (IgG) complet ciblant un antigène (Ag) capable d’être internalisé une fois le complexe Ac-Ag formé et dont le taux de surexpression est extrêmement élevé. Ces ADC sont conjugués à des inhibiteurs de polymérisation de la tubuline en utilisant des techniques de bioconjugaison stochastiques [4]. Cependant, les ADC utilisant un format d’IgG complète sont caractérisés par des ratios tumeur/sang et tumeur/organe sub-optimaux, ainsi que par des problèmes de pénétration des tumeurs riches en stroma [40, 41], et sont recyclés par le récepteur Fc néo-natal (FcRn), conduisant à une distribution indésirable de l’ADC dans l’endothélium vasculaire et le foie, responsable d’effets indésirables. De plus, après internalisation, l’efficacité des ADC repose sur un trafic intracellulaire favorable pour atteindre le lysosome, où leur dégradation permettra la libération contrôlée du cytotoxique. Cependant, cette stratégie présente plusieurs facteurs limitants. Premièrement, la capacité d’internalisation des ADC est intimement liée à la forte expression de l’Ag de surface (par exemple, CD30 et HER2/neu) [42], ce qui explique pourquoi ces ADC utilisant des inhibiteurs classiques de la polymérisation de la tubuline (par exemple, les auristatines et les maytansinoïdes) ne présentent pas d’activité cytotoxique sur les cellules à faible expression antigénique. Des cytotoxiques très puissants (par exemple, des dimères de pyrrolobenzodiazépine) ont été développés pour surmonter ces limitations, mais les ADC correspondants présentent un index thérapeutique limité, en particulier dans les tumeurs solides. Deuxièmement, les ADC internalisants, y compris le Kadcyla®, induisent une résistance des tumeurs par plusieurs mécanismes. En effet, des perturbations concernant l’internalisation, le trafic intracellulaire ou le recyclage de l’AcM, le relargage de l’Ag (shedding) et/ou une dégradation lysosomale défectueuse des ADC entraînent une libération réduite du médicament dans le cytosol, compromettant ainsi l’efficacité de ces derniers [34, 35, 43]. Il existe donc aujourd’hui un besoin important de développer de nouvelles technologies afin de faire progresser le développement des ADC. Pour surmonter les limitations précédemment mentionnées, des ADC innovants ont été conçus et font actuellement l’objet d’évaluations précliniques et d’études en phase clinique. Ces nouveaux ADC sont caractérisés par des innovations concernant la chimie de bioconjugaison (menant à des ADC homogènes), la partie ciblage (anticorps ou fragments), l’espaceur (mécanisme de libération) ou le cytotoxique (mécanisme d’action).
Chaque stratégie est discutée dans l’article suivant en tant qu’alternative potentielle aux ADC hétérogènes internalisants utilisés aujourd’hui en clinique pour élargir leurs champs d’applications [1].
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Le glutathion est un tripeptide contenant des fonctions thiol présent en concentrations micromolaires dans le plasma et les cellules. Il prévient les dommages dus aux radicaux libres et aux peroxydes.
Voir le paragraphe de la partie 2 « Stratégies combinées au-delà des dogmes: ADC en phase II pivotale ou phase III ».
Voir le paragraphe de la partie 2 « Nouveaux ciblages et systèmes de libération associés ».
La réaction de Michael permet la bioconjugaison d’un espaceur maléimide sur une cystéine. À l’inverse, la réaction de déconjugaison est appelée réaction de rétro-Michael.
Références
- Joubert N, Denevault-Sabourin C, Bryden F, et al. Towards antibody-drug conjugates and prodrug strategies with extracellular stimuli-responsive drug delivery in the tumor microenvironment for cancer therapy. Eur J Med Chem 2017 ; 142: 393–415. [CrossRef] [PubMed] [Google Scholar]
- Beck A, Terral G, Debaene F, et al. Cutting-edge mass spectrometry methods for the multi-level structural characterization of antibody-drug conjugates. Expert Rev Proteomics 2016 ; 13: 157–183. [PubMed] [Google Scholar]
- Haeuw JF, Caussanel V, Beck A. Les immunoconjugués, anticorps « armés » pour combattre le cancer. Med/Sci (Paris) 2009 ; 25: 1046–1052. [CrossRef] [Google Scholar]
- Beck A, Goetsch L, Dumontet C, et al. Strategies and challenges for the next generation of antibody–drug conjugates. Nat Rev Drug Discov 2017 ; 16: 315–337. [CrossRef] [PubMed] [Google Scholar]
- Martin C, Kizlik-Masson C, Pèlegrin A, et al. Antibody-drug conjugates: design and development for therapy and imaging in and beyond cancer, labEx MAbImprove industrial workshop, July 27–28, 2017, Tours. France. MAbs 2017 ; 10: 210–221. [CrossRef] [PubMed] [Google Scholar]
- Joubert N, Viaud-Massuard MC. Antibody-drug conjugates: historical developments and mechanisms of action. Optimizing antibody-drug conjugates for targeted Delivery of Therapeutics. Bielefeld University, Germany: Future Science Ltd, 2015: 6–21. [CrossRef] [Google Scholar]
- Linenberger ML, Hong T, Flowers D, et al. Multidrug-resistance phenotype and clinical responses to gemtuzumab ozogamicin. Blood 2001 ; 98: 988–994. [Google Scholar]
- Hamann PR, Hinman LM, Hollander I, et al. Gemtuzumab ozogamicin, a potent and selective anti-CD33 antibody-calicheamicin conjugate for treatment of acute myeloid leukemia. Bioconjug Chem 2002 ; 13: 47–58. [CrossRef] [PubMed] [Google Scholar]
- Ricart AD. Antibody-drug conjugates of calicheamicin derivative: gemtuzumab ozogamicin and inotuzumab ozogamicin. Clin Cancer Res 2011 ; 17: 6417–6427. [CrossRef] [PubMed] [Google Scholar]
- Trail P, Willner D, Lasch S, et al. Cure of xenografted human carcinomas by BR96-doxorubicin immunoconjugates. Science 1993 ; 261: 212–215. [Google Scholar]
- Kantarjian HM, DeAngelo DJ, Stelljes M, et al. Inotuzumab ozogamicin versus standard therapy for acute lymphoblastic leukemia. N Engl J Med 2016 ; 375: 740–753. [Google Scholar]
- Chari RVJ. Targeted cancer therapy: conferring specificity to cytotoxic drugs. Acc Chem Res 2008 ; 41: 98–107. [CrossRef] [PubMed] [Google Scholar]
- Erickson HK, Widdison WC, Mayo MF, et al. Tumor delivery and in vivo processing of disulfide-linked and thioether-linked antibody-maytansinoid conjugates. Bioconjug Chem 2010 ; 21: 84–92. [CrossRef] [PubMed] [Google Scholar]
- Erickson HK, Lewis Phillips GD, Leipold DD, et al. The effect of different linkers on target cell catabolism and pharmacokinetics/pharmacodynamics of trastuzumab maytansinoid conjugates. Mol Cancer Ther 2012 ; 11: 1133–1142. [Google Scholar]
- Sun MMC, Beam KS, Cerveny CG, et al. Reduction-alkylation strategies for the modification of specific monoclonal antibody bisulfides. Bioconjug Chem 2005 ; 16: 1282–1290. [CrossRef] [PubMed] [Google Scholar]
- Doronina SO, Toki BE, Torgov MY, et al. Development of potent monoclonal antibody auristatin conjugates for cancer therapy. Nat Biotech 2003 ; 21: 778–784. [CrossRef] [PubMed] [Google Scholar]
- Katz J, Janik JE, Younes A. Brentuximab vedotin (SGN-35). Clin Cancer Res 2011 ; 17: 6428–6436. [CrossRef] [PubMed] [Google Scholar]
- Li F, Emmerton KK, Jonas M, et al. Intracellular released payload influences potency and bystander-killing effects of antibody-drug conjugates in preclinical models. Cancer Res 2016 ; 76: 2710–2719. [Google Scholar]
- Kovtun Y V., Audette CA, Ye Y, et al. Antibody-drug conjugates designed to eradicate tumors with homogeneous and heterogeneous expression of the target antigen. Cancer Res 2006 ; 66: 3214–3221. [Google Scholar]
- Ogitani Y, Hagihara K, Oitate M, et al. Bystander killing effect of DS-8201a, a novel anti-human epidermal growth factor receptor 2 antibody-drug conjugate, in tumors with human epidermal growth factor receptor 2 heterogeneity. Cancer Sci 2016 ; 107: 1039–1046. [CrossRef] [PubMed] [Google Scholar]
- Dal Corso A, Cazzamalli S, Gébleux R, et al. Protease-cleavable linkers modulate the anticancer activity of noninternalizing antibody-drug conjugates. Bioconjug Chem 2017; 28: 1826–33. [CrossRef] [PubMed] [Google Scholar]
- Teicher B.. Antibody-drug conjugate targets. Curr Cancer Drug Targets 2009 ; 9: 982–1004. [CrossRef] [PubMed] [Google Scholar]
- Pfeifer M, Zheng B, Erdmann T, et al. Anti-CD22 and anti-CD79B antibody drug conjugates are active in different molecular diffuse large B-cell lymphoma subtypes. Leukemia 2015 ; 29: 1578–1586. [CrossRef] [PubMed] [Google Scholar]
- An anti-CD79B antibody-drug conjugate is active in non-Hodgkin lymphoma. Cancer Discov 2015; 5: 576. doi: 10.1158/2159-8290.CD-RW2015-085. [Google Scholar]
- Alley SC, Benjamin DR, Jeffrey SC, et al. Contribution of linker stability to the activities of anticancer immunoconjugates. Bioconjug Chem 2008 ; 19: 759–765. [CrossRef] [PubMed] [Google Scholar]
- Donaghy H.. Effects of antibody, drug and linker on the preclinical and clinical toxicities of antibody-drug conjugates. MAbs 2016 ; 8: 659–671. [CrossRef] [PubMed] [Google Scholar]
- Dorywalska M, Dushin R, Moine L, et al. Molecular basis of valine-citrulline-PABC linker instability in site-specific ADCs and Its mitigation by linker design. Mol Cancer Ther 2016 ; 15: 958–970. [Google Scholar]
- Zhao H, Gulesserian S, Malinao MC, et al. A potential mechanism for ADC-induced neutropenia: role of neutrophils in their own demise. Mol Cancer Ther 2017 ; 16: 1866–1876. [Google Scholar]
- Castaigne S, Pautas C, Terré C, et al. Effect of gemtuzumab ozogamicin on survival of adult patients with de-novo acute myeloid leukaemia (ALFA-0701): a randomised, open-label, phase 3 study. Lancet 2012 ; 379: 1508–1516. [CrossRef] [PubMed] [Google Scholar]
- A phase 2 study of brentuximab vedotin in patients with relapsed or refractory CD30-positive non-Hodgkin lymphomas: interim results in patients with DLBCL and other B-cell lymphomas. Clin Adv Hematol Oncol 2014; 12: 3–4. [Google Scholar]
- Connors JM, Jurczak W, Straus DJ, et al. Brentuximab vedotin with chemotherapy for stage III or IV Hodgkin’s lymphoma. N Engl J Med 2018 ; 378: 331–344. [Google Scholar]
- Younes A, Connors JM, Park SI, et al. Brentuximab vedotin combined with ABVD or AVD for patients with newly diagnosed Hodgkin’s lymphoma: a phase 1, open-label, dose-escalation study. Lancet Oncol 2013 ; 14: 1348–1356. [CrossRef] [PubMed] [Google Scholar]
- Carlson JA, Nooruddin Z, Rusthoven C, et al. Trastuzumab emtansine and stereotactic radiosurgery: an unexpected increase in clinically significant brain edema. Neuro Oncol 2014 ; 16: 1006–1009. [CrossRef] [PubMed] [Google Scholar]
- Loganzo F, Tan X, Sung M, et al. Tumor cells chronically treated with a trastuzumab-maytansinoid antibody-drug conjugate develop varied resistance mechanisms but respond to alternate treatments. Mol Cancer Ther 2015 ; 14: 952–963. [Google Scholar]
- Chen R, Hou J, Newman E, et al. CD30 downregulation, MMAE resistance, and MDR1 upregulation are all associated with resistance to brentuximab vedotin. Mol Cancer Ther 2015 ; 14: 1376–1384. [Google Scholar]
- Hamblett KJ, Jacob AP, Gurgel JL, et al. SLC46A3 is required to transport catabolites of noncleavable antibody maytansineconjugates from the lysosome to the cytoplasm. Cancer Res 2015 ; 75: 5329–5340. [Google Scholar]
- Sauveur J, Matera E-L, Chettab K, et al. Esophageal cancer cells resistant to T-DM1 display alterations in cell adhesion and the prostaglandin pathway. Oncotarget 2018; 9. [Google Scholar]
- Yu SF, Zheng B, Go M, et al. A novel anti-CD22 anthracycline-based antibody-drug conjugate (ADC) that overcomes resistance to auristatin-based ADCs. Clin Cancer Res 2015 ; 21: 3298–3306. [CrossRef] [PubMed] [Google Scholar]
- Chang CH, Wang Y, Zalath M, et al. Combining ABCG2 Inhibitors with IMMU-132, an anti-trop-2 antibody conjugate of SN-38, overcomes resistance to SN-38 in breast and gastric cancers. Mol Cancer Ther 2016 ; 15: 1910–1919. [Google Scholar]
- Yasunaga M, Manabe S, Matsumura Y. New concept of cytotoxic immunoconjugate therapy targeting cancer-induced fibrin clots. Cancer Sci 2011 ; 102: 1396–1402. [CrossRef] [PubMed] [Google Scholar]
- Yasunaga M, Manabe S, Tarin D, et al. Cancer-stroma targeting therapy by cytotoxic immunoconjugate bound to the collagen 4 network in the tumor tissue. Bioconjug Chem 2011 ; 22: 1776–1783. [CrossRef] [PubMed] [Google Scholar]
- Lambert JM, Morris CQ. Antibody-drug conjugates (ADCs) for personalized treatment of solid tumors: a review. Adv Ther 2017 ; 34: 1015–1035. [CrossRef] [PubMed] [Google Scholar]
- Barok M, Joensuu H, Isola J. Trastuzumab emtansine: mechanisms of action and drug resistance. Breast Cancer Res 2014 ; 16: 3378. [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1. Représentation des 5 ADC approuvés par la FDA: Mylotarg®, Adcetris®, Kadcyla®, Besponsa® et Polivy®. |
| Dans le texte | |
 |
Figure 2. Représentation schématique d’un ADC ou anticorps armé. |
| Dans le texte | |
 |
Figure 3. Mécanisme d’action du Mylotarg® ou du Besponsa®. Les différentes étapes sont: (1) liaison à un antigène (Ag) spécifique, suivie de l’internalisation du complexe ADC-Ag selon un mécanisme dépendant de la clathrine ; (2) transfert dans les endosomes ; (3) le clivage du linker dans les lysosomes s’effectue au niveau de l’hydrazone acido-sensible ; (4) transfert de la pro-calichéamycine dans le lysosome ; (5) clivage du pont disulfure pour donner la calichéamycine puis (6) transfert de la calichéamycine dans le cytoplasme ; (7) transfert de la calichéamycine dans le noyau. (8) Alternativement à 7, transfert de la calichéamycine dans le cytoplasme puis: (9) diffusion de la calichéamycine dans les cellules cancéreuses voisines pour obtenir un effet bystander cytotoxique ; (10) toutes les étapes précédentes conduisent à la mort cellulaire. |
| Dans le texte | |
 |
Figure 4. Mécanisme d’action du Kadcyla®. Les différentes étapes sont: (1) fixation du Kadcyla® sur son antigène (Ag) spécifique HER2/neu, suivie d’une internalisation du complexe T-DM1-HER2/neu par un mécanisme dépendant de la clathrine ; (2) transfert dans l’endosome puis (3) dans le lysosome ; (4) digestion complète du trastuzumab pour libérer le métabolite actif, l’acide LYS-NCL-DM1 ; (5) transfert dans le cytoplasme. (6) Pas d’effet bystander cytotoxique, et transfert vers la tubuline. (7) Toutes les étapes précédentes conduisent à la mort cellulaire de la cellule cancéreuse HER2-positive. |
| Dans le texte | |
 |
Figure 5. Mécanisme d’action de l’Adcetris® ou du Polivy®. Les différentes étapes sont: (1) liaison à un antigène (Ag) spécifique, suivie de l’internalisation du complexe ADC-Ag selon un mécanisme dépendant de la clathrine ; (2) transfert dans les endosomes puis (3) dans les lysosomes ; (4) le clivage du linker dans les lysosomes s’effectue entre la séquence peptidique (ValCit) et l’espaceur auto-immolable (PAB) ; (5) transfert de la MMAE dans le cytoplasme. (6) La MMAE peut également être libérée avant internalisation, puis (7) entrer dans la cellule ciblée (ou une cellule proche voisine). (8) Dans tous les cas, la MMAE libérée peut ensuite agir sur la tubuline. Alternativement à (8), (9) diffusion de la MMAE dans les cellules cancéreuses voisines non ciblées par l’ADC conduisant à un effet bystander cytotoxique. Toutes les étapes précédentes conduisent à la mort cellulaire. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




