| Issue |
Med Sci (Paris)
Volume 30, Number 4, Avril 2014
|
|
|---|---|---|
| Page(s) | 415 - 421 | |
| Section | Microenvironnements tumoraux : conflictuels et complémentaires | |
| DOI | https://doi.org/10.1051/medsci/20143004016 | |
| Published online | 5 mai 2014 | |
ERO, NADPH oxydases et vascularisation des tumeurs
ROS and NADPH oxidase: key regulators of tumor vascularisation
Centre médical universitaire, département pathologie et immunologie, faculté de médecine, université de Genève, 1, rue Michel Servet, 1211
Genève, Suisse
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
**
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
***
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Le stress oxydatif est la conséquence d’un déséquilibre entre la production d’espèces réactives de l’oxygène (ERO) et les mécanismes anti-oxydants permettant leur élimination. Il se manifeste par des dommages de tous les constituants cellulaires : ADN, protéines et lipides. Les ERO sont pourtant importants pour la physiologie de l’organisme, puisqu’ils participent à la défense immunitaire innée et à la signalisation intracellulaire. Ils jouent également un rôle important dans la tumorigenèse, en favorisant la vascularisation des tumeurs, un phénomène essentiel à la croissance et à la dissémination tumorale. Il existe de nombreuses sources cellulaires d’ERO, dont les enzymes NOX (oxydases dépendantes du NADPH), qui ont comme unique fonction de produire des ERO. Cet article traite du rôle des NOX dans l’angiogenèse tumorale.
Abstract
Oxidative stress is the result of an imbalance between the production of reactive oxygen species (ROS) and antioxidant mechanisms. It is characterized by damage of all cellular components, DNA, proteins, lipids. ROS are nevertheless important for the physiology of an organism, as they are involved in the innate immune defense and several intracellular signaling pathways. They play an important role in tumorigenesis by promoting tumor vasculature, which is essential to their growth and metastatic processes. There are many sources of ROS in the cells, but the NOX enzymes (NADPH oxidase-dependent) are now recognized to have a major role in the oxidative stress process. Indeed, they are present in many tissues where their only function is to produce ROS. This article discusses the NOX in endothelial cells and their role in the tumor angiogenesis.
Cet article fait partie du numéro thématique publié par médecine/sciences en avril 2014 et intitulé « Microenvironnement tumoral ».
© 2014 médecine/sciences – Inserm
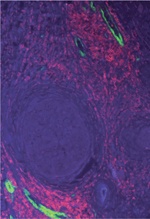
L’angiogenèse : une nécessité pour la tumeur
La vascularisation est un processus physiologique essentiel lors du développement embryonnaire, durant lequel se succède une phase de vasculogenèse, qui consiste en la formation d’un plexus vasculaire primitif à partir de progéniteurs angioblastiques, suivie d’une phase angiogénique, qui permet l’extension et la ramification de ce plexus primitif. Chez l’individu adulte, la formation de néovaisseaux est un mécanisme qui a lieu régulièrement lors des processus de cicatrisation, mais également durant le cycle menstruel et la grossesse.
Lors de situations pathologiques, en particulier le développement d’un cancer, la formation de néovaisseaux est un facteur critique pour la croissance des tumeurs solides. Les vaisseaux sanguins permettent l’oxygénation, l’apport en nutriments, mais également la dissémination des cellules tumorales métastatiques. Sans la formation de nouveaux vaisseaux, les tumeurs solides ne sont pas capables de croître au-delà d’environ 2 mm. En effet, les cellules au centre de la masse tumorale n’ont plus accès aux nutriments et à l’oxygène, et ne peuvent plus proliférer, ce qui stoppe le développement de la tumeur, laquelle devient dormante et peut même régresser [1]. Ces dernières années, une attention particulière a été portée aux thérapies anti-angiogéniques pour le traitement des cancers. En 2004 déjà, un anticorps thérapeutique anti-VEGF-A (vascular endothelial growth factor-A) humain (Avastin/bévacizumab) a été introduit en clinique en combinaison avec des traitements cytostatiques, notamment pour le traitement de cancers colorectaux métastatiques [2]. Depuis, de nombreux composés anti-angiogéniques ont été développés par l’industrie pharmaceutique et font actuellement l’objet d’études cliniques (pour revue voir [3]).
Les cellules tumorales utilisent plusieurs stratégies pour assurer leur apport en oxygène et en nutriments [42] (→) : (1) l’angiogenèse, qui consiste en la formation de nouveaux vaisseaux à partir de vaisseaux préexistants ; (2) la co-option, une situation dans laquelle les tumeurs détournent les vaisseaux existants pour croître sans angiogenèse ; (3) le mimétisme vasculaire, où des cellules tumorales acquièrent un phénotype de cellules endothéliales et forment des vaisseaux ; et (4) le recrutement de progéniteurs endothéliaux circulants dans le sang périphérique [4]. Néanmoins, c’est l’angiogenèse qui contribue majoritairement à la vascularisation des tumeurs. Ce processus nécessite plusieurs étapes (Figure 1). Une cellule endothéliale quiescente acquiert un phénotype migratoire et invasif lorsqu’elle est stimulée par des facteurs pro-angiogéniques, tels que le VEGF ou le FGF (fibroblast growth factor), qui sont sécrétés par le microenvironnement vasculaire (cellules tumorales, immunitaires ou stromales). Les péricytes, cellules périvasculaires, jouent un rôle essentiel dans la mise en place du processus : ils se détachent de la barrière endothéliale et sécrètent des métalloprotéinases qui vont dégrader la membrane basale et permettre la migration des cellules endothéliales sous-jacentes. Certaines cellules endothéliales, dites tip cells (cellules du front), migrent à travers le milieu extracellulaire, initiant la formation d’un néovaisseau qui va servir de support pour les cellules adjacentes, appelées stalk cells, qui prolifèrent pour allonger le néovaisseau formé par les tip cells. Une lumière se forme ensuite par fusion de vacuoles intracellulaires. Lors du processus d’angiogenèse physiologique, le néovaisseau se stabilise ensuite en rétablissant les jonctions inter-endothéliales et en recrutant des cellules périvasculaires. Mais lors de l’angiogenèse tumorale, les néovaisseaux formés restent inachevés, peu de péricytes sont recrutés et les jonctions intercellulaires ne sont pas complètement refermées, ce qui rend les vaisseaux très perméables. De plus, le réseau formé par les vaisseaux tumoraux est tortueux et irrégulier [5].
(→) Voir la Synthèse de S. Azzi et J. Gavard, page 408 de ce numéro
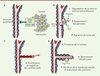 |
Figure 1. L’angiogenèse physiologique. A. La formation de nouveaux vaisseaux à partir d’un vaisseau préexistant quiescent est déclenchée par la stimulation exogène de facteurs de croissance (VEGF, FGF, PDGF-BB, etc.) sécrétés, par exemple, par des cellules tumorales et/ou des cellules immunitaires infiltrant une tumeur. B. Une cellule endothéliale répond au stimulus en migrant et en dégradant la matrice extracellulaire, puis elle devient une tip cell. Cette migration nécessite, en premier lieu, le détachement des péricytes pour permettre la migration des cellules endothéliales sous-jacentes. L’activation des cellules voisines de la cellule sélectionnée est inhibée par la voie de signalisation Notch/Dll4 (delta-like ligand 4), ce qui empêche la formation de plusieurs branchements émergents. C. Pour étendre le vaisseau naissant, les cellules stalk prolifèrent et migrent en suivant la tip cell. D. Pour finaliser le processus, une lumière se forme par fusion de vacuoles intracellulaires ; ensuite, des péricytes sont recrutés le long des cellules endothéliales pour stabiliser le vaisseau par sécrétion d’une matrice extracellulaire qui va former la membrane basale. Les cellules forment de nouvelles jonctions intercellulaires matures. Enfin, des signaux de quiescence, tels que Ang1 (angiopoïétine 1)/Tie2, permettent de stabiliser le nouveau vaisseau par inhibition de la prolifération. |
L’angiogenèse peut être induite par un stress cellulaire comme l’ischémie, mais aussi par les espèces réactives de l’oxygène (ERO), souvent appelées radicaux libres. En effet, les ERO stabilisent HIF1-α (hypoxia-induced factor 1-α), un facteur de transcription responsable de la production de facteurs pro-angiogéniques par les cellules tumorales [6, 43] (→). Les cellules tumorales, lors de leur développement, acquièrent la capacité d’induire la formation de nouveaux vaisseaux par la sécrétion de facteurs pro-angiogéniques, tels que le VEGF ou le FGF. En sécrétant des chimiokines, les cellules tumorales attirent des cellules immunitaires comme les monocytes ou les macrophages qui, à leur tour, sécrètent des facteurs proangiogéniques. Le mécanisme qui permet à la tumeur de passer d’un phénotype quiescent à un phénotype angiogénique s’appelle le switch angiogénique [7].
(→) Voir la Synthèse de M. Hasmim et al., pages 422 de ce numéro
De nombreux facteurs de croissance stimulent la formation de vaisseaux. Le plus étudié et le mieux caractérisé est le VEGF. La liaison du VEGF au récepteur VEGFR-2 (Flk1/KDR) active les voies de signalisation ERK (extracellular signal-regulated kinase) et Akt (protéine kinase B), qui conduisent à la prolifération et la migration des cellules endothéliales. L’angiogenèse tumorale peut également être stimulée par des cellules inflammatoires infiltrant la tumeur. De nombreuses études ont montré que des molécules anti-oxydantes diminuent l’angiogenèse tumorale en neutralisant les ERO qui contrôlent la signalisation tumorale [8]. Ces molécules anti-oxydantes peuvent aussi agir sur les ERO générés par les leucocytes infiltrant la tumeur [9]. Toutefois, le bénéfice des thérapies anti-oxydantes n’a, à ce jour, pas été confirmé en clinique [10], probablement à cause du manque de spécificité de ces molécules. Une nouvelle approche consiste à cibler la source des ERO plutôt que d’essayer de les neutraliser une fois qu’ils ont été produits [11–13].
Stress oxydatif et NADPH oxydase
Les phénomènes d’oxydation sont régulés par l’équilibre entre les ERO - l’O2-•, H2O2, ONOO-•, O1•, RO• - et les systèmes anti-oxydants de la cellule. À forte dose, les ERO ont des effets délétères sur les cellules car ils oxydent l’ADN, les protéines et les lipides. Ce phénomène est appelé stress oxydatif et conduit à la mort cellulaire. Toutefois, à faible dose, les ERO ont une action régulatrice impliquée dans de nombreux processus physiologiques, en activant notamment différentes voies de signalisation cellulaire. Par exemple, dans le cas de l’angiogenèse, ils peuvent activer des kinases comme la MAPK (mitogen activator protein kinase) ou la PI3-K (phospho-inositol-3 kinase) ou des facteurs de transcription comme NF-κB (nuclear factor kB) [14]. NF-κB est un élément central de la signalisation induite par les ERO, parce que celles-ci régulent son activité à différents niveaux de sa cascade d’activation, mais aussi parce que plusieurs de ses gènes cibles influencent la formation d’ERO [15].
Les ERO générées sont souvent des produits secondaires des réactions enzymatiques utilisant l’oxygène, mais dans le cas des enzymes NAPDH oxydases, elles sont le principal produit de la réaction.
Les NADPH oxydases (NOX) constituent une famille de sept enzymes transmembranaires qui catalysent le transfert d’électrons à travers les membranes cellulaires en utilisant le NADPH comme donneur d’électron pour réduire l’oxygène moléculaire et produire l’anion superoxyde O2-• (Figure 2A). Chaque membre de la famille présente un profil d’expression tissulaire et un mode de régulation qui lui sont propres (pour revue voir [16, 17]).
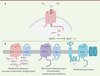 |
Figure 2. Mécanisme d’action et structure des NAPDH oxydases. A. Les enzymes NOX catalysent le transfert d’électrons à travers la membrane plasmique en utilisant le NADPH comme donneur d’électron (e) et l’oxygène comme accepteur. Cette réaction génère l’anion superoxyde comme produit principal de réaction, et du NADP+ et des protons (H+) comme produits secondaires. B. Structure des complexes NAPDH. Les NOX contiennent six hélices α (sept pour les DUOX) transmembranaires et une queue cytoplasmique qui contient un domaine de fixation du NAPDH et du FAD. NOX-1, -2, -3 et -4 s’associent à la sous-unité membranaire p22phox. Pour NOX-1, -2 et -3, le complexe comprend, en plus, des sous-unités cytosoliques régulatrices (p67phox/NOXA1, Rac1/2, p40phox) et organisatrices (p47phox/NOXO1) essentielles pour leur activité enzymatique. L’activité catalytique des DUOX est dépendante du calcium, ce qui permet l’activation du centre catalytique enzymatique, mais également de deux sous-unités membranaires, DUOXA1/2. NOX-5 est, quant à elle, uniquement dépendante du calcium, ce qui permet l’activation de son centre catalytique. |
Toutes les NOX sont exprimées à la membrane plasmique dans les radeaux lipidiques au sein de diverses structures comme les caveolae, les endosomes ou les phagosomes (pour NOX-2 uniquement), à l’exception de NOX-4 qui est localisée dans des organites intracellulaires comme le réticulum endoplasmique, les mitochondries et le noyau [18]. NOX-1, -2 et -3 ont besoin d’être associées à des sous-unités régulatrices et organisatrices : p22phox, p40phox, p47phox (NOXO1), p67phox (NOXA1), et Rac1/2 (Figure 2B). La sous-unité membranaire p22phox stabilise l’enzyme NOX à la membrane et sert de point d’ancrage pour la sous-unité p47phox grâce à ses séquences riches en proline. Dans le cytoplasme d’une cellule quiescente, p40phox, p47phox (NOXO1), et p67phox (NOXA1) forment un complexe qui, sous l’action d’un stimulus, est transporté à la membrane. Rac1 est, lui, recruté au niveau du complexe membranaire de manière indépendante [19]. Récemment, deux nouveaux régulateurs de l’activité de NOX-1, Tks4 et Tks5, ont été identifiés. Ces protéines font partie de la famille de p47phox et se lient à NOXA1 pour réguler son activité, notamment dans les cellules tumorales invasives où ces complexes se localisent dans les invadopodia [20]. De nouveaux régulateurs de l’activité de NOX-2 dans les cellules endothéliales ont également été identifiés : Prdx6 (peroxiredoxin 6) et le récepteur de l’adénosine A2A [21, 22]. NOX-4, quant à elle, ne nécessite pas les sous-unités régulatrices, mais s’associe à p22phox qui est essentielle à son activité (Figure 2B). Deux autres partenaires de NOX-4, récemment décrits, pourraient être importants pour sa régulation : NOXR1 et Poldip2 (polymerase delta-interacting protein 2). NOX-5, et les DUOX-1 et 2, sont activées par l’augmentation du niveau intracellulaire de calcium qui se lie à des domaines de type EF-hand (Figure 2B). Cependant, DUOX-1 et 2 requièrent tout de même pour leur activité catalytique des facteurs de maturation membranaire : DUOXA1 et DUOXA2.
Leur expression différentielle au niveau tissulaire et leur localisation subcellulaire leur permettent de répondre à des stimulus de manière relativement spécifique.
Dans les cellules du système vasculaire, NOX-1, NOX-2 et NOX-4 sont les membres de la famille NOX les plus exprimés (Figure 3). Plusieurs variants de NOX-5 sont fortement exprimés par les cellules endothéliales vasculaires humaines, mais leur fonction dans la physiologie endothéliale est encore très peu connue, principalement en raison de l’absence de modèle animal (cette protéine n’étant pas exprimée chez les rongeurs).
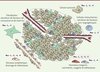 |
Figure 3. Les NOX sont exprimées dans les différents compartiments du microenvironnement tumoral. Les tumeurs croissent en développant autour d’elles un microenvironnement constitué de plusieurs types de cellules : des cellules immunitaires, des fibroblastes, des cellules endothéliales (vasculaires et lymphatiques) et des péricytes. Ce microenvironnement contribue à la progression et à la dissémination de la tumeur. Les cellules de ce microenvironnement expriment différentes combinaisons d’isoformes de NOX qui peuvent être ciblées dans le cadre d’un protocole thérapeutique. |
Les NOX régulent la physiologie endothéliale
NOX-1
NOX-1 est fortement exprimée dans l’épithélium colorectal, en particulier dans les cancers colorectaux, mais sa fonction dans ce tissu reste peu connue. En revanche, bien que l’expression basale de NOX-1 soit très faible dans les cellules vasculaires, elle peut être induite par différents stimulus, tels que des stimulus mécaniques, des facteurs de croissance pro-angiogéniques (EGF [epidermal growth factor], VEGF, PDGF [plateled-derived growth factor]), ou l’angiotensine 2 [23, 24].
Le rôle de NOX-1 dans le processus de transformation oncogénique a été étudié par Shinohara et ses collègues. La surexpression du facteur oncogénique K-Ras dans des cellules rénales de rat induit la surexpression de NOX-1 et une augmentation de la production d’ERO qui mène à l’activation de la voie NFκ-B [25]. L’activation de NF-κB promeut le phénotype invasif des cellules transformées, notamment en induisant l’expression de la métalloprotéase matricielle MMP-9 [26]. Dans les cellules tumorales, NOX-1 est également activée par l’acide arachidonique, qui induit le renouvellement des intégrines, et la prolifération et la migration des cellules [27]. Les ERO produites par NOX-1 dans les cellules tumorales peuvent agir sur la vascularisation des tumeurs en stimulant la sécrétion de VEGF par les cellules tumorales, ou en activant directement les cellules endothéliales via une sécrétion extracellulaire.
Notre équipe a récemment montré que NOX-1 participe également à l’angiogenèse tumorale. En effet, l’angiogenèse des souris déficientes pour NOX-1 est fortement diminuée, bien que ces souris présentent un phénotype vasculaire normal en condition basale. L’administration d’un composé inhibiteur de l’activité de NOX-1, GKT13901 (GenKyoTex), réduit de manière importante la vascularisation des tumeurs implantées dans des souris et, par conséquent, leur croissance. Ces données démontrent que l’inhibition de NOX-1 représente potentiellement une nouvelle approche thérapeutique antitumorale. Cet effet est comparable à celui de l’inhibiteur de l’angiogenèse précédemment décrit, l’anticorps anti-VEGFR2 (DC101). Cependant, contrairement au VEGFR2 qui induit l’angiogenèse en activant la voie ERK, les ERO générées par NOX-1 stimulent l’angiogenèse en inactivant le peroxisome proliferator activator receptor-a (PPAR-α) qui contrôle l’activité de NF-κB, [23] (Figure 4A). Le mécanisme par lequel les ERO produites par NOX-1 inhibent PPAR-α n’est pas encore élucidé. Elles modifient l’expression, mais également l’activité de PPAR-α, et ceci probablement par une modification post-traductionnelle.
 |
Figure 4. Les enzymes NOX jouent un rôle coordonné dans les cellules endothéliales et tumorales. A. Dans les cellules tumorales, NOX-1 peut être activée par un oncogène (K-ras) ou par des acides gras, comme l’acide arachidonique (AA). Les ERO produites en conséquence activent HIF-1α, NF-κB [26] et le renouvellement des intégrines [27], ce qui contribue, respectivement, à la migration des cellules tumorales, à la sécrétion de facteurs angiogéniques et à la prolifération des cellules tumorales. Dans les cellules endothéliales, NOX-1 est activée par Rac1 qui est elle-même activée par le VEGFR. NOX-1 sécrète des ERO qui bloquent l’activation du facteur de transcription PPAR-α, un inhibiteur de NF-κB. Les ERO produites par NOX-1 activent, par conséquent, la migration et l’invasion des cellules endothéliales [23]. B. Dans les cellules tumorales, NOX-4 contribue à la prolifération et à la survie des cellules par l’activation des voies Akt et NF-κB. NOX-4 participe également à l’angiogenèse par l’activation d’HIF-2α, qui active la production de VEGF [39]. Dans les cellules endothéliales, NOX-4, qui est exprimée au niveau du réticulum endoplasmique, sécrète des ERO qui activent les MAP kinases, ce qui promeut la prolifération des cellules endothéliales. En parallèle, NOX-4 inhibe l’apoptose par l’inhibition de la production d’eNOS [38]. NOX-4 peut être activée par l’angiotensine 2 ou par l’hypoxie. C. Dans les cellules tumorales, l’activation de NOX-2 par l’interleukine-3 (IL-3) et le VEGF participe au processus de survie des cellules, notamment dans des cellules leucémiques [40]. Dans les cellules endothéliales, NOX-2 est située dans les radeaux lipidiques et s’associe avec IQGAP1 au niveau du front migratoire des cellules endothéliales pour orienter la migration des cellules durant les processus angiogéniques [31]. Les ERO produites par NOX-2 inhibent la voie d’apoptose des caspases 3/7, ce qui contribue à la survie des cellules [41]. |
Par ailleurs, NOX-1 inhibe l’apoptose dans les cellules endothéliales sinusoïdales [28] et est impliquée dans l’effet protecteur anti-apoptotique du resvératrol, un polyphénol naturel du raisin, sur les cellules endothéliales [29].
L’avantage qu’il y avait à cibler cette enzyme dans le cadre d’une thérapie anti-angiogénique découle de deux choses : (1) NOX-1 est, à l’état basal, faiblement exprimée dans des vaisseaux quiescents, ce qui laisse présager peu d’effets secondaires sur les tissus sains ; (2) en revanche, NOX-1 est exprimée par certaines cellules tumorales. Une thérapie ciblant NOX-1 serait plus efficace, car elle agirait simultanément sur la tumeur et sur les vaisseaux.
NOX-2
NOX-2 est très fortement exprimée dans les neutrophiles et les macrophages où elle exerce une activité microbicide essentielle à la défense immunitaire. Des mutations affectant le gène de NOX-2 conduisent à une maladie génétique, la granulomatose septique chronique, caractérisée par des infections récurrentes et des phénomènes inflammatoires. Au niveau des processus angiogéniques, il a été montré, dans un modèle in vivo dans lequel l’angiogenèse est stimulée par une éponge imbibée de facteur pro-angiogénique, que le défaut de NOX-2 entraîne une réduction de la vascularisation des éponges dépendante du VEGF [30]. Dans un autre modèle utilisant le bFGF comme stimulant de l’angiogenèse, notre équipe a montré que la vascularisation des implants chez des souris knock-out (KO) pour NOX-2 était similaire à celle des implants des souris sauvages [23]. Cela suggère que l’effet de NOX-2 sur l’angiogenèse est dépendant de la nature de la stimulation.
Dans les cellules endothéliales, il a été montré que NOX-2 est, à l’état basal, faiblement exprimée, mais semble tout de même importante pour la migration des cellules endothéliales. En effet NOX-2 s’associe à IQGAP1 (Ras GTPase-activating-like protein), une molécule d’échafaudage du réseau d’actine, et cette interaction oriente la sécrétion d’ERO au niveau du front de migration des cellules. Dans cette étude, les auteurs ont montré que, lors d’un test de cicatrisation d’une monocouche de cellules endothéliales, NOX-2 est localisée au front de migration où l’enzyme co-localise avec les filaments d’actine et la molécule d’échafaudage IQGAP1. Si l’expression d’IQGAP1 est abolie par interférence ARN, la translocation de NOX-2 n’est plus observée et les cellules ne migrent plus [31] (Figure 4C). Lors d’une stimulation par le VEGF en condition d’ischémie, les ERO produites par NOX-2 inhibent par oxydation la phosphatase PTP qui, elle-même, inhibe la voie de signalisation des adhésions focales qui participe à la migration des cellules endothéliales [32].
NOX-2 pourrait participer à la vascularisation des tumeurs par un autre processus que l’angiogenèse, par le recrutement de progéniteurs, comme le suggèrent les études récentes du groupe de Ralf Brandes. Ces travaux montrent l’implication de NOX-2 dans la mobilisation de progéniteurs endothéliaux de la moelle osseuse, en réponse à différents stimulus, tels que l’hypoxie ou l’HGF (hepatocyte growth factor) [33].
NOX-4
NOX-4 est faiblement exprimée par beaucoup de types cellulaires, mais fortement par les cellules de l’épithélium rénal, les fibroblastes ainsi que les cellules endothéliales. Ces dernières expriment d’ailleurs NOX-4 à un niveau plus élevé que les autres NOX (NOX-1, -2 et -5) [34]. NOX-4 est également fortement exprimée dans plusieurs carcinomes, tels que le mélanome, le gliome, le cancer pancréatique, ainsi que dans les cancers rénaux et ovariens, mais aussi dans des tumeurs vasculaires (hémangiome) [12, 35]. Le rôle de NOX-4 dans les cellules tumorales et endothéliales est principalement de contrôler la prolifération [12, 36]. En effet, la production de peroxyde d’hydrogène par NOX-4 active par oxydation les voies de signalisation Akt et NF-κB dans les cellules tumorales pancréatiques, et les voies MAPK et Src dans les cellules endothéliales, ce qui participe à leur survie (Figure 4B) [37]. En parallèle de l’activation de la prolifération, NOX-4 inhibe l’apoptose des cellules endothéliales par l’inhibition de la voie eNOS [38].
NOX-4 participe également au développement tumoral par l’induction de l’angiogenèse en activant le facteur de transcription HIF2-α, qui induit l’expression de facteurs pro-angiogéniques, comme le VEGF ou l’angiopoïétine-2 (Figure 4B) [39, 43] (→).
(→) Voir la Synthèse de M. Hasmim et al., page 422 de ce numéro
Aucune étude n’a, à l’heure actuelle, montré de rôle de NOX-4 dans la migration des cellules endothéliales. Notre équipe n’a pas observé de différence de capacité migratoire des cellules endothéliales déficientes en NOX-4 ; de même, les souris NOX-4 KO ne présentent pas de défaut de vascularisation d’implant sous-cutané [23].
Conclusion
NOX-1, NOX-2 et NOX-4 sont des générateurs d’ERO dans les cellules endothéliales et régulent de nombreuses fonctions physiologiques. Leurs différentes localisations subcellulaires suggèrent une spécificité d’action vis-à-vis de différents stimulus. NOX-1 et NOX-2 sont localisées à la membrane plasmique, ce qui leur permet de répondre à des stimulus extracellulaires via l’activation d’un récepteur transmembranaire, tel que le VEGFR. NOX-2 est, de plus, associée aux microfilaments d’actine et peut influencer le remodelage du cytosquelette pendant la prolifération et la migration des cellules endothéliales. NOX-4 est localisée au niveau des membranes périnucléaires et du réticulum endoplasmique, ce qui lui confère une activité sur la prolifération des cellules par l’activation des voies de signalisation MAPK ou Src.
Les ERO sont impliquées dans différents processus pathologiques. La possibilité d’inhiber leur production à leur source, c’est-à-dire en bloquant l’activité catalytique des NOX, représente un nouveau concept thérapeutique à fort potentiel, d’autant plus que certaines NOX sont exprimées par les cellules tumorales elles-mêmes. De nouveaux inhibiteurs de NOX sont d’ailleurs développés par l’industrie pharmaceutique, mais aucune molécule n’a, pour l’instant, franchi l’étape d’une étude d’efficacité. Dans ce contexte, un inhibiteur spécifique de NOX capable d’inhiber l’angiogenèse tumorale sans autre effet secondaire représenterait une avancée déterminante dans la thérapie cancéreuse.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Folkman J. Angiogenesis: an organizing principle for drug discovery? Nat Rev Drug Discov 2007 ; 6 : 273–286. [CrossRef] [PubMed] [Google Scholar]
- Hurwitz H, Fehrenbacher L, Novotny W, et al. Bevacizumab plus irinotecan, fluorouracil, and leucovorin for metastatic colorectal cancer. N Engl J Med 2004 ; 350 : 2335–2342. [CrossRef] [PubMed] [Google Scholar]
- Al-Husein B, Abdalla M, Trepte M, et al. Antiangiogenic therapy for cancer: an update. Pharmacotherapy 2012 ; 32 : 1095–1111. [CrossRef] [PubMed] [Google Scholar]
- Carmeliet P, Jain RK. Molecular mechanisms and clinical applications of angiogenesis. Nature 2011 ; 473 : 298–307. [CrossRef] [PubMed] [Google Scholar]
- Farnsworth RH, Lackmann M, Achen MG, Stacker SA. Vascular remodeling in cancer. Oncogene 2013 ; doi : 10.1038/onc.2013.304. [Google Scholar]
- Chandel NS, Maltepe E, Goldwasser E, et al. Mitochondrial reactive oxygen species trigger hypoxia-induced transcription. Proc Natl Acad Sci USA 1998 ; 95 : 11715–11720. [CrossRef] [Google Scholar]
- Bensimon J. Le switch angiogénique ou comment réveiller les cellules tumorales dormantes. Med Sci (Paris) 2012 ; 28 : 1069–1071. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Tertil M, Jozkowicz A, Dulak J. Oxidative stress in tumor angiogenesis–therapeutic targets. Curr Pharm Des 2010 ; 16 : 3877–3894. [CrossRef] [PubMed] [Google Scholar]
- Gregory AD, Houghton AM. Tumor-associated neutrophils: new targets for cancer therapy. Cancer Res 2011 ; 71 : 2411–2416. [CrossRef] [PubMed] [Google Scholar]
- Creagan ET, Moertel CG, O’Fallon JR, et al. Failure of high-dose vitamin C (ascorbic acid) therapy to benefit patients with advanced cancer. A controlled trial. N Engl J Med 1979 ; 301 : 687–690. [CrossRef] [PubMed] [Google Scholar]
- Laleu B, Gaggini F, Orchard M, et al. First in class, potent, and orally bioavailable NADPH oxidase isoform 4 (Nox4) inhibitors for the treatment of idiopathic pulmonary fibrosis. J Med Chem 2010 ; 53 : 7715–7730. [CrossRef] [PubMed] [Google Scholar]
- Bonner MY, Arbiser JL. Targeting NADPH oxidases for the treatment of cancer and inflammation. Cell Mol Life Sci 2012 ; 69 : 2435–2442. [CrossRef] [PubMed] [Google Scholar]
- Gray SP, Di Marco E, Okabe J, et al. NADPH oxidase 1 plays a key role in diabetes mellitus-accelerated atherosclerosis. Circulation 2013 ; 127 : 1888–1902. [CrossRef] [PubMed] [Google Scholar]
- Ushio-Fukai M. Redox signaling in angiogenesis: role of NADPH oxidase. Cardiovasc Res 2006 ; 71 : 226–235. [CrossRef] [PubMed] [Google Scholar]
- Morgan MJ, Liu ZG. Crosstalk of reactive oxygen species and NF-kappaB signaling. Cell Res 2011 ; 21 : 103–115. [CrossRef] [PubMed] [Google Scholar]
- Bedard K, Krause KH. The NOX family of ROS-generating NADPH oxidases: physiology and pathophysiology. Physiol Rev 2007 ; 87 : 245–313. [CrossRef] [PubMed] [Google Scholar]
- Guichard C, Pedruzzi E, Fay M, et al. Les Nox/Duox : une nouvelle famille de NADPH oxydases. Med Sci (Paris) 2006 ; 22 : 953–959. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Lambeth JD, Kawahara T, Diebold B. Regulation of Nox and Duox enzymatic activity and expression. Free Radic Biol Med 2007 ; 43 : 319–331. [CrossRef] [PubMed] [Google Scholar]
- Lambeth JD. NOX enzymes and the biology of reactive oxygen. Nat Rev Immunol 2004 ; 4 : 181–189. [CrossRef] [PubMed] [Google Scholar]
- Gianni D, DerMardirossian C, Bokoch GM. Direct interaction between Tks proteins and the N-terminal proline-rich region (PRR) of NoxA1 mediates Nox1-dependent ROS generation. Eur J Cell Biol 2011 ; 90 : 164–171. [CrossRef] [PubMed] [Google Scholar]
- Chatterjee S, Feinstein SI, Dodia C, et al. Peroxiredoxin 6 phosphorylation and subsequent phospholipase A2 activity are required for agonist-mediated activation of NADPH oxidase in mouse pulmonary microvascular endothelium and alveolar macrophages. J Biol Chem 2011 ; 286 : 11696–11706. [CrossRef] [PubMed] [Google Scholar]
- Thakur S, Du J, Hourani S, et al. Inactivation of adenosine A2A receptor attenuates basal and angiotensin II-induced ROS production by Nox2 in endothelial cells. J Biol Chem 2010 ; 285 : 40104–40113. [CrossRef] [PubMed] [Google Scholar]
- Garrido-Urbani S, Jemelin S, Deffert C, et al. Targeting vascular NADPH oxidase 1 blocks tumor angiogenesis through a PPARalpha mediated mechanism. PLoS One 2011 ; 6 : e14665. [CrossRef] [PubMed] [Google Scholar]
- Frey RS, Ushio-Fukai M, Malik AB. NADPH oxidase-dependent signaling in endothelial cells: role in physiology and pathophysiology. Antioxid Redox Signal 2009 ; 11 : 791–810. [CrossRef] [PubMed] [Google Scholar]
- Shinohara M, Shang WH, Kubodera M, et al. Nox1 redox signaling mediates oncogenic Ras-induced disruption of stress fibers and focal adhesions by down-regulating Rho. J Biol Chem 2007 ; 282 : 17640–17648. [CrossRef] [PubMed] [Google Scholar]
- Shinohara M, Adachi Y, Mitsushita J, et al. Reactive oxygen generated by NADPH oxidase 1 (Nox1) contributes to cell invasion by regulating matrix metalloprotease-9 production and cell migration. J Biol Chem 2010 ; 285 : 4481–4488. [CrossRef] [PubMed] [Google Scholar]
- Sadok A, Bourgarel-Rey V, Gattacceca F, et al. Nox1-dependent superoxide production controls colon adenocarcinoma cell migration. Biochim Biophys Acta 2008 ; 1783 : 23–33. [CrossRef] [PubMed] [Google Scholar]
- Kobayashi S, Nojima Y, Shibuya M, Maru Y. Nox1 regulates apoptosis and potentially stimulates branching morphogenesis in sinusoidal endothelial cells. Exp Cell Res 2004 ; 300 : 455–462. [CrossRef] [PubMed] [Google Scholar]
- Chen F, Qian LH, Deng B, et al. Resveratrol protects vascular endothelial cells from high glucose-induced apoptosis through inhibition of NADPH oxidase activation-driven oxidative stress. CNS Neurosci Ther 2013 ; 19 : 675–681. [CrossRef] [PubMed] [Google Scholar]
- Ushio-Fukai M, Tang Y, Fukai T, et al. Novel role of gp91(phox)-containing NAD(P)H oxidase in vascular endothelial growth factor-induced signaling and angiogenesis. Circ Res 2002 ; 91 : 1160–1167. [CrossRef] [PubMed] [Google Scholar]
- Ikeda S, Yamaoka-Tojo M, Hilenski L, et al. IQGAP1 regulates reactive oxygen species-dependent endothelial cell migration through interacting with Nox2. Arterioscler Thromb Vasc Biol 2005 ; 25 : 2295–2300. [CrossRef] [PubMed] [Google Scholar]
- Ushio-Fukai M. VEGF signaling through NADPH oxidase-derived ROS. Antioxid Redox Signal 2007 ; 9 : 731–739. [CrossRef] [PubMed] [Google Scholar]
- Schroder K, Schutz S, Schloffel I, et al. Hepatocyte growth factor induces a proangiogenic phenotype and mobilizes endothelial progenitor cells by activating Nox2. Antioxid Redox Signal 2011 ; 15 : 915–923. [CrossRef] [PubMed] [Google Scholar]
- Ago T, Kitazono T, Ooboshi H, et al. Nox4 as the major catalytic component of an endothelial NAD(P)H oxidase. Circulation 2004 ; 109 : 227–233. [CrossRef] [PubMed] [Google Scholar]
- Bhandarkar SS, Jaconi M, Fried LE, et al. Fulvene-5 potently inhibits NADPH oxidase 4 and blocks the growth of endothelial tumors in mice. J Clin Invest 2009 ; 119 : 2359–2365. [PubMed] [Google Scholar]
- Petry A, Djordjevic T, Weitnauer M, et al. NOX2 and NOX4 mediate proliferative response in endothelial cells. Antioxid Redox Signal 2006 ; 8 : 1473–1484. [CrossRef] [PubMed] [Google Scholar]
- Mochizuki T, Furuta S, Mitsushita J, et al. Inhibition of NADPH oxidase 4 activates apoptosis via the AKT/apoptosis signal-regulating kinase 1 pathway in pancreatic cancer PANC-1 cells. Oncogene 2006 ; 25 : 3699–3707. [CrossRef] [PubMed] [Google Scholar]
- Schroder K, Zhang M, Benkhoff S, et al. Nox4 is a protective reactive oxygen species generating vascular NADPH oxidase. Circ Res 2012 ; 110 : 1217–1225. [CrossRef] [PubMed] [Google Scholar]
- Fried L, Arbiser JL. The reactive oxygen-driven tumor: relevance to melanoma. Pigment Cell Melanoma Res 2008 ; 21 : 117–122. [CrossRef] [PubMed] [Google Scholar]
- Maraldi T, Prata C, Vieceli Dalla Sega F, et al. NAD(P)H oxidase isoform Nox2 plays a prosurvival role in human leukaemia cells. Free Radic Res 2009 ; 43 : 1111–1121. [CrossRef] [PubMed] [Google Scholar]
- Peshavariya H, Dusting GJ, Jiang F, et al. NADPH oxidase isoform selective regulation of endothelial cell proliferation and survival. Naunyn Schmiedebergs Arch Pharmacol 2009 ; 380 : 193–204. [CrossRef] [PubMed] [Google Scholar]
- Azzi S, Gavard J. Vaisseaux sanguins et tumeurs ou l’art du dialogue. Med Sci (Paris) 2014 ; 30 : 408–414. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Hasmim M, Messai Y, Zaeem M, Chouaib S. L’hypoxie tumorale : un déterminant clé de la réactivité stromale et de la réponse antitumorale. Med Sci (Paris) 2014 ; 30 : 422–428. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. L’angiogenèse physiologique. A. La formation de nouveaux vaisseaux à partir d’un vaisseau préexistant quiescent est déclenchée par la stimulation exogène de facteurs de croissance (VEGF, FGF, PDGF-BB, etc.) sécrétés, par exemple, par des cellules tumorales et/ou des cellules immunitaires infiltrant une tumeur. B. Une cellule endothéliale répond au stimulus en migrant et en dégradant la matrice extracellulaire, puis elle devient une tip cell. Cette migration nécessite, en premier lieu, le détachement des péricytes pour permettre la migration des cellules endothéliales sous-jacentes. L’activation des cellules voisines de la cellule sélectionnée est inhibée par la voie de signalisation Notch/Dll4 (delta-like ligand 4), ce qui empêche la formation de plusieurs branchements émergents. C. Pour étendre le vaisseau naissant, les cellules stalk prolifèrent et migrent en suivant la tip cell. D. Pour finaliser le processus, une lumière se forme par fusion de vacuoles intracellulaires ; ensuite, des péricytes sont recrutés le long des cellules endothéliales pour stabiliser le vaisseau par sécrétion d’une matrice extracellulaire qui va former la membrane basale. Les cellules forment de nouvelles jonctions intercellulaires matures. Enfin, des signaux de quiescence, tels que Ang1 (angiopoïétine 1)/Tie2, permettent de stabiliser le nouveau vaisseau par inhibition de la prolifération. |
| Dans le texte | |
 |
Figure 2. Mécanisme d’action et structure des NAPDH oxydases. A. Les enzymes NOX catalysent le transfert d’électrons à travers la membrane plasmique en utilisant le NADPH comme donneur d’électron (e) et l’oxygène comme accepteur. Cette réaction génère l’anion superoxyde comme produit principal de réaction, et du NADP+ et des protons (H+) comme produits secondaires. B. Structure des complexes NAPDH. Les NOX contiennent six hélices α (sept pour les DUOX) transmembranaires et une queue cytoplasmique qui contient un domaine de fixation du NAPDH et du FAD. NOX-1, -2, -3 et -4 s’associent à la sous-unité membranaire p22phox. Pour NOX-1, -2 et -3, le complexe comprend, en plus, des sous-unités cytosoliques régulatrices (p67phox/NOXA1, Rac1/2, p40phox) et organisatrices (p47phox/NOXO1) essentielles pour leur activité enzymatique. L’activité catalytique des DUOX est dépendante du calcium, ce qui permet l’activation du centre catalytique enzymatique, mais également de deux sous-unités membranaires, DUOXA1/2. NOX-5 est, quant à elle, uniquement dépendante du calcium, ce qui permet l’activation de son centre catalytique. |
| Dans le texte | |
 |
Figure 3. Les NOX sont exprimées dans les différents compartiments du microenvironnement tumoral. Les tumeurs croissent en développant autour d’elles un microenvironnement constitué de plusieurs types de cellules : des cellules immunitaires, des fibroblastes, des cellules endothéliales (vasculaires et lymphatiques) et des péricytes. Ce microenvironnement contribue à la progression et à la dissémination de la tumeur. Les cellules de ce microenvironnement expriment différentes combinaisons d’isoformes de NOX qui peuvent être ciblées dans le cadre d’un protocole thérapeutique. |
| Dans le texte | |
 |
Figure 4. Les enzymes NOX jouent un rôle coordonné dans les cellules endothéliales et tumorales. A. Dans les cellules tumorales, NOX-1 peut être activée par un oncogène (K-ras) ou par des acides gras, comme l’acide arachidonique (AA). Les ERO produites en conséquence activent HIF-1α, NF-κB [26] et le renouvellement des intégrines [27], ce qui contribue, respectivement, à la migration des cellules tumorales, à la sécrétion de facteurs angiogéniques et à la prolifération des cellules tumorales. Dans les cellules endothéliales, NOX-1 est activée par Rac1 qui est elle-même activée par le VEGFR. NOX-1 sécrète des ERO qui bloquent l’activation du facteur de transcription PPAR-α, un inhibiteur de NF-κB. Les ERO produites par NOX-1 activent, par conséquent, la migration et l’invasion des cellules endothéliales [23]. B. Dans les cellules tumorales, NOX-4 contribue à la prolifération et à la survie des cellules par l’activation des voies Akt et NF-κB. NOX-4 participe également à l’angiogenèse par l’activation d’HIF-2α, qui active la production de VEGF [39]. Dans les cellules endothéliales, NOX-4, qui est exprimée au niveau du réticulum endoplasmique, sécrète des ERO qui activent les MAP kinases, ce qui promeut la prolifération des cellules endothéliales. En parallèle, NOX-4 inhibe l’apoptose par l’inhibition de la production d’eNOS [38]. NOX-4 peut être activée par l’angiotensine 2 ou par l’hypoxie. C. Dans les cellules tumorales, l’activation de NOX-2 par l’interleukine-3 (IL-3) et le VEGF participe au processus de survie des cellules, notamment dans des cellules leucémiques [40]. Dans les cellules endothéliales, NOX-2 est située dans les radeaux lipidiques et s’associe avec IQGAP1 au niveau du front migratoire des cellules endothéliales pour orienter la migration des cellules durant les processus angiogéniques [31]. Les ERO produites par NOX-2 inhibent la voie d’apoptose des caspases 3/7, ce qui contribue à la survie des cellules [41]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




