| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 226 - 230 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026024 | |
| Published online | 20 March 2026 | |
Contrôle d’identité ! Les virus Influenza détournent la synthèse du phospatidylinositol-4-phosphate pour exporter les génomes viraux
(Lip)ID, please! Influenza viruses hijack phospatidylinositol-4-phosphate synthesis to promote viral genome egress
1
Université Paris Cité, Inserm U1151, CNRS UMR8253, Institut Necker Enfants Malades, Paris, France
2
Interfaculty institute of bioengineering and global health institute, École Polytechnique Fédérale de Lausanne, Lausanne, Suisse
3
Institut Pasteur, Université Paris Cité, CNRS UMR3569, Biologie des ARN et virus Influenza, Paris, France
4
Sorbonne Université, Institut Curie, Université Paris Sciences et Lettres, CNRS UMR144, Biologie cellulaire et cancer, Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Contributions équivalentes
Les infections par les virus Influenza demeurent un enjeu majeur de santé publique par leur impact continu sur la santé humaine et animale. Chez l’Homme, ils sont responsables des épidémies récurrentes de grippe saisonnière, qui causent environ 500 000 décès annuels (Organisation mondiale de la santé, 2025). Les virus Influenza de type A, du fait de l’existence d’un réservoir animal, sont régulièrement à l’origine de l’émergence de nouveaux virus pouvant donner lieu à des zoonoses, voire à des pandémies [1]. L’un des mécanismes de leur variabilité génétique repose sur la nature segmentée de leur génome, constitué de huit molécules distinctes d’ARN viral (ARNv), chacune associée à des protéines spécifiques du virus au sein d’un complexe ribonucléoprotéique (RNP). Lorsqu’un hôte est coinfecté par un virus d’origine humaine et un virus d’origine animale, un échange de segments génomiques (réassortiment génomique) peut survenir, favorisant l’émergence de nouveaux génotypes viraux potentiellement plus virulents. La propagation mondiale, depuis 2021, de virus Influenza aviaires fortement pathogènes de sous-type H5N1, appartenant au clade 2.3.4.4b, constitue une préoccupation majeure. Ces virus, détectés sur la quasi-totalité des continents, présentent un spectre d’hôtes élargi, ce qui accroît leur potentiel zoonotique et le risque pour la santé publique [2].
Le processus de réassortiment génomique dépend des mécanismes qui contrôlent l’assemblage et le transport coordonné des RNP viraux dans la cellule, depuis leur site nucléaire de réplication jusqu’à la membrane plasmique, site du bourgeonnement des virions. La petite GTPase RAB11A, une protéine cellulaire impliquée dans le recyclage des endosomes, joue un rôle essentiel dans le transport de ces RNP vers la périphérie de la cellule [3], mais les mécanismes moléculaires de ce transport restent mal compris. Différentes études ont montré qu’au cours de l’infection, RAB11A est détournée de sa fonction canonique et perd sa capacité à interagir avec certains de ses partenaires, comme les protéines RAB11-FIP [4] ou le moteur moléculaire dynéine [5]. Les résultats d’autres études indiquent qu’au cours de l’infection, RAB11A est relocalisée à proximité de membranes du réticulum endoplasmique fortement remodelées. Elle contribue à la formation d’organelles liquides qui favorisent les interactions entre segments génomiques [6], et de structures vésiculaires atypiques recouvertes de RNP viraux (irregularly coated vesicles, ICV), qui semblent se former à partir des membranes du réticulum endoplasmique et sont également présentes à la membrane plasmique [7]. Cependant, ni les facteurs moléculaires impliqués dans la biogenèse des ICV, ni la composition des membranes du réticulum endoplasmique dont elles sont issues n’ont été élucidés.
C’est dans ce contexte que notre étude a permis de mettre au jour une machinerie cellulaire détournée par le virus et qui, en coordination avec RAB11A, modifie la composition lipidique des membranes du réticulum endoplasmique pour favoriser l’export des RNP viraux vers les sites de bourgeonnement des virions à la membrane plasmique [8].
L’infection par les virus influenza A remodèle le réticulum endoplasmique et y mobilise RAB11A pour assurer le trafic cellulaire des RNP viraux
Pour caractériser la nature des membranes du réticulum endoplasmique dont l’architecture est modifiée au cours de l’infection, nous avons analysé par immunofluorescence les feuillets (contenant la protéine CLIMP63) et les tubules1 (contenant la protéine RTN3) dans des cellules A5492, infectées ou non par le virus influenza A/WSN/33 (H1N1). Alors que les membranes du réticulum contenant RTN3 ont une distribution inchangée en cas d’infection, celles contenant CLIMP63 présentent au contraire un profil aberrant et s’étendent vers la périphérie des cellules infectées, tandis qu’elles s’accumulent dans la région périnucléaire dans les cellules non infectées (Figure 1A). Cette redistribution indique que l’infection par le virus influenza A induit une réorganisation spécifique des feuillets du réticulum endoplasmique. Nous avons ensuite évalué le rôle potentiel de la protéine RAB11A dans ce remodelage. Sa déplétion par la technique des petits ARN interférents (siRNA) ne perturbe pas le remodelage viro-induit des feuillets du réticulum endoplasmique, mais elle empêche la formation des inclusions cytoplasmiques typiques des RNP viraux, détectées par immunofluorescence en utilisant un anticorps dirigé contre la nucléoprotéine virale NP (Figure 1B). L’analyse des profils d’intensité de fluorescence indique que la déplétion de RAB11A tend même à renforcer la proximité spatiale des RNP viraux et des membranes des feuillets du réticulum endoplasmique [8]. Le fait qu’en absence de RAB11A, les RNP viraux continuent à s’associer aux membranes du réticulum endoplasmique remodelées par l’infection et s’y accumulent suggère que RAB11A est requise en aval de cette interaction, pour faciliter le transfert des RNP viraux à la membrane plasmique.
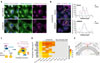 |
Figure 1 Les virus Influenza de type A remodèlent les membranes du réticulum endoplasmique et y mobilisent la GTPase RAB11A associée à une machinerie de synthèse de PI4P. A. Des cellules A549 ont été infectées ou non pendant 8 heures avec le virus A/WSN/33 (à une multiplicité d’infection de 5 PFU1/cellule), puis fixées et immunomarquées pour révéler les protéines cellulaires RTN3 (présente dans les tubules du réticulum endoplasmique et CLIMP63 (présente dans les feuillets du réticulum endoplasmique). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. B. Des cellules A549, préalablement traitées avec un petit ARN interférent (small interfering RNA, siRNA) spécifique de RAB11A (siRAB11A) ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures avec la souche A/WSN/33 du virus influenza A, puis fixées et immunomarquées pour les protéines CLIMP63 et NP (nucléoprotéine virale, un composant majeur des complexes ribonucléoprotéiques viraux). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. Les intensités de fluorescence associées ont été mesurées le long de la ligne jaune à partir du cercle, et indiquent une association plus étroite entre les feuillets du réticulum endoplasmique (CLIMP63+) et les complexes ribonucléoprotéiques viraux (NP+) en absence de RAB11A. C. RAB11A a été fusionnée à une biotine ligase (TurboID), ce qui permet de biotinyler les protéines voisines dans un rayon d’environ 10 nm. D. Identification, par spectrométrie de masse, des protéines biotinylées dans des cellules A549 produisant la protéine de fusion TurboID-RAB11A, infectées ou non par le virus A/WSN/33. Le graphique indique que les protéines liées au métabolisme des phosphoinositides (PI) ne sont identifiées que dans les cellules infectées (R1-R4 indiquent 4 répétitions indépendantes de la même expérience). E. Le phosphatidylnositol-4-phosphate (PI4P) peut être synthétisé par plusieurs voies métaboliques impliquant la phosphorylation du phosphatidylinositol (PI) par les enzymes de type kinase PI4K (incluant FAM126A), ou la déphosphorylation du phosphatidylinositol-4,5-biphosphate (PI4,5P2) par l’enzyme phosphatase INPP5K (Figure adaptée de [8]). 1 Plaque-forming unit : unité de formation de plaque, correspondant à une unité infectieuse capable de former une plage de lyse sur un tapis cellulaire. |
Le virus Influenza A détourne à son profit une machinerie de synthèse locale de PI4P au réticulum endoplasmique
Afin d’identifier les partenaires de RAB11A impliqués dans le transport des RNP viraux depuis les membranes du réticulum endoplasmique, nous avons utilisé une technique d’étiquetage de proximité à la biotine dans une lignée de cellules A549 produisant une protéine de fusion entre RAB11A et la biotine ligase TurboID, une enzyme qui permet de biotinyler de manière covalente les protéines situées à son voisinage immédiat (à une distance inférieure à 10 nm) (Figure 1C) [9]. Ces cellules ont été infectées ou non par le virus influenza A, puis mises en présence de biotine afin d’étiqueter l’interactome de RAB11A. Les protéines biotinylées ont ensuite été purifiées en utilisant des billes recouvertes de streptavidine3, puis identifiées par spectrométrie de masse4. L’analyse a révélé, dans les cellules infectées, un enrichissement en enzymes associées avec la synthèse du phosphatidylinositol-4-phosphate (PI4P), un phosphoinositide5 clé dans le contrôle du trafic vésiculaire. Parmi les protéines identifiées, figurent notamment les protéines FAM126A (hyccine) et INPP5K (inositol polyphosphate-5-phosphatase K), ainsi que la protéine autophagique ATG16L1 (autophagy-related 16-like 1), toutes trois connues pour leur contribution à la synthèse ou à la stabilisation du PI4P (Figure 1D). Ce résultat suggère que la production de PI4P est localement modulée au sein des membranes associées à RAB11A lors de l’infection virale (Figure 1E). Pour confirmer cette hypothèse, nous avons analysé la distribution intracellulaire du PI4P dans des cellules U2OS6 produisant la protéine résidente du réticulum endoplasmique Sec61ß fusionnée au fluorophore mEmerald, afin de visualiser les membranes du réticulum. Les cellules, infectées ou non, ont été fixées puis traitées avec la sonde protéique SNAP-SidC qui se lie spécifiquement au PI4P. Nous avons constaté que l’infection provoque une forte augmentation du signal SNAP-SidC, en particulier dans les membranes Sec61b+, ce qui traduit une accumulation de PI4P dans les membranes du réticulum endoplasmique (Figure 2A, 2B). De plus, nous avons montré que la déplétion des protéines FAM126A, INPP5K, ou ATG16L1 par la technique des siRNA réduit considérablement cet enrichissement des membranes du réticulum endoplasmique en PI4P induit par l’infection (Figure 2C), ce qui indique que cette « machinerie moléculaire » est nécessaire à la synthèse locale de PI4P [8].
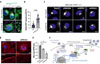 |
Figure 2 ATG16L1 orchestre la synthèse locale de PI4P au réticulum endoplasmique pour favoriser le transport des génomes viraux à la membrane plasmique. A. Des cellules U2OS produisant la protéine résidente du réticulum endoplasmique Sec61ß fusionnée à mEmerald ont été infectées ou non pendant 8 heures par le virus A/WSN/33 (à une multiplicité d’infection de 5 PFU/cellule), fixées, puis marquées à l’aide de la sonde SNAP-SidC qui se lie spécifiquement au phosphatidylnositol-4-phosphate (PI4P). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. B. Quantifications, à partir des marquages illustrés en (A), du pourcentage de points révélés par la sonde SNAP-SidC qui sont associés à la membrane du réticulum endoplasmique. On constate une augmentation viro-induite de la quantité de PI4P associée aux membranes du réticulum endoplasmique (RE). C. Des cellules A549, préalablement traitées avec un petit ARN interférent (small interfering RNA, siRNA) spécifique de l’une ou l’autre des protéines candidates (siFAM126A, siINPP5K, siATG16L1), ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées à l’aide de la sonde SNAP-SidC, qui se lie spécifiquement au PI4P. Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de FAM126A, INPP5K ou ATG16L1 inhibe l’augmentation viro-induite de PI4P. D. Des cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1) ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées pour la nucléoprotéine virale NP, afin de visualiser la localisation subcellulaire des complexes ribonucléoprotéiques viraux (RNP viraux). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de ATG16L1 réduit l’accumulation des RNP viraux à la membrane plasmique (indiquée par un trait blanc en pointillé). E. Titrage de la quantité de particules virales infectieuses présentes dans le milieu de culture de cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1), de RAB11A (siRAB11A), ou avec un siRNA témoin (Témoin), 24 heures post-infection par le virus A/WSN/33 (à une multiplicité d’infection de 0,001 PFU/cellule). La déplétion de ATG16L1 ou de RAB11A réduit la production virale d’un ou de deux log, respectivement. F. Modèle proposé. Le virus influenza A pénètre dans la cellule hôte par endocytose, et le génome viral est libéré dans le cytoplasme. Les segments génomiques viraux, sous la forme de RNP viraux, sont importés dans le noyau, où ils sont répliqués, donnant lieu à la synthèse de nouveaux RNP viraux. Ceux-ci sont exportés du noyau et s’associent aux membranes remodelées des feuillets du réticulum endoplasmique. La protéine RAB11A est recrutée au réticulum endoplasmique du fait d’une production locale de PI4P viro-induite, orchestrée par ATG16L1 et des enzymes de la voie de biosynthèse du PI4P. RAB11A favorise la biogenèse des ICV (irregularly coated vesicles), qui servent de véhicules pour le transport des RNP viraux vers la périphérie cellulaire. Parvenus à la membrane plasmique, les RNP viraux, assemblés en groupes de 8 segments génomiques distincts, sont incorporés dans les néo-virions qui bourgeonnent à partir de la membrane plasmique. Figure adaptée de [8]. |
La production de PI4P dépendante de ATG16L1 dans les membranes du réticulum endoplasmique est nécessaire au transfert des RNP viraux à la membrane plasmique
Pour évaluer l’importance du contrôle de la composition en PI4P des membranes du réticulum endoplasmique pour l’export des RNP viraux vers la membrane plasmique, nous avons analysé la localisation subcellulaire de ces RNP en absence ou en présence de siRNA dirigés contre ATG16L1. Cette protéine, connue pour stabiliser la production locale de PI4P, s’associe aux membranes du réticulum au cours de l’infection [8]. En l’absence de ces siRNA, après 8 heures d’infection par le virus influenza A, les RNP viraux forment, comme attendu, des inclusions cytoplasmiques, et s’accumulent à la membrane plasmique, siège du bourgeonnement des virions. En revanche, l’extinction de ATG16L1 par les siRNA entraîne l’accumulation des RNP viraux dans le cytoplasme et leur quasi-absence à la membrane plasmique (Figure 2D). Ce résultat, ainsi qu’un résultat similaire obtenu en utilisant un inhibiteur pharmacologique de la synthèse de PI4P (GSK-A1), indiquent que l’augmentation de la production de PI4P dans les membranes du réticulum endoplasmique favorisée par ATG16L1 au cours de l’infection est nécessaire pour l’export des RNP viraux du cytoplasme vers la périphérie cellulaire. De plus, nous avons confirmé que la suppression de ATG16L1 ou de RAB11A par la technique des siRNA réduit considérablement la quantité de particules virales infectieuses sécrétées dans le milieu extracellulaire (Figure 2E) [8].
Perspectives
La combinaison de méthodes d’étiquetage de proximité à la biotine et d’imagerie de haute résolution dans des cellules infectées par un virus influenza A a permis de révéler l’existence d’un programme viro-induit de synthèse locale de PI4P dans les membranes du réticulum endoplasmique. Le détournement d’une « machinerie cellulaire » permettant de produire localement PI4P, et notamment de la protéine ATG16L1, s’avère essentiel pour assurer le transport des segments génomiques viraux jusqu’à la membrane plasmique, et, de ce fait, pour la production des particules virales infectieuses. Nous proposons que l’enrichissement en PI4P amorce une signalisation intracellulaire permettant le recrutement de RAB11A, et favorise ainsi la biogenèse des ICV, qui servent de véhicules pour l’export des génomes viraux (Figure 2F). Dans cette perspective, les inhibiteurs de la synthèse des phosphoinositides, et plus spécifiquement du PI4P, apparaissent comme des candidats prometteurs pour le développement d’approches antivirales, seuls ou en combinaison avec d’autres thérapies ciblant différentes étapes du cycle viral. Nos résultats confirment le rôle central du réticulum endoplasmique, véritable plateforme membranaire détournée non seulement par le virus influenza A, mais aussi par de nombreux autres virus [10]. Ils étendent également au virus influenza A la capacité de moduler l’identité des endomembranes pour favoriser son cycle de réplication. Enfin, ils renforcent l’idée que les protéines « de l’autophagie » représentent une cible privilégiée du virus influenza A pour assurer le transport du génome viral [11], et ce indépendamment de la voie canonique de l’autophagie. Ils s’inscrivent ainsi dans le concept émergent selon lequel les protéines de l’autophagie sont impliquées dans d’autres fonctions cellulaires, en particulier dans le contrôle du trafic membranaire.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Krammer F, Smith GJD, Fouchier RAM, et al. Influenza. Nat Rev Dis Primers 2018 ; 4 : 3. [CrossRef] [PubMed] [Google Scholar]
- Capelastegui F, Goldhill DH. H5N1 2.3.4.4b: a review of mammalian adaptations and risk of pandemic emergence. J Genl Virol 2025 ; 106. [Google Scholar]
- Amorim MJ. A comprehensive review on the interaction between the host GTPase Rab 11 and Influenza A virus. Front Cell Dev Biol 2019 ; 6 : 176. [CrossRef] [PubMed] [Google Scholar]
- Vale-Costa S, Alenquer M, Sousa AL, et al. Influenza A virus ribonucleoproteins modulate host recycling by competing with Rab 11 effectors. J Cell Sci 2016 ; 129 : 1697–710. [Google Scholar]
- Bhagwat AR, Le Sage V, Nturibi E, et al. Quantitative live cell imaging reveals influenza virus manipulation of Rab 11A transport through reduced dynein association. Nat Commun 2020 ; 11 : 23. [Google Scholar]
- Alenquer M, Vale-Costa S, Etibor TA, et al. Influenza A virus ribonucleoproteins form liquid organelles at endoplasmic reticulum exit sites. Nat Commun 2019 ; 10 : 1629. [Google Scholar]
- De Castro Martin IF, Fournier G, Sachse M, et al. Influenza virus genome reaches the plasma membrane via a modified endoplasmic reticulum and Rab11-dependent vesicles. Nat Commun 2017 ; 8 : 1396. [CrossRef] [PubMed] [Google Scholar]
- Alemany C, Da Graça J, Giai Gianetto Q, et al. Influenza A virus induces PI 4P production at the endoplasmic reticulum in an ATG16L1-dependent manner to promote the egress of viral ribonucleoproteins. PLoS Biol 2025 ; 23 : e3002958. [Google Scholar]
- Cho KF, Branon TC, Udeshi ND, et al. Proximity labeling in mammalian cells with TurboID and split-TurboID. Nat Protoc 2020 ; 15 : 3971–99. [Google Scholar]
- Bare Y, Defourny K, Bretou M, et al. The endoplasmic reticulum as a cradle for virus and extracellular vesicle secretion. Trends Cell Biol 2025 ; 35 : 282–93. [Google Scholar]
- Vale-Costa S, Etibor TA, Brás D, et al. ATG9A regulates the dissociation of recycling endosomes from microtubules to form liquid influenza A virus inclusions. PLoS Biol 2023 ; 21 : e3002290. [Google Scholar]
Le réticulum endoplasmique est un continuum membranaire organisé en deux structures architecturales distinctes : les feuillets et les tubules. Les feuillets, localisés à proximité du noyau, sont plats et le plus souvent associés aux ribosomes (organites responsables de la synthèse des protéines). Les tubules sont des structures périphériques courbées et lisses, qui forment des sites de contact avec les autres organites de la cellule.
Lignée cellulaire dérivée d’un adénocarcinome pulmonaire humain.
La biotine se lie à la streptavidine avec une très forte affinité.
Cette technique permet d’identifier et de quantifier des molécules en mesurant le rapport masse/charge de leurs ions. Elle est fréquemment utilisée pour identifier les protéines.
Les phosphoinositides sont des lipides membranaires dérivés du phosphatidylinositol (PI), dont le cycle inositol peut être phosphorylé sur une ou plusieurs positions spécifiques, ce qui produit différentes espèces moléculaires de fonctions et localisations distinctes.
Lignée cellulaire dérivée d’un ostéosarcome humain.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Les virus Influenza de type A remodèlent les membranes du réticulum endoplasmique et y mobilisent la GTPase RAB11A associée à une machinerie de synthèse de PI4P. A. Des cellules A549 ont été infectées ou non pendant 8 heures avec le virus A/WSN/33 (à une multiplicité d’infection de 5 PFU1/cellule), puis fixées et immunomarquées pour révéler les protéines cellulaires RTN3 (présente dans les tubules du réticulum endoplasmique et CLIMP63 (présente dans les feuillets du réticulum endoplasmique). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. B. Des cellules A549, préalablement traitées avec un petit ARN interférent (small interfering RNA, siRNA) spécifique de RAB11A (siRAB11A) ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures avec la souche A/WSN/33 du virus influenza A, puis fixées et immunomarquées pour les protéines CLIMP63 et NP (nucléoprotéine virale, un composant majeur des complexes ribonucléoprotéiques viraux). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. Les intensités de fluorescence associées ont été mesurées le long de la ligne jaune à partir du cercle, et indiquent une association plus étroite entre les feuillets du réticulum endoplasmique (CLIMP63+) et les complexes ribonucléoprotéiques viraux (NP+) en absence de RAB11A. C. RAB11A a été fusionnée à une biotine ligase (TurboID), ce qui permet de biotinyler les protéines voisines dans un rayon d’environ 10 nm. D. Identification, par spectrométrie de masse, des protéines biotinylées dans des cellules A549 produisant la protéine de fusion TurboID-RAB11A, infectées ou non par le virus A/WSN/33. Le graphique indique que les protéines liées au métabolisme des phosphoinositides (PI) ne sont identifiées que dans les cellules infectées (R1-R4 indiquent 4 répétitions indépendantes de la même expérience). E. Le phosphatidylnositol-4-phosphate (PI4P) peut être synthétisé par plusieurs voies métaboliques impliquant la phosphorylation du phosphatidylinositol (PI) par les enzymes de type kinase PI4K (incluant FAM126A), ou la déphosphorylation du phosphatidylinositol-4,5-biphosphate (PI4,5P2) par l’enzyme phosphatase INPP5K (Figure adaptée de [8]). 1 Plaque-forming unit : unité de formation de plaque, correspondant à une unité infectieuse capable de former une plage de lyse sur un tapis cellulaire. |
| Dans le texte | |
 |
Figure 2 ATG16L1 orchestre la synthèse locale de PI4P au réticulum endoplasmique pour favoriser le transport des génomes viraux à la membrane plasmique. A. Des cellules U2OS produisant la protéine résidente du réticulum endoplasmique Sec61ß fusionnée à mEmerald ont été infectées ou non pendant 8 heures par le virus A/WSN/33 (à une multiplicité d’infection de 5 PFU/cellule), fixées, puis marquées à l’aide de la sonde SNAP-SidC qui se lie spécifiquement au phosphatidylnositol-4-phosphate (PI4P). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. B. Quantifications, à partir des marquages illustrés en (A), du pourcentage de points révélés par la sonde SNAP-SidC qui sont associés à la membrane du réticulum endoplasmique. On constate une augmentation viro-induite de la quantité de PI4P associée aux membranes du réticulum endoplasmique (RE). C. Des cellules A549, préalablement traitées avec un petit ARN interférent (small interfering RNA, siRNA) spécifique de l’une ou l’autre des protéines candidates (siFAM126A, siINPP5K, siATG16L1), ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées à l’aide de la sonde SNAP-SidC, qui se lie spécifiquement au PI4P. Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de FAM126A, INPP5K ou ATG16L1 inhibe l’augmentation viro-induite de PI4P. D. Des cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1) ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées pour la nucléoprotéine virale NP, afin de visualiser la localisation subcellulaire des complexes ribonucléoprotéiques viraux (RNP viraux). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de ATG16L1 réduit l’accumulation des RNP viraux à la membrane plasmique (indiquée par un trait blanc en pointillé). E. Titrage de la quantité de particules virales infectieuses présentes dans le milieu de culture de cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1), de RAB11A (siRAB11A), ou avec un siRNA témoin (Témoin), 24 heures post-infection par le virus A/WSN/33 (à une multiplicité d’infection de 0,001 PFU/cellule). La déplétion de ATG16L1 ou de RAB11A réduit la production virale d’un ou de deux log, respectivement. F. Modèle proposé. Le virus influenza A pénètre dans la cellule hôte par endocytose, et le génome viral est libéré dans le cytoplasme. Les segments génomiques viraux, sous la forme de RNP viraux, sont importés dans le noyau, où ils sont répliqués, donnant lieu à la synthèse de nouveaux RNP viraux. Ceux-ci sont exportés du noyau et s’associent aux membranes remodelées des feuillets du réticulum endoplasmique. La protéine RAB11A est recrutée au réticulum endoplasmique du fait d’une production locale de PI4P viro-induite, orchestrée par ATG16L1 et des enzymes de la voie de biosynthèse du PI4P. RAB11A favorise la biogenèse des ICV (irregularly coated vesicles), qui servent de véhicules pour le transport des RNP viraux vers la périphérie cellulaire. Parvenus à la membrane plasmique, les RNP viraux, assemblés en groupes de 8 segments génomiques distincts, sont incorporés dans les néo-virions qui bourgeonnent à partir de la membrane plasmique. Figure adaptée de [8]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




