Figure 2
Télécharger l'image originale
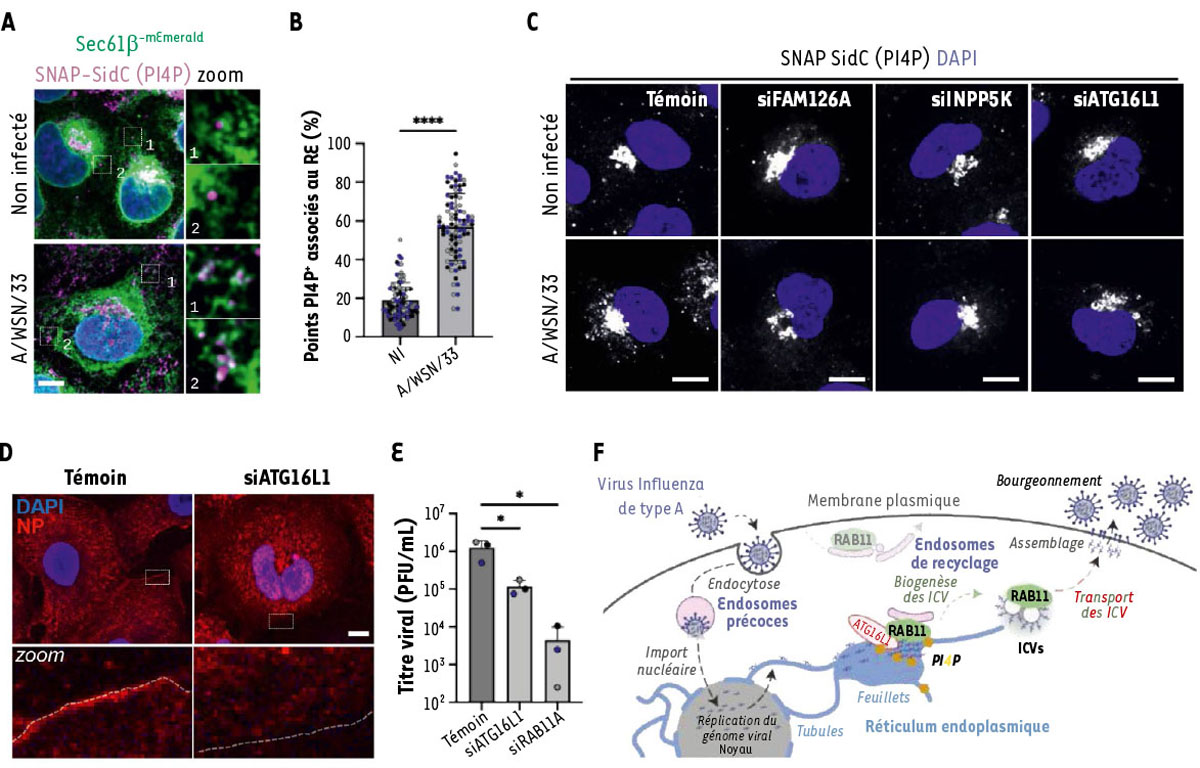
ATG16L1 orchestre la synthèse locale de PI4P au réticulum endoplasmique pour favoriser le transport des génomes viraux à la membrane plasmique. A. Des cellules U2OS produisant la protéine résidente du réticulum endoplasmique Sec61ß fusionnée à mEmerald ont été infectées ou non pendant 8 heures par le virus A/WSN/33 (à une multiplicité d’infection de 5 PFU/cellule), fixées, puis marquées à l’aide de la sonde SNAP-SidC qui se lie spécifiquement au phosphatidylnositol-4-phosphate (PI4P). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. B. Quantifications, à partir des marquages illustrés en (A), du pourcentage de points révélés par la sonde SNAP-SidC qui sont associés à la membrane du réticulum endoplasmique. On constate une augmentation viro-induite de la quantité de PI4P associée aux membranes du réticulum endoplasmique (RE). C. Des cellules A549, préalablement traitées avec un petit ARN interférent (small interfering RNA, siRNA) spécifique de l’une ou l’autre des protéines candidates (siFAM126A, siINPP5K, siATG16L1), ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées à l’aide de la sonde SNAP-SidC, qui se lie spécifiquement au PI4P. Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de FAM126A, INPP5K ou ATG16L1 inhibe l’augmentation viro-induite de PI4P. D. Des cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1) ou avec un siRNA témoin (Témoin), ont été infectées ou non pendant 8 heures, puis fixées et marquées pour la nucléoprotéine virale NP, afin de visualiser la localisation subcellulaire des complexes ribonucléoprotéiques viraux (RNP viraux). Les noyaux ont été marqués par le DAPI (en bleu). Barre d’échelle : 10 µm. La déplétion de ATG16L1 réduit l’accumulation des RNP viraux à la membrane plasmique (indiquée par un trait blanc en pointillé). E. Titrage de la quantité de particules virales infectieuses présentes dans le milieu de culture de cellules A549, préalablement traitées avec un siRNA spécifique de ATG16L1 (siATG16L1), de RAB11A (siRAB11A), ou avec un siRNA témoin (Témoin), 24 heures post-infection par le virus A/WSN/33 (à une multiplicité d’infection de 0,001 PFU/cellule). La déplétion de ATG16L1 ou de RAB11A réduit la production virale d’un ou de deux log, respectivement. F. Modèle proposé. Le virus influenza A pénètre dans la cellule hôte par endocytose, et le génome viral est libéré dans le cytoplasme. Les segments génomiques viraux, sous la forme de RNP viraux, sont importés dans le noyau, où ils sont répliqués, donnant lieu à la synthèse de nouveaux RNP viraux. Ceux-ci sont exportés du noyau et s’associent aux membranes remodelées des feuillets du réticulum endoplasmique. La protéine RAB11A est recrutée au réticulum endoplasmique du fait d’une production locale de PI4P viro-induite, orchestrée par ATG16L1 et des enzymes de la voie de biosynthèse du PI4P. RAB11A favorise la biogenèse des ICV (irregularly coated vesicles), qui servent de véhicules pour le transport des RNP viraux vers la périphérie cellulaire. Parvenus à la membrane plasmique, les RNP viraux, assemblés en groupes de 8 segments génomiques distincts, sont incorporés dans les néo-virions qui bourgeonnent à partir de la membrane plasmique. Figure adaptée de [8].
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




