| Issue |
Med Sci (Paris)
Volume 40, Number 5, Mai 2024
|
|
|---|---|---|
| Page(s) | 421 - 427 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2024046 | |
| Published online | 31 May 2024 | |
Effets de la 2′-O-méthylation de l’ARN génomique du VIH-1 sur la réplication virale
How do 2′-O-methylations within Human Immunodeficiency Virus type 1 (HIV-1) genome regulate its replication?
1
AFMB (Architecture et fonction des macromolécules biologiques), UMR 7257 - CNRS / Université Aix-Marseille, Marseille, France
2
IRIM (Institut de recherche en infectiologie de Montpellier), UMR 9004 - CNRS / Université de Montpellier, Montpellier, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Les ARN du virus de l’immunodéficience humaine sont décorés par des marques épitranscriptomiques, dont des 2′-O-méthylations internes. Ces marques ajoutées par une enzyme cellulaire, FTSJ3, sont des marqueurs du « soi ». Elles ont des effets proviraux en protégeant l’ARN viral de la détection par le senseur de l’immunité innée MDA5, et en limitant sa dégradation par l’exonucléase cellulaire ISG20, induite par l’interféron. Ces méthylations ont également un effet antiviral, dans la mesure où elles perturbent la rétrotranscription du génome ARN du virus, in vitro et dans des cellules quiescentes. Un équilibre subtil existe donc entre les effets proviraux et antiviraux des 2′-O-méthylations, assurant ainsi une réplication optimale du virus. Ces découvertes ouvrent des perspectives d’optimisation des ARN thérapeutiques à effet antiviral, par la méthylation sélective de certains nucléotides.
Abstract
The genomic RNA of HIV-1 is modified by epitranscriptomic modifications, including 2′-O-methylations, which are found on 17 internal positions. These methylations are added by the cellular methyltransferase FTSJ3, and have pro-viral effects, since they shield the viral genome from the detection by the innate immune sensor MDA5. In turn, the production of interferons by infected cells is reduced, limiting the expression of interferon-stimulated genes (ISGs) with antiviral activities. Moreover, 2′-O-methylations protect the HIV-1 genome from its degradation by ISG20, an interferon-induced exonuclease. Conversely, these methylations also exhibit antiviral effects, as they impede reverse-transcription in vitro or in quiescent cells, which are known to contain low nucleotide concentrations. Altogether, these observations suggest a balance between the proviral effect of 2′-O-methylations, related to the protection of the viral genome from detection by MDA5 and degradation by ISG20, and the antiviral effect, associated with the negative impact of 2′-O-methylations on the viral replication. These findings pave the way for further optimization of therapeutic RNA, by selective methylation of specific nucleotides.
© 2024 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Vignette (© Étienne Decroly).
L’ARN génomique du VIH-1 présente des modifications épitranscriptomiques
Les ARN sont des molécules clés du vivant qui présentent une vaste diversité de structures (tige boucle, boucle multiple, hernie, simple ou double brin, etc.) et de fonctions. Ils sont impliqués dans de nombreux processus biologiques, tels que l’expression et la régulation des gènes (ARN messager, ARN interférant), la traduction (ARN ribosomique, ARN de transfert) et des activités enzymatiques (ribozyme). Les ARN sont également le support de l’information génétique de certains virus, comme c’est le cas pour le virus de l’immunodéficience humaine de type 1 (VIH-1).
Longtemps considérés comme des copies transitoires de l’ADN, nécessaires à la production de protéines, les ARN messagers (ARNm) sont en réalité des molécules extrêmement complexes, modifiées de façon dynamique par de nombreuses marques post-transcriptionnelles, également appelées marques épitranscriptomiques [1, 24] (→).
(→) Voir Le mot de la science d’Anna Salvetti, m/s n° 3, mars 2024, page 287
Historiquement, ces marques n’avaient été observées que sur des ARN non codants abondants dans les cellules, tels que les ARN ribosomiques ou les ARN de transfert. C’est grâce au récent développement de nouvelles techniques d’analyses moléculaires qu’a été révélé le caractère abondant et ubiquitaire de ces modifications, qui concernent aussi bien les ARNm cellulaires [2] que les ARN viraux (ARNv) [3]. Ce nouveau degré de complexité révolutionne aujourd’hui notre compréhension du monde des ARN, et questionne quant au rôle régulateur des marques épitranscriptomiques dans les fonctions biologiques de ces molécules.
Les marques épitranscriptomiques sont des modifications biochimiques des nucléotides incorporés au sein des molécules d’ARN. À ce jour, plus de 150 modifications nucléotidiques différentes ont été identifiées [1], incluant des processus aussi divers que l’ajout d’une structure coiffe à l’extrémité 5′ des ARN, des modifications de la base des ribonucléotides, comme la désamination, ou la décoration des nucléotides sur des positions variées par des groupements chimiques, comme les acétyles ou les méthyles (Figure 1). La spectrométrie de masse et le développement de nouveaux outils fondés sur l’utilisation de méthodes de séquençage ont révélé l’abondance des N6-méthyladénosines (m6A, méthylation en position 6 de l’adénosine) sur les ARN du VIH [4], et la présence de N5-méthylcytosines (m5C, méthylation en position 5 de la cytosine) [5], d’inosines (I) [6,7], et de 2′-O-méthylations (Nm, N représentant un nucléotide) [5,8]. La 2′-O-méthylation, qui fait l’objet de cet article, consiste en l’ajout d’un groupe méthyl lié de façon covalente à l’oxygène en position 2′ du ribose des nucléotides de l’ARN. Cette marque est ajoutée par des 2′-O-méthyltransférases (2′-O-MTases). Contrairement aux m6A, dont la synthèse et l’excision sont très dynamiques, les Nm sont des modifications stables de l’ARN. Les Nm sont ubiquitaires : elles sont présentes sur tous types d’ARN, et dans tous les règnes du vivant. Chez les métazoaires, les Nm décorent le premier et parfois le second nucléotide de la structure coiffe à l’extrémité 5′ des ARNm. Ces méthylations spécifiques sont assurées post-transcriptionnellement par les 2′-O-MTases de la coiffe, CMTR1 (cap methyltransferase 1) et CMTR2 (cap methyltransferase 2) [9], lors de la synthèse de l’ARNm réalisée par l’ARN-polymérase II (ARN pol II). Les Nm sont également observées sur des positions internes de l’ARN, déposées co-transcriptionnellement dans le noyau, par des 2′-O-MTases cellulaires, comme la Fibrillarine (FBL), une protéine nucléolaire associée à l’ARN, ou la méthyltransférase FTSJ3 (FtsJ RNA 2′-O-methyltransferase 3), chez l’être humain.
 |
Figure 1. Illustrations de quelques modifications épitranscriptomiques fréquemment retrouvées sur les ARNm des métazoaires ou sur les ARNv. Molécules extraites de la base de données MODOMICS [1]. |
L’importance de la structure coiffe 2′-O-méthylée des ARNv
Les ARN génomiques du virus VIH-1 sont décorés par l’ajout de structure coiffe à leur extrémité 5′. La synthèse de cette structure dépend d’enzymes cellulaires recrutées par l’ARN pol II qui assure la transcription des ARN viraux [10]. En effet, lorsque les ARN viraux sont synthétisés, l’ARN pol II recrute, via son extrémité carboxy-terminale (CTD, carboxy-terminal domain), un complexe multi-protéique de coiffage, constitué d’une triphosphatase, d’une guanylyltransférase et de la N7-MTase (RNA N7-methyltransferase), responsable du transfert du méthyl en position 7 de la base [9]. Ce complexe assure le transfert d’une molécule de GDP (guanosine-5′-diphosphate), liée par une liaison 5′-5′ triphosphate à l’extrémité des ARN. Les structures coiffe sont ensuite N7-méthylées (coiffe m7GpppNp-ARN que l’on nomme « coiffe 0 »), avant l’export des ARN viraux du noyau vers le cytoplasme cellulaire. Certains ARN du VIH-1 subissent des méthylations supplémentaires, appelées 2,2,7-triméthylguanosines (TMG), au niveau de la guanosine de la coiffe [11]. Tous les ARN viraux sont ensuite exportés vers le cytoplasme de la cellule où la 2′-O-MTase cellulaire CMTR1 les prend en charge afin d’assurer la 2′-O-méthylation du ribose du premier nucléotide (m7GpppNmp-ARN), modifiant la « coiffe 0 » en « coiffe 1 » [12].
Bien que le rôle des TMG dans le cycle de réplication du VIH-1 reste mal compris, la présence de la structure coiffe à l’extrémité 5′ des ARN viraux (ARNv) joue un rôle essentiel dans la réplication virale. Outre la protection des ARNv contre la dégradation par les 5′-exonucléases cellulaires, la coiffe permet leur recrutement au niveau des ribosomes par la protéine EIF4E (eukaryotic initiation factor 4E), assurant ainsi leur traduction en protéines virales [13]. Le rôle joué par les 2′-O-méthylations de la coiffe a été élucidé en comparant la réplication de virus (coronavirus et flavivirus) dont l’activité de leur propre 2′-O-MTase avait été mutée ou non [14,15]. Ce type de méthylation, qui a récemment été identifié comme un marqueur du soi, assure le camouflage des ARNv, les rendant indiscernables des ARN cellulaires. En effet, l’extrémité 5′ des ARNm mal coiffés (non 2′-O-méthylés) est détectée par RIG-I (retinoic acid-inducible gene I) [16], un senseur cytoplasmique de l’immunité innée, de la famille des hélicases. La liaison de RIG-I aux ARNm mal coiffés induit, après une cascade d’événements intracellulaires, la production des interférons de type I (IFN-I)1. Les IFN-I ainsi produits diffusent localement, et induisent, par voies autocrine et paracrine, la synthèse de centaines de gènes spécifiques, les ISG (interferon-stimulated genes). Certains produits de ces ISG sont capables d’inhiber directement la réplication virale, à l’instar des protéines IFIT (interferon-induced proteins with tetratricopeptide repeats), qui reconnaissent et séquestrent les ARN viraux mal coiffés qui ne seront pas traduits en protéines, ce qui limitera considérablement la réplication virale [17,18].
En résumé, les cellules disposent ainsi d’un système de détection spécifique des ARN mal coiffés par RIG-I, couplé à un mécanisme de signalement local de l’infection, qui résulte dans la synthèse de facteurs de restrictions, comme les IFIT, qui assurent la défense cellulaire en limitant la traduction des ARNv (Figure 2).
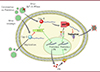 |
Figure 2. Mécanismes de détection des ARNv mal coiffés par RIG-I et de restriction par les protéines IFIT. Certains virus à ARN sont connus pour produire des ARNv coiffés et méthylés sur le premier nucléotide (Cap-1) grâce à leur propre 2′-O-MTase. Ces ARNv ne sont pas reconnus par le senseur de l’immunité innée RIG-I. Ces virus se répliquent ainsi dans le cytoplasme sans stimuler la production d’IFN, et de protéines IFIT. Lorsque ces mêmes virus sont mutés et n’ont pas de 2′-O-MTase (∆2′-O-MTase), les ARNv produits dans le cytoplasme cellulaires et non méthylés sur le premier nucléotide (Cap-0) sont détectés par RIG-I, qui induit une cascade d’événements conduisant à la production d’IFN-I. L’IFN-I se fixe sur son récepteur IFNAR qui induit la voie de signalisation JAK/STAT conduisant à l’expression de centaines d’ISG. Parmi les ISG, les protéines IFIT sont capables de reconnaître les ARN mal coiffés (Cap-0) et bloquent leur traduction en protéines virales. (Figure partiellement réalisée à partir d’images Servier Medical Art, sous licence Creative Commons Attribution 3.0 Unported License - https://creativecommons.org/licenses/by/3.0/). |
Le génome du VIH-1 est 2′-O-méthylé par une enzyme cellulaire, limitant la détection du virus par la cellule
Des 2′-O-méthylations additionnelles ont récemment été identifiées sur le génome du VIH-1 par RiboMeth-seq2 [8] et spectrométrie de masse [5]. Or, dans la mesure où le VIH-1 ne code pas de 2′-O-MTase dans son génome, ces méthylations indiquent l’activité d’une 2′-O-MTase cellulaire. Des expériences de co-immunoprécipitation ont permis d’identifier la 2′-O-MTase cellulaire FTSJ3 (FtsJ RNA 2′-O-methyltransferase 3) et de mettre en évidence son recrutement par le facteur cellulaire TRBP (TAR RNA binding protein), connu pour interagir avec les ARN du VIH [8]. En comparant la méthylation du génome viral dans des cellules sauvages ou des cellules dépourvues de la méthyltransférase (∆FTSJ3), il a été montré que FTSJ3 était responsable de la méthylation d’au moins 17 sites internes du génome du VIH-1. Ces 2′-O-méthylations concernent préférentiellement des adénosines et des uridines (Figure 3A).
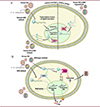 |
Figure 3. Mécanismes de détection par MDA5 des ARNv ne contenant pas de 2′-O-méthylations internes, et restriction par la nucléase ISG20. A. Lors de l’infection de cellules sauvages par le VIH, la transcription inverse du génome ARN méthylé débute simultanément avec le transit de la capside, du cytoplasme jusqu’au noyau. Le génome rétrotranscrit en ADN est intégré au génome de la cellule hôte avant d’être transcrit par l’ARN pol II. La 2′-O-MTase cellulaire FTSJ3 est recrutée au niveau du site de transcription des ARNv du VIH-1, et induit la méthylation du génome viral sur au moins 17 positions conservées. Les ARN génomiques sont encapsidés dans les nouveaux virions. Dans des cellules ∆FTSJ3, les ARNv produits et encapsidés dans les virions néosynthétisés sont en revanche hypo-méthylés. B..Lors de l’infection d’une cellule par des virions dont le génome ARN est normalement méthylé, les ARNv ne sont pas efficacement détectés par le senseur de l’immunité innée MDA5. La production d’IFN-I n’est donc pas stimulée. En revanche, les virions produits par les cellules ∆FTSJ3 produisent des ARNv hypo-méthylés, qui sont détectés par MDA5. MDA5 induit une cascade d’événements conduisant à une production d’IFN-I. Les IFN-I se fixent sur aux récepteurs IFNAR, qui déclenchent la voie de signalisation JAK/STAT conduisant à l’expression de centaines d’ISG. Parmi les ISG, l’exonucléase ISG20 dégrade les ARN hypo-méthylés, qui ne seront pas traduits, ce qui inhibe la réplication virale. (Figure partiellement réalisée à partir d’images Servier Medical Art, sous licence Creative Commons Attribution 3.0 Unported License - https://creativecommons.org/licenses/by/3.0/). |
Un point majeur de cette étude a été l’analyse des effets immunomodulateurs des 2′-O-méthylations identifiées au sein du génome viral. Des virions sauvages ou hypo-méthylés ont été produits en infectant des cellules sauvages ou des cellules ∆FTSJ3 afin d’étudier les conséquences de ces méthylations sur l’induction de la réponse antivirale. La transfection d’une lignée monocytaire par les ARN de ces virus a montré que les ARN viraux hypo-méthylés induisent fortement l’expression des interférons de type I, IFN-α et IFN-β, en comparaison avec des ARN viraux produits par des cellules sauvages. Ces observations ont ensuite été confirmées par des expériences d’infection avec des virus produits par ces mêmes cellules (sauvages ou ∆FTSJ3), et il a été possible de démontrer le rôle clé du senseur de l’immunité innée MDA5 (melanoma differentiation-associated protein 5) dans l’induction de la réponse IFN liée à la détection des génomes viraux hypométhylés. Cette étude démontrait ainsi que la réduction du niveau de 2′-O-méthylation du génome du VIH-1 induit l’activation du système immunitaire inné, confirmant que les 2′-O-méthylations sont des marqueurs du soi, et que leur absence est détectée par le senseur MDA5 (Figure 3B).
Les 2′-O-méthylations protègent le génome viral de la dégradation par ISG20
Lorsqu’un senseur protéique détecte des motifs étrangers liés à une infection par un agent pathogène, il induit généralement, en aval, l’expression de facteurs de restriction spécifiques du motif détecté. Comme expliqué précédemment, dans le cas du senseur RIG-I, qui détecte l’absence de méthylation Nm sur la structure coiffe, la restriction spécifique est liée à l’expression des protéines IFIT capables de séquestrer les ARN mal coiffés. Un facteur de restriction relié au senseur MDA5, qui discrimine les ARN qui ne portent pas de Nm internes, a donc été recherché, avec un intérêt particulier pour l’exonucléase ISG20 (interferon-stimulated gene 20 kDa protein), une exonucléase 3′-5′ induite par l’IFN-α, capable d’inhiber la réplication de nombreux virus à ARN, dont le VIH-1 [19, 25, 26] (→).
(→) Voir les Nouvelles de N. Rousseaux et L. Andrieux, m/s n° 11, novembre 2021, page 1070, et de B. Chardès et al., m/s n° 5, mai 2018, page 388
L’effet des méthylations Nm sur l’activité d’hydrolyse de l’ARNv par ISG20 a été étudié in vitro [20]. Les ARNv non méthylés sont efficacement dégradés par ISG20. En revanche, la dégradation de l’ARN 2′-O-méthylé s’interrompt deux nucléotides en amont du résidu méthylé, ainsi qu’au niveau du résidu lui-même. Des analyses structure-fonction ont permis de comprendre les mécanismes moléculaires responsables de l’arrêt de l’hydrolyse en présence de 2′-O-méthylations : l’inhibition de l’activité enzymatique est liée à un conflit stérique entre les résidus R53 (arginine en position 53 de la séquence protéique) et D90 (aspartate en position 90) d’ISG20 et le nucléotide 2′-O-méthylé de l’ARNv. Les génomes du VIH-1 hypo-méthylés produits dans des cellules ∆FTSJ3 sont ainsi davantage dégradés par l’ISG20, en comparaison avec des ARNv produits dans des cellules sauvages. De même, l’infectivité du VIH-1 portant un génome hypométhylé est altérée dans les lymphocytes T surexprimant l’ISG20 en réponse à un traitement par l’IFN. L’ensemble de ces expériences montrent que la restriction de la réplication virale médiée par l’ISG20 est contrecarrée par la capacité du virus à recruter FTSJ3 afin d’assurer la 2′-O-méthylation de son génome (Figure 3B).
L’ISG20 est donc un facteur de restriction associé à la détection d’ARNv exogène par le senseur de l’immunité innée MDA5. Les 2′-O-méthylations du génome du VIH-1, qui limitent la détection du virus par RIG-I et MDA5 et empêchent la restriction par les protéines IFIT et ISG20, ont ainsi des effets proviraux (Figures 2, 3).
Les 2′-O-méthylations altèrent la rétrotranscription du génome viral
Bien que le rôle proviral de la 2′-O-méthylation ait été clairement établi, l’impact de cette marque épitranscriptomique sur d’autres étapes de la réplication virale restait à déterminer. Le processus de transcription inverse est une étape précoce et majeure du cycle réplicatif du virus, au cours de laquelle la polymérase du virus (RT) recopie le génome viral ARN en ADN qui sera ensuite intégré au génome de la cellule hôte [21]. Il avait été précédemment documenté que, en présence de basses concentrations en nucléotides, les polymérases d’autres rétrovirus (virus de la leucémie murine de Moloney [MMLV], virus de la myéloblastose aviaire [AMV]) marquent des pauses avant le site 2′-O-méthylé [22]. Néanmoins, aucune information n’était disponible au sujet de la RT du VIH.
La capacité de la RT du virus VIH-1 à rétrotranscrire in vitro des ARN synthétiques, méthylés ou non, a donc été examinée. Des expériences d’extension d’amorces d’ADN sur des matrices d’ARN, 2′-O-méthylées ou non, ont permis de révéler que, comme dans le cas des polymérases des autres rétrovirus, la RT du VIH-1 effectue une pause avant le nucléotide méthylé. L’inhibition de la rétrotranscription est particulièrement marquée lorsque la concentration en nucléotides est faible, alors qu’en présence de concentrations élevées en nucléotides, la RT est capable de rétrotranscrire efficacement les ARN méthylés. Des analyses cinétiques ont permis d’expliquer ce phénomène, d’une part par une diminution de l’affinité du nucléotide à incorporer en face d’un site méthylé et, d’autre part, par une altération de l’étape de translocation de la RT sur la matrice d’ARN, qui est défavorisée en présence d’une 2′-O-méthylation. Une modélisation structurale de la matrice d’ARN méthylée dans le site actif de la polymérase révèle une gêne stérique et un environnement polaire non favorable à la présence de cette modification de l’ARN. Enfin, la génération de nombreux mutants de la polymérase du VIH-1 a permis d’identifier l’importance du résidu K70 (lysine en position 70) jusqu’ici seulement suspecté de jouer un rôle dans l’étape d’incorporation de nucléotides, pour permettre à la RT d’outrepasser un site méthylé.
Ces résultats obtenus in vitro sur des ARN viraux ont été confirmées par des expériences de rétrotranscription endogène réalisées avec des virus issus de l’infection de cellules sauvages ou de cellules ∆FTSJ3. Les résultats montrent en effet que la rétrotranscription des génomes hypométhylés est plus efficace que celle des génomes provenant de cellules sauvages. En accord avec ces observations, des expériences d’infection de cellules dont le réservoir en nucléotides est réduit, indiquent que lorsque les virions sont produits par des cellules ∆FTSJ3, la transcription inverse a un rendement plus élevé, par rapport aux virus issus de cellules sauvages. Les méthylations du génome du VIH-1 limitent donc la réplication virale lors de l’infection de cellules quiescentes, alors que leur effet est probablement moindre dans des cellules activées, dans lesquelles les nucléotides sont présents en concentrations plus élevées (Figure 4).
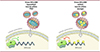 |
Figure 4. Les 2′-O-méthylations internes du génome du VIH-1, produites par la MTase cellulaire FTSJ3, bloquent le processus de rétrotranscription de l’ARNv dans des cellules quiescentes. Les ARNv hypo-méthylés - suite à la délétion du gène FTSJ3 - sont plus efficacement rétrotranscrits par la polymérase du VIH (RT) que les ARN des virus sauvages, lorsque la concentration en désoxyribonucléotides (dNTP) est faible, comme c’est le cas dans des cellules quiescentes. Par conséquent, la réplication du VIH-1 naturellement 2′-O-méthylé est réduite dans les cellules quiescentes, par rapport à la réplication dans des cellules activées, qui sont riches en dNTP. |
Conclusion et perspectives thérapeutiques
Les 2′-O-méthylations présentes sur le génome du virus VIH-1 ont à la fois des effets proviraux, dans la mesure où elles rendent le génome viral indétectable et résistant à la dégradation, et des effets antiviraux liés à l’inhibition de la rétrotranscription dans les cellules quiescentes. Il existe probablement une régulation fine de l’ajout de ces marques épitranscriptomiques au cours du cycle viral, assurant une réplication efficace.
Plus largement, la découverte de l’inhibition de la RT du VIH-1 par les 2′-O-méthylations de son génome suggère que les réplicases virales d’autres virus pourraient être affectées par la présence de résidus méthyles sur leur génome ARN ou sur leurs ARNm, et suggère que des 2′-O-méthyltransférases cellulaires pourraient jouer le rôle de facteur de restriction [23]. Il reste à déterminer dans quelle mesure ces méthylations perturbent d’autres étapes du cycle viral, comme l’encapsidation du génome ou l’efficacité de la traduction des ARNv.
Ces travaux portaient uniquement sur l’effet de la 2′-O-méthylation du génome viral. Or, des centaines de marques épitranscriptomiques peuvent affecter les ARN. L’étude de ces modifications constitue un nouveau domaine de recherche en virologie, en plein essor. L’épitranscriptome devrait être considéré comme un nouveau niveau de lecture de la complexité des ARN, indissociable de l’étude de leur fonction. Gageons que ces recherches ouvriront la voie à de nouvelles stratégies antivirales, fondées sur la modulation de ces modifications. Le rôle des 2′-O-méthylations sur la structure, la fonction des ARN et leurs interactions avec les senseurs de l’immunité innée et la protection des ARN contre la nucléase ISG20, ouvrent des perspectives vers une meilleure conception d’ARN thérapeutiques. En effet, une connaissance approfondie des marques épitranscriptomiques pourrait permettre de synthétiser des ARN capables d’induire une haute tolérance immunitaire ou, à l’inverse, d’ARN capables d’induire spécifiquement certaines réponses immunitaires, en fonctions de la stratégie thérapeutique envisagée. Les marques épitranscriptomiques permettraient également de moduler la stabilité des molécules d’ARN, pour accroître leur conservation, ou leur durée de vie dans les cellules, et de diriger des interactions protéiques spécifiques.
L’épitranscriptomique marque donc une nouvelle page de l’histoire de la recherche sur les ARN, qui promet des avancées majeures dans de nombreux domaines de recherche en virologie, biologie, et sciences de la santé.
Liens d’intérêts
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Ce travail a été financé par l’Agence nationale de la recherche (ANR-20-CE11-0024-02, ANR-17-CE15-0029) ; l’Agence nationale de la recherche sur le SIDA et les hépatites virales (ECT280C/U160) ; la Fondation Méditerranée infection ; la Fondation pour la recherche médicale (FRM-REPLI80C/U160, FDT202204014965).
Les IFN de type I sont les principaux IFN produits au cours d’une infection virale.
La technique RiboMeth-Seq permet d’identifier et de quantifier les résidus 2′-O-methylés présents au sein des ARN.
Références
- Boccaletto P, Stefaniak F, Ray A, et al. MODOMICS: a database of RNA modification pathways. 2021 update. Nucleic Acids Res 2022; 50 : D231–5. [Google Scholar]
- Linder B, JaffreySR. Discovering and Mapping the Modified Nucleotides That Comprise the Epitranscriptome of mRNA. Cold Spring Harb. Perspect. Biol 2019 ; 11 : a032201. [CrossRef] [Google Scholar]
- Netzband R, Pager CT. Epitranscriptomic marks: Emerging modulators of RNA virus gene expression. WIREs RNA 2020; 11 : e1576. [CrossRef] [PubMed] [Google Scholar]
- Lichinchi G, Gao S, Saletore Y, et al. Dynamics of the human and viral m(6)A RNA methylomes during HIV-1 infection of T cells. Nat Microbiol 2016 ; 1 : 16011. [CrossRef] [PubMed] [Google Scholar]
- Courtney DG, Tsai K, Bogerd HP, et al. Epitranscriptomic Addition of m5C to HIV-1 Transcripts Regulates Viral Gene Expression. Cell Host Microbe 2019 ; 26 : 217–27.e6. [CrossRef] [PubMed] [Google Scholar]
- Doria M, Neri F, Gallo A, et al. Editing of HIV-1 RNA by the double-stranded RNA deaminase ADAR1 stimulates viral infection. Nucleic Acids Res 2009 ; 37 : 5848–5858. [Google Scholar]
- Phuphuakrat A, Kraiwong R, Boonarkart C, et al. Double-stranded RNA adenosine deaminases enhance expression of human immunodeficiency virus type 1 proteins. J Virol 2008 ; 82 : 10864–10872. [CrossRef] [Google Scholar]
- Ringeard M, Marchand V, Decroly E, et al. FTSJ3 is an RNA 2′-O-methyltransferase recruited by HIV to avoid innate immune sensing. Nature 2019 ; 565 : 500–504. [CrossRef] [PubMed] [Google Scholar]
- Smietanski M, Werner M, Purta E, et al. Structural analysis of human 2′-O-ribose methyltransferases involved in mRNA cap structure formation. Nat Commun 2014 ; 5 : 3004. [CrossRef] [PubMed] [Google Scholar]
- Zhou M, Deng L, Kashanchi F, et al. The Tat/TAR-dependent phosphorylation of RNA polymerase II C-terminal domain stimulates cotranscriptional capping of HIV-1 mRNA. Proc Natl Acad Sci USA 2003 ; 100 : 12666–12671. [CrossRef] [PubMed] [Google Scholar]
- Yedavalli VSRK, Jeang K-T. Trimethylguanosine capping selectively promotes expression of Rev-dependent HIV-1 RNAs. Proc Natl Acad Sci USA 2010 ; 107 : 14787–14792. [CrossRef] [PubMed] [Google Scholar]
- Bélanger F, Stepinski J, Darzynkiewicz E, et al. Characterization of hMTr1, a Human Cap1 2′-O-Ribose Methyltransferase. J Biol Chem 2010 ; 285 : 33037–33044. [CrossRef] [PubMed] [Google Scholar]
- Hsu PC, Hodel MR, Thomas JW, et al. Structural requirements for the specific recognition of an m7G mRNA cap. Biochemistry 2000 ; 39 : 13730–13736. [CrossRef] [PubMed] [Google Scholar]
- Devarkar SC, Wang C, Miller MT, et al. Structural basis for m7G recognition and 2′-O-methyl discrimination in capped RNAs by the innate immune receptor RIG-I. Proc Natl Acad Sci USA 2016 ; 113 : 596–601. [CrossRef] [PubMed] [Google Scholar]
- Züst R, Dong H, Li X-F, et al. Rational design of a live attenuated dengue vaccine: 2′-o-methyltransferase mutants are highly attenuated and immunogenic in mice and macaques. PLoS Pathog 2013 ; 9 : e1003521. [CrossRef] [PubMed] [Google Scholar]
- Hornung V, Ellegast J, Kim S, et al. 5′-Triphosphate RNA is the ligand for RIG-I. Science 2006 ; 314 : 994–997. [CrossRef] [PubMed] [Google Scholar]
- Daffis S, Szretter KJ, Schriewer J, et al. 2′-O methylation of the viral mRNA cap evades host restriction by IFIT family members. Nature 2010 ; 468 : 452–456. [CrossRef] [PubMed] [Google Scholar]
- Abbas YM, Laudenbach BT, Martínez-Montero S, et al. Structure of human IFIT1 with capped RNA reveals adaptable mRNA binding and mechanisms for sensing N1 and N2 ribose 2′-O methylations. Proc Natl Acad Sci USA 2017 ; 114 : E2106–E2115. [CrossRef] [PubMed] [Google Scholar]
- Espert L, Degols G, Lin Y-L, et al. Interferon-induced exonuclease ISG20 exhibits an antiviral activity against human immunodeficiency virus type 1. J Gen Virol 2005 ; 86 : 2221–2229. [CrossRef] [PubMed] [Google Scholar]
- El Kazzi P, Rabah N, Chamontin C, et al. Internal RNA 2′O-methylation in the HIV-1 genome counteracts ISG20 nuclease-mediated antiviral effect. Nucleic Acids Res 2023; 51 : 2501–15. [Google Scholar]
- Decombe A, Peersen O, Sutto-Ortiz P, et al. Internal RNA 2′-O-methylation on the HIV-1 genome impairs reverse transcription. Nucleic Acids Res 2023; gkad1134. [Google Scholar]
- Maden BEH. Mapping 2′-O-Methyl Groups in Ribosomal RNA. Methods 2001 ; 25 : 374–382. [CrossRef] [PubMed] [Google Scholar]
- Decombe A, El Kazzi P, Decroly E. Interplay of RNA 2′-O-methylations with viral replication. Curr Opin Virol 2023; 59 : 101302. [CrossRef] [PubMed] [Google Scholar]
- Salvetti A. Épitranscriptome. Med Sci (Paris) 2024; 40 : 287. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Rousseaux N, Andrieux L. Un facteur antiviral qui discrimine la traduction du soi et du non-soi. Med Sci (Paris) 2021; 37 : 1070–2. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Chardès B, Lucifora J, Salvetti A. La protéine ISG20, un nouveau facteur de restriction contre le virus de l’hépatite B ? Med Sci (Paris) 2018; 34 : 388–91. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. Illustrations de quelques modifications épitranscriptomiques fréquemment retrouvées sur les ARNm des métazoaires ou sur les ARNv. Molécules extraites de la base de données MODOMICS [1]. |
| Dans le texte | |
 |
Figure 2. Mécanismes de détection des ARNv mal coiffés par RIG-I et de restriction par les protéines IFIT. Certains virus à ARN sont connus pour produire des ARNv coiffés et méthylés sur le premier nucléotide (Cap-1) grâce à leur propre 2′-O-MTase. Ces ARNv ne sont pas reconnus par le senseur de l’immunité innée RIG-I. Ces virus se répliquent ainsi dans le cytoplasme sans stimuler la production d’IFN, et de protéines IFIT. Lorsque ces mêmes virus sont mutés et n’ont pas de 2′-O-MTase (∆2′-O-MTase), les ARNv produits dans le cytoplasme cellulaires et non méthylés sur le premier nucléotide (Cap-0) sont détectés par RIG-I, qui induit une cascade d’événements conduisant à la production d’IFN-I. L’IFN-I se fixe sur son récepteur IFNAR qui induit la voie de signalisation JAK/STAT conduisant à l’expression de centaines d’ISG. Parmi les ISG, les protéines IFIT sont capables de reconnaître les ARN mal coiffés (Cap-0) et bloquent leur traduction en protéines virales. (Figure partiellement réalisée à partir d’images Servier Medical Art, sous licence Creative Commons Attribution 3.0 Unported License - https://creativecommons.org/licenses/by/3.0/). |
| Dans le texte | |
 |
Figure 3. Mécanismes de détection par MDA5 des ARNv ne contenant pas de 2′-O-méthylations internes, et restriction par la nucléase ISG20. A. Lors de l’infection de cellules sauvages par le VIH, la transcription inverse du génome ARN méthylé débute simultanément avec le transit de la capside, du cytoplasme jusqu’au noyau. Le génome rétrotranscrit en ADN est intégré au génome de la cellule hôte avant d’être transcrit par l’ARN pol II. La 2′-O-MTase cellulaire FTSJ3 est recrutée au niveau du site de transcription des ARNv du VIH-1, et induit la méthylation du génome viral sur au moins 17 positions conservées. Les ARN génomiques sont encapsidés dans les nouveaux virions. Dans des cellules ∆FTSJ3, les ARNv produits et encapsidés dans les virions néosynthétisés sont en revanche hypo-méthylés. B..Lors de l’infection d’une cellule par des virions dont le génome ARN est normalement méthylé, les ARNv ne sont pas efficacement détectés par le senseur de l’immunité innée MDA5. La production d’IFN-I n’est donc pas stimulée. En revanche, les virions produits par les cellules ∆FTSJ3 produisent des ARNv hypo-méthylés, qui sont détectés par MDA5. MDA5 induit une cascade d’événements conduisant à une production d’IFN-I. Les IFN-I se fixent sur aux récepteurs IFNAR, qui déclenchent la voie de signalisation JAK/STAT conduisant à l’expression de centaines d’ISG. Parmi les ISG, l’exonucléase ISG20 dégrade les ARN hypo-méthylés, qui ne seront pas traduits, ce qui inhibe la réplication virale. (Figure partiellement réalisée à partir d’images Servier Medical Art, sous licence Creative Commons Attribution 3.0 Unported License - https://creativecommons.org/licenses/by/3.0/). |
| Dans le texte | |
 |
Figure 4. Les 2′-O-méthylations internes du génome du VIH-1, produites par la MTase cellulaire FTSJ3, bloquent le processus de rétrotranscription de l’ARNv dans des cellules quiescentes. Les ARNv hypo-méthylés - suite à la délétion du gène FTSJ3 - sont plus efficacement rétrotranscrits par la polymérase du VIH (RT) que les ARN des virus sauvages, lorsque la concentration en désoxyribonucléotides (dNTP) est faible, comme c’est le cas dans des cellules quiescentes. Par conséquent, la réplication du VIH-1 naturellement 2′-O-méthylé est réduite dans les cellules quiescentes, par rapport à la réplication dans des cellules activées, qui sont riches en dNTP. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




