| Issue |
Med Sci (Paris)
Volume 35, Number 12, Décembre 2019
Anticorps monoclonaux en thérapeutique
|
|
|---|---|---|
| Page(s) | 1054 - 1061 | |
| Section | Les anticorps armés | |
| DOI | https://doi.org/10.1051/medsci/2019205 | |
| Published online | 06 January 2020 | |
Immunotoxines et immunocytokines
Immunotoxins and immunocytokines
Laboratoires Pierre Fabre, Centre d’Immunologie Pierre Fabre, 5 Avenue Napoléon III, 74160 St Julien en genevois, France
Les cytokines et les toxines biologiques représentent deux classes de biomolécules qui ont longtemps été explorées pour leur potentiel thérapeutique. Des effets secondaires considérables et des mauvaises propriétés pharmacocinétiques sont fréquemment observés chez chacune d’elles, ce qui limite leur application. L’ingénierie des protéines recombinantes a permis la création d’immunocytokines et d’immunotoxines qui visent à utiliser les propriétés avantageuses des immunoglobulines, pour résoudre ces problèmes. Des anticorps entiers, des fragments d’anticorps, des domaines constants et des dérivés ont été génétiquement fusionnés à une gamme de cytokines et de toxines. Cette revue présente les stratégies déployées et les problèmes à résoudre au cours de l’évaluation clinique pour cette classe de biothérapeutiques.
Abstract
Cytokines and biological toxins represent two potent classes of biomolecules that have long been explored for their potential as therapeutics. Considerable side effects and poor pharmacokinetics frequently observed with both have limited their broad application. Recombinant protein engineering has allowed the construction of immunocytokines and immunotoxins that seek to exploit the advantageous properties of immunoglobulins to address these issues. Whole antibodies, antibody fragments, constant domains and derivatives have been fused genetically to a range of cytokines and toxins. This review considers the strategies that have been employed and the problems sought to be resolved in the clinical evaluation of this class of biotherapeutic.
© 2019 médecine/sciences – Inserm
Au cours de l’évolution, la nature a développé une vaste gamme de biomolécules extrêmement puissantes qui peuvent contrôler ou détruire les systèmes biologiques. Le système immunitaire en est un parfait exemple avec plus de 130 cytokines pouvant le moduler. Les toxines ont elles-mêmes évolué en tant qu’inhibiteurs très efficaces de multiples systèmes biologiques. L’induction de réponses à de très faibles concentrations est une caractéristique commune aux cytokines et aux toxines ; ainsi l’interleukine-2 (IL-2) active son récepteur à des concentrations pico-molaires [1], tandis que la toxine diphtérique (DiT) possède une DL50 (dose létale 50) de 0,1 µg/kg [2]. La formidable efficacité de ces biomolécules génère aujourd’hui un intérêt thérapeutique grandissant visant à induire chez les patients une réponse biologique telle que la régulation du système immunitaire avec les cytokines ou la destruction cellulaire ciblée via les toxines. À ce jour, un petit nombre de cytokines ont été approuvées pour une utilisation thérapeutique, parmi lesquelles l’IL-2 recombinante (Aldesleukin) pour le traitement des mélanomes et carcinomes rénaux [3,4], ou l’interféron alpha (IFN-α) pour le traitement de cancers [5] et d’infections virales [6]. Toutefois, la grande puissance de cette classe de molécules a aussi limité leur spectre d’utilisation car leur administration systémique provoque de nombreux effets indésirables tels qu’une toxicité neuronale avec l’IFN-α [7] ou le syndrome de fuite capillaire lié à l’IL-2 [8].
Les anticorps monoclonaux (AcM) et leurs dérivés représentent une classe thérapeutique à succès due à leur action ciblée, leur longue demi-vie et leurs fonctions effectrices modulables [9]. Par des approches d’ingénierie des protéines, certaines caractéristiques des AcM ont ainsi été exploitées afin d’améliorer le potentiel thérapeutique des cytokines et des toxines menant à la création d’une nouvelle classe de biomolécules: les immunocytokines [10] et immunotoxines [11]. Cette revue propose un état de l’art des développements cliniques de ces deux classes de biomolécules. Il est à noter que le couplage chimique de drogue sur les anticorps (antibody drug conjugates) ne sera pas traité ici, mais est largement couvert dans la littérature [12].
Les différentes stratégies identifiées pour délivrer les cytokines et/ou toxines aux patients sont présentées en fonction de l’état d’avancement des développements cliniques de ces biomolécules.
Molécules approuvées en clinique
Malgré les efforts réalisés, seulement deux molécules ont été approuvées à ce jour par la FDA (food and drug administration) et/ ou l’EMA (agence européenne des médicaments). Denileukin difinitox [13], est une protéine de fusion cytokine-toxine permettant l’adressage de la toxine diphtérique via le module cytokinique aux cellules immunitaires exprimant le récepteur de l’IL-2. Bien que n’étant pas à proprement parler une immunocytokine ou une immunotoxine, denileukin difinitox est considéré comme un premier exemple de « cytokine ciblée » approuvée en 1999 pour le traitement des lymphomes cutanés à lymphocytes T. Elle a toutefois été retirée du marché en 2014 à la suite de problèmes de fabrication [14]. En revanche, le moxétumomab pasudotox est une véritable immunotoxine, approuvée en 2018 par la FDA pour le traitement de leucémie à tricholeucocytes réfractaire, avec des réponses complètes chez 41 % des patients dans une étude de phase III [15,16]. Moxetumomab pasudotox est une protéine de fusion entre un fragment variable (Fv) d’un anticorps (Figure 1e, Tableau I) ciblant CD22 et une forme tronquée de l’endotoxine de Pseudomonas (Pseudomonas exotoxin, PE), appelée PE38 [17]. L’affinité et la stabilité du domaine Fv ont été optimisées pour obtenir une molécule pouvant être développée jusqu’à un stade de production industrielle à large échelle pour une éventuelle commercialisation [15].
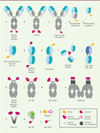 |
Figure 1. Structure des immunotoxines et immunocytokines. |
Immunotoxines et immunocytokines en étude clinique. LMNH-B: lymphome malin non-Hodgkinien de type B ; CBNPC: cancer bronchique non à petites cellules ; LLA: leucémie lymphoïde aiguë.
Molécules en phase III
Les essais cliniques avancés sont actuellement dominés par des cytokines et toxines ciblant le microenvironnement tumoral. L’immunotoxine oportuzumab monatox (Figure 1f, Tableau I) cible la protéine EpCam (epithelial cell adhesion molecule) par une simple chaîne fragment variable (scFv) fusionnée à la PE avec un taux de réponse complète de 44 % chez les patients atteints de cancer de la vessie [18]. La PE est un puissant immunogène et des efforts considérables ont été réalisés afin de désimmuniser cette toxine. La récente description de la neutralisation de la PE par la défensine humaine HNP-1 (human neutrophil peptide-1) [19] pourrait cependant avoir un impact négatif sur le potentiel thérapeutique de ce type de composé [11]. Le naptumomab estéfénatox [20] (Figure 1d) utilise une approche complètement différente. L’entérotoxine A de Staphyloccocus (SEA) est fusionnée à un Fab (fragment antigen binding) ciblant l’antigène oncofoetal 5T4, mais la toxicité directe n’est pas ici le mode d’action prioritaire. Le naptumomab estéfénatox active en effet les lymphocytes T au contact des cellules cancéreuses. La liaison de la SEA au complexe majeur d’histocompatibilité de classe II a également été réduite afin de masquer la réponse immunitaire du patient contre la SEA native et ainsi augmenter la fenêtre thérapeutique [20]. Le naptumomab estéfénatox est actuellement testé dans le traitement des carcinomes rénaux en combinaison avec l’IFN-α [21].
Le Daromun®, l’immunocytokine la plus avancée (Tableau I), est constituée non pas d’un composé unique, mais de deux composés ciblant le domaine ED-B (extra domain-B) de la fibronectine [22] via le scFv L19 configuré différemment selon la cytokine fusionnée dans chacun de ces composés [23]. Le premier composé, Darleukin® (Figure 1g) combine deux fragments scFv L19 fusionnés à l’IL-2 alors que le second, le Fibromun® (Figure 1i) assemble un trimère de TNF-α (tumor necrosis factor alpha) via trois fragments scFv L19. Darleukin® et Fibromun® utilisent le scFv L19 pour adresser les cytokines à la tumeur, où elles peuvent induire une réponse immunitaire à la fois locale et abscopale1. L’absence des domaines constants de l’anticorps dans ces molécules induit une demi-vie circulante courte. Par conséquent, les investigations cliniques de ces composés se sont jusqu’à présent concentrées sur des injections intratumorales.
La protéine de fusion NGR-hTNF n’est pas une immunocytokine au sens strict, mais une cytokine ciblée (Figure 1r). Fusionné au TNF-α, le motif peptidique cyclique CNGRS cible l’alanine aminopeptidase (CD13) et permet d’augmenter la dose thérapeutique de TNF-α sans toxicité induite. NGR-hTNF a été évaluée en phase III dans le mésothéliome pleural malin où des taux élevés de CD13 et une forte angiogenèse sont observés, et pour lequel les options de traitement sont limitées [24]. Malgré de nombreuses évaluations cliniques, le développement de la NGR-hTNF semble arrêté depuis 2017.
Molécules en phase II
Sept immunocytokines, deux immunotoxines et un conjugué cytokine-toxine sont en cours d’évaluation dans des essais de phase II (Tableau I). Trois des sept immunocytokines ne possèdent pas de domaine de ciblage par un anticorps, mais exploitent la propriété de demi-vie prolongée fournie par leur partie Fc à laquelle ces cytokines sont fusionnées, qui permet son recyclage par le récepteur Fc néonatal (FcRn). Ainsi, ALT-803 est un complexe protéique associant une protéine de fusion et l’IL-15. ATL-803 est en effet constitué d’une protéine de fusion contenant deux copies du récepteur de l’IL-15 (IL15-Rα) fusionné à une région Fc d’IgG, produite en cellules de mammifère. Grâce à ses deux récepteurs, cette protéine de fusion fixent deux molécules d’IL-15 mutées (IL-15mut), ayant une très haute affinité pour le récepteur, produite en système bactérien. Cette fixation protéine de fusion (IL-15R-Fc) avec l’IL-15mut permet d’obtenir le produit final, ALT-803 [25]. ALT-803 cherche à exploiter la capacité de l’IL-15 à activer les cellules NK (natural killer) et à induire la prolifération de certaines sous-populations de lymphocytes T [26] pour cibler de nombreux cancers, mais aussi les infections par le VIH (virus de l’immunodéficience humaine). ALT-803 est notamment en cours d’évaluation en combinaison avec des anticorps anti-points de contrôle immunitaires, PD-1 et PD-L1 [27]. Les deux autres protéines de fusion de cette catégorie combinent soit l’IL-2 (AMG592), soit l’IL-22 (RG7880) à une région Fc. Évaluée dans les pathologies inflammatoires, AMG592 n’est pas seulement conçue pour augmenter la demi-vie de l’IL-2 mais aussi pour stimuler spécifiquement la prolifération des lymphocytes T régulateurs (Treg), grâce à une version modifiée de l’IL-2 [28]. C’est un exemple raffiné de modulation de l’activité pléiotrope des cytokines, pour obtenir un résultat clinique précis. Le Dekavil (Figure 1g) combine deux scFv ciblant le domaine ED-A de la fibronectin [11] à l’IL-10, pour traiter les pathologies inflammatoires, comme la polyarthrite rhumatoïde [29].
Les autres molécules développées permettent de délivrer l’IL-2 au site de la tumeur par des stratégies très différentes. RG7461 (Figure 1a), une immunocytokine classique, est issue d’une fusion de l’IL-2 à l’extrémité C-terminale d’un anticorps dirigé contre la protéine d’activation des fibroblastes (FAP). Dans ce format, l’IL-2 est mutée pour éliminer son interaction avec CD25 et donc réduire son activité sur les lymphocytes Treg. Enfin, ALT-801 combine l’IL-2 à une TcR (récepteur des lymphocytes T) simple chaîne spécifique de la protéine p53 qui est surexprimée à la surface de nombreuses cellules cancéreuses [30].
Parmi les composés évalués dans des essais de phase II, fondés sur l‘utilisation de toxines, OXS-1550 [31] et Resimmune® [32] permettent l’adressage de la toxine DiT (Figure 1h). OXS-1550, aussi appelé DT2219ARL, combine deux scFv ciblant CD19 et CD22 [31] avec les domaines catalytiques et de translocation de la DiT. Le double ciblage de CD19 et CD22 vise à élargir le potentiel thérapeutique de ce composé dans le traitement des leucémies et des lymphomes non Hodgkiniens. Resimmune®, quant à lui, utilise la DiT comme cytotoxique et l’adresse par deux ScFv ciblant cette fois la sous-unité CD3ε du TcR. L’utilisation de deux scFv est requise dans cette approche afin d’atteindre une efficacité de liaison similaire à celle de l’anticorps parental UCH1 [33]. Resimmune® est actuellement évalué pour le traitement des mélanomes, des lymphomes T et des mycoses.
MDNA-55, dernière fusion cytokine-toxine évaluée en phase II (Tableau I), exploite à nouveau la toxicité de la PE dont le ciblage est assuré cette fois par l’IL-4 [34]. MDNA-55 est une fusion de l’IL-4, ayant subi une permutation circulaire, avec une PE tronquée (Figure 1q), pour induire une toxicité accrue de 3 à 30 fois vis-à-vis des cellules tumorales. Le récepteur de l’IL-4 étant très exprimé dans les glioblastomes, MDNA-55 est en cours d’évaluation dans cette indication.
Molécules en phase I et I/II
Sans surprise, le plus grand nombre de molécules en développement est identifié en phase clinique précoce avec 20 composés en cours d’évaluation au moment de l’écriture de cette revue (Tableau I). Les immunocytokines sont majoritaires et seules trois immunotoxines sont évaluées. La littérature portant sur les composés précoces, souvent limitée et parcellaire, nous a conduits à limiter les détails pour couvrir pleinement le champ d’application.
Présente dans sept composés en phase I/II, l’IL-2 est la cytokine d’intérêt la plus fréquemment utilisée en développement. Darleukin et RG7461, précédemment utilisés dans des phases avancées, explorent, dans des phases précoces, de nouvelles indications et/ou de nouveaux régimes d’administration. Teleukin, tout comme Darleukin (Figure 1g), est une fusion de l’IL-2 à deux scFv ciblant cette fois-ci le domaine c de la Ténascine C [35]. Teleukin a été évaluée en combinaison avec plusieurs agents de chimiothérapie et un AcM dirigé contre CD33, un antigène spécifique des cellules de la lignée myéloïde et qui contrôle l’activation des monocytes. Elle est aujourd’hui en clinique en combinaison avec la cytarabine pour le traitement de la leucémie myéloïde aiguë. Le cergutuzumab amunaleukin cible l’antigène carcino-embrionnaire (ACE) [36], marqueur fréquent des tumeurs solides. Tout comme le RG7461 décrit ci-dessus, le cergutuzumab amunaleukin permet de délivrer au site tumoral un variant d’IL-2 ayant perdu la capacité de lier CD25 via un anticorps complet. Toutefois, cette molécule présente une seule molécule d’IL-2 au lieu de deux (Figure 1c) afin de favoriser l’interaction avec l’ACE plutôt qu’avec le récepteur de l’IL-2 (IL-2R) et ainsi augmenter les perspectives thérapeutiques de ce composé. Dernier composé de cette série, RG7835 consiste en la fusion d’une IL-2 mutée à une région Fc dont la capacité de liaison aux RFcg a été abolie. Cette mutation de l’IL-2 (N88D), qui diminue sa liaison au récepteur IL-2Rbg mais non au récepteur IL-2Rabg exprimé préférentiellement par les lymphocytes T régulateurs (Treg) permet de tester le RG7835 dans le traitement des maladies auto-immunes du fait de l’expansion des lymphocytes Treg que cette molécule de fusion induit, avec une demi-vie prolongée, et à faible concentration grâce à la stabilisation due à la présence de la région Fc [37]. Le même format est également utilisé afin d’augmenter la demi-vie de l’IL-22 dans le RG7880 (Figure 1k), actuellement testé pour le contrôle des maladies inflammatoires [38].
HyLeukin-7 utilise une région Fc hybride non-cytolytique composé de la région charnière d’une IgD et des domaines CH2-CH3 d’une IgG4, le tout fusionné à un homodimère d’IL-7 (Figure 1k). L’objectif de ce type de fusion avec l’IL-7 est d’amplifier les populations de lymphocytes T chez les patients atteints de cancer [39]. OMP-336B11 [40] utilise à nouveau un format de fusion à une région Fc pour présenter à la tumeur le GITR (glucocorticoid-induced TNFR family related gene), une cytokine trimérique appartenant à la superfamille des ligands du TNF. Deux trimères de GITRL sont fusionnés à une région Fc pour créer un complexe moléculaire mimant les capacités immunostimulatrices du GITRL natif (Figure 1m). MEDI1873 cherche également à reproduire le complexe formé par le GITRL natif fusionné à une région Fc, mais par une approche plus atypique (Figure 1n). Chaque molécule de GITRL est fusionnée à un domaine de trimérisation isoleucine zipper et à une région Fc dans un assemblage hexamèrique pouvant activer les lymphocytes T [41].
Bien qu’elle soit déjà approuvée en clinique, l’IFN-α est une cytokine associée à de sérieux effets secondaires. Deux immunocytokines cherchent à limiter cette toxicité systémique par le ciblage de l’IFN-α vers le microenvironnement tumoral (Tableau I). TAK573 fusionne une molécule d’IFN-α atténué avec une IgG4 ciblant CD38 pour stimuler les voies antiprolifératives des cellules tumorales (Figure 1a). La seconde molécule, IGN-002, combine un anticorps anti-CD20 et l’IFN-α avec pour effet l’augmentation de la mort des cellules malignes [42].
La protéine de fusion M-9241 contenant l’IL-12 présente la particularité d’une cytokine hétérodimérique (Figure 1b) non fusionnée à la partie C-terminale de l’anticorps par une liaison polypeptidique [43]. Le ciblage par l’anticorps vise à réduire la toxicité systémique associée à l’IL-12 seule [44]. L’utilisation du ligand de 4-1BB (4-1BBL) a précédemment mis en évidence des hépatotoxicités au cours de développements cliniques. Le composé RG7827 adresse le 4-1BBL à la tumeur en ciblant la protéine d’activation des fibroblastes (FAP), pour induire la stimulation des lymphocytes T avec une toxicité réduite [45]. Des essais cliniques concernant FasL, le ligand de FAS (CD95/APO-1), n’ont pas montré d’efficacité. Cependant, le composé APO010 – bien que n’étant pas une véritable immunocytokine car présentant FasL sous une forme trimérique fusionnée à des domaines de dimérisation adiponectique (Figure 1o) – vise à activer l’apoptose dans les cancers hématologiques [46]. La dernière immunocytokine en phase I/II considérée est l’OXS-3550, dont le format « TriKE » (tri-specific killer engager) combine un scFv anti-CD16, engageant les cellules NK, lié via l’IL-15 à un scFv anti-CD33 ciblant les cellules myéloïdes tumorales. Cette protéine de fusion a pour objectif d’induire l’expansion, la survie, et l’activation des cellules NK contre les populations cellulaires tumorales CD33+ [47].
Les essais cliniques de phase I des trois immunotoxines restantes incluent le naptumomab estafénatox, qui cible l’antigène oncofœtal 5T4 et qui est couplé à la SEA, et est testé dans le cancers bronchiques non à petites cellules (CBNPC) [48]. Le D2C7-IT (Figure 1f) conjugue une forme terminale tronquée de la PE avec un scFv stabilisé par un pont disulfure ciblant le type sauvage du récepteur de l’EGF (facteur de croissance épidermique) et le mutant EGFRvIII de ce récepteur. Ce dernier est restreint au glioblastome [49], indication dans laquelle D2C7-IT est actuellement évalué. Enfin, le composé MT-3724 résulte de la fusion d’une toxine Shiga-like toxin 1a modifiée avec un scFv dirigé contre CD20 [50] induisant une inhibition de la synthèse des protéines et une apoptose des cellules ciblées. Commune à toutes les immunotoxines, l’extension de la demi-vie liée au couplage reste un point sensible. En effet, une élimination rapide de cette classe de composés est préférable pour limiter les effets indésirables.
Perspectives
À ce jour, l’utilisation des cytokines ou des toxines est limitée par la toxicité hors cible, des fenêtres thérapeutiques étroites, et des effets systémiques puissants, qui sont à l’opposé d’une activité ciblée et contrôlée sur le site de la pathologie à traiter. Les avancées décrites ici pour les immunocytokines et immunotoxines tentent de répondre à ces problèmes. Cependant, la validation clinique est rare. Les stratégies nouvelles et formats thérapeutiques nécessitent des investigations cliniques nombreuses pour assurer l’efficacité et l’innocuité de ces composés. Certaines constructions thérapeutiques décrites ici sont susceptibles d’obtenir une autorisation de mise sur le marché dans un futur proche. Cependant, la biologie complexe – tant des fractions de ciblage que des charges fonctionnelles – de ces fusions innovantes signifie que le succès clinique d’un composé donné ne garantit pas un avantage pour les déclinaisons de ce même format en termes de cible ou de charge. L’efficacité thérapeutique d’une ou plusieurs molécules pourra galvaniser les stratégies futures, mais la complexité à traiter en termes de charges, monomères, hétérodimères, trimères – voire des molécules plus complexes – nécessitera une validation complète de chaque étape. L’extrême puissance des cytokines et des toxines rend toutes ces stratégies nécessaires pour la vectorisation thérapeutique. C’est cette même puissance qui restera à la base des développements futurs.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Leong JW, Chase JM, Romee R, et al. Pre-activation with IL-12, IL-15, and IL-18 induces CD25 and a functional high affinity IL-2 receptor on human cytokine-induced memory-like NK cells. Biol Blood Marrow Transpl 2014 ; 20: 463–473. [CrossRef] [Google Scholar]
- Gill DM. Bacterial toxins: a table of lethal amounts. Microbiol Rev 1982 ; 46: 86–94. [CrossRef] [PubMed] [Google Scholar]
- Kintzel PE, Calis KA. Recombinant interleukin-2: a biological response modifier. Clin Pharm 1991 ; 10: 110–128. [PubMed] [Google Scholar]
- Whittington R, Faulds D. Interleukin-2. A review of its pharmacological properties and therapeutic use in patients with cancer. Drugs 1993 ; 46: 446–514. [CrossRef] [PubMed] [Google Scholar]
- Ferrantini M, Capone I, Belardelli F. Interferon-α and cancer: mechanisms of action and new perspectives of clinical use. Biochimie 2007 ; 89: 884–893. [CrossRef] [PubMed] [Google Scholar]
- Aghemo A, Rumi MG, Colombo M. Pegylated interferons α2a and α2b in the treatment of chronic hepatitis C. Nat Rev Gastroenterol Hepatol 2010 ; 7: 485–494. [CrossRef] [PubMed] [Google Scholar]
- Sleijfer S, Bannink M, Van Gool AR, et al. Side effects of interferon-alpha therapy. Pharm World Sci 2005 ; 27: 423–431. [CrossRef] [PubMed] [Google Scholar]
- Schwartz RN, Stover L, Dutcher JP. Managing toxicities of high-dose interleukin-2. Oncology (Williston Park, NY) 2002; 16: 11–20. [Google Scholar]
- Elgundi Z, Reslan M, Cruz E, et al. The state-of-play and future of antibody therapeutics. Adv Drug Deliv Rev 2017 ; 122: 2–19. [CrossRef] [PubMed] [Google Scholar]
- Neri D.. Antibody-cytokine fusions: Versatile products for the modulation of anticancer immunity. Cancer Immunol Res 2019 ; 7: 348–354. [CrossRef] [PubMed] [Google Scholar]
- Alewine C, Hassan R, Pastan I. Advances in anticancer immunotoxin therapy. The Oncologist 2015 ; 20: 176–185. [CrossRef] [PubMed] [Google Scholar]
- Beck A, Goetsch L, Dumontet C, et al. Strategies and challenges for the next generation of antibody-drug conjugates. Nat Rev Drug Discov 2017 ; 16: 315–337. [CrossRef] [PubMed] [Google Scholar]
- Foss FM. Interleukin-2 fusion toxin: targeted therapy for cutaneous T cell lymphoma. Ann NY Acad Sci 2001 ; 941: 166–176. [CrossRef] [Google Scholar]
- Wang Z, Zheng Q, Zhang H, et al. Ontak-like human IL-2 fusion toxin. J Immunol Methods 2017 ; 448: 51–58. [CrossRef] [PubMed] [Google Scholar]
- Kreitman RJ, Dearden C, Zinzani PL, et al. Moxetumomab pasudotox in relapsed/refractory hairy cell leukemia. Leukemia 2018 ; 32: 1768–1777. [CrossRef] [PubMed] [Google Scholar]
- Fancher KM, Lally-Montgomery ZC. Moxetumomab pasudotox: a first-in-class treatment for hairy cell leukemia. J Oncol Pharm Pract 2019 ; 1078155219838041. [Google Scholar]
- Kreitman RJ, Pastan I. Antibody fusion proteins: anti-CD22 recombinant immunotoxin moxetumomab pasudotox. Clin Cancer Res 2011 ; 17: 6398–6405. [CrossRef] [PubMed] [Google Scholar]
- Kowalski M, Guindon J, Brazas L, et al. A phase II study of oportuzumab monatox: an immunotoxin therapy for patients with noninvasive urothelial carcinoma in situ previously treated with bacillus Calmette-Guérin. J Urol 2012 ; 188: 1712–1718. [CrossRef] [PubMed] [Google Scholar]
- Zou G, de Leeuw E. Neutralization of Pseudomonas auruginosa exotoxin a by human neutrophil peptide 1. Biochem Biophys Res Commun 2018 ; 501: 454–457. [Google Scholar]
- Eisen T, Hedlund G, Forsberg G, et al. Naptumomab estafenatox: targeted immunotherapy with a novel immunotoxin. Curr Oncol Rep 2014 ; 16: 370. [CrossRef] [PubMed] [Google Scholar]
- Hawkins RE, Gore M, Shparyk Y, et al. A randomized phase II/III study of Naptumomab Estafenatox + IFNα versus IFNα in renal cell carcinoma: final analysis with baseline biomarker subgroup and trend analysis. Clin Cancer Res 2016 ; 22: 3172–3181. [CrossRef] [PubMed] [Google Scholar]
- Viti F, Tarli L, Giovannoni L, et al. Increased binding affinity and valence of recombinant antibody fragments lead to improved targeting of tumoral angiogenesis. Cancer Res 1999 ; 59: 347–352. [Google Scholar]
- Borsi L, Balza E, Bestagno M, et al. Selective targeting of tumoral vasculature: comparison of different formats of an antibody (L19) to the ED-B domain of fibronectin. Int J Cancer 2002 ; 102: 75–85. [CrossRef] [PubMed] [Google Scholar]
- Gregorc V, Zucali PA, Santoro A, et al. Phase II study of asparagine-glycine-arginine-human tumor necrosis factor alpha, a selective vascular targeting agent, in previously treated patients with malignant pleural mesothelioma. J Clin Oncol 2010 ; 28: 2604–2611. [CrossRef] [PubMed] [Google Scholar]
- Xu W, Jones M, Liu B, et al. Efficacy and mechanism-of-action of a novel superagonist interleukin-15: Interleukin-15 receptor αSu/Fc fusion complex in syngeneic murine models of multiple myeloma. Cancer Res 2013 ; 73: 3075–3086. [Google Scholar]
- Wong HC, Jeng EK, Rhode PR. The IL-15-based superagonist ALT-803 promotes the antigen-independent conversion of memory CD8+ T cells into innate-like effector cells with antitumor activity. Oncoimmunology 2013; 2. [Google Scholar]
- Wrangle JM, Velcheti V, Patel MR, et al. ALT-803, an IL-15 superagonist, in combination with nivolumab in patients with metastatic non-small cell lung cancer: a non-randomised, open-label, phase 1b trial. Lancet Oncol 2018 ; 19: 694–704. [CrossRef] [PubMed] [Google Scholar]
- Tchao N, Gorski KS, Yuraszeck T, et al. PS7:135 Amg 592 is an investigational il-2 mutein that induces highly selective expansion of regulatory t cells. Lupus Sci Med 2018 ; 5: A102. [Google Scholar]
- Schwager K, Kaspar M, Bootz F, et al. Preclinical characterization of DEKAVIL (F8-IL10), a novel clinical-stage immunocytokine which inhibits the progression of collagen-induced arthritis. Arthritis Res Ther 2009 ; 11: R142. [PubMed] [Google Scholar]
- Fishman MN, Thompson JA, Pennock GK, et al. Phase I trial of ALT-801, an interleukin-2/T-cell receptor fusion protein targeting p53 (aa264-272)/HLA-A*0201 complex, in patients with advanced malignancies. Clin Cancer Res 2011 ; 17: 7765–7775. [CrossRef] [PubMed] [Google Scholar]
- Vallera DA, Chen H, Sicheneder AR, et al. Genetic alteration of a bispecific ligand-directed toxin targeting human CD19 and CD22 receptors resulting in improved efficacy against systemic B cell malignancy. Leuk Res 2009 ; 33: 1233–1242. [CrossRef] [PubMed] [Google Scholar]
- Frankel AE, Woo JH, Ahn C, et al. Resimmune, an anti-CD3ε recombinant immunotoxin, induces durable remissions in patients with cutaneous T-cell lymphoma. Haematologica 2015 ; 100: 794–800. [CrossRef] [PubMed] [Google Scholar]
- Thompson J, Stavrou S, Weetall M, et al. Improved binding of a bivalent single-chain immunotoxin results in increased efficacy for in vivo T-cell depletion. Protein Eng Des Sel 2001 ; 14: 1035–1041. [Google Scholar]
- Kawakami M, Kawakami K, Puri RK. Interleukin-4-Pseudomonas exotoxin chimeric fusion protein for malignant glioma therapy. J Neurooncol 2003 ; 65: 15–25. [CrossRef] [PubMed] [Google Scholar]
- Garin-Chesa P, Old LJ, Rettig WJ. Cell surface glycoprotein of reactive stromal fibroblasts as a potential antibody target in human epithelial cancers. Proc Natl Acad Sci USA 1990 ; 87: 7235–7239. [CrossRef] [Google Scholar]
- Klein C, Waldhauer I, Nicolini VG, et al. Cergutuzumab amunaleukin (CEA-IL2v), a CEA-targeted IL-2 variant-based immunocytokine for combination cancer immunotherapy: Overcoming limitations of aldesleukin and conventional IL-2-based immunocytokines. Oncoimmunology 2017 ; 6: e1277306. [CrossRef] [PubMed] [Google Scholar]
- Bell CJM, Sun Y, Nowak UM, et al. Sustained in vivo signaling by long-lived IL-2 induces prolonged increases of regulatory T cells. J Autoimmun 2015 ; 56: 66–80. [CrossRef] [PubMed] [Google Scholar]
- Rothenberg ME, Wang Y, Lekkerkerker A, et al. Randomized phase I healthy volunteer study of UTTR1147A (IL-22Fc): a potential therapy for epithelial injury. Clin Pharmacol Ther 2019 ; 105: 177–189. [CrossRef] [PubMed] [Google Scholar]
- Nguyen V, Mendelsohn A, Larrick JW. Interleukin-7 and immunosenescence. J Immunol Res 2017 ; 2017: 4807853. [CrossRef] [PubMed] [Google Scholar]
- Chan IH, Xie MH, Lam A, et al. A In vitro functional activity of OMP-336B11, a GITRL-Fc fusion protein, on primary human immune cells. Cancer Res 2018; 78: 2726 (abstract 2726). [Google Scholar]
- Tigue NJ, Bamber L, Andrews J, et al. MEDI1873, a potent, stabilized hexameric agonist of human GITR with regulatory T-cell targeting potential. Oncoimmunology 2017 ; 6: e1280645. [CrossRef] [PubMed] [Google Scholar]
- Xuan C, Steward KK, Timmerman JM, et al. Targeted delivery of interferon-alpha via fusion to anti-CD20 results in potent antitumor activity against B-cell lymphoma. Blood 2010 ; 115: 2864–2871. [Google Scholar]
- Fallon J, Tighe R, Kradjian G, et al. The immunocytokine NHS-IL12 as a potential cancer therapeutic. Oncotarget 2014; 5. [PubMed] [Google Scholar]
- Braun F, Behrend M. 37-Drugs that act on the immune system: cytokines and monoclonal antibodies. In: Aronson JK, ed. Side effects of drugs annual. A worldwide yearly survey of new data and trends in adverse drug reactions and interactions. New York: Elsevier, 2008: 435–51. [Google Scholar]
- Umana P. FAP-4-1BBL: a next generation, targeted costimulatory agonist for cancer immunotherapy. Cancer Res 2018; 78: DDT02-01-DDT02-01 (abstract DDT02-01). [Google Scholar]
- Greaney P, Nahimana A, Lagopoulos L, et al. A Fas agonist induces high levels of apoptosis in haematological malignancies. Leuk Res 2006 ; 30: 415–426. [CrossRef] [PubMed] [Google Scholar]
- Vallera DA, Felices M, McElmurry R, et al. IL15 trispecific killer engagers (TriKE) make natural killer cells specific to CD33+ targets while also inducing persistence, in vivo expansion, and enhanced function. Clin Cancer Res 2016 ; 22: 3440–3450. [CrossRef] [PubMed] [Google Scholar]
- Borghaei H, Alpaugh K, Hedlund G, et al. Phase I dose escalation, pharmacokinetic and pharmacodynamic study of naptumomab estafenatox alone in patients with advanced cancer and with docetaxel in patients with advanced non-small-cell lung cancer. J Clin Oncol 2009 ; 27: 4116–4123. [CrossRef] [PubMed] [Google Scholar]
- Chandramohan V, Bao X, Keir ST, et al. Construction of an immunotoxin, D2C7-(scdsFv)-PE38KDEL, targeting EGFRwt and EGFRvIII for brain tumor therapy. Clin Cancer Res. 2013 ; 19: 4717–4727. [CrossRef] [PubMed] [Google Scholar]
- Huang S, Jiang C, Zhang H, et al. The CD20-specific engineered toxin antibody MT-3724 exhibits lethal effects against mantle cell lymphoma. Blood Cancer J 2018 ; 8: 33. [CrossRef] [PubMed] [Google Scholar]
Liste des tableaux
Immunotoxines et immunocytokines en étude clinique. LMNH-B: lymphome malin non-Hodgkinien de type B ; CBNPC: cancer bronchique non à petites cellules ; LLA: leucémie lymphoïde aiguë.
Liste des figures
 |
Figure 1. Structure des immunotoxines et immunocytokines. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




