| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 340 - 343 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026049 | |
| Published online | 24 April 2026 | |
Humanine
Un peptide caché dans la mitochondrie au service de la résolution de l’inflammation
Humanin: a mitochondria-hidden peptide serving inflammation resolution
1
UMR RIGHT, Université Marie et Louis Pasteur, Établissement français du sang Bourgogne Franche-Comté, Inserm, LabEx LipSTIC, Besançon, France
2
Institut pour l’avancée des biosciences, Équipe « Immunologie translationnelle et immunothérapie dans les maladies chroniques », Inserm U1209, CNRS UMR5309, Université Grenoble Alpes, Établissement français du sang Auvergne-Rhône-Alpes, Grenoble, France
3
Laboratoire d’immunorhumatologie moléculaire, Université de Strasbourg, Centre de recherche d’immunologie et d’hématologie, Centre de recherche en biomédecine de Strasbourg (CRBS), Faculté de médecine, Fédération de médecine translationnelle de Strasbourg (FMTS), Inserm UMR-S 1109, Fédération hospitalo-universitaire OMICARE, Institut thématique interdisciplinaire (ITI) Transplantex NG, Laboratoire d’immunologie, Pôle de biologie, Centre hospitalier universitaire de Strasbourg, Strasbourg, France
a
This email address is being protected from spambots. You need JavaScript enabled to view it.
b
This email address is being protected from spambots. You need JavaScript enabled to view it.
c
This email address is being protected from spambots. You need JavaScript enabled to view it.
L’inflammation est une arme à double tranchant : indispensable pour défendre l’organisme contre les agents pathogènes et autres agressions, elle doit cependant être régulée pour éviter de se retourner contre l’hôte. Lorsqu’elle persiste ou s’emballe, cette réponse protectrice devient délétère et provoque des maladies chroniques telles que l’arthrite, la parodontite, l’athérosclérose, ou encore certaines maladies neurodégénératives. Les macrophages sont des acteurs clés du contrôle de l’inflammation. Capables à la fois de déclencher et de soutenir la réponse immunitaire face à une infection, ils peuvent aussi, en temps voulu, en orchestrer la fin. L’efférocytose1, processus de phagocytose des macrophages permettant l’élimination des cellules mortes présentes dans les tissus enflammés, est au cœur de cette transition vers la résolution de l’inflammation [1] (→).
(→) Voir m/s n° 5, 2024, page 428
L’efférocytose ne permet pas seulement le « nettoyage » du tissu enflammé, elle reprogramme les macrophages. Les alliés de l’inflammation d’hier deviennent alors ses modérateurs, en sécrétant une multi-tude de médiateurs anti-inflammatoires et prorésolutifs, tels que les médiateurs lipidiques prorésolutifs (specialized pro-resolving mediators [SPM]), le TGF-β (transforming growth factor-β), l’interleukine-10 (IL-10), ou encore l’annexine A1, qui freinent l’inflammation tout en favorisant la réparation tissulaire [2]. Au fil du temps, la liste de ces médiateurs s’est considérablement enrichie, révélant un réseau complexe de molécules aux propriétés multiples, capables non seulement de résoudre l’inflammation, mais aussi d’exercer des fonctions antibactériennes ou analgésiques. Ainsi, comprendre leurs mécanismes de production et leurs actions anti-inflammatoires et réparatrices constitue aujourd’hui un enjeu majeur de la « pharmacologie résolutive » afin de concevoir de nouvelles stratégies thérapeutiques [1, 2].
Nous avons entrepris d’explorer le transcriptome de macrophages dérivés de monocytes humains et rendus « efférocytiques » (c’est-à-dire ayant phagocyté des cellules mourantes, des granulocytes neutrophiles apoptotiques dans nos modèles), afin d’identifier de nouveaux effecteurs prorésolutifs. L’analyse a révélé une modulation de la transcription des gènes associés au métabolisme mitochondrial, accompagnée de l’expression inattendue d’isoformes nucléaires d’un gène mitochondrial codant une protéine appelée humanine. En effet, grâce à des cadres de lecture (open reading frames [ORF]) alternatifs, certains gènes mitochondriaux produisent de petits peptides bioactifs (mitochondria-derived peptides [MDP]), ou mitokines. L’humanine, issue d’un ORF alternatif situé dans le gène MT-RNR2 codant l’ARN ribosomique 16S mitochondrial, est l’une de ces mitokines. Ce peptide est constitué de 21 à 24 acides aminés, sa longueur variant selon qu’il est produit dans la mitochondrie ou dans le cytoplasme. Il a été découvert en 2001 lors de l’analyse d’une banque d’ADN complémentaires construite à partir de tissu cérébral sain d’individus décédés atteints de la maladie d’Alzheimer [3]. Initialement identifiée pour ses propriétés neuroprotectrices, l’humanine s’est depuis imposée comme une molécule cytoprotectrice et anti-apoptotique aux effets bénéfiques dans divers modèles de maladies neurodégénératives, métaboliques, ou cardiovasculaires [4].
Des études bioinformatiques portant sur le gène codant l’humanine ont révélé d’importantes disparités entre espèces de mammifères [5]. Chez l’Homme, 13 séquences nucléotidiques similaires à celle de ce gène (annotées MT-RNR2-like) sont dispersées dans le génome nucléaire, dont certaines peuvent coder des peptides. En revanche, aucune de ces copies nucléaires n’a été identifiée chez le rat (chez lequel le peptide mitochondrial homologue de l’humanine a été nommé rattine). Chez la souris, la séquence codante mitochondriale présente une forte similarité avec celle de l’Homme, mais elle ne comporte apparemment pas de codon d’initiation de la traduction fonctionnel. Cependant, une séquence nucléaire semble coder une forme d’humanine chez ce rongeur [5, 6] (→).
(→) Voir m/s n° 1, 2019, page 46
L’humanine peut exercer ses effets à plusieurs niveaux (Figure 1). Dans la cellule, elle peut interagir avec des protéines pro-apoptotiques de la famille BCL-2, telles que BAX, BIM, BID, ou encore IGFBP-3 [7]. Elle agit comme un peptide signal et peut donc être sécrétée pour se lier à différents récepteurs membranaires, notamment FPR2 (formyl peptide-receptor-2) et le récepteur tripartite CNTFR / IL-27Rα / gp130, composé du ciliary neurotrophic factor receptor (CNTFR), de la chaîne α du récepteur de l’interleukine-27 (IL-27Rα) et de la glycoprotéine transmembranaire gp130 [7]. L’activation des récepteurs de l’humanine entraîne celle de voies de signalisation dépendantes de ERK1/2 et STAT3. Elle peut également activer les voies impliquant AMPK et PI3K/AKT, et inhiber des facteurs proinflammatoires tels que NF-κB (nuclear factor-κB) par des mécanismes encore non élucidés [7]. En tant qu’acteur clé de la réponse au stress cellulaire, l’humanine est impliquée dans le maintien de l’activité mitochondriale. Elle inhibe la voie mitochondriale de l’apoptose (ou voie intrinsèque), stimule la biogenèse mitochondriale et l’oxydation phosphorylante, favorisant la production d’ATP. Parallèlement, elle diminue la production de médiateurs de l’inflammation et d’espèces réactives de l’oxygène. Elle renforce également les défenses anti-oxydantes via l’activation du facteur Nrf2, et favorise l’élimination de protéines oxydées via l’activation de l’autophagie relayée par les protéines chaperonnes (chaperone-mediated autophagy) [8]. L’ensemble de ces actions lui permet de soutenir le métabolisme du glucose et des lipides, notamment en stimulant la sécrétion d’insuline par les cellules β du pancréas ou en réduisant l’accumulation de graisses [8] (Figure 1).
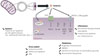 |
Figure 1 Différents mécanismes d’action de l’humanine. L’humanine est un peptide mitochondrial de 21 à 24 acides aminés, codé par une séquence nucléotidique située dans le gène de l’ARN ribosomique 16S (ARNr 16S) mitochondrial [3]. Il s’agit du premier membre identifié de la famille des MDP (mitochondria-derived peptides), un groupe de petits peptides produits par la mitochondrie en réponse à diverses agressions, et qui jouent un rôle clé dans la communication entre la mitochondrie et le reste de la cellule. L’humanine interagit avec différentes protéines, dont des acteurs pro-apoptotiques de la famille BCL-2 (notamment BAX, BAD et BIMEL) et IGFBP-3. Elle agit également en se liant à deux récepteurs : le récepteur FPR2 et un complexe tripartite formé des chaînes CNTFR, IL-27Rα et gp130. La stimulation des cellules par l’humanine déclenche plusieurs voies de signalisation, dépendant notamment de STAT3, ERK1/2, AMPK, PI3K/AKT, et conduit souvent à l’inhibition de NF-κB. Ces différents mécanismes contribuent aux effets cytoprotecteurs de l’humanine, incluant l’inhibition de l’apoptose, du stress oxydant, de l’inflammation, ainsi que la stimulation des défenses antioxydantes, de l’autophagie impliquant des protéines chaperonnes, et du métabolisme énergétique. ROS : reactive oxygen species ; CMA : chaperone-mediated autophagy ; OXPHOS : oxydation phosphorylante ; BAX : Bcl-2-associated protein x ; BID : BH3-interacting domain death agonist ; BIMEL : Bcl-2-interacting mediator of cell death extra long isoform ; IGFBP3 : insulin-like growth factor-binding protein 3 ; CNTFR : ciliary neurotrophic factor receptor ; IL-27Rα : interleukin-27 receptor α ; gp130 : glycoprotein 130 ; FPR2 : formyl peptide receptor-2 ; STAT3 : signal transducer and activator of transcription 3 ; ERK1/2 : extracellular signal-regulated kinase 1/2 ; AMPK : AMP-activated protein kinase ; PI3K/AKT : phosphoinositide 3-kinase/protein kinase B ; NF-κB : nuclear factor κB. |
Malgré de nombreuses preuves de l’implication de l’humanine dans le contrôle des processus inflammatoires, les informations disponibles quant à son implication dans le contrôle de l’immunité demeuraient limitées. Nos travaux de recherche ont mis en lumière l’implication de l’humanine dans les processus résolutifs de l’inflammation [9]. Après avoir montré qu’elle est produite par les macrophages efférocytiques humains (Figure 2A), nous avons constaté que sa production au cours d’une inflammation à résolution spontanée, dans un modèle murin de péritonite induite par le zymosane (extrait de la membrane de Saccharomyces cerevisiae), coïncidait avec l’entrée dans la phase de résolution de l’inflammation (Figure 2B). L’injection préventive de l’humanine aux souris a permis d’évaluer son impact sur le déroulement de la réaction inflammatoire : les résultats témoignent de l’effet anti-inflammatoire de ce peptide, en montrant une réduction de l’infiltration du péritoine par des granulocytes neutrophiles et des monocytes, ainsi qu’une diminution de la concentration péritonéale en cytokines pro-inflammatoires (TNFα, interleukines 6 et 1β). Cette atténuation de l’activation inflammatoire semble impliquer directement les macrophages. En effet, l’isolement de ces cellules au pic de l’inflammation (12 heures après l’injection du zymosane), suivi d’une stimulation par du lipopolysaccharide (LPS) bactérien, montre que l’humanine diminue leur capacité à sécréter du TNFα. L’humanine diminue également la sécrétion de TNFα par les granulocytes neutrophiles humains activés par le LPS (Figure 2A).
 |
Figure 2 Rôles de l’humanine dans la résolution de l’inflammation. L’ingestion de cellules apoptotiques par les macrophages, ou efférocytose, constitue une étape clé du basculement de la phase aigüe de l’inflammation vers sa résolution. L’efférocytose reprogramme les macrophages inflammatoires, qui acquièrent alors des propriétés anti-inflammatoires, freinant la migration et l’activation des leucocytes et leur sécrétion de cytokines pro-inflammatoires, ainsi que des fonctions prorésolutives, favorisant l’apoptose des granulocytes neutrophiles résiduels, la reprogrammation d’autres macrophages, l’activation d’une immunité adaptative régulatrice, et la réparation des tissus endommagés. Les médiateurs prorésolutifs produits au cours de l’efférocytose sont divers, tant par leur nature que par leurs fonctions. Ils incluent des protéines (TGF-β, IL-10, annexine A1, DEL-1, etc.) et des lipides bioactifs, tels que les médiateurs lipidiques prorésolutifs (specialized pro-resolving mediators [SPM]). A. La synthèse d’humanine, un peptide d’origine mitochondriale, est induite dans les macrophages humains à la suite de l’ingestion de granulocytes neutrophiles apoptotiques. Ce peptide exerce un effet anti-inflammatoire sur les granulocytes neutrophiles humains stimulés par du lipopolysaccharide (LPS) bactérien en réduisant leur sécrétion de TNFα (tumor necrosis factor α). B. Dans un modèle murin de péritonite induite par le zymosane, un modèle d’inflammation à résolution spontanée, l’humanine est produite à la fin de la phase aigüe, période correspondant au déclenchement des processus prorésolutifs, après l’efférocytose. L’injection préventive d’humanine à ces souris diminue le recrutement des granulocytes neutrophiles et des monocytes dans le tissu enflammé, réduit la production de cytokines proinflammatoires, et favorise l’apparition précoce de macrophages prorésolutifs CD11blow « en satiété » (macrophages efférocytiques ayant perdu leur capacité à ingérer de nouvelles cellules apoptotiques). IL : interleukine. |
Au-delà de son effet sur l’activation des cellules immunitaires, l’humanine semble également influencer la dynamique des macrophages au cours de la résolution de l’inflammation. Dans ce modèle murin de péritonite, la progression dans la phase résolutive s’accompagne de l’apparition de macrophages efférocytiques « en satiété », qui cessent de phagocyter les cellules apoptotiques et ont en retour des propriétés réparatrices et antifibrotiques accrues. Ces macrophages sont notamment caractérisés par une diminution du marqueur de surface CD11b, et par une augmentation de la production de l’enzyme ALOX15 (arachidonate 15-lipoxygénase) [10]. Nous avons constaté que l’injection préventive d’humanine chez les souris accélère l’émergence, dans le péritoine, de ces macrophages non-phagocytaires et prorésolutifs, qui présentent une expression accrue des gènes Alox15 et Retnla (Resistin-like α) [9] (Figure 2B).
La synthèse d’humanine peut être induite par de nombreux agents toxiques et dans diverses situations pathologiques inflammatoires, notamment en réponse au stress oxydant [8]. Chez des personnes souffrant de parodontite2, nous avons pu constater que la concentration d’humanine dans le fluide gingival est plus élevée durant la phase active de la maladie, après la phase d’induction de l’inflammation, qu’en période de rémission obtenue par un traitement mécanique non médicamenteux [9].
Ainsi, nos résultats confirment l’effet anti-inflammatoire de l’humanine et mettent en évidence son rôle actif dans la résolution de l’inflammation, en particulier par la modulation de l’activité des macrophages. Toutefois, plusieurs questions demeurent sans réponse, tant sur le contrôle de sa production, que sur la nature précise de ses effets selon le contexte tissulaire. Par ailleurs, d’autres isoformes de l’humanine, ainsi que d’autres mitokines, pourraient également contribuer à la modulation des réponses immunitaires et à la résolution de l’inflammation. Cela ouvre un nouveau champ de recherche, dans lequel la mitochondrie apparaît comme un acteur central.
Remerciements
Les travaux de recherche concernant la résolution de l’inflammation ont bénéficié d’une aide de l’État gérée par l’Agence nationale de la recherche (ANR) au titre du programme « Investissements d’avenir » (ANR-11-LABX-0021-01).
Conflits d’intérêt
Les auteurs déclarent qu’ils n’ont aucun conflit d’intérêt.
Références
- Vetter M, Saas P. « Fort comme la mort », ou comment l’efferocytose contrôle la résolution de l’inflammation. Med Sci (Paris) 2024 ; 40 : 428-36. [Google Scholar]
- Perretti M, Dalli J. Resolution pharmacology: Focus on pro-resolving annexin A1 and lipid mediators for therapeutic innovation in inflammation. Annu Rev Pharmacol Toxicol 2023 ; 63 : 449-69. [Google Scholar]
- Hashimoto Y, Niikura T, Tajima H, et al. A rescue factor abolishing neuronal cell death by a wide spectrum of familial Alzheimer’s disease genes and Ab. Proc Natl Acad Sci USA 2001 ; 98 : 6336-41. [Google Scholar]
- Li Y, Li Z, Ren Y, et al. Mitochondrial-derived peptides in cardiovascular disease: Novel insights and therapeutic opportunities. J Adv Res 2023 ; 64 : 99-115. [Google Scholar]
- Bodzioch M, Lapicka-Bodzioch K, Zapala B, et al. Evidence for potential functionality of nuclearly-encoded humanin isoforms. Genomics 2009 ; 94 : 247-56. [Google Scholar]
- Angers A, Ouimet P, Tsyvian-Dzyabko A, et al. L’ADN mitochondrial, un potentiel codant mésestimé. Med Sci (Paris) 2019 ; 35 : 46-54. [Google Scholar]
- Zhu S, Hu X, Bennett S, et al. The molecular structure and role of humanin in neural and skeletal diseases, and in tissue regeneration. Front Cell Dev Biol 2022 ; 10 : 823354. [Google Scholar]
- Cai H, Liu Y, Men H, et al. Protective mechanism of humanin against oxidative stress in aging-related cardiovascular diseases. Front Endocrinol 2021 ; 12 : 683151. [Google Scholar]
- Maraux M, Vetter M, Dal Zuffo L, et al. HUMANIN produced by human efferocytic macrophages promotes the resolution of inflammation. Cell Death Dis 2025 ; 16 : 656. [Google Scholar]
- Schif-Zuck S, Gross N, Assi S, et al. Saturated-efferocytosis generates pro-resolving CD11blow macrophages: modulation by resolvins and glucocorticoids. Eur J Immunol 2011 ; 41 : 366-79. [Google Scholar]
Nom dérivé du verbe latin efferre signifiant « emporter dans la tombe/enterrer ».
La parodontite désigne l’inflammation des tissus de soutien des dents, qui conduit à la formation d’une poche entre la gencive et la dent. Dans la plupart des cas, l’élimination mécanique des bactéries et du tartre fixés sur les racines permet à la gencive d’adhérer de nouveau à la dent. Ce traitement mécanique entraîne généralement une résolution spontanée de l’inflammation, sans nécessité d’un traitement anti-inflammatoire médicamenteux.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Différents mécanismes d’action de l’humanine. L’humanine est un peptide mitochondrial de 21 à 24 acides aminés, codé par une séquence nucléotidique située dans le gène de l’ARN ribosomique 16S (ARNr 16S) mitochondrial [3]. Il s’agit du premier membre identifié de la famille des MDP (mitochondria-derived peptides), un groupe de petits peptides produits par la mitochondrie en réponse à diverses agressions, et qui jouent un rôle clé dans la communication entre la mitochondrie et le reste de la cellule. L’humanine interagit avec différentes protéines, dont des acteurs pro-apoptotiques de la famille BCL-2 (notamment BAX, BAD et BIMEL) et IGFBP-3. Elle agit également en se liant à deux récepteurs : le récepteur FPR2 et un complexe tripartite formé des chaînes CNTFR, IL-27Rα et gp130. La stimulation des cellules par l’humanine déclenche plusieurs voies de signalisation, dépendant notamment de STAT3, ERK1/2, AMPK, PI3K/AKT, et conduit souvent à l’inhibition de NF-κB. Ces différents mécanismes contribuent aux effets cytoprotecteurs de l’humanine, incluant l’inhibition de l’apoptose, du stress oxydant, de l’inflammation, ainsi que la stimulation des défenses antioxydantes, de l’autophagie impliquant des protéines chaperonnes, et du métabolisme énergétique. ROS : reactive oxygen species ; CMA : chaperone-mediated autophagy ; OXPHOS : oxydation phosphorylante ; BAX : Bcl-2-associated protein x ; BID : BH3-interacting domain death agonist ; BIMEL : Bcl-2-interacting mediator of cell death extra long isoform ; IGFBP3 : insulin-like growth factor-binding protein 3 ; CNTFR : ciliary neurotrophic factor receptor ; IL-27Rα : interleukin-27 receptor α ; gp130 : glycoprotein 130 ; FPR2 : formyl peptide receptor-2 ; STAT3 : signal transducer and activator of transcription 3 ; ERK1/2 : extracellular signal-regulated kinase 1/2 ; AMPK : AMP-activated protein kinase ; PI3K/AKT : phosphoinositide 3-kinase/protein kinase B ; NF-κB : nuclear factor κB. |
| Dans le texte | |
 |
Figure 2 Rôles de l’humanine dans la résolution de l’inflammation. L’ingestion de cellules apoptotiques par les macrophages, ou efférocytose, constitue une étape clé du basculement de la phase aigüe de l’inflammation vers sa résolution. L’efférocytose reprogramme les macrophages inflammatoires, qui acquièrent alors des propriétés anti-inflammatoires, freinant la migration et l’activation des leucocytes et leur sécrétion de cytokines pro-inflammatoires, ainsi que des fonctions prorésolutives, favorisant l’apoptose des granulocytes neutrophiles résiduels, la reprogrammation d’autres macrophages, l’activation d’une immunité adaptative régulatrice, et la réparation des tissus endommagés. Les médiateurs prorésolutifs produits au cours de l’efférocytose sont divers, tant par leur nature que par leurs fonctions. Ils incluent des protéines (TGF-β, IL-10, annexine A1, DEL-1, etc.) et des lipides bioactifs, tels que les médiateurs lipidiques prorésolutifs (specialized pro-resolving mediators [SPM]). A. La synthèse d’humanine, un peptide d’origine mitochondriale, est induite dans les macrophages humains à la suite de l’ingestion de granulocytes neutrophiles apoptotiques. Ce peptide exerce un effet anti-inflammatoire sur les granulocytes neutrophiles humains stimulés par du lipopolysaccharide (LPS) bactérien en réduisant leur sécrétion de TNFα (tumor necrosis factor α). B. Dans un modèle murin de péritonite induite par le zymosane, un modèle d’inflammation à résolution spontanée, l’humanine est produite à la fin de la phase aigüe, période correspondant au déclenchement des processus prorésolutifs, après l’efférocytose. L’injection préventive d’humanine à ces souris diminue le recrutement des granulocytes neutrophiles et des monocytes dans le tissu enflammé, réduit la production de cytokines proinflammatoires, et favorise l’apparition précoce de macrophages prorésolutifs CD11blow « en satiété » (macrophages efférocytiques ayant perdu leur capacité à ingérer de nouvelles cellules apoptotiques). IL : interleukine. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




