| Numéro |
Med Sci (Paris)
Volume 29, Numéro 11, Novembre 2013
|
|
|---|---|---|
| Page(s) | 1026 - 1033 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/20132911020 | |
| Publié en ligne | 20 novembre 2013 | |
L’effet Warburg
De la théorie du cancer aux applications thérapeutiques en cancérologie
The Warburg effect: from theory to therapeutic applications in cancer
Institut de recherche en cancérologie de Montpellier, Inserm U896, 208, rue des Apothicaires, 34298 Montpellier, France
*
catherine.teyssier@inserm.fr
Le métabolisme des cellules cancéreuses décrit par Otto Warburg dans les années 1930 est devenu une marque spécifique associée au cancer, appelée « effet Warburg ». Les cellules cancéreuses puisent leur énergie essentiellement à partir du glucose, à travers la glycolyse, afin de répondre à leurs besoins en énergie, mais également à leur besoin en biomasse nécessaire à leur division accrue. Dans cette revue, nous décrivons les mécanismes responsables de l’effet Warburg au niveau moléculaire et cellulaire, ainsi que l’implication de voies de signalisation et de différents facteurs de transcription. Cause ou conséquence de la cancérogenèse, l’effet Warburg constitue une nouvelle cible thérapeutique prometteuse dans la lutte contre le cancer.
Abstract
Cancer cell metabolism described by Otto Warburg in the thirties became a cancer specific hallmark, also called “Warburg effect”. Cancer cells use essentially glucose as fuel, through glycolysis, in order to meet their energy and biomass needs to insure their cell proliferation. Recent advances describe Warburg effect regulation by oncogenes and tumor suppressor genes. Moreover, mutations in some glycolysis enzymes are found in various cancers, highlighting the role of cell metabolism in cancer. In this review, we describe the mechanisms responsible for the Warburg effect at the molecular and cellular level, the role of cell signalling along with the implication of different transcription factors. As a cause or a consequence of tumorigenesis, the Warburg effect is now considered as a promising therapeutic target in the fight against cancer.
© 2013 médecine/sciences – Inserm
Vignette (Photo © Inserm - Aurélie Chiche).
De la théorie à l’effet Warburg
Dans les années 1930, lors de ses observations sur des cellules cancéreuses, Otto H. Warburg (Figure 1) remarqua une concentration anormalement élevée d’ions lactate, l’un des sels de l’acide lactique. Or, cet acide est typiquement le résultat d’une fermentation du glucose. Cette glycolyse accrue engendre une respiration cellulaire défectueuse illustrée notamment par une diminution de l’oxydation du succinate, de l’effet Pasteur1 et d’une respiration découplée. Ayant démontré que les cellules cancéreuses changent leur métabolisme pour adopter un métabolisme anaérobie, Otto Warburg a aussi formulé l’hypothèse selon laquelle les cellules cancéreuses n’ont pas besoin d’un milieu riche en oxygène pour se développer. Warburg établit donc un postulat sur la formation, en deux phases, des cellules cancéreuses à partir des cellules normales : il se produit, d’abord, un dysfonctionnement irréversible de la respiration cellulaire dans les mitochondries qui entraîne une perte d’énergie fatale à certaines cellules, alors que d’autres s’adaptent à cette diminution d’énergie et modifient leur morphologie pour se dédifférencier et croître de manière anarchique [1]. Fort de ses résultats, Warburg va plus loin et au cours de son exposé à Lindau en 1966, lors de la conférence des lauréats des prix Nobel, il recommande des régimes riches en groupes activateurs des enzymes de la respiration (fer, riboflavine, nicotinamide, etc.) comme prévention et même traitement des cancers. Son style percutant et ses déclarations déclencheront une polémique en Europe. Cependant, malgré l’avancée considérable qu’ont suscité les travaux de Warburg, des pièces manquent au puzzle. Il faudra attendre les progrès de la biologie moléculaire et de la génétique pour que cette théorie se concrétise sous le nom d’effet Warburg. Cependant, plusieurs travaux ont prouvé que les mitochondries fonctionnent normalement dans les cellules cancéreuses et que le blocage de la phosphorylation oxydative constitue un événement adaptatif [2, 3].
 |
Figure 1. Otto H. Warburg. Otto Heinrich Warburg est né le 8 octobre 1883 à Fribourg-en-Brisgau en Allemagne. Il a étudié la chimie sous la direction d’Emil Fischer, et a obtenu le diplôme de docteur en chimie à Berlin en 1906. En 1911, il devient docteur en médecine à Heidelberg, et en 1918, il est nommé professeur à l’Institut Kaiser Wilhelm à Berlin. En 1931, il devient directeur du département de physiologie cellulaire de cet institut. O.H. Warburg était avant tout un pionnier dans la création de nouveaux outils de recherche. Il mettra au point de nombreuses méthodes d’analyses spectrophotométriques d’identification des constituants cellulaires et des enzymes, des méthodes manométriques pour l’étude du métabolisme des cellules, et des méthodes pour la purification des constituants cellulaires et pour la cristallisation des enzymes. Ses travaux sur la caractérisation de l’enzyme responsable de la respiration cellulaire, aujourd’hui connue comme la cytochrome-oxydase, lui valurent le prix Nobel de médecine en 1931. Sa carrière scientifique fut très prolifique et la liste de l’ensemble de ses découvertes est considérable. O.H. Warburg fut membre étranger de la Société royale de Londres (1934) et membre des Académies de Berlin, de La Halle, de Copenhague, de Rome, et d’Inde. Il fut décoré de l’Ordre du Mérite de la Grande Croix, et de l’étoile et du ruban d’épaule de la Bundesrepublik. En 1965, il est élu docteur honoris causa à l’université d’Oxford. Il décède en 1970 à l’âge de 87 ans |
En fait, Warburg n’avait pas démontré la cause principale du cancer, mais il avait identifié une des caractéristiques majeures liée à la transformation maligne qui suscitera d’innombrables travaux.
Les conséquences métaboliques de l’effet Warburg sur la prolifération tumorale
En présence d’oxygène, la plupart des cellules différenciées métabolisent le glucose en pyruvate dans le cytoplasme, puis en dioxyde de carbone au cours du cycle de Krebs dans le compartiment mitochondrial (Figure 2). Cette réaction permet une production maximale d’ATP et une production limitée de lactate (forme ionisée de l’acide lactique). Cette réaction n’est possible qu’en présence d’oxygène : c’est la glycolyse aérobie observée dans toutes les cellules saines. À l’inverse, la glycolyse anaérobie est utilisée par plusieurs types cellulaires afin d’approvisionner en lactate un autre type cellulaire à proximité, comme dans l’exemple du couplage métabolique entre astrocytes et neurones. Cette réaction convertit le glucose en acide lactique en absence d’oxygène, produisant ainsi de grandes quantités de lactate et peu d’ATP.
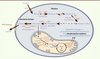 |
Figure 2. Glycolyse anaérobie et effet Warburg. Le glucose pénètre dans la cellule grâce aux transporteurs de glucose (GLUT). Il est ensuite métabolisé en pyruvate par une suite de réactions enzymatiques (étape 1 à 10 ). Les enzymes responsables des réactions irréversibles 1 , 3 , et 10 sont décrites dans le Tableau I. Lors de la phosphorylation oxydative, le pyruvate entre dans la mitochondrie où il est transformé en acétyl-CoA qui est dégradé dans le cycle de Krebs pour produire de l’énergie via la chaîne de transport des électrons de la membrane mitochondriale interne. Au cours de l’effet Warburg (flèches noires et rouges), le pyruvate est transformé en lactate qui est expulsé hors de la cellule par les transporteurs de monocarboxylate (MCT). Le lactate sécrété contribue alors à l’acidification extracellulaire locale. |
Les cellules en phase proliférative ont besoin de ressources énergétiques et organiques afin de reproduire les composants de la cellule (ADN, membranes, protéines). Le glucose est essentiel car, outre l’ATP, il fournit également les intermédiaires métaboliques qui participent aux réactions anaboliques. Dans le cas des cellules tumorales, la captation cellulaire de glucose et sa dégradation sont accrues, en l’absence ou en présence d’oxygène, pour permettre aux cellules de satisfaire la demande en dérivés glycosylés nécessaires à la prolifération cellulaire rapide [4]. La conversion du pyruvate en lactate par la lactate déshydrogénase A (LDHA) et l’expulsion du lactate par les transporteurs de monocarboxylate contribuent à l’acidification du milieu environnant. De plus, la production de lactate génère le NAD+, nécessaire au maintien de la glycolyse.
Les facteurs responsables de l’effet Warburg
Le contrôle enzymatique du métabolisme du glucose
Étape 1 : hexokinase (Hk)
Deux isoformes Hk1 et Hk2 sont décrites. Ainsi, si Hk1 est l’isoforme exprimée de manière dominante dans le tissu cérébral sain, Hk2 est l’isoforme prédominante dans les cancers. L’expression de Hk2 est surexprimée dans le glioblastome humain multiforme (GBM, tumeur cérébrale maligne la plus fréquente) et y est associée à un mauvais pronostic [5]. Des facteurs favorisant la croissance des GBM, tels que l’insuline, myc, le glucagon et l’AMPc modulent l’expression et l’activité de Hk2, mais n’ont aucun effet sur l’expression de Hk1 (Figure 3, Tableau I). La diminution de l’expression de Hk2 restaure le métabolisme oxydatif du glucose et augmente la sensibilité cellulaire à des inducteurs de mort cellulaire. De plus, une inhibition de l’expression de Hk2 dans des xénogreffes intracrâniennes de cellules de GBM entraîne une diminution de la prolifération et de l’angiogenèse, alors que leur capacité invasive augmente. À l’inverse, une surexpression de Hk2 dans les cellules de GBM induit une augmentation de la prolifération. Cette prolifération est dépendante de la phosphorylation du glucose induite par la voie de signalisation Akt (protéine kinase B)-PI3K (phosphatidylinositol 3-kinase) [6].
 |
Figure 3. Les multiples points de contrôle de l’effet Warburg. De nombreux effecteurs vont contrôler la cascade de la glycolyse. Les oncogènes Akt, Ras et Myc vont favoriser cette voie métabolique, tout comme la kinase AMPK et les récepteurs nucléaires orphelins ERRα et ERRγ, le facteur HIF1α et les facteurs E2F. De nombreuses synergies existent, par exemple entre Myc et HIF1α, ou entre ERR et Myc, ou encore entre HIF1α et p53, ajoutant une complexité supplémentaire à la régulation de l’effet Warburg. À l’inverse, le gène suppresseur de tumeur p53 inhibe la voie en agissant de manière indirecte via le contrôle de l’expression de GLUT3 par la voie NF-κB, via le contrôle de la respiration mitochondriale (SCO2) ou encore via le contrôle de l’expression de TIGAR, un inhibiteur de la fructose 2,6-bisphosphate. De plus, différents miARN participent également à la régulation de la glycolyse en interagissant avec les différents facteurs de transcription impliqués. Les étapes 1 , 3 et 10 sont irréversibles. HK : hexokinase ; GPI : glucose phosphoisomérase ; PFK : phosphofructokinase ; ALD : aldolase ; TPI : triose phosphoisomérase ; DH : déshydrogénase ; PGK : phosphoglycérate kinase ; PGM : phosphoglycérate mutase ; ENO : énolase ; PK : pyruvate kinase ; PDH : pyruvate déshydrogénase ; LDH : lactate déshydrogénase ; SCO : synthesis of cytochrome c oxidase ; TIGAR : TP53-induced glycolysis regulator ; HIF1α : hypoxia inducible factor 1α ; PDK : pyruvate déshydrogénase kinase ; AMPK : AMP-activated protein kinase ; OxPhos : oxydative phosphorylation. |
Les enzymes importantes de la glycolyse.
Étape 2 : phosphofructokinase-2 (PFK-2)
L’ARNm codant pour l’isoforme PFK-2 contient de nombreuses répétitions d’un motif instable : AUUUA au niveau de l’extrémité 3’ non traduite du brin (3’UTR) [7]. Ce motif est généralement retrouvé dans des gènes de réponse précoce qui codent pour des protéines, comme des cytokines inflammatoires ou des proto-oncogènes, qui répondent à des stimulus extracellulaires, comme des facteurs de croissance ou des neurotransmetteurs. En effet, l’expression de l’isoenzyme PFK-2 est induite par une réaction pro-inflammatoire. PFK-2 est exprimée dans plusieurs lignées de cellules cancéreuses et elle est nécessaire à la croissance des cellules tumorales in vitro et in vivo. Lorsque l’expression de l’isoenzyme PFK-2 est inhibée, le taux intracellulaire de 5-phosphoribosyl-1-pyrophosphate (produit de la voie des pentoses et précurseur important pour la biosynthèse des bases puriques et pyrimidiques) diminue. En effet, le glucose est à la fois un substrat pour la production d’énergie et pour les précurseurs nécessaires à la synthèse des acides nucléiques via la voie des pentoses. L’isoforme PFK-2 semble donc établir un lien entre la glycolyse aérobie et la prolifération cellulaire accrue des cellules cancéreuses (Figure 3, Tableau I).
Pyruvate kinase isoenzyme type M2 (PKM2)
L’isoenzyme PKM2 est trouvée dans les cellules indifférenciées et les cellules cancéreuses, contrairement à l’isoenzyme M1 (PKM1), normalement exprimée dans des cellules différenciées. Les deux isoformes sont issues de l’épissage alternatif d’un gène unique PKM. Ce gène PKM contient douze exons, le neuvième exon étant spécifique de l’isoforme PKM1 et le dixième de l’isoforme PKM2 [8]. Au cours de l’épissage alternatif dans les cellules cancéreuses, l’exon 9 est éliminé favorisant l’expression de l’isoforme PKM2, supprimant la production de l’isoforme PKM1 et permettant un gain d’énergie, non plus par la respiration cellulaire, mais via l’effet Warburg [9]. En effet, PKM2 contribue à la croissance des cellules tumorales en réduisant le flux de carbone à travers la voie catabolique et en déviant les intermédiaires de la glycolyse en amont vers les voies anaboliques, ce qui facilite la synthèse d’acides nucléiques et de composés nécessaires à la prolifération cellulaire [10] (Figure 3, Tableau I).
Les voies de signalisation impliquées
Akt
La sérine/thréonine kinase Akt, un effecteur en aval de la signalisation de la PI3K, transmet les signaux émanant de facteurs de croissance et contrôlant la survie des cellules. L’activation d’Akt est observée fréquemment dans les cellules cancéreuses du fait des mutations du gène codant pour PTEN, une phosphatase dont le substrat principal est la PIP3 (phosphatidylinositol 3,4,5-triphosphate). Cependant, le maintien de l’activation de la kinase Akt n’augmente pas la prolifération de cellules cancéreuses en culture mais affecte leur glycolyse en présence d’oxygène. En effet, Akt stimule la consommation de glucose sans modifier le taux de phosphorylation oxydative. De plus, les cellules exprimant Akt deviennent dépendantes du glucose pour proliférer [11]. Les effets d’Akt sur la croissance et la prolifération cellulaires sont étroitement liés à son impact sur le métabolisme énergétique, notamment à travers le contrôle de l’activation de mTORC1 (complex mammalian target of rapamycin 1), un senseur d’ATP [12]. De plus, en réponse à des stimulus métaboliques (insuline) ou oncogéniques (Ras), Akt activée entraîne une augmentation de l’expression et de la distribution du transporteur de glucose GLUT1 à la membrane [13].
Ras
L’oncogène Ras, muté dans plus de 35 % des tumeurs, induit une expression accrue de plusieurs gènes impliqués dans l’effet Warburg, comme par exemple le gène codant pour la LDHA (lactate déshydrogénase A) [14]. Les cellules transformées par le mutant K-Ras présentent plusieurs désordres métaboliques, comme une augmentation de la captation du glucose, de la glycolyse et de la production d’acide lactique, ainsi qu’un dysfonctionnement mitochondrial. De plus, le potentiel prolifératif des cellules transformées par K-Ras requiert une forte concentration en glucose et en glutamine dans le milieu de culture [15].
AMP-activated protein kinase (AMPK)
Le senseur métabolique AMPK est activé par phosphorylation par la sérine-thréonine kinase LKB1 lors d’une diminution de la concentration intracellulaire d’ATP (augmentation du ratio AMP/ATP) [42]. L’activation de cascades de signalisation qui en résulte aboutit, entre autres, à la régulation du métabolisme mitochondrial via l’inhibition de mTOR. Dans certains cancers, l’AMPK participe également à la régulation de l’effet Warburg lorsqu’il existe des mutations de la kinase LBK1 qui bloquent les fonctions d’AMPK et de ses cibles en aval. En effet, son inactivation entraîne une augmentation de la glycolyse aérobie (l’effet Warburg), une augmentation de la croissance tumorale et la transformation du glucose en lipides. Ces effets nécessitent la stabilisation de HIF1α (hypoxia inducible factor 1α) en conditions de normoxie et contribuent à la lymphogenèse induite par Myc [16].
Les régulations transcriptionnelles
Hypoxia inducible factor 1α (HIF1α)
Les tumeurs solides présentent une déprivation en oxygène conduisant au phénomène d’hypoxie qui active le régulateur sensible à l’oxygène HIF1α. Ce régulateur est un facteur de transcription impliqué dans la régulation de l’expression de nombreux gènes qui contrôlent différentes fonctions cellulaires, comme l’angiogenèse, la survie et l’invasion cellulaires, ainsi que le métabolisme. L’équipe de J. Pouysségur a décrit en détail l’implication de HIF1α dans la progression tumorale en réponse à l’hypoxie [17]. HIF1α augmente l’expression des enzymes de la glycolyse, comme la 6-phosphofructo-2-kinase/fructose-2,6-bisphosphatase-3 (PFKFB3), l’aldolase A ou encore GLUT3. Cependant, l’expression de HIF1α peut être induite en conditions de normoxie par la glycolyse aérobie [18].
Myc
De nombreux gènes impliqués dans la dégradation du glucose en pyruvate et, finalement, en lactate, sont des cibles directes de l’oncogène Myc. Parmi ces gènes, on trouve la LDHA, le transporteur de glucose GLUT1, Hk2, la phosphofructokinase et l’énolase 1 (ENO1) [19]. Par ailleurs, Myc induit la dégradation de la glutamine en stimulant l’expression de la glutaminase, qui transforme la glutamine en glutamate. Ce dernier peut, soit être excrété, soit rentrer dans le cycle de Krebs où il est transformé en α-cétoglutarate. Les cellules exprimant l’oncogène Myc deviennent dépendantes de la glutamine et entrent en apoptose quand ce composé est retiré du milieu de culture [20]. Myc favorise donc la glycolyse et la dégradation de la glutamine des cellules cancéreuses, leur conférant ainsi une dépendance énergétique.
p53
Le facteur de transcription p53, considéré comme « gardien du génome », contribue à la stabilité génomique en induisant l’arrêt du cycle cellulaire et la mort cellulaire après des dommages à l’ADN. En plus de cette fonction de gène suppresseur de tumeur, p53 participe à la régulation du métabolisme [21, 43]. En effet, p53 contrôle négativement la glycolyse en activant l’expression de TIGAR (TP53-induced glycolysis regulator), qui réduit le niveau du fructose-2,6-bisphosphate intracellulaire [22]. De plus, p53 réduit le taux de glucose intracellulaire en inhibant l’expression des transporteurs du glucose GLUT1 et GLUT4 [23]. L’inactivation de p53 induit l’activation de la voie NF-κB, la surexpression de GLUT3 et donc l’accélération de la glycolyse aérobie [24]. Ces résultats suggèrent que les mutations de p53 associées à un caractère malin favoriseraient la croissance tumorale par un apport constant d’énergie. La protéine p53 régule également la respiration mitochondriale en induisant l’expression de SCO2 (synthesis of cytochrome c oxidase). Les cellules cancéreuses colorectales HCT116 p53-/- présentent un déficit respiratoire mitochondrial que corrige la surexpression de SCO2 [25]. Par ailleurs, p53 est également capable d’inhiber l’expression de la pyruvate kinase déshydrogénase 2 (pdk2), impliquée dans la conversion du pyruvate en acétyl-CoA, favorisant ainsi la production de ce dernier [26]. L’inactivation de p53 pourrait promouvoir la tumorigenèse en diminuant la dépendance cellulaire à l’oxygène et en permettant la croissance dans des conditions d’hypoxie. Cependant, les effets de p53 dépendent de son niveau d’expression et/ou d’activation, ce qui explique la complexité du contrôle, par p53, des différentes voies métaboliques.
Les facteurs E2F
Les facteurs E2F apparaissent impliqués dans le contrôle de l’expression de nombreux gènes du métabolisme des adipocytes [27]. La phosphorylation des protéines à poche pRb (retinoblastoma protein) induite par les Cdk (cyclin-dependent protein kinase) libère les complexes transcriptionnels E2F qui peuvent alors induire l’expression de gènes nécessaires à la progression du cycle cellulaire. L’activité des facteurs E2F étant augmentée dans de nombreux cancers humains (glioblastomes, et cancers du poumon, de l’ovaire, du sein, de l’estomac et du côlon) [28], on peut imaginer qu’elle touche également le métabolisme des cellules cancéreuses. En effet, E2F1 peut activer l’expression du gène codant pour la luciférase placé sous le contrôle du promoteur pdk2 (pyruvate dehydrogenase kinase, isozyme 2), cette activation étant réprimée par p53 [26]. E2F1 est aussi capable de réguler l’expression du gène pdk4 [29]. Ces résultats suggèrent que les facteurs E2F1 favoriseraient la production de lactate en inhibant les PDK et en entraînant l’inhibition du complexe de la pyruvate déshydrogénase. On peut imaginer que les autres facteurs E2F participent également à la régulation du métabolisme des cellules cancéreuses.
Les récepteurs nucléaires ERR
Les ERR (estrogen receptor-related receptor) sont des récepteurs nucléaires orphelins qui contrôlent le métabolisme énergétique en orchestrant la biogenèse mitochondriale et l’oxydation des acides gras. ERRα et ERRγ contrôlent l’expression de nombreuses enzymes de la glycolyse en se fixant sur le promoteur des gènes correspondants. Les ERR activent la transcription des gènes codant pour ces enzymes de manière synergique avec Myc. À l’inverse, l’inhibition de l’expression des ERR dans les cellules cancéreuses réduit la prise de glucose, entraînant une diminution de l’effet Warburg et de la croissance cellulaire [30].
Les miARN
Les miARN sont des ARN non codants, courts et endogènes, qui inhibent la traduction de leurs transcrits cibles. Ils sont considérés comme des régulateurs essentiels de nombreux processus physiologiques, et des dérégulations de leur expression participent à des processus pathologiques. Les miARN participent à l’effet Warburg en régulant l’expression de facteurs tels que HIF1α, p53 ou Myc. Ainsi, miR-23a/b cible Myc et intervient par ce biais dans la régulation de l’expression de la glutaminase mitochondriale dans des lymphomes humains et dans des cellules cancéreuses de la prostate [31]. Mais ils peuvent également contrôler directement l’expression des gènes du métabolisme. Le miR-378∗ inhibe l’expression des gènes cibles de ERRα, induisant une inhibition de la consommation d’oxygène et une augmentation de la production d’acide lactique et de la prolifération cellulaire dans des cellules cancéreuses mammaires [32]. Les miR-155 et miR-143 contrôlent l’expression de Hk2 dans des cellules cancéreuses mammaires [31].
Les applications thérapeutiques de l’effet Warburg
Les caractéristiques métaboliques des cellules cancéreuses ont permis la mise au point de la technique de tomographie par émission de positons (TEP) au 2-(18)fluoro-2-déoxyglucose (18F-FDG), utilisée pour la détection des tumeurs. Le 18F-FDG se comporte comme le glucose mais, contrairement à celui-ci, il n’est pas une source d’énergie utilisable par la cellule. Le 18F-FDG est phosphorylé, ce qui l’empêche de ressortir de la cellule. En accumulant le 18F-FDG, la cellule émet des rayonnements qui peuvent être détectés à l’aide d’une caméra TEP. Le tissu cancéreux est ainsi localisé sous la forme d’une image d’hyperfixation [33].
Les impacts de l’effet Warburg sur la prolifération des cellules tumorales font de ce mécanisme une cible thérapeutique intéressante. Bloquer l’apport énergétique des cellules cancéreuses pourrait provoquer leur mort en inhibant leur reprogrammation métabolique [34]. Ainsi, un inhibiteur de GLUT1 provoque l’arrêt du cycle cellulaire et inhibe la croissance des cellules cancéreuses en diminuant le taux d’ATP intracellulaire. Un inhibiteur de la PFKFB3, qui induit la mort cellulaire, ou des molécules activatrices de PKM2, qui diminuent la tumorigenèse, constituent également des pistes thérapeutiques prometteuses. La toxicité de ces molécules sur le métabolisme des cellules normales en phase proliférative peut cependant limiter leur utilisation [35]. Des essais cliniques étudiant l’efficacité de la metformine dans le traitement de différents cancers sont en cours [43] (→). La metformine est utilisée dans le traitement du diabète de type 2 pour son blocage de la gluconéogenèse via la voie LKB1 (liver kinase B1)/AMPK [36]. Par ailleurs, des analyses globales du métabolome des cellules cancéreuses ont contribué à la caractérisation d’oncométabolites comme le 2-hydroxyglutarate et le fumarate, qui pourraient être considérés comme des biomarqueurs diagnostiques et/ou pronostiques [2].
(→) Voir aussi la Synthèse de M. Foretz et B. Viollet, m/s 2013 (sous presse)
Les autres voies métaboliques dans la cancérogenèse
L’effet Warburg apparaît maintenant comme la partie émergée de l’iceberg représentant les voies métaboliques dérégulées dans la cancérogenèse. En effet, d’autres voies sont impliquées comme, notamment, celle des pentoses phosphates. Afin de répondre aux besoins élevés en biosynthèse de nucléotides, les cellules néoplasiques dérivent le flux glycolytique vers la branche non oxydative de la voie des pentoses phosphates pour produire le ribose-5-phosphate [37]. La synthèse de novo d’acides gras facilite la production de lipides qui régulent l’activité de différents oncogènes. Par exemple, la voie de signalisation des lipides, tels que le phosphatidylinositol, la phosphatidylsérine ou la phosphatidylcholine activent les voies de prolifération et de survie, notamment les voies PI3K/Akt et Ras. La synthèse de novo d’acides gras dans les cellules cancéreuses est marquée par l’expression et l’hyperactivité des enzymes lipogéniques, telles que l’ATP citrate lyase, l’acétyl-CoA carboxylase, ou l’acide gras synthase (FAS). Des expériences utilisant des inhibiteurs chimiques de l’activité de FAS ont montré une diminution de la prolifération cellulaire et une augmentation de l’apoptose des cellules cancéreuses [38]. Le métabolisme de la glutamine, de la sérine et de la glycine est aussi impliqué dans la prolifération tumorale, et les effecteurs de ces voies pourraient constituer des cibles thérapeutiques intéressantes [2]. D’autres voies métaboliques impliquées dans la cancérogenèse restent sans doute à identifier.
Conclusion : l’effet Warburg, cause ou conséquence de la carcinogenèse ?
Les oncogènes sont responsables des changements métaboliques observés dans les cellules cancéreuses, transformations métaboliques qui contribuent à une prolifération soutenue de ces cellules, ainsi qu’au maintien de l’activité des oncogènes, créant ainsi une boucle de rétrocontrôle positif. Cependant, les enzymes métaboliques peuvent être elles-mêmes responsables de la croissance cellulaire tumorale [42]. Par exemple, les mutations activatrices de l’isocitrate déshydrogénase 1 dans des glioblastomes humains suggèrent que le contrôle métabolique est un élément clé de la carcinogenèse [3]. De même, PKM2 exerce un contrôle direct sur la progression du cycle cellulaire en activant la β-caténine et participe ainsi à l’activation de la tumorigenèse induite par le facteur de croissance épidermique (EGF) [39].
Par ailleurs, les métabolites, tels que le NAD+ et l’acétyl-CoA, produits en excès par une glycolyse accrue, influencent également l’activité d’enzymes responsables de modifications épigénétiques de la chromatine. Ces enzymes participent à la régulation de l’expression des gènes et une modification de leur activité peut entraîner des désordres de la prolifération cellulaire [40]. Ainsi, des liens entre composés métaboliques et régulations épigénétiques émergent de plus en plus. L’invalidation du gène codant pour la sirtuine 6 (SIRT6) induit un effet Warburg et la transformation des cellules, renforçant l’hypothèse d’un rôle causal de l’effet Warburg dans la tumorigenèse [41].
L’hétérogénéité génétique et phénotypique des tumeurs conduit à ce que des cellules au sein d’une même tumeur expriment des signatures métaboliques différentes. Par exemple, 30 % des cancers ne sont pas détectés par la technique 18FDG-PET, soit parce que leur utilisation du glucose se situe sous le seuil de détection, soit parce que ces tumeurs utilisent des voies métaboliques non glucidiques pour générer leur énergie. La réponse métabolique d’une cellule tumorale dépend à la fois de mutations d’oncogènes et/ou de suppresseurs de tumeurs, ainsi que du contexte environnemental. La caractérisation des différentes voies métaboliques mises en jeu lors du développement et de la progression de la tumeur est donc nécessaire à l’élaboration de thérapies efficaces.
« L’oxygène joue un rôle important dans la régulation de la glycolyse des cellules pourvues de mitochondries. La respiration, en fournissant l’oxygène à la chaîne respiratoire, permet la création d’un gradient chimio-osmotique à travers la membrane interne de la mitochondrie. Ce gradient favorise l’entrée du pyruvate dans la mitochondrie où il sera le substrat des enzymes de la glycolyse aérobie dont le rendement en ATP est très supérieur à celui de la glycolyse anaérobie. Ce rendement permettra donc une grande économie de glucose, et donc le ralentissement de la glycolyse cytoplasmique, qui définit l’effet Pasteur » (Source : cours université Pierre et Marie Curie, http://www.chups.jussieu.fr).
Références
- Warburg O. On the origin of cancer cells. Science 1956 ; 123 : 309–314. [CrossRef] [PubMed] [Google Scholar]
- Ward PS, Thompson CB. Metabolic reprogramming : a cancer hallmark even Warburg did not anticipate. Cancer Cell 2012 ; 21 : 297–308. [CrossRef] [PubMed] [Google Scholar]
- Dang CV. Links between metabolism and cancer. Genes Dev 2012 ; 26 : 877–890. [CrossRef] [PubMed] [Google Scholar]
- Vander Heiden MG, Cantley LC, Thompson CB. Understanding the Warburg effect : the metabolic requirements of cell proliferation. Science 2009 ; 324 : 1029–1033. [CrossRef] [PubMed] [Google Scholar]
- Wolf A, Agnihotri S, Micallef J, et al. Hexokinase 2 is a key mediator of aerobic glycolysis and promotes tumor growth in human glioblastoma multiform. J Exp Med 2011 ; 208 : 313–326. [CrossRef] [PubMed] [Google Scholar]
- Gottlob K, Majewski N, Kennedy S, et al. Inhibition of early apoptotic events by Akt/PKB is dependent on the first committed step of glycolysis and mitochondrial hexokinase. Genes Dev 2001 ; 15 : 1406–1418. [CrossRef] [PubMed] [Google Scholar]
- Chesney J, Mitchell R, Benigni F, et al. An inducible gene product for 6-phosphofructo-2-kinase with an AU-rich instability element : role in tumor cell glycolysis and the Warburg effect. Proc Natl Acad Sci USA 1999 ; 96 : 3047–3052. [CrossRef] [Google Scholar]
- Christofk HR, Vander Heiden MG, Harris MH, et al. The M2 splice isoform of pyruvate kinase is important for cancer metabolism and tumour growth. Nature 2008 ; 452 : 230–233. [CrossRef] [PubMed] [Google Scholar]
- David CJ, Chen M, Assanah M, et al. HnRNP proteins controlled by c-Myc deregulate pyruvate kinase mRNA splicing in cancer. Nature 2010 ; 463 : 364–368. [CrossRef] [PubMed] [Google Scholar]
- Wang Z, Jeon HY, Rigo F, et al. Manipulation of PK-M mutually exclusive alternative splicing by antisense oligonucleotides. Open Biol 2012 ; 2 : 120133. [CrossRef] [PubMed] [Google Scholar]
- Elstrom RL, Bauer DE, Buzzai M, et al. Akt stimulates aerobic glycolysis in cancer cells. Cancer Res 2004 ; 64 : 3892–3899. [CrossRef] [PubMed] [Google Scholar]
- Robey RB, Hay N. Is Akt the Warburg kinase? Akt-energy metabolism interactions and oncogenesis. Semin Cancer Biol 2009 ; 19 : 25–31. [CrossRef] [PubMed] [Google Scholar]
- Wofford JA, Wieman HL, Jacobs SR, et al. IL-7 promotes Glut1 trafficking and glucose uptake via STAT5-mediated activation of Akt to support T-cell survival. Blood 2008 ; 111 : 2101–2111. [CrossRef] [PubMed] [Google Scholar]
- Chiaradonna F, Sacco E, Manzoni R, et al. Ras-dependent carbon metabolism and transformation in mouse fibroblasts. Oncogene 2006 ; 25 : 5391–404. [CrossRef] [PubMed] [Google Scholar]
- Yun J, Rago C, Cheong I, et al. Glucose deprivation contributes to the development of KRAS pathway mutations in tumor cells. Science 2009 ; 325 : 1555–1559. [CrossRef] [PubMed] [Google Scholar]
- Faubert B, Boily G, Izreig S, et al. AMPK is a negative regulator of the Warburg effect and suppresses tumor growth in vivo. Cell Metab 2013 ; 17 : 113–124. [CrossRef] [PubMed] [Google Scholar]
- Brahimi-Horn C, Pouyssegur J. The role of the hypoxia-inducible factor in tumor metabolism growth and invasion. Bull Cancer 2006 ; 93 : E73–E80. [PubMed] [Google Scholar]
- Lu H, Forbes RA, Verma A. Hypoxia-inducible factor 1 activation by aerobic glycolysis implicates the Warburg effect in carcinogenesis. J Biol Chem 2002 ; 277 : 23111–23115. [CrossRef] [PubMed] [Google Scholar]
- Dang CV, Le A, Gao P. MYC-induced cancer cell energy metabolism and therapeutic opportunities. Clin Cancer Res 2009 ; 15 : 6479–6483. [CrossRef] [PubMed] [Google Scholar]
- Yuneva M, Zamboni N, Oefner P, et al. Deficiency in glutamine but not glucose induces MYC-dependent apoptosis in human cells. J Cell Biol 2007 ; 178 : 93–105. [CrossRef] [PubMed] [Google Scholar]
- Shen L, Sun X, Fu Z, et al. The fundamental role of the p53 pathway in tumor metabolism and its implication in tumor therapy. Clin Cancer Res 2012 ; 18 : 1561–1567. [CrossRef] [PubMed] [Google Scholar]
- Bensaad K, Tsuruta A, Selak MA, et al. TIGAR, a p53-inducible regulator of glycolysis and apoptosis. Cell 2006 ; 126 : 107–120. [CrossRef] [PubMed] [Google Scholar]
- Schwartzenberg-Bar-Yoseph F, Armoni M, Karnieli E. The tumor suppressor p53 down-regulates glucose transporters GLUT1 and GLUT4 gene expression. Cancer Res 2004 ; 64 : 2627–2633. [CrossRef] [PubMed] [Google Scholar]
- Kawauchi K, Araki K, Tobiume K, et al. p53 regulates glucose metabolism through an IKK-NF-kappaB pathway and inhibits cell transformation. Nat Cell Biol 2008 ; 10 : 611–618. [CrossRef] [PubMed] [Google Scholar]
- Matoba S, Kang JG, Patino WD, et al. p53 regulates mitochondrial respiration. Science 2006 ; 312 : 1650–1653. [CrossRef] [PubMed] [Google Scholar]
- Contractor T, Harris CR. p53 negatively regulates transcription of the pyruvate dehydrogenase kinase Pdk2. Cancer Res 2012 ; 72 : 560–567. [CrossRef] [PubMed] [Google Scholar]
- Lagarrigue S, Blanchet E, Annicotte JS, et al. Le double jeu des régulateurs du cycle cellulaire. Med Sci (Paris) 2011 ; 27 : 508–513. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Chen HZ, Tsai SY. Leone G Emerging roles of E2Fs in cancer : an exit from cell cycle control. Nat Rev Cancer 2009 ; 9 : 785–797. [CrossRef] [PubMed] [Google Scholar]
- Hsieh MC, Das D, Sambandam N, et al. Regulation of the PDK4 isozyme by the Rb-E2F1 complex. J Biol Chem 2008 ; 283 : 27410–27417. [CrossRef] [PubMed] [Google Scholar]
- Cai Q, Lin T, Kamarajugadda S, et al. Regulation of glycolysis and the Warburg effect by estrogen-related receptors. Oncogene 2013 ; 32 : 2079–2086. [CrossRef] [PubMed] [Google Scholar]
- Gao P, Sun L, He X, et al. MicroRNAs and the Warburg effect : new players in an old arena. Curr Gene Ther 2012 ; 12 : 285–291. [CrossRef] [PubMed] [Google Scholar]
- Eichner LJ, Perry MC, Dufour CR, et al. miR-378* mediates metabolic shift in breast cancer cells via the PGC-1beta/ERRgamma transcriptional pathway. Cell Metab 2010 ; 12 : 352–361. [CrossRef] [PubMed] [Google Scholar]
- Gatenby RA, Gillies RJ. Why do cancers have high aerobic glycolysis? Nat Rev Cancer 2004 ; 4 : 891–899. [Google Scholar]
- Terret C, Solari F. L’homéostasie métabolique au cœur du vieillissement. Med Sci (Paris) 2012 ; 28 : 311–315. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Vander Heiden MG Targeting cancer metabolism : a therapeutic window opens. Nat Rev Drug Discov 2011 ; 10 : 671–684. [CrossRef] [PubMed] [Google Scholar]
- Foretz M, Viollet B. Mécanisme d’inhibition de la production hépatique de glucose par la metformine. Med Sci (Paris) 2010 ; 26 : 663–666. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Tong X, Zhao F, Thompson CB. The molecular determinants of de novo nucleotide biosynthesis in cancer cells. Curr Opin Genet Dev 2009 ; 19 : 32–37. [CrossRef] [PubMed] [Google Scholar]
- Kuhajda FP. Fatty-acid synthase and human cancer : new perspectives on its role in tumor biology. Nutrition 2000 ; 16 : 202–208. [CrossRef] [PubMed] [Google Scholar]
- Yang W, Xia Y, Ji H, et al. Nuclear PKM2 regulates beta-catenin transactivation upon EGFR activation. Nature 2011 ; 480 : 118–122. [CrossRef] [PubMed] [Google Scholar]
- Lu C, Thompson CB. Metabolic regulation of epigenetics. Cell Metab 2012 ; 16 : 9–17. [CrossRef] [PubMed] [Google Scholar]
- Sebastian C, Zwaans BM, Silberman DM, et al. The histone deacetylase SIRT6 is a tumor suppressor that controls cancer metabolism. Cell 2012 ; 151 : 1185–1199. [CrossRef] [PubMed] [Google Scholar]
- Foretz M, Taleux N, Guigas B, et al. Régulation du métabolisme par l’AMPK : une nouvelle voie thérapeutique pour le traitement des maladies métaboliques et cardiaques. Med Sci (Paris) 2006 ; 22 : 381–388. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Foretz M, Viollet B. Les nouvelles promesses de la metformine : vers une meilleure compréhension de ses mécanismes d’action. Med Sci (Paris) 2013 ; 29 (sous presse). [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1. Otto H. Warburg. Otto Heinrich Warburg est né le 8 octobre 1883 à Fribourg-en-Brisgau en Allemagne. Il a étudié la chimie sous la direction d’Emil Fischer, et a obtenu le diplôme de docteur en chimie à Berlin en 1906. En 1911, il devient docteur en médecine à Heidelberg, et en 1918, il est nommé professeur à l’Institut Kaiser Wilhelm à Berlin. En 1931, il devient directeur du département de physiologie cellulaire de cet institut. O.H. Warburg était avant tout un pionnier dans la création de nouveaux outils de recherche. Il mettra au point de nombreuses méthodes d’analyses spectrophotométriques d’identification des constituants cellulaires et des enzymes, des méthodes manométriques pour l’étude du métabolisme des cellules, et des méthodes pour la purification des constituants cellulaires et pour la cristallisation des enzymes. Ses travaux sur la caractérisation de l’enzyme responsable de la respiration cellulaire, aujourd’hui connue comme la cytochrome-oxydase, lui valurent le prix Nobel de médecine en 1931. Sa carrière scientifique fut très prolifique et la liste de l’ensemble de ses découvertes est considérable. O.H. Warburg fut membre étranger de la Société royale de Londres (1934) et membre des Académies de Berlin, de La Halle, de Copenhague, de Rome, et d’Inde. Il fut décoré de l’Ordre du Mérite de la Grande Croix, et de l’étoile et du ruban d’épaule de la Bundesrepublik. En 1965, il est élu docteur honoris causa à l’université d’Oxford. Il décède en 1970 à l’âge de 87 ans |
| Dans le texte | |
 |
Figure 2. Glycolyse anaérobie et effet Warburg. Le glucose pénètre dans la cellule grâce aux transporteurs de glucose (GLUT). Il est ensuite métabolisé en pyruvate par une suite de réactions enzymatiques (étape 1 à 10 ). Les enzymes responsables des réactions irréversibles 1 , 3 , et 10 sont décrites dans le Tableau I. Lors de la phosphorylation oxydative, le pyruvate entre dans la mitochondrie où il est transformé en acétyl-CoA qui est dégradé dans le cycle de Krebs pour produire de l’énergie via la chaîne de transport des électrons de la membrane mitochondriale interne. Au cours de l’effet Warburg (flèches noires et rouges), le pyruvate est transformé en lactate qui est expulsé hors de la cellule par les transporteurs de monocarboxylate (MCT). Le lactate sécrété contribue alors à l’acidification extracellulaire locale. |
| Dans le texte | |
 |
Figure 3. Les multiples points de contrôle de l’effet Warburg. De nombreux effecteurs vont contrôler la cascade de la glycolyse. Les oncogènes Akt, Ras et Myc vont favoriser cette voie métabolique, tout comme la kinase AMPK et les récepteurs nucléaires orphelins ERRα et ERRγ, le facteur HIF1α et les facteurs E2F. De nombreuses synergies existent, par exemple entre Myc et HIF1α, ou entre ERR et Myc, ou encore entre HIF1α et p53, ajoutant une complexité supplémentaire à la régulation de l’effet Warburg. À l’inverse, le gène suppresseur de tumeur p53 inhibe la voie en agissant de manière indirecte via le contrôle de l’expression de GLUT3 par la voie NF-κB, via le contrôle de la respiration mitochondriale (SCO2) ou encore via le contrôle de l’expression de TIGAR, un inhibiteur de la fructose 2,6-bisphosphate. De plus, différents miARN participent également à la régulation de la glycolyse en interagissant avec les différents facteurs de transcription impliqués. Les étapes 1 , 3 et 10 sont irréversibles. HK : hexokinase ; GPI : glucose phosphoisomérase ; PFK : phosphofructokinase ; ALD : aldolase ; TPI : triose phosphoisomérase ; DH : déshydrogénase ; PGK : phosphoglycérate kinase ; PGM : phosphoglycérate mutase ; ENO : énolase ; PK : pyruvate kinase ; PDH : pyruvate déshydrogénase ; LDH : lactate déshydrogénase ; SCO : synthesis of cytochrome c oxidase ; TIGAR : TP53-induced glycolysis regulator ; HIF1α : hypoxia inducible factor 1α ; PDK : pyruvate déshydrogénase kinase ; AMPK : AMP-activated protein kinase ; OxPhos : oxydative phosphorylation. |
| Dans le texte | |
Les statistiques affichées correspondent au cumul d'une part des vues des résumés de l'article et d'autre part des vues et téléchargements de l'article plein-texte (PDF, Full-HTML, ePub... selon les formats disponibles) sur la platefome Vision4Press.
Les statistiques sont disponibles avec un délai de 48 à 96 heures et sont mises à jour quotidiennement en semaine.
Le chargement des statistiques peut être long.




