| Issue |
Med Sci (Paris)
Volume 29, Number 8-9, Août–Septembre 2013
|
|
|---|---|---|
| Page(s) | 715 - 721 | |
| Section | Diabète : approches thérapeutiques émergentes | |
| DOI | https://doi.org/10.1051/medsci/2013298009 | |
| Published online | 05 September 2013 | |
Les récepteurs membranaires des acides gras de la cellule β
De nouvelles cibles thérapeutiques pour le traitement du diabète de type 2 ?
Membrane fatty acid receptors in the β-cell: novel therapeutic targets for type 2 diabetes
Centre de recherche du diabète de Montréal, Centre hospitalier de l’université de Montréal, CRCHUM - Technopole Angus, département de médecine de l’université de Montréal, 2901 Rachel Est, Montréal H1W 4A4, Québec, Canada
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
L’homéostasie du glucose repose sur une régulation très fine de la sécrétion d’insuline par les cellules β pancréatiques. Celle-ci est principalement stimulée par le glucose, mais elle est aussi modulée par d’autres nutriments, notamment les acides gras à longue chaîne qui augmentent la sécrétion d’insuline induite par le glucose. La découverte de récepteurs couplés aux protéines G qui lient les acides gras et d’autres dérivés lipidiques et qui sont exprimés à la surface de différents types cellulaires, dont la cellule β, a ajouté une nouvelle dimension à notre compréhension du contrôle de l’homéostasie glucidique par les acides gras. Parmi ces récepteurs, le G protein-coupled receptor 40 (GPR40) et GPR119 ont suscité un grand intérêt comme cibles thérapeutiques potentielles pour augmenter la sécrétion d’insuline dans le diabète de type 2. De fait, les résultats prometteurs d’un agoniste de GPR40 dans un essai clinique de phase 2 ont apporté une preuve de concept à cette stratégie thérapeutique. Cependant, notre compréhension de la biologie et de la pharmacologie de ces récepteurs reste très incomplète.
Abstract
Glucose homeostasis requires a tight regulation of insulin secretion from pancreatic β-cells. Insulin release is chiefly stimulated by glucose, but also modulated by other nutrients, including long-chain fatty acids which potentiate glucose-induced insulin secretion. The discovery of G-protein coupled receptors activated by fatty acids (and other lipid derivatives) and expressed at the surface of various cell types, including β-cells, has added a new dimension to our understanding of the control of glucose homeostasis by fatty acids. Amongst these receptors, GPR40 and GPR119 have generated great interest as potential therapeutic targets to augment insulin secretion in type 2 diabetes. In fact, the promising results of a phase 2 clinical trial with a GPR40 agonist have provided a proof of concept for this therapeutic strategy. However, our understanding of the biology and pharmacology of these receptors remains incomplete.
Cet article fait partie du numéro thématique « Diabète : approches thérapeutiques émergentes ».
© 2013 médecine/sciences – Inserm

Les acides gras, bien connus comme des substrats énergétiques majeurs, sont également des modulateurs de la signalisation cellulaire et des voies métaboliques dans différentes conditions physiopathologiques, dont le diabète de type 2 (DT2). En particulier, les acides gras à longue chaîne amplifient la sécrétion d’insuline en réponse au glucose, et ils sont essentiels à la réponse sécrétoire à une charge en glucose après le jeûne [1]. L’effet potentialisateur des acides gras sur la sécrétion d’insuline en réponse au glucose a été longtemps attribué à leur métabolisme intracellulaire [2]. L’identification de récepteurs membranaires couplés aux protéines G1 (RCPG) qui lient les acides gras a ouvert de nouvelles hypothèses quant à leur rôle comme molécules de signalisation. Dans cette revue seront discutés le rôle de ces RCPG dans la régulation de la sécrétion d’insuline et de l’homéostasie glycémique, ainsi que leur utilisation possible pour le traitement du DT2.
Distribution tissulaire et rôle physiologique des récepteurs membranaires des acides gras
Cinq RCPG activés par les acides gras ont été identifiés depuis le début des années 2000 : GPR40 (ou FFA1, free fatty acid receptor 1), GPR41 (FFA3), GPR43 (FFA2), GPR84 et GPR120 (FFA4) (Tableau I). GPR40 et GPR120 sont activés par les acides gras saturés et insaturés à chaîne moyenne et longue (C12-C22 ; incluant les acides palmitique, oléique, linoléique, eicosapentaénoïque [EPA], docosahexaénoïque [DHA], etc.) à des concentrations de l’ordre du micromolaire [3-5]. GPR41 et GPR43 ont pour ligands les acides gras à chaîne courte (acides propionique, acétique et butyrique) [6, 7]. GPR84 est un récepteur pour les acides gras à chaîne moyenne (C9-C14 ; acides caprique, undécylique et laurique [8]). GPR119 est activé par des lysophospholipides et des amides d’acides gras (par exemple, l’oléoyléthanolamide [9]). Ce n’est donc pas un récepteur des acides gras au sens strict, mais il sera néanmoins discuté dans cette revue compte tenu de son rôle dans l’homéostasie glucidique et de son potentiel comme cible thérapeutique.
Récepteurs des acides gras couplés aux protéines G.
GPR40
GPR40 est majoritairement exprimé dans les cellules β pancréatiques. De nombreuses études utilisant des approches pharmacologiques ou génétiques (inhibition de l’expression de GPR40 par interférence à l’ARN dans les cellules insulinosécrétrices ou invalidation du gène dans des souris ; voir revue dans [10]) ont montré que GPR40 est responsable, au moins en partie, de l’effet potentialisateur des acides gras sur la sécrétion d’insuline en réponse au glucose. À l’inverse, la surexpression de GPR40 dans les cellules β pancréatiques prévient l’apparition de l’hyperglycémie chez des souris nourries avec une diète riche en lipides, et améliore l’insulinosécrétion et la tolérance au glucose chez des souris diabétiques [11]. Chez l’homme, un variant hypomorphe du gène GPR40 est associé à une diminution de l’insulinosécrétion en réponse aux acides gras [12].
Contrairement à leurs effets aigus potentialisateurs de la sécrétion d’insuline en réponse au glucose, à long terme des niveaux élevés d’acides gras inhibent la fonction des cellules β pancréatiques selon l’hypothèse de la glucolipotoxicité [13]. Un rôle possible de GPR40 dans la glucolipotoxicité des cellules β a été suggéré par une étude qui a montré que des souris dont le gène gpr40 était invalidé ne développaient pas d’insulinorésistance lorsqu’elles étaient soumises à une diète riche en lipides. Par ailleurs, des souris transgéniques surexprimant le gène gpr40 dans les îlots de Langerhans présentaient des îlots dysmorphiques et dysfonctionnels [14]. Plusieurs équipes de recherche, dont la nôtre, n’ont pas confirmé le lien entre GPR40 et les effets délétères des acides gras à long terme. De fait, la majorité des études récentes sont en accord avec le concept que l’hyperinsulinémie induite par les acides gras représente un mécanisme compensatoire face à l’insulinorésistance (voir revue dans [10]), et que cette réponse est compromise par l’inactivation fonctionnelle de GPR40 [15]. Cette notion est corroborée par les effets bénéfiques du traitement par des agonistes de GPR40 sur l’homéostasie glycémique chez les rongeurs [16-19] et, surtout, chez les patients diabétiques [20, 21].
Le récepteur GPR40 peut aussi potentialiser la sécrétion d’insuline en réponse au glucose par des mécanismes indirects qui dépendent de la sécrétion des incrétines. Ces hormones, dont le glucose-dependent insulinotropic polypeptide (GIP), le glucagon-like peptide-1 (GLP-1) et la cholécystokinine (CCK), sont sécrétées par les cellules entéroendocrines en réponse à la prise alimentaire et potentialisent la sécrétion d’insuline. GPR40 est exprimé dans plusieurs types de cellules entéroendocrines et semble impliqué dans la sécrétion des incrétines en réponse aux acides gras [19, 22, 23]. L’expression de GPR40 dans les cellules α du pancréas est controversée [24, 25], et son rôle dans la sécrétion du glucagon reste à établir de manière concluante [26, 27].
GPR120
GPR120 est principalement exprimé par les cellules L intestinales et régule l’homéostasie glycémique via sa capacité à stimuler la sécrétion de GLP-1 et de CCK suite à son activation par des acides gras insaturés [5, 28]. Il est également exprimé par les adipocytes et les macrophages, deux types cellulaires qui contribuent à la physiopathologie du DT2. Oh et al. [29] ont montré, chez des souris invalidées pour le gène gpr120, que ce récepteur est responsable des effets anti-inflammatoires et insulinosensibilisants des acides gras oméga-3, DHA et EPA, in vivo. Ces observations chez la souris sont corroborées par la découverte récente d’une mutation du gène GPR120 associée à une augmentation de 60 % du risque d’obésité chez l’homme [30]. L’expression de GPR120 dans les cellules β a été détectée par RT-PCR (reverse transcriptase-polymerase chain reaction) [31], mais son rôle physiologique dans ce type cellulaire est mal connu. Son activation par l’EPA semble avoir un effet anti-apoptotique dans les îlots pancréatiques humains [32]. GPR120 est aussi exprimé dans les papilles gustatives et semble jouer un rôle dans la détection et la préférence pour les lipides [33].
GPR41 et GPR43
Les récepteurs GPR41 et GPR43 sont exprimés dans les cellules entéroendocrines et stimulent la sécrétion d’hormones peptidiques comme le GLP-1 et le peptide YY [34, 35]. L’activation de ces RCPG par les acides gras à chaîne courte, produits en majorité dans le côlon par fermentation bactérienne, contribue aux effets métaboliques bénéfiques des fibres alimentaires. De plus, GPR43 est exprimé par les polynucléaires neutrophiles et éosinophiles [7, 36], et les souris dont le gène gpr43 est invalidé ont un profil inflammatoire [37]. L’expression de GPR43 est aussi détectable dans les adipocytes blancs [38], mais celle de GPR41 reste controversée [39]. Diverses publications suggèrent que ces récepteurs jouent un rôle dans la régulation de l’adipogenèse [38], la lipolyse [40] et la sécrétion de leptine [39] par les adipocytes. Ximenes et al. [41] ont par ailleurs montré que l’acide propionique, un ligand de GPR41 et GPR43, inhibe la sécrétion d’insuline en réponse au glucose dans les îlots de rats. Des effets similaires ont été observés dans des cellules insulinosécrétrices avec un agoniste mixte de GPR41 et GPR43 [42]. Néanmoins, le rôle de ces récepteurs dans les cellules β pancréatiques et, plus généralement, dans la régulation de l’homéostasie énergétique reste à préciser.
GPR119
GPR119 est principalement exprimé par les cellules β pancréatiques et les cellules entéroendocrines et son activation, par des agonistes endogènes et synthétiques, stimule la sécrétion d’insuline en réponse au glucose [43]. Dans les cellules entéroendocrines, GPR119 stimule la sécrétion de GLP-1 et GIP [43]. Des agonistes de GPR119 administrés par voie orale chez la souris provoquent une augmentation de la sécrétion d’insuline et de GLP-1 et une amélioration de la tolérance au glucose [44, 45]. Ces effets ne sont pas observés chez les souris dont le gène gpr119 a été invalidé. La sécrétion de GLP-1 en réponse aux nutriments est atténuée chez ces souris, suggérant un rôle physiologique de GPR119 dans le contrôle de la sécrétion de GLP-1 en réponse à la prise alimentaire [46].
Voies de signalisation et mode d’action des récepteurs membranaires des acides gras
La sécrétion d’insuline est un processus finement régulé qui comprend une voie de couplage majeure et plusieurs voies de potentialisation. La voie de couplage majeure implique les étapes successives suivantes : le transport, la phosphorylation et le métabolisme du glucose, l’augmentation du rapport ATP/ADP intracellulaire, la dépolarisation de la membrane plasmique, l’influx calcique et l’exocytose des granules d’insuline. Les voies de potentialisation modulent cette voie de couplage majeure en réponse aux incrétines, aux agonistes du récepteur muscarinique et aux acides gras. Ainsi, l’ensemble des RCPG qui répondent aux acides gras dans la cellule β modulent la réponse au glucose (Figure 1) mais, comme les incrétines, sont incapables de déclencher la sécrétion d’insuline en l’absence de glucose. Cette propriété fait de ces RCPG des cibles thérapeutiques intéressantes, puisque leur effet insulinosécrétoire est strictement dépendant du glucose.
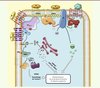 |
Figure 1. Récepteurs membranaires aux acides gras exprimés à la surface des cellules β pancréatiques. GPR40 et GPR120 sont activés par les acides gras à chaîne moyenne et longue et s’associent à la protéine Gq/11. GPR41 et GPR43 ont pour ligands les acides gras à chaîne courte ; GPR41 est couplé à la protéine Gi, alors que GPR43 s’associe à Gi et Gq/11. GPR119 lie des dérivés d’acides gras à longue chaîne (oléoyléthanolamide [OEA] et lysophosphatidylcholine [LPC]). Gαq/11 activée stimule l’hydrolyse du phosphatidylinositol-4,5-biphosphate (PIP2), un phospholipide membranaire, par la phospholipase Cβ (PLCβ et stimule la production d’inositol-1,4,5-triphosphate (IP3) et de diacylglycérol (DAG). L’IP3 stimule l’efflux calcique du réticulum endoplasmique (RE) via sa fixation au récepteur IP3R, qui provoque l’ouverture de ce canal ionique. Le DAG induit la phosphorylation et l’activation de la protéine kinase D1 (PKD1). À son tour, PKD1 phosphoryle et provoque, via des cibles qui restent à identifier, le remodelage des filaments d’actine et l’amplification de la sécrétion d’insuline. L’activation de la protéine Gs stimule la production d’AMP cyclique (APMc) via l’activation de l’adénylate cyclase (AC), alors que l’activation de Gi produit une réponse inverse. L’AMPc et le Ca2+ agissent de manière coordonnée et complémentaire pour potentialiser la sécrétion d’insuline en réponse au glucose. AG : acides gras. Le point d’interrogation après GPR40 représente l’incertitude de l’importance de la voie IP3/efflux calcique du réticulum endoplasmique dans le rôle de GPR40 sur la potentialisation de la sécrétion d’insuline en réponse au glucose. Le point d’interrogation après PKD1 signifie que les cibles PKD1 en aval de GPR40 restent inconnues. Figure produite grâce à Servier medical art (www.servier.com/Powerpoint-image-bank). |
GPR40 est couplé à la protéine G hétérotrimerique Gq/11 [4]. L’activation de la sous-unité α de cette protéine G stimule la phospholipase Cβ (PLCβ), qui hydrolyse le phosphatidylinositol-4,5-biphosphate pour générer deux seconds messagers : l’inositol triphosphate (IP3) et le diacylglycérol (DAG). Le DAG active la protéine kinase C et l’IP3 stimule l’efflux calcique du réticulum endoplasmique. L’inhibition pharmacologique de Gαq/11 ou de la PLC bloque la potentialisation de la sécrétion d’insuline en réponse au glucose par les acides gras in vitro. De plus, la synthèse d’IP3 dans les îlots de Langerhans en réponse aux acides gras est dépendante de GPR40 [47]. Une étude récente dans notre laboratoire a identifié un rôle prépondérant de la voie des DAG en aval de GPR40, et l’activation subséquente de la protéine kinase D1. Cette kinase stimule le remodelage des filaments d’actine et permet ainsi le recrutement des granules d’insuline du cytoplasme vers la membrane plasmique, étape indispensable à l’amplification de la seconde phase de sécrétion d’insuline en réponse au glucose par les acides gras [48] (Figure 1).
GPR120, comme GPR40, est couplé à la protéine G hétérotrimérique Gq/11 (Figure 1). Ce mécanisme est responsable de la sécrétion d’incrétines induite par les acides gras insaturés dans les cellules entéroendocrines [5]. L’activation de GPR120 provoque sa phosphorylation, le recrutement de la β-arrestine 2, sa désensibilisation et son internalisation [49]. Cette voie de signalisation de GPR120, via la β-arrestine 2, est à l’origine des effets anti-inflammatoires du récepteur mentionnés plus haut [29].
Les récepteurs GPR41 et GPR43 sont couplés à la sous-unité Gαi, qui provoque une diminution de la concentration intracellulaire d’AMP cyclique (AMPc) [7, 36] (Figure 1). La conséquence fonctionnelle de leur activation devrait donc être une diminution de la sécrétion d’insuline. Ceci reste à démontrer expérimentalement, d’autant que GPR43 peut également s’associer à la sous-unité Gαq/11 [7, 36].
GPR119 s’associe de manière préférentielle à la sous-unité Gαs et son activation augmente donc la synthèse d’AMPc [9]. Il provoque également une augmentation des niveaux de Ca2+ intracellulaires en réponse à l’oléoyléthanolamide [50]. Le mode d’action de GPR119 est donc similaire à celui du récepteur au GLP-1.
Utilisation thérapeutique des récepteurs membranaires des acides gras
Depuis leur « déorphelinisation » au début des années 2000, les RCPG activés par les acides gras ont généré beaucoup d’intérêt comme cibles pharmacologiques potentielles pour le traitement des maladies métaboliques. Parmi eux, GPR40 est celui pour lequel le développement d’agonistes est le plus avancé sur le plan clinique. Burant et al. [20] ont publié les résultats très encourageants d’une étude randomisée de phase 2 avec l’agoniste de GPR40 TAK-875 (Takeda). Après 12 semaines de traitement, les taux d’hémoglobine glyquée avaient diminué de manière significative (environ 1,2 %) chez les patients traités par le TAK-875, une efficacité similaire à celle observée avec le médicament de référence, la glimépiride. En revanche, l’incidence d’épisodes hypoglycémiques était de 19 % sous glimépiride, mais de 2 % (non significatif par rapport au groupe témoin) sous TAK-875. Bien que l’efficacité et l’innocuité à long terme de cette nouvelle classe thérapeutique restent à démontrer dans des études de phase 3 (qui sont en cours pour TAK-875), les données cliniques préliminaires montrent que ces molécules améliorent la sécrétion d’insuline dans le DT2 sans augmenter le risque d’hypoglycémie. De fait, TAK-875 n’a pas d’effet sur la glycémie des individus non diabétiques [51]. Récemment, une autre série d’agonistes de GPR40, incluant AMG-837 et ses dérivés (Amgen), a été proposée [18, 19]. Certaines de ces molécules agissent comme des modulateurs allostériques et potentialisent les effets insulinotropes des acides gras [52].
Des agonistes de GPR119 sont également en cours de développement clinique pour le traitement du DT2 [53]. L’intérêt de cibler ce récepteur est qu’il stimule la sécrétion d’insuline de manière directe (via son effet sur la cellule β) et indirecte (via la sécrétion de GLP-1) [54]. Une étude randomisée testant l’effet de l’agoniste JNJ-38431055 (Johnson & Johnson) administré pendant 14 jours consécutifs à des patients diabétiques de type 2 n’a cependant pas montré d’effet bénéfique sur la glycémie malgré une augmentation des taux postprandiaux d’incrétines [55]. L’utilité thérapeutique des agonistes de GPR119 chez l’homme reste donc à démontrer.
Enfin, des composés synthétiques ciblant les récepteurs GPR41 et GPR43 sont en phase préclinique de développement [56]. La méconnaissance du rôle précis de ces récepteurs et la difficulté de synthétiser des molécules spécifiques pour chacun d’eux demeurent des obstacles majeurs à leur utilisation comme cibles thérapeutiques.
Conclusions
La « déorphelinisation » des RCPG membranaires activés par les acides gras a mis en évidence le rôle de ces molécules dans la signalisation intracellulaire. GPR40 et GPR119 sont exprimés à la surface des cellules β et leur activation, respectivement par les acides gras à chaîne longue et des dérivés lipidiques, potentialise la sécrétion d’insuline induite par le glucose. Ces deux récepteurs sont également exprimés dans les cellules entéroendocrines et sont impliqués dans la sécrétion d’incrétines en réponse aux acides gras. GPR120 est activé par les acides gras à chaîne longue et semble impliqué dans les effets anti-inflammatoires des acides gras oméga-3 dans le tissu adipeux. Son rôle potentiel dans la cellule β reste à démontrer. Les récepteurs aux acides gras à chaîne courte, GPR41 et GPR43, sont exprimés dans la cellule β, mais leur fonction est à ce jour inconnue. Les résultats prometteurs d’un essai clinique de phase 2 de l’agoniste de GPR40 TAK-875 illustrent le potentiel de cette famille de récepteurs comme cibles thérapeutiques pour le DT2, mais demandent à être confirmés avec d’autres composés et des études à plus long terme. Les résultats cliniques d’agonistes de GPR119 sont en revanche décevants. Une meilleure compréhension de la biologie et de la pharmacologie de ces récepteurs devrait permettre le développement de molécules plus sélectives, efficaces et sûres pour le traitement des maladies métaboliques.
Liens d’intérêt
V. Poitout déclare participer à des interventions ponctuelles (essais cliniques, conférences, actions de formation) pour l’entreprise Takeda.
A.D. Mancini déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Voir le numéro thématique de m/s d’octobre 2012 consacré aux RCPG, vol. 28, n° 10.
Références
- Stein DT, Esser V, Stevenson BE, et al. Essentiality of circulating fatty acids for glucose-stimulated insulin secretion in the fasted rat. J Clin Invest 1996 ; 97 : 2728–2735. [CrossRef] [PubMed] [Google Scholar]
- Nolan CJ, Madiraju MS, Delghingaro-Augusto V, et al. Fatty acid signaling in the {beta}-cell and insulin secretion. Diabetes 2006 ; 55 : S16–23. [CrossRef] [PubMed] [Google Scholar]
- Briscoe CP, Tadayyon M, Andrews JL, et al. The orphan G protein-coupled receptor GPR40 is activated by medium and long chain fatty acids. J Biol Chem 2003 ; 278 : 11303–11311. [CrossRef] [PubMed] [Google Scholar]
- Itoh Y, Kawamata Y, Harada M, et al. Free fatty acids regulate insulin secretion from pancreatic beta cells through GPR40. Nature 2003 ; 422 : 173–176. [CrossRef] [PubMed] [Google Scholar]
- Hirasawa A, Tsumaya K, Awaji T, et al. Free fatty acids regulate gut incretin glucagon-like peptide-1 secretion through GPR120. Nat Med 2005 ; 11 : 90–94. [CrossRef] [PubMed] [Google Scholar]
- Nilsson NE, Kotarsky K, Owman C, Olde B. Identification of a free fatty acid receptor, FFA2R, expressed on leukocytes and activated by short-chain fatty acids. Biochem Biophys Res Commun 2003 ; 303 : 1047–1052. [CrossRef] [PubMed] [Google Scholar]
- Le Poul E, Loison C, Struyf S, et al. Functional characterization of human receptors for short chain fatty acids and their role in polymorphonuclear cell activation. J Biol Chem 2003 ; 278 : 25481–25489. [CrossRef] [PubMed] [Google Scholar]
- Wang J, Wu X, Simonavicius N, et al. Medium-chain fatty acids as ligands for orphan G protein-coupled receptor GPR84. J Biol Chem 2006 ; 281 : 34457–34464. [CrossRef] [PubMed] [Google Scholar]
- Overton HA, Babbs AJ, Doel SM, et al. Deorphanization of a G protein-coupled receptor for oleoylethanolamide and its use in the discovery of small-molecule hypophagic agents. Cell Metab 2006 ; 3 : 167–175. [CrossRef] [PubMed] [Google Scholar]
- Mancini AD, Poitout V. The fatty acid receptor FFA1/GPR40 a decade later : how much do we know? Trends Endocrinol Metab 2013 ; doi : 10.1016/j.tem.2013.03.003. [Google Scholar]
- Nagasumi K, Esaki R, Iwachidow K, et al. Overexpression of GPR40 in pancreatic beta-cells augments glucose-stimulated insulin secretion and improves glucose tolerance in normal and diabetic mice. Diabetes 2009 ; 58 : 1067–1076. [CrossRef] [PubMed] [Google Scholar]
- Vettor R, Granzotto M, De Stefani D, et al. Loss-of-function mutation of the GPR40 gene associates with abnormal stimulated insulin secretion by acting on intracellular calcium mobilization. J Clin Endocrinol Metab 2008 ; 93 : 3541–3550. [CrossRef] [PubMed] [Google Scholar]
- Poitout V, Amyot J, Semache M, et al. Glucolipotoxicity of the pancreatic beta cell. Biochim Biophys Acta 2010 ; 1801 : 289–298. [CrossRef] [PubMed] [Google Scholar]
- Steneberg P, Rubins N, Bartoov-Shifman R, et al. The FFA receptor GPR40 links hyperinsulinemia, hepatic steatosis, and impaired glucose homeostasis in mouse. Cell Metabol 2005 ; 1 : 245–258. [CrossRef] [Google Scholar]
- Alquier T, Poitout V. GPR40 : good cop, bad cop? Diabetes 2009 ; 58 : 1035–1036. [CrossRef] [PubMed] [Google Scholar]
- Tan CP, Feng Y, Zhou YP, et al. Selective small-molecule agonists of G protein-coupled receptor 40 promote glucose-dependent insulin secretion and reduce blood glucose in mice. Diabetes 2008 ; 57 : 2211–2219. [CrossRef] [PubMed] [Google Scholar]
- Tsujihata Y, Ito R, Suzuki M, et al. TAK-875, an orally available G protein-coupled receptor 40/free fatty acid receptor 1 agonist, enhances glucose-dependent insulin secretion and improves both postprandial and fasting hyperglycemia in type 2 diabetic rats. J Pharmacol Exp Ther 2011 ; 339 : 228–237. [CrossRef] [PubMed] [Google Scholar]
- Lin DC, Zhang J, Zhuang R, et al. AMG 837 : a novel GPR40/FFA1 agonist that enhances insulin secretion and lowers glucose levels in rodents. PLoS One 2011 ; 6 : e27270. [CrossRef] [PubMed] [Google Scholar]
- Luo J, Swaminath G, Brown SP, et al. A potent class of GPR40 full agonists engages the enteroinsular axis to promote glucose control in rodents. PLoS One 2012 ; 7 : e46300. [CrossRef] [PubMed] [Google Scholar]
- Burant CF, Viswanathan P, Marcinak J, et al. TAK-875 versus placebo or glimepiride in type 2 diabetes mellitus : a phase 2, randomised, double-blind, placebo-controlled trial. Lancet 2012 ; 379 : 1403–1411. [CrossRef] [PubMed] [Google Scholar]
- Kaku K, Araki T, Yoshinaka R. Randomized, double-Blind, dose-ranging study of TAK-875, a novel GPR40 agonist, in Japanese patients with inadequately controlled type 2 diabetes. Diabetes Care 2013 ; 36 : 245–250. [CrossRef] [PubMed] [Google Scholar]
- Liou AP, Lu X, Sei Y, et al. The G protein-coupled receptor GPR40 directly mediates long chain fatty acid-induced secretion of cholecystokinin. Gastroenterology 2011 ; 140 : 903–912. [CrossRef] [PubMed] [Google Scholar]
- Edfalk S, Steneberg P, Edlund H. Gpr40 is expressed in enteroendocrine cells and mediates free fatty acid stimulation of incretin secretion. Diabetes 2008 ; 57 : 2280–2287. [CrossRef] [PubMed] [Google Scholar]
- Flodgren E, Olde B, Meidute-Abaraviciene S, et al. GPR40 is expressed in glucagon producing cells and affects glucagon secretion. Biochem Biophys Res Commun 2007 ; 354 : 240–245. [CrossRef] [PubMed] [Google Scholar]
- Hirasawa A, Itsubo C, Sadakane K, et al. Production and characterization of a monoclonal antibody against GPR40 (FFAR1; free fatty acid receptor 1). Biochem Biophys Res Commun 2008 ; 365 : 22–28. [CrossRef] [PubMed] [Google Scholar]
- Wang L, Zhao Y, Gui B, et al. Acute stimulation of glucagon secretion by linoleic acid results from GPR40 activation and [Ca2+]i increase in pancreatic islet (alpha)-cells. J Endocrinol 2011 ; 210 : 173–179. [CrossRef] [PubMed] [Google Scholar]
- Yashiro H, Tsujihata Y, Takeuchi K, et al. The effects of TAK-875, a selective G protein-coupled receptor 40/free fatty acid 1 agonist, on insulin and glucagon secretion in isolated rat and human islets. J Pharmacol Exp Ther 2012 ; 340 : 483–489. [CrossRef] [PubMed] [Google Scholar]
- Tanaka T, Katsuma S, Adachi T, et al. Free fatty acids induce cholecystokinin secretion through GPR120. Naunyn-Schmiedeberg’s Arch Pharmacol 2008 ; 377 : 523–527. [CrossRef] [Google Scholar]
- Oh da Y, Talukdar S, Bae EJ, et al. GPR120 is an omega-3 fatty acid receptor mediating potent anti-inflammatory and insulin-sensitizing effects. Cell 2010 ; 142 : 687–698. [CrossRef] [PubMed] [Google Scholar]
- Ichimura A, Hirasawa A, Poulain-Godefroy O, et al. Dysfunction of lipid sensor GPR120 leads to obesity in both mouse and human. Nature 2012 ; 483 : 350–354. [CrossRef] [PubMed] [Google Scholar]
- Kebede MA, Alquier T, Latour MG, Poitout V. Lipid receptors and islet function : therapeutic implications? Diabetes Obes Metab 2009 ; 11 : 10–20. [CrossRef] [Google Scholar]
- Taneera J, Lang S, Sharma A, et al. A systems genetics approach identifies genes and pathways for type 2 diabetes in human islets. Cell Metabolism 2012 ; 16 : 122–134. [CrossRef] [PubMed] [Google Scholar]
- Martin C, Passilly-Degrace P, Chevrot M, et al. Lipid-mediated release of GLP-1 by mouse taste buds from circumvallate papillae : putative involvement of GPR120 and impact on taste sensitivity. J Lipid Res 2012 ; 53 : 2256–2265. [Google Scholar]
- Kaji I, Karaki S, Tanaka R, Kuwahara A. Density distribution of free fatty acid receptor 2 (FFA2)-expressing and GLP-1-producing enteroendocrine L cells in human and rat lower intestine, and increased cell numbers after ingestion of fructo-oligosaccharide. J Mol Histol 2011 ; 42 : 27–38. [CrossRef] [PubMed] [Google Scholar]
- Tolhurst G, Heffron H, Lam YS, et al. Short-chain fatty acids stimulate glucagon-like peptide-1 secretion via the G-protein-coupled receptor FFAR2. Diabetes 2012 ; 61 : 364–371. [CrossRef] [PubMed] [Google Scholar]
- Brown AJ, Goldsworthy SM, Barnes AA, et al. The Orphan G protein-coupled receptors GPR41 and GPR43 are activated by propionate and other short chain carboxylic acids. J Biol Chem 2003 ; 278 : 11312–11319. [Google Scholar]
- Maslowski KM, Vieira AT, Ng A, et al. Regulation of inflammatory responses by gut microbiota and chemoattractant receptor GPR43. Nature 2009 ; 461 : 1282–1286. [CrossRef] [PubMed] [Google Scholar]
- Hong YH, Nishimura Y, Hishikawa D, et al. Acetate and propionate short chain fatty acids stimulate adipogenesis via GPCR43. Endocrinology 2005 ; 146 : 5092–5099. [CrossRef] [PubMed] [Google Scholar]
- Zaibi MS, Stocker CJ, O’Dowd J, et al. Roles of GPR41 and GPR43 in leptin secretory responses of murine adipocytes to short chain fatty acids. FEBS Lett 2010 ; 584 : 2381–2386. [CrossRef] [PubMed] [Google Scholar]
- Ge H, Li X, Weiszmann J, et al. Activation of G protein-coupled receptor 43 in adipocytes leads to inhibition of lipolysis and suppression of plasma free fatty acids. Endocrinology 2008 ; 149 : 4519–4526. [CrossRef] [PubMed] [Google Scholar]
- Ximenes HMA, Hirata AE, Rocha MS, et al. Propionate inhibits glucose-induced insulin secretion in isolated rat pancreatic islets. Cell Biochem Funct 2007 ; 25 : 173–178. [CrossRef] [PubMed] [Google Scholar]
- Schmidt J, Smith NJ, Christiansen E, et al. Selective orthosteric free fatty acid receptor 2 (FFA2) agonists : identification of the structural and chemical requirements for selective activation of FFA2 versus FFA3. J Biol Chem 2011 ; 286 : 10628–10640. [CrossRef] [PubMed] [Google Scholar]
- Chu ZL, Jones RM, He H, et al. A role for beta-cell-expressed G protein-coupled receptor 119 in glycemic control by enhancing glucose-dependent insulin release. Endocrinology 2007 ; 148 : 2601–2609. [CrossRef] [PubMed] [Google Scholar]
- Chu ZL, Carroll C, Chen R, et al. N-oleoyldopamine enhances glucose homeostasis through the activation of GPR119. Mol Endocrinol 2010 ; 24 : 161–170. [CrossRef] [PubMed] [Google Scholar]
- Lauffer LM, Iakoubov R, Brubaker PL. GPR119 is essential for oleoylethanolamide-induced glucagon-like peptide-1 secretion from the intestinal enteroendocrine L-cell. Diabetes 2009 ; 58 : 1058–1066. [CrossRef] [PubMed] [Google Scholar]
- Lan H, Vassileva G, Corona A, et al. GPR119 is required for physiological regulation of glucagon-like peptide-1 secretion but not for metabolic homeostasis. J Endocrinol 2009 ; 201 : 219–230. [CrossRef] [PubMed] [Google Scholar]
- Alquier T, Peyot ML, Latour MG, et al. Deletion of GPR40 impairs glucose-induced insulin secretion in vivo in mice without affecting intracellular fuel metabolism in islets. Diabetes 2009 ; 58 : 2607–2615. [CrossRef] [PubMed] [Google Scholar]
- Ferdaoussi M, Bergeron V, Zarrouki B, et al. G protein-coupled receptor (GPR)40-dependent potentiation of insulin secretion in mouse islets is mediated by protein kinase D1. Diabetologia 2012 ; 55 : 2682–2692. [CrossRef] [PubMed] [Google Scholar]
- Watson SJ, Brown AJH, Holliday ND. Differential signaling by splice variants of the human free fatty acid receptor GPR120. Mol Pharmacol 2012 ; 81 : 631–642. [CrossRef] [PubMed] [Google Scholar]
- Ning Y, O’Neill K, Lan H, et al. Endogenous and synthetic agonists of GPR119 differ in signalling pathways and their effects on insulin secretion in MIN6c4 insulinoma cells. Br J Pharmacol 2008 ; 155 : 1056–1065. [CrossRef] [PubMed] [Google Scholar]
- Naik H, Vakilynejad M, Wu J, et al. Safety, tolerability, pharmacokinetics, and pharmacodynamic properties of the GPR40 agonist TAK-875 : results from a double-blind, placebo-controlled single oral dose rising study in healthy volunteers. J Clin Pharmacol 2012 ; 52 : 1007–1016. [CrossRef] [PubMed] [Google Scholar]
- Lin DC, Guo Q, Luo J, et al. Identification and pharmacological characterization of multiple allosteric binding sites on the free fatty acid 1 receptor. Mol Pharmacol 2012 ; 82 : 843–859. [CrossRef] [PubMed] [Google Scholar]
- Ohishi T, Yoshida S. The therapeutic potential of GPR119 agonists for type 2 diabetes. Expert Opin Investig Drugs 2012 ; 21 : 321–328. [CrossRef] [PubMed] [Google Scholar]
- Lauffer L, Iakoubov R, Brubaker PL. GPR119 : Double-dipping for better glycemic control. Endocrinology 2008 ; 149 : 2035–2037. [CrossRef] [PubMed] [Google Scholar]
- Katz LB, Gambale JJ, Rothenberg PL, et al. Effects of JNJ-38431055, a novel GPR119 receptor agonist, in randomized, double-blind, placebo-controlled studies in subjects with type 2 diabetes. Diabetes Obes Metab 2012 ; 14 : 709–716. [CrossRef] [PubMed] [Google Scholar]
- Ulven T. Short-chain free fatty acid receptors FFA2/GPR43 and FFA3/GPR41 as new potential therapeutic targets. Front Endocrinol 2012 ; 3 : 111. [CrossRef] [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1. Récepteurs membranaires aux acides gras exprimés à la surface des cellules β pancréatiques. GPR40 et GPR120 sont activés par les acides gras à chaîne moyenne et longue et s’associent à la protéine Gq/11. GPR41 et GPR43 ont pour ligands les acides gras à chaîne courte ; GPR41 est couplé à la protéine Gi, alors que GPR43 s’associe à Gi et Gq/11. GPR119 lie des dérivés d’acides gras à longue chaîne (oléoyléthanolamide [OEA] et lysophosphatidylcholine [LPC]). Gαq/11 activée stimule l’hydrolyse du phosphatidylinositol-4,5-biphosphate (PIP2), un phospholipide membranaire, par la phospholipase Cβ (PLCβ et stimule la production d’inositol-1,4,5-triphosphate (IP3) et de diacylglycérol (DAG). L’IP3 stimule l’efflux calcique du réticulum endoplasmique (RE) via sa fixation au récepteur IP3R, qui provoque l’ouverture de ce canal ionique. Le DAG induit la phosphorylation et l’activation de la protéine kinase D1 (PKD1). À son tour, PKD1 phosphoryle et provoque, via des cibles qui restent à identifier, le remodelage des filaments d’actine et l’amplification de la sécrétion d’insuline. L’activation de la protéine Gs stimule la production d’AMP cyclique (APMc) via l’activation de l’adénylate cyclase (AC), alors que l’activation de Gi produit une réponse inverse. L’AMPc et le Ca2+ agissent de manière coordonnée et complémentaire pour potentialiser la sécrétion d’insuline en réponse au glucose. AG : acides gras. Le point d’interrogation après GPR40 représente l’incertitude de l’importance de la voie IP3/efflux calcique du réticulum endoplasmique dans le rôle de GPR40 sur la potentialisation de la sécrétion d’insuline en réponse au glucose. Le point d’interrogation après PKD1 signifie que les cibles PKD1 en aval de GPR40 restent inconnues. Figure produite grâce à Servier medical art (www.servier.com/Powerpoint-image-bank). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




