| Issue |
Med Sci (Paris)
Volume 28, Number 6-7, Juin–Juillet 2012
|
|
|---|---|---|
| Page(s) | 639 - 645 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2012286018 | |
| Published online | 16 July 2012 | |
Legionella, légionellose
Legionella, Legionnaires’ disease
1
Université de Lyon, Inserm U851, centre national de référence des Legionella, IFR 128 université Lyon 1, centre d’infectiologie, 321, avenue Jean Jaurès, 69007 Lyon, France
2
Service des maladies infectieuses et tropicales, hospices civils de Lyon, hôpital de la Croix-Rousse, Lyon, France
3
Centre de biologie Est, hospices civils de Lyon, Bron, France
Legionella est l’agent étiologique d’une pneumonie souvent sévère appelée légionellose. La détection de l’antigène de Legionella pneumophila sérogroupe 1 dans les urines a permis d’écourter le délai avant le diagnostic et la mise en route du traitement, et de diminuer la mortalité. La surveillance des réseaux d’eau douce, habitat naturel de la bactérie, a également amélioré la prévention collective. En France, nous disposons du Centre national de référence des légionelles qui recueille l’ensemble des souches cliniques responsables de cas sporadiques ou épidémiques. Ce centre permet de confronter les données issues de l’analyse génétique des souches aux données épidémiocliniques. Sur le plan fondamental, d’importantes avancées ont amélioré notre compréhension, non seulement des mécanismes permettant à L. pneumophila d’exploiter le métabolisme de la cellule hôte, mais aussi des mécanismes immunitaires permettant de limiter le développement de l’infection.
Abstract
Legionella is the causative agent of Legionnaires’ disease, a severe form of pneumonia. Detection of Legionella pneumophila serogroup 1 antigen in urine samples has shortened the delay of diagnosis and subsequent treatment initiation resulting in decreased mortality. Improved surveillance of potable water system reinforces the community prevention. In France, the National Reference Center for Legionella collects the strains responsible for sporadic or epidemic cases and crosslinks the data including epidemiological pattern, clinical presentation, and genetic analysis of the strains. Regarding host-pathogen interactions, major advances have been made recently in the understanding of L. pneumophila ability to subvert the host intracellular trafficking and the innate immune response leading to infection control.
© 2012 médecine/sciences – Inserm / SRMS
Legionella est une bactérie intracellulaire d’origine environnementale qui se multiplie dans les protozoaires colonisant les eaux douces (amibes). Legionella pneumophila (L. pneumophila) est la principale espèce responsable d’infections sévères chez l’homme. Quand une source hydrique domestique est contaminée, la contamination se produit via l’inhalation de gouttelettes vaporisées dans l’environnement. La multiplication des bactéries dans les macrophages pulmonaires conduit au développement de la maladie des légionnaires ou légionellose. Il s’agit d’une pneumonie progressive, sévère, survenant préférentiellement dans un contexte d’immunodépression. Un diagnostic précoce et un traitement antibiotique adapté permettent la guérison dans la majorité des cas. C’est une maladie à déclaration obligatoire, qui impose une enquête et une intervention environnementale si une source d’émission est identifiée.
Des progrès majeurs sont intervenus ces dernières années dans la connaissance de L. pneumophila par l’étude de l’épidémiologie environnementale et de la relation hôte-pathogène du point de vue de la biologie cellulaire et de l’immunologie (Encadré 1). Cette revue synthétise l’avancée des connaissances dans ces domaines et résume la démarche diagnostique et de prise en charge de la légionellose.
1 Caractéristiques microbiologiques
Genre Legionella
Cinquante-trois espèces comprenant 70 sérogroupes (90 % des cas humains de légionellose sont dus au sérogroupe 1 de l’espèce pneumophila).
Bactérie Gram-négatif aérobie stricte
Croissance intracellulaire
Hôte naturel environnemental : protozoaires aquatiques du genre amibe. Quatorze espèces d’amibes libres et deux espèces de protozoaires ciliés (Acanthamoeba castellanii et Hartmanella vermiformis) sont les plus répandues [1–3].
In vivo : croissance dans les monocytes-macrophages et les cellules épithéliales pulmonaires (pneumocytes de type II) [4].
Aspect évolutif
Au cours de l’évolution, la survie dans les protozoaires environnementaux eucaryotes résulte de la sélection de caractères d’espèces. Ils ont permis à Legionella d’assurer sa réplication en exploitant le trafic cellulaire de l’hôte mammifère.
Plasticité et diversité génétique [5]
Aspect quantitatif
L’ADN, de grande taille, représente un patrimoine génétique d’environ 3 000 gènes.
Dans l’espèce pneumophila, on constate 80 % d’homologie de séquences entre les souches constituant le patrimoine génétique commun ou core génome.
En revanche, 7 à 11 % du génome sont spécifiques de la souche, indiquant une grande diversité génétique.
Aspect qualitatif
Trente gènes codent pour des protéines eucaryote-like ; 32 gènes codent pour des protéines porteuses de domaines eucaryotes impliqués dans les interactions protéine-protéine.
Le core génome regroupe les gènes de virulence majeurs qui sont très conservés
Alternance phénotypique ou switch de phase
L’expression ou la répression de certains groupes de gènes conduit à deux états phénotypiques distincts :
Une forme intravacuolaire (non virulente, dédiée à la multiplication) ; la bactérie est longue, filamenteuse et non flagellée.
Une forme mature (virulente) ; la bactérie est courte, flagellée, très mobile et riche en inclusions cétoniques (énergie carbonique).
Facteurs de virulence
Legionella possède tous les systèmes de sécrétion (SST) à l’exception du type III.
Le système de sécrétion de type IV (SST4) est le facteur de virulence majeur de L. pneumophila [6] (Figure 1). C’est un système conjugatif codé par 25 gènes Dot/lcm, qui transporte environ 300 protéines effectrices à l’intérieur de la cellule et qui contrôle toutes les étapes de survie et de multiplication intracellulaires.
Autres facteurs de virulence connus : la flagelline et le lipopolysaccharide (LPS) dont la fraction Lipide A possède une structure originale [7].
Environnement et Legionella
Cycle intracellulaire
La coévolution de Legionella avec les protozoaires aquatiques eucaryotes a permis l’acquisition de caractères génétiques codant pour des facteurs de virulence. L’appareil de sécrétion de type IV (SST4) - ou système Dot/Icm - de L. pneumophila joue un rôle majeur dans le cycle intracellulaire de la bactérie. Il promeut l’internalisation de la bactérie par la cellule hôte, permet la formation à partir du réticulum endoplasmique d’une vacuole autonome nommée Legionella-containing vacuole (LCV) et empêche la fusion endosome-lysosome. Toutes les étapes conduisant à la multiplication bactérienne dans la LCV sont contrôlées par la translocation de substrats et d’effecteurs protéiques par Dot/Icm. L’étude de la régulation temporelle et spatiale de ces effecteurs dans des cellules eucaryotes environnementales ou humaines constitue actuellement un champ de recherche majeur [6] (Figure 1). On a décrit plus de 300 substrats, parfois redondants, dont certains ont des fonctions enzymatiques et d’autres agissent comme des protéines régulatrices de l’hôte grâce à leur fonction eucaryote-like (pour revue des principaux substrats Dot/Icm et de leur fonction, voir [6]).
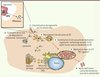 |
Figure 1. Trafic intracellulaire de Legionella dans l’hôte eucaryote. (1) Après sa phagocytose, (2) Legionella échappe à la fusion endosome-lysosome, (3 et 4) recrute des vésicules du réticulum endoplasmique (RE) et amorce une phase de multiplication dans une vacuole autonome nommée legionella-containing vacuole (LCV) (5) puis induit la lyse de la cellule hôte pour infecter les cellules voisines (6) . Toutes ces étapes sont sous le contrôle direct du système Dot/Icm ou SST4 (d’après [6]). |
Génomique comparative
L’étude des bases moléculaires déterminant le saut transitionnel entre l’environnement et l’homme a pour but de discriminer les souches environnementales à risque. Ainsi, par la génomique fonctionnelle (étude des gènes régulant les fonctions de virulence) [8, 9], l’étude de la réponse de Legionella aux stress génotoxiques a révélé que, contrairement à la plupart des bactéries, celle-ci ne développe pas une réponse de type SOS (réparation de l’ADN et mutagenèse) [44], mais développe une compétence (état physiologique génétiquement programmé conférant la capacité de recueillir de l’ADN provenant de l’environnement) [10]. Cette particularité favorise la diversité génétique, l’acquisition de nouveaux gènes et augmente la virulence de la bactérie. Parmi la cinquantaine d’espèces de Legionella, l’espèce L. pneumophila est associée à plus de 90 % des cas de légionellose diagnostiqués dans le monde et le sérogroupe 1 de cette espèce est de loin le plus important en pathologie humaine (ce qui n’est pas le cas dans l’environnement où la diversité des espèces est importante). La génomique comparative des espèces montre qu’un groupe de gènes spécifiques du sérogroupe 1 et codant pour les protéines impliquées dans la biosynthèse du LPS (lipopolysaccharide) est présent dans des contextes génomiques divers. Ce résultat suggère que le LPS du sérogroupe 1 est le principal facteur de virulence responsable de la prédominance des souches de ce sérogroupe dans les cas de légionellose
L’Institut Pasteur a développé une ressource web des séquences de Legionella 1 et une base de données des légionelles2.
Surveillance épidémiologique
Des outils moléculaires sont utilisés pour établir les liens entre les souches isolées chez les patients malades et les souches environnementales afin d’identifier les sources de contamination. Ces mêmes outils ont révélé que la majorité des isolats cliniques correspond à un nombre très limité de souches présentes dans l’environnement [11, 12]. Ainsi, au sein même des L. pneumophila sérogroupe 1, toutes les souches ne semblent pas présenter le même potentiel pathogène vis-à-vis de l’homme. Les méthodes de typage font de plus en plus appel aux techniques de PCR (polymerase chain reaction). Des techniques de PCR suivies d’un séquençage (sequence-based-typing ou SBT) ont été développées ; elles sont directement applicables aux prélèvements pulmonaires en l’absence de souches identifiées en culture [13, 14]. Enfin, le développement récent de techniques de surveillance environnementale, comme la qPCR de Legionella, devrait permettre d’améliorer encore la prévention au niveau des installations collectives [15].
Réponse de l’hôte à une infection par Legionella
Facteurs de risque
Les facteurs de risque liés au terrain sont l’âge avancé, le tabagisme ainsi que toute situation d’immunodépression (cancer, hémopathie, diabète, infection par le VIH [virus de l’immunodéficience humaine], corticothérapie et traitement immunosuppresseur) [16]. Les facteurs de risque liés à l’exposition sont représentés par un contact prolongé ou répété avec les réservoirs. Ils sont détaillés dans l’Encadré 2. La baisse de production d’IFN-γ (interféron-³) ou l’inhibition du TNF-α (tumor necrosis factor-α) au long cours par un traitement neutralisant (adalimumab, étanercept ou infliximab), dans le cadre d’une polyarthrite rhumatoïde par exemple, majorerait le risque d’infection à L. pneumophila (le risque relatif augmentant de 16,5 à 21) [17, 18].
2 Épidémiologie de la légionellose
Épidémiologie environnementale
-
Infection émergente des sociétés économiquement développées.
-
La colonisation des réseaux domestiques d’eau douce y est endémique.
-
Dans ces réseaux, deux réservoirs : les protozoaires aquatiques (amibes) et le biofilm (communauté de microorganismes multiespèces contenus dans une matrice extracellulaire à la surface d’un support polymérique).
-
Les installations collectives ou individuelles (température de l’eau comprise entre 25 et 42 °C) générant des aérosols contaminés sont les tours aéroréfrigérantes, les fontaines, les spas, les nébuliseurs, les dispositifs d’air conditionné, les douches ou les robinets.
-
Transmission directe3 à l’homme par inhalation d’aérosols contenant des Legionella.
Épidémiologie clinique en France (1998-2008) [16]
-
Situation parmi les pneumonies :
premier agent bactérien intracellulaire responsable de pneumonie aiguë communautaire (un test diagnostique simple est disponible); hospitalisation dans 98 % des cas confirmés ;
40 % des patients hospitalisés avec un diagnostic de légionellose admis en réanimation.
Cas sporadiques ou cas groupés : individuels ou touchant une collectivité.
Origine : 91 % communautaire versus 9 % nosocomiale.
1 115 cas par an au total, soit un taux d’incidence moyen de 1,6 cas/100 000 habitants/an avec une incidence dépassant 5 cas/100 000 habitants/an si l’âge dépasse 80 ans.
14 épisodes de cas groupés en France entre 1998 et 2008, soit 380 cas identifiés.
Âge médian : 61 ans ; sex ratio (H/F) : 2,9.
Létalité moyenne : 13 % (22 % en 1998 versus 11 % en 2008).
Facteurs favorisants retrouvés dans 70 % des cas : tabac (57 %), diabète (13 %), cancer (10 %).
Exposition à un risque documentée dans 40 % des cas.
Réponse immunitaire
La réponse immunitaire innée de l’hôte vis-à-vis de L. pneumophila est déterminante pour contrôler la multiplication bactérienne. Tout d’abord, l’infection des cellules dendritiques par L. pneumophila induit leur apoptose [19]. Au niveau des macrophages, trois types de récepteurs sont impliqués dans la détection de L. pneumophila : les récepteurs Toll-like (TLR), Nod-like (NLR) et RIG-I-like (RLR) [45] (Figure 2). Les ligands bactériens sont le LPS, la flagelline bactérienne et le SST4 [20]. Les TLR2 et 5 reconnaissent L. pneumophila à la surface cellulaire, tandis que la reconnaissance par TLR9 s’opère dans le compartiment endosomal précoce [46]. Une fois activés, les TLR induisent une réponse antimicrobienne via l’induction du facteur transcriptionnel NF-κB, qui déclenche la production de cytokines pro-inflammatoires (IFN-γ, TNF-α). Les NLR, présents dans le cytosol, reconnaissent la flagelline de L. pneumophila et sont à l’origine de l’activation de complexes protéiques appelés collectivement « inflammasomes » : NAIP5 (NLR family, apoptosis inhibitory protein 5, aussi appelé BIRC1e), ASC (apoptosis-associated speck-like protein) et NLRC4 (NLR family, CARD domain containing 4 ; aussi appelé caspase-recruitment domain 12 ou CARD12 ou Ipaf) qui génèrent l’activation d’une protéase spécifique, la caspase-1 [21, 22]. La caspase-1 active par clivage les interleukines (IL) pro-inflammatoires IL-1β et IL-18 et induit la formation de pores membranaires entraînant une lyse osmotique de la cellule, appelée pyroptose. Ce mécanisme de mort cellulaire inflammatoire est bénéfique dans la mesure où il limite le développement de l’infection. Les RLR reconnaissent l’ADN de L. pneumophila dans le cytoplasme et favorisent l’expression des gènes codant pour l’IFN de type I, générant la production d’IFN-β [23, 24]. Enfin, les lymphocytes natural killer, recrutés et activés par les cytokines pro-inflammatoires provenant des macrophages et des cellules dendritiques, produisent de l’IFN-γ en réponse à l’action principale de l’IL-18 [20].
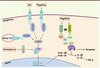 |
Figure 2. Réponse immunitaire innée à l’infection par L. pneumophila. Les récepteurs TLR 2, 5 et 9 reconnaissent respectivement le LPS, la flagelline et l’ADN de L. pneumophila. Les récepteurs cytosoliques NOD1 et NOD2 sont activés par les peptidoglycanes de L. pneumophila entraînant l’activation transcriptionelle de NF-κB et la synthèse de cytokines pro-inflammatoires. La flagelline de L. pneumophila est le ligand des récepteurs NAIP5 et NLRC4 et l’activateur de l’inflammasome afférent. Cet inflammasome permet le clivage protéolytique de la caspase-1 en forme active, entraînant la production de formes actives d’IL-1β et d’IL-18, et la pyroptose. PYR : pyrin domain ; MyD88 : myeloid differentiation primary response gene 88 ; IRAK4 : interleukin-1 receptor-associated kinase 4. |
Les cellules de l’immunité adaptative sont également recrutées à la phase précoce de l’infection. Les cellules T CD4+ interagissent avec les macrophages par l’intermédiaire du complexe majeur d’histocompatibilité (CMH) de type II, surexprimé par les macrophages activés [25]. En revanche, le CMH de type I est sous-exprimé au cours de l’infection par L. pneumophila [26]. Le rôle important de l’immunité humorale, via l’action des cellules B, a été confirmé, notamment par l’observation d’une séroconversion [27], mais également par le succès des vaccinations dans des modèles animaux [28]. Il y a production de lymphocytes B mémoires et d’anticorps dont le rôle protecteur a été démontré au cours des réinfections [29]. Le switch isotypique des IgM vers les IgG est dépendant des lymphocytes T régulateurs CD4+. Le recrutement et l’activation des cellules de l’immunité adaptative, ainsi que les interactions entre les différents types cellulaires, sont cependant encore largement méconnus.
Vers la description de groupes génétiques à risque ?
L’approche fondée sur l’analyse de profils de polymorphismes génétiques permet progressivement d’individualiser des sous-groupes à risque. Chez l’homme, le polymorphisme TLR5 pourrait augmenter la susceptibilité de l’hôte au développement de la légionellose [30].
Diagnostic de la légionellose
Symptomatologie clinique
Il n’y a pas de signe clinique spécifique de la légionellose. Elle se manifeste essentiellement par une pneumonie d’évolution progressive et sévère sans atteinte ORL et par la présence de signes extrarespiratoires (30 % des cas) devant attirer l’attention [31]. Ces manifestations incluent céphalées, confusion, diarrhée, myalgies ou encore insuffisance rénale aiguë [32]. En comparaison avec le tableau clinique d’une pneumopathie à pneumocoque, la fièvre élevée supérieure à 39 °C (OR [odds ratio] = 10,3 – IC 95 % = 2,71-38,84) et l’échec d’un traitement probabiliste par les β-lactamines (OR = 19,9 – IC 95 % = 3,47–114,24) sont des facteurs orientant vers la légionellose [33]. De plus, la littérature rapporte que 40 à 50 % des patients atteints de légionellose et présentant des signes extrarespiratoires développent une manifestation neurologique liée à la maladie [34]. La plus fréquente est la confusion qui traduit l’atteinte encéphalique dont la physiopathologie est inconnue. La présence d’une méningite (avec un profil inflammatoire du liquide cérébrospinal) n’est pas habituelle [35]. En comparaison, la fréquence des signes neurologiques ne dépasse pas 10 % au cours des pneumopathies aiguës communautaires d’étiologie différente [36].
Les examens d’imagerie pulmonaire retrouvent souvent une atteinte bilatérale, systématisée ou non, asymétrique et alvéolo-interstitielle [37]. Du point de vue biologique, on décrit classiquement une hyponatrémie (témoin d’une sécrétion inappropriée d’ADH [hormone antidiurétique]) dans la moitié des cas, une cytolyse hépatique et une élévation des créatine-phosphokinases sanguines. Une étude rapporte que l’hypophosphorémie est évocatrice du diagnostic [38]. Enfin, une hématurie microscopique et, rarement, une protéinurie, peuvent témoigner de l’atteinte rénale. Une étude récente suggère qu’une valeur du rapport CRP (protéine C-réactive)/PCT (procalcitonine) supérieure à 1,25 oriente plutôt vers une infection à Legionella, et une valeur inférieure à 0,5 vers une infection à S. pneumoniae [39].
Diagnostic microbiologique
Seuls les examens microbiologiques apportent la certitude diagnostique. Deux méthodes présentent un intérêt majeur.
La recherche d’antigènes solubles dans les urines
C'est la technique la plus rapide. Elle devient positive dès les 24 à 48 premières heures suivant le début des symptômes et le reste plusieurs semaines (2 mois en moyenne). Les tests utilisés actuellement ne détectent que L. pneumophila du sérogroupe 1. L’antigène détecté est un composant du LPS de la paroi cellulaire de L. pneumophila. En moyenne, la valeur prédictive positive des tests utilisés en France est de 85 % et leur valeur prédictive négative de 95 %. La sensibilité de la détection des antigènes urinaires est associée à la sévérité clinique de la maladie [40]. Si un patient est suspect de légionellose mais que le premier test est négatif, il n’est pas opportun d’en réaliser un second. Il est préférable de réaliser une culture et/ou une PCR sur un prélèvement pulmonaire. En Europe, la proportion de cas diagnostiqués par dosage des antigènes urinaires a beaucoup progressé depuis 1998 (15 % en 1995 versus > 90 % en 2006).
La culture de prélèvements respiratoires
Elle reste la méthode de référence. Elle est recommandée si la détection des antigènes urinaires est positive pour identifier la souche et réaliser l’enquête épidémiologique (recommandation de l’Afssaps [Agence française de sécurité sanitaire des produits de santé] - juillet 2011). Elle peut permettre le diagnostic de légionellose à L. pneumophila d’un sérogroupe différent du sérogroupe 1, et à un autre groupe que L. pneumophila si le test urinaire est négatif (en cas de forte suspicion de légionellose). Elle peut être réalisée à partir des expectorations ou de tout autre prélèvement trachéobronchique (aspiration trachéale, lavage bronchoalvéolaire, brossage protégé). La culture présente une spécificité de 100 % et une sensibilité variable de 25 à 80 %. La culture est réalisée sur milieux spécifiques. L. pneumophila peut habituellement être détectée au 3e jour de culture mais certaines souches non pneumophila peuvent nécessiter une culture prolongée. Des techniques de coculture de prélèvements pulmonaires sur tapis amibien, prenant en compte le fait que la bactérie se développe en intracellulaire, permettent dans certains cas d’augmenter la sensibilité de la culture en détruisant la flore oropharyngée contaminante.
La PCR sur prélèvement respiratoire
Elle permet un diagnostic rapide (résultat dans la journée). Sa sensibilité est de 80-100 % et sa spécificité est proche de 100 %. Le taux d’ADN de Legionella apparaît corrélé à la sévérité de l’infection [41, 42]. Seuls quelques kits commercialisés sont actuellement disponibles. Les gènes cibles les plus souvent utilisés sont les gènes codant pour les ARN ribosomaux 5S et 16S pour les techniques spécifiques du genre Legionella, et le gène mip (macrophage infectivity potentiator) pour les techniques spécifiques de l’espèce L. pneumophila. La PCR réalisée sur des prélèvements non respiratoires (urine et sérum) est séduisante car elle serait applicable aux patients qui n’expectorent pas, et éviterait la réalisation de prélèvements invasifs. Les études sont limitées, mais montrent que les sensibilités sont nettement inférieures à celles des PCR sur prélèvements respiratoires.
La sérologie
Elle a pour inconvénient son résultat tardif (délai de 10 jours à 5 semaines) et la nécessité de confirmer le diagnostic par un second prélèvement : l’intervalle recommandé entre le premier prélèvement (début des symptômes) et le second est d’environ trois à quatre semaines. Les anticorps apparaissent le plus souvent deux semaines après le début de l’infection, le pic étant atteint environ quatre à cinq semaines après le début de l’infection. La mise en évidence d’un titre d’anticorps multiplié par quatre est significative. La sérologie possède surtout une valeur épidémiologique. Sa sensibilité s’établit entre 41 et 94 %, et varie selon les techniques : 64 % pour l’Elisa, 61 % pour l’IF (immunofluorescence) indirecte.
La légionellose est une maladie à déclaration obligatoire basée sur une liste de critères diagnostiques (Tableau I). Une enquête autour du ou des cas est nécessaire et impose une intervention environnementale si une source d’émission est identifiée.
Critères à prendre en compte pour la déclaration obligatoire.
Traitement de la légionellose
Le délai de mise en route d’un traitement adapté expose au risque de mortalité accrue [44]. Les pneumopathies aiguës communautaires sévères étant le plus fréquemment dues à Streptococcus pneumoniae ou L. pneumophila, la présence de facteurs de gravité clinique implique de prescrire une antibiothérapie couvrant Legionella.
Compte-tenu de la localisation intracellulaire de la bactérie, les macrolides, les fluoroquinolones et la rifampicine sont utilisables (Figure 3). La rifampicine n’est pas recommandée en monothérapie. Legionella possède une résistance naturelle vis-à-vis des β-lactamines. Aucune résistance acquise vis-à-vis des molécules recommandées n’a été rapportée à ce jour.
 |
Figure 3. Organigramme décisionnel du traitement de la légionellose. |
Les modalités thérapeutiques en cas de légionellose confirmée prennent en considération les paramètres suivants (Afssaps - juillet 2011) :
terrain sous-jacent : présence d’une immunodépression (voir ci-dessus), polymédication, troubles hépatiques ou digestifs ;
présentation clinique : critères de gravité des pneumopathies aiguës communautaires ;
efficacité in vitro et in vivo : concentrations minimales inhibitrices comparatives des antibiotiques ;
prescription raisonnée : épargne des quinolones (émergence d’antibiorésistance), effets secondaires, interactions médicamenteuses.
La stratégie thérapeutique doit être adaptée selon le degré de sévérité4 :
les formes peu graves (patient ambulatoire ou hospitalisé en service d’urgences ou de médecine) sont traitées par voie orale. L’azithromycine est l’antibiotique le plus actif, mais il n’a pas l’AMM (autorisation de mise sur le marché) dans cette indication en France. Clarithromycine, roxithromycine, josamycine et spiramycine représentent les alternatives. L’érythromycine n’est plus l’antibiotique de choix en raison d’effets indésirables fréquents.
Les formes sévères (hospitalisation en soins intensifs ou en réanimation, contexte d’immunodépression) impliquent un traitement par voie intraveineuse. La monothérapie par fluoroquinolones trouve ici son indication. L’association de deux antibiotiques choisis dans les trois familles utilisables est une alternative. Pour les macrolides, la spiramycine est préférée à l’érythromycine.
La durée de traitement est de 8 à 14 jours dans les formes non graves ; elle doit être poursuivie 21 jours dans les formes graves et/ou chez l’immunodéprimé.
Liens d’Intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Rowbotham TJ. Preliminary report on the pathogenicity of Legionella pneumophila for freshwater and soil amoebae. J Clin Pathol 1980 ; 33 : 1179–1183. [Google Scholar]
- Holden EP, Winkler HH, Wood DO, et al. Intracellular growth of Legionella pneumophila within Acanthamoeba castellanii Neff. Infect Immun 1984 ; 45 : 18–24. [PubMed] [Google Scholar]
- Philippe C, Blech MF, Hartemann P. Multiplication intra-amibienne de Legionella pneumophila et rôle potentiel des amibes dans la transmission de la légionellose. Med Mal Infect 2006 ; 36 : 196–200. [CrossRef] [PubMed] [Google Scholar]
- Maruta K, Miyamoto H, Hamada T, et al. Entry and intracellular growth of Legionella dumoffii in alveolar epithelial cells. Am J Respir Crit Care Med 1998 ; 157 : 1967–1974. [CrossRef] [PubMed] [Google Scholar]
- Cazalet C, Rusniok C, Brüggemann H, et al. Evidence in the Legionella pneumophila genome for exploitation of host cell functions and high genome plasticity. Nat Genet 2004 ; 36 : 1165–1173. [CrossRef] [PubMed] [Google Scholar]
- Hubber A, Roy CR. Modulation of host cell function by Legionella pneumophila type IV effectors. Annu Rev Cell Dev Biol 2010 ; 26 : 261–283. [CrossRef] [PubMed] [Google Scholar]
- Girard R, Pedron T, Uematsu S, et al. Lipopolysaccharides from Legionella and Rhizobium stimulate mouse bone marrow granulocytes via Toll-like receptor 2. J Cell Sci 2003 ; 116 : 293–302. [CrossRef] [PubMed] [Google Scholar]
- Albert-Weissenberger C, Sahr T, Sismeiro O, et al. Control of flagellar gene regulation in Legionella pneumophila and its relation to growth phase. J Bacteriol 2010 ; 192 : 446–455. [CrossRef] [PubMed] [Google Scholar]
- Sahr T, Brüggemann H, Jules M, et al. Two small ncRNAs jointly govern virulence and transmission in Legionella pneumophila. Mol Microbiol 2009 ; 72 : 741–762. [CrossRef] [PubMed] [Google Scholar]
- Charpentier X, Kay E, Schneider D, et al. Antibiotics and UV radiation induce competence for natural transformation in Legionella pneumophila. J Bacteriol 2011 ; 193 : 1114–1121. [CrossRef] [PubMed] [Google Scholar]
- Harrison TG, Afshar B, Doshi N, et al. Distribution of Legionella pneumophila serogroups, monoclonal antibody subgroups and DNA sequence types in recent clinical and environmental isolates from England and Wales (2000–2008). Eur J Clin Microbiol Infect Dis 2009 ; 28 : 781–791. [CrossRef] [PubMed] [Google Scholar]
- Kozak NA, Benson RF, Brown E, et al. Distribution of lag-1 alleles and sequence-based types among Legionella pneumophila serogroup 1 clinical and environmental isolates in the United States. J Clin Microbiol 2009 ; 47 : 2525–2535. [CrossRef] [PubMed] [Google Scholar]
- Coscollá M, González-Candelas F. Direct sequencing of Legionella pneumophila from respiratory samples for sequence-based typing analysis. J Clin Microbiol 2009 ; 47 : 2901–2905. [CrossRef] [PubMed] [Google Scholar]
- Ginevra C, Lopez M, Forey F, et al. Evaluation of a nested-PCR-derived sequence-based typing method applied directly to respiratory samples from patients with Legionnaires’ disease. J Clin Microbiol 2009 ; 47 : 981–987. [CrossRef] [PubMed] [Google Scholar]
- Hilbi H, Jarraud S, Hartland E, et al. Update on Legionnaires’ disease: pathogenesis, epidemiology, detection and control. Mol Microbiol 2010 ; 76 : 1–11. [CrossRef] [PubMed] [Google Scholar]
- Campese C, Bitar D, Jarraud S, et al. Progress in the surveillance and control of Legionella infection in France, 1998–2008. Int J Infect Dis 2010 ; 15 : e30–e37. [CrossRef] [PubMed] [Google Scholar]
- Tubach F, Ravaud P, Salmon-Céron D, et al. Emergence of Legionella pneumophila pneumonia in patients receiving tumor necrosis factor-alpha antagonists. Clin Infect Dis 2006 ; 43 : e95–100. [CrossRef] [PubMed] [Google Scholar]
- Lettinga KD, Weijer S, Speelman P, et al. Reduced interferon-gamma release in patients recovered from Legionnaires’ disease. Thorax 2003 ; 58 : 63–67. [CrossRef] [PubMed] [Google Scholar]
- Nogueira CV, Lindsten T, Jamieson AM, et al. Rapid pathogen-induced apoptosis: a mechanism used by dendritic cells to limit intracellular replication of Legionella pneumophila. PLoS Pathog 2009 ; 5 : e1000478. [CrossRef] [PubMed] [Google Scholar]
- Archer KA, Alexopoulou L, Flavell RA, et al. Multiple MyD88-dependent responses contribute to pulmonary clearance of Legionella pneumophila. Cell Microbiol 2009 ; 11 : 21–36. [CrossRef] [PubMed] [Google Scholar]
- Zamboni DS, Kobayashi KS, Kohlsdorf T, et al. The Birc1e cytosolic pattern-recognition receptor contributes to the detection and control of Legionella pneumophila infection. Nat Immunol 2006 ; 7 : 318–325. [CrossRef] [PubMed] [Google Scholar]
- Ren T, Zamboni DS, Roy CR, et al. Flagellin-deficient Legionella mutants evade caspase-1- and Naip5-mediated macrophage immunity. PLoS Pathog 2006 ; 2 : e18. [CrossRef] [PubMed] [Google Scholar]
- Stetson DB, Medzhitov R. Recognition of cytosolic DNA activates an IRF3-dependent innate immune response. Immunity 2006 ; 24 : 93–103. [CrossRef] [PubMed] [Google Scholar]
- Monroe KM, McWhirter SM, Vance RE., Identification of host cytosolic sensors, bacterial factors regulating the type I interferon response to Legionella pneumophila. PLoS Pathog 2009 ; 5 : e1000665. [CrossRef] [PubMed] [Google Scholar]
- Shim HK, Kim JY, Kim MJ, et al. Legionella lipoprotein activates toll-like receptor 2 and induces cytokine production and expression of costimulatory molecules in peritoneal macrophages. Exp Mol Med 2009 ; 41 : 687–694. [CrossRef] [PubMed] [Google Scholar]
- Neumeister B, Faigle M, Spitznagel D, et al. Legionella pneumophila down-regulates MHC class I expression of human monocytic host cells and thereby inhibits T cell activation. Cell Mol Life Sci 2005 ; 62 : 578–588. [CrossRef] [PubMed] [Google Scholar]
- Horwitz MA. Cell-mediated immunity in Legionnaires’ disease. J Clin Invest 1983 ; 71 : 1686–1697. [CrossRef] [PubMed] [Google Scholar]
- Blander SJ, Breiman RF, Horwitz MA. A live avirulent mutant Legionella pneumophila vaccine induces protective immunity against lethal aerosol challenge. J Clin Invest 1989 ; 83 : 810–815. [CrossRef] [PubMed] [Google Scholar]
- Joller N, Spörri R, Hilbi H, et al. Induction and protective role of antibodies in Legionella pneumophila infection. Eur J Immunol 2007 ; 37 : 3414–3423. [CrossRef] [PubMed] [Google Scholar]
- Hawn TR, Verbon A, Lettinga KD, et al. A common dominant TLR5 stop codon polymorphism abolishes flagellin signaling and is associated with susceptibility to legionnaires’ disease. J Exp Med 2003 ; 198 : 1563–1572. [CrossRef] [PubMed] [Google Scholar]
- Fraser DW, Tsai TR, Orenstein W, et al. Legionnaires’ disease: description of an epidemic of pneumonia. N Engl J Med 1977 ; 297 : 1189–1197. [CrossRef] [PubMed] [Google Scholar]
- Fiumefreddo R, Zaborsky R, Haeuptle J, et al. Clinical predictors for Legionella in patients presenting with community-acquired pneumonia to the emergency department. BMC Pulm Med 2009 ; 9 : 4. [CrossRef] [PubMed] [Google Scholar]
- Fernández-Sabé N, Rosón B, Carratalà J, et al. Clinical diagnosis of Legionella pneumonia revisited: evaluation of the community-based pneumonia incidence study group scoring system. Clin Infect Dis 2003 ; 37 : 483–489. [CrossRef] [PubMed] [Google Scholar]
- Johnson JD, Raff MJ, Van Arsdall JA. Neurologic manifestations of Legionnaires’ disease. Medicine (Baltimore) 1984 ; 63 : 303–310. [CrossRef] [PubMed] [Google Scholar]
- Cunha BA. The atypical pneumonias: clinical diagnosis and importance. Clin Microbiol Infect 2006 ; 12 : 12–24. [CrossRef] [PubMed] [Google Scholar]
- Guleria R, Nisar N, Chawla TC, et al. Mycoplasma pneumoniae and central nervous system complications: a review. J Lab Clin Med 2005 ; 146 : 55–63. [CrossRef] [PubMed] [Google Scholar]
- Macfarlane JT, Miller AC, Roderick Smith WH, et al. Comparative radiographic features of community acquired Legionnaires’ disease, pneumococcal pneumonia, mycoplasma pneumonia, and psittacosis. Thorax 1984 ; 39 : 28–33. [CrossRef] [PubMed] [Google Scholar]
- Cunha BA. Hypophosphatemia: diagnostic significance in Legionnaires’ disease. Am J Med 2006 ; 119 : e5–e6. [CrossRef] [PubMed] [Google Scholar]
- Bellmann-Weiler R, Ausserwinkler M, Kurz K, et al. Clinical potential of C-reactive protein and procalcitonin serum concentrations to guide differential diagnosis and clinical management of pneumococcal and Legionella pneumonia. J Clin Microbiol 2010 ; 48 : 1915–1917. [CrossRef] [PubMed] [Google Scholar]
- Yzerman EPF, Boer JW den, Lettinga KD, et al. Sensitivity of three urinary antigen tests associated with clinical severity in a large outbreak of Legionnaires’ disease in The Netherlands. J Clin Microbiol 2002 ; 40 : 3232–3236. [CrossRef] [PubMed] [Google Scholar]
- Maurin M, Hammer L, Gestin B, et al. Quantitative real-time PCR tests for diagnostic and prognostic purposes in cases of legionellosis. Clin Microbiol Infect 2010 ; 16 : 379–384. [CrossRef] [PubMed] [Google Scholar]
- Diederen BMW, Bruin JP, den Boer JW, et al. Sensitivity of Legionella pneumophila DNA detection in serum samples in relation to disease severity. J Med Microbiol 2007 ; 56 : 1255. [CrossRef] [PubMed] [Google Scholar]
- Heath CH, Grove DI, Looke DF. Delay in appropriate therapy of Legionella pneumonia associated with increased mortality. Eur J Clin Microbiol Infect Dis 1996 ; 15 : 286–290. [CrossRef] [PubMed] [Google Scholar]
- Da Re S, Ploy MC. Antibiotiques et réponse SOS bactérienne une voie efficace d’acquisition des résistances aux antibiotiques. Med Sci (Paris) 2012 ; 28 : 179–184. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Kowalinski E, Louber J, Gerlier D, Cusack S. RIG-I - Un commutateur moléculaire détecteur d’ARN viral. Med Sci (Paris) 2012 ; 28 : 136–138. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Alexopoulou L, Desnues B, Demaria O. Le récepteur Toll-like 8 : un TLR pas comme les autres. Med Sci (Paris) 2012 ; 28 : 96–102. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1. Trafic intracellulaire de Legionella dans l’hôte eucaryote. (1) Après sa phagocytose, (2) Legionella échappe à la fusion endosome-lysosome, (3 et 4) recrute des vésicules du réticulum endoplasmique (RE) et amorce une phase de multiplication dans une vacuole autonome nommée legionella-containing vacuole (LCV) (5) puis induit la lyse de la cellule hôte pour infecter les cellules voisines (6) . Toutes ces étapes sont sous le contrôle direct du système Dot/Icm ou SST4 (d’après [6]). |
| Dans le texte | |
 |
Figure 2. Réponse immunitaire innée à l’infection par L. pneumophila. Les récepteurs TLR 2, 5 et 9 reconnaissent respectivement le LPS, la flagelline et l’ADN de L. pneumophila. Les récepteurs cytosoliques NOD1 et NOD2 sont activés par les peptidoglycanes de L. pneumophila entraînant l’activation transcriptionelle de NF-κB et la synthèse de cytokines pro-inflammatoires. La flagelline de L. pneumophila est le ligand des récepteurs NAIP5 et NLRC4 et l’activateur de l’inflammasome afférent. Cet inflammasome permet le clivage protéolytique de la caspase-1 en forme active, entraînant la production de formes actives d’IL-1β et d’IL-18, et la pyroptose. PYR : pyrin domain ; MyD88 : myeloid differentiation primary response gene 88 ; IRAK4 : interleukin-1 receptor-associated kinase 4. |
| Dans le texte | |
 |
Figure 3. Organigramme décisionnel du traitement de la légionellose. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




