| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
Nos jeunes pousses ont du talent !
|
|
|---|---|---|
| Page(s) | 402 - 405 | |
| Section | Partenariat médecine/sciences - Écoles doctorales - Masters | |
| DOI | https://doi.org/10.1051/medsci/2026063 | |
| Published online | 24 April 2026 | |
La thérapie cellulaire du diabète de type 1
Progrès et défis restants
Cellular therapy of type 1 diabetes: progress and remaining challenges
Master 2 Innovation en Biotechnologies, Sorbonne Université, Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
Contexte du diabète de type 1 : les traitements actuels et leurs limites
Le pancréas est un organe ayant pour fonctions la sécrétion de sucs digestifs par les cellules acineuses du compartiment exocrine et la production d’insuline dans les îlots de Langerhans (appelé aussi îlots pancréatiques) par les cellules β du compartiment endocrine (Figure 1A).
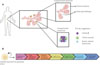 |
Figure 1 Génération de cellules bêta dérivées de cellules souches pluripotentes (PSC) pour la transplantation. A. Le pancréas est constitué d’un compartiment exocrine et d’îlots de Langerhans. Ces derniers contiennent les cellules endocrines (notamment les cellules β), des cellules neurales et endothéliales. B. Différenciation dirigée des cellules souches pluripotentes (PSC) en cellules β pancréatiques. Ce processus reproduit in vitro les grandes étapes du développement pancréatique embryonnaire et repose sur une succession progressive de phases définies par l’activation de voies de signalisation spécifiques et l’expression de facteurs de transcription clés. Les PSC sont d’abord engagées vers l’endoderme définitif (SOX17, FOXA2), puis vers l’intestin primitif et l’intestin antérieur postérieur, avant la spécification des progéniteurs pancréatiques (PDX1, NKX6.1). L’activation du programme endocrinien (NGN3) conduit ensuite à la formation de progéniteurs endocriniens, puis de cellules β immatures produisant de l’insuline, qui acquièrent progressivement une maturation fonctionnelle caractérisée par une sécrétion d’insuline dépendante du glucose (MAFA). Figure réalisée sur BioRender. |
Le diabète de type 1 (DT1) est une maladie auto-immune caractérisée par la destruction des cellules β pancréatiques. Cette destruction est médiée, principalement, par les lymphocytes T qui vont infiltrer les îlots de Langerhans afin d’induire leur apoptose via des mécanismes cytotoxiques et inflammatoires. L’insuline est essentielle pour réguler la glycémie en permettant aux cellules, comme les cellules musculaires ou les adipocytes d’internaliser le glucose. L’absence d’insuline conduit à une hyperglycémie chronique qui, par des mécanismes délétères tels que le stress oxydatif et la glycation des protéines, favorise l’apparition de complications graves comme la néphropathie, la neuropathie ou la rétinopathie. Ce type de diabète apparaît tout au long de la vie mais possède un pic d’incidence chez l’enfant et l’adulte, nécessitant une insulinothérapie à vie [1, 2].
Aujourd’hui, les traitements reposent principalement sur des pompes à insuline ou des injections sous cutanées pluri quotidiennes d’insuline. Cependant, ces approches présentent des limites : risques d’hypoglycémies, charge mentale et complications à long terme (infection du site d’injection, lipohypertrophie, variabilité de l’absorption de l’insuline). Les technologies avancées, comme les pancréas artificiels, bien que prometteuses, restent difficiles d’accès à grande échelle et coûteuses (Figure 2). Cette technologie combine des capteurs de glucose qui transmettent en continu les valeurs glycémiques à l’algorithme qui calcule la quantité d’insuline à administrer et envoie l’ordre à la pompe, ce qui permet ainsi d’automatiser l’administration d’insuline en continu imitant ainsi la fonction des cellules β pancréatiques et de réduire les risques d’hypoglycémie. Cependant, le patient devient dépendant de la fiabilité des capteurs (erreur, retard de mesure) et des risques techniques [3, 4].
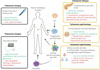 |
Figure 2 Schéma de différentes thérapies pour le traitement du diabète de type 1, de leurs avantages et inconvénients. Les cellules souches pluripotentes (PSC) peuvent être différenciées en progéniteurs pancréatiques, îlots de Langerhans ou cellules bêta, puis transplantées pour restaurer la production d’insuline. Pompe à insuline/biosimilaires : permettent une administration continue et ajustable de l’insuline en fonction des besoins du patient, améliorant le contrôle glycémique au quotidien ; limites : ne restaurent pas la régulation physiologique par les cellules β, exposent à des pannes techniques et représentent un coût chronique élevé. Pancréas artificiel : combine capteur de glucose, algorithme et pompe pour automatiser partiellement la délivrance d’insuline, réduisant les variations glycémiques ; limites : système encore imparfait (retard de capteur, erreurs algorithmiques), dépendance permanente à un dispositif externe et coût important. Transplantation de pancréas entier : restaure une sécrétion endogène d’insuline physiologique et un contrôle glycémique durable ; limites : chirurgie lourde avec morbidité significative, immunosuppression à vie, risque de rejet et pénurie d’organes. Transplantation d’îlots pancréatiques : procédure moins invasive que la greffe de pancréas, permettant une sécrétion partielle d’insuline et une réduction des hypoglycémies sévères ; limites : perte progressive des îlots, immunosuppression nécessaire, efficacité souvent transitoire et disponibilité limitée des donneurs. Cellules souches différenciées en progéniteurs, îlots ou cellules β : offrent une source potentiellement illimitée de cellules productrices d’insuline et une standardisation des greffons ; limites : différenciation souvent incomplète entraînant une hétérogénéité cellulaire, faible maturité fonctionnelle, risque de rejet immunitaire et risque tumoral en cas de cellules pluripotentes résiduelles. Figure réalisée sur BioRender. |
Une autre approche est la transplantation de pancréas par un donneur compatible. Elle implique une intervention chirurgicale lourde associée à un traitement immunosuppresseur, une forte mortalité et morbidité [5-7]. La transplantation d’îlots pancréatiques à partir de donneurs cadavériques, est une alternative puisqu’elle est peu invasive, ne nécessite pas de chirurgie et permet une récupération plus rapide, tout en améliorant le contrôle glycémique du patient. Cependant, elle pose des problèmes d’approvisionnement avec un nombre de pancréas disponibles restreint, de rejet immunitaire et d’échec de la greffe. En effet, un grand nombre d’îlots transplantés est nécessaire, entraînant souvent l’utilisation de plusieurs pancréas donneurs, donc des cellules de plusieurs origines génétiques et donc des profils immunitaires différents, ce qui peut augmenter les réponses immunitaires du patient et le rejet de la greffe (Figure 2) [2-4, 7-10].
Ainsi, face à ces limitations, les thérapies cellulaires, qui utilisent la greffe de cellules naturelles ou modifiées (encapsulation, différenciation ou modifications visant la protection immune) afin de restaurer la fonction d’un tissu ou d’un organe, apparaissent comme une alternative. Leur objectif est de restaurer la fonction insulinique par la transplantation de cellules β fonctionnelles, générées à partir de cellules souches ou issues de donneurs (Figure 1B) [5, 6].
Thérapies cellulaires pour traiter le diabète de type 1
Les cellules souches pluripotentes humaines (hPSC : human Pluripotent Stem Cells) sont un outil potentiel pour traiter le DT1 car elles ont la capacité de s’auto-renouveler et de se différencier en différents types cellulaires fonctionnels [7-9, 11]. Il en existe deux types : les cellules souches embryonnaires (hESC : human Embryonic Stem Cells) et les cellules souches pluripotentes induites (hiPSC : human induced Pluripotent Stem Cells). Ces dernières sont issues de cellules somatiques reprogrammées en cellules souches pluripotentes. L’utilisation des hiPSC induit moins de considérations éthiques que les hESC, puisqu’elles proviennent en général de fibroblastes de la peau ou de cellules sanguines périphériques du patient alors que les hESC dérivent de blastocystes humains, des embryons très précoces issus de fécondations in vitro.
Les hPSC sont différenciées en cellules β pancréatiques grâce à des protocoles expérimentaux qui visent à reproduire le développement embryonnaire du pancréas (Figure 1). Malgré des décennies d’optimisation des protocoles de différenciation, la production in vitro de ces cellules est difficile du fait de différenciation incomplète, de la perte importante de cellules après transplantation, mais aussi de la production trop faible d’insuline [4, 9, 11]. Les cellules progénitrices pancréatiques peuvent aussi être transplantées et se différencier in vivo en cellules endocrines productrices d’insuline. Cependant, la transplantation de cellules progénitrices présente un risque accentué de formation de tumeurs, puisque ces cellules sont immatures et hautement prolifératives [2, 4, 5]. Enfin, la transplantation d’îlots pancréatiques dérivés de cellules souches (hiPSC ou hESC) est une possibilité mais nécessite une immunosuppression car celles-ci sont souvent allogéniques (provenant d’un donneur génétiquement différent du patient) (Figure 2) [8, 11, 12].
L’avantage d’utiliser les hPSC pour la thérapie cellulaire est d’avoir une source illimitée de cellules β [3, 5]. De plus, l’utilisation des cellules somatiques du patient lui-même permet de limiter les risques de rejet immunitaire [3, 12, 13]. Enfin, cette thérapie ne nécessite pas d’intégrer plusieurs types de cellules, contrairement à une greffe d’organe. Malgré l’utilisation des cellules du patient pour créer les hiPSC, la réponse autoimmune contre les cellules greffées reste un problème majeur. En effet, le processus de reprogrammation et de différenciation peut changer l’expression des antigènes pouvant ainsi les rendre partiellement immunogènes [3, 7].
Les essais cliniques associés
Les premiers essais cliniques chez des patients atteints de DT1 utilisant la technologie des cellules souches ont été menés avec la transplantation de cellules endodermiques pancréatiques (progéniteurs pancréatiques) dérivées de cellules souches. Un essai clinique, mené par l’entreprise ViaCyte, a débuté en 2014. Les cellules transplantées se différencient in vivo grâce à un système d’encapsulation sous-cutanée et les signaux physiologiques de l’hôte, en cellules endocrines pancréatiques productrices d’insuline. De plus, cette capsule imperméable permet de protéger les cellules du système immunitaire du patient et de limiter le risque de tératome. Les tératomes sont des tumeurs matures ou immatures dus à la présence résiduelle de cellules pluripotentes non différenciées capables de proliférer après transplantation. Cet essai clinique a été arrêté malgré les faibles effets indésirables (réponse immunitaire locale, fibrose autour de la capsule) en raison d’une prise de greffe fonctionnelle insuffisante (environ 15 %). En effet, aucune sécrétion d’insuline n’a été détectée car de la fibrose au niveau de la capsule a induit la perte du greffon [3-5, 7-11, 14]. Pour surmonter ce problème, un nouvel essai clinique a été conduit en 2017 par ViaCyte, utilisant toujours des cellules progénitrices pancréatiques, mais avec des perforations dans la membrane des capsules favorisant la vascularisation du greffon par l’hôte mais nécessitant un traitement immunosuppresseur. Ce dispositif transplanté par voie sous-cutanée a permis la survie du greffon chez 32 % des patients et une fonction endocrine chez environ 30 %, évaluée par l’expression d’insuline endogène et de marqueurs endocriniens dans les greffons, sans que des formations tumorales soient observées. Cependant, la production d’insuline était trop faible et les greffons étaient très hétérogènes du fait de la présence de plusieurs types cellulaires issus d’une différenciation des PSC (cellules endocrines immatures, cellules non endocrines et cellules β-like fonctionnelles), expliquant la faible production d’insuline, les différences inter-patients et la survie inégale des cellules transplantées [3, 7, 10].
En 2021, des îlots de Langerhans entièrement différenciés dérivés de cellules souches ont été transplantés chez des patients atteints de DT1 dans le cadre d’un essai clinique de phase 1/2 mené par Vertex Pharmaceuticals. Il s’agit d’une thérapie qui nécessite l’utilisation d’immunosuppresseurs pour protéger les cellules transplantées contre le rejet de greffe. Cette thérapie n’est destinée qu’aux patients atteints d’hypoglycémie sévère car ils nécessitent un contrôle glycémique stable et que les options existantes soient insuffisantes. Les résultats ont montré une restauration de la production d’insuline et du contrôle glycémique pour les six patients et une indépendance à l’insuline exogène chez quatre des patients. Ainsi, en 2024, l’essai clinique de Vertex est entré en phase 3. C’est la première fois qu’une thérapie cellulaire pour des patients atteints de DT1 arrive en phase 3 des essais cliniques [7, 8, 10, 14, 15]. Vertex a ensuite initié un deuxième essai clinique en 2023, évaluant leur thérapie cellulaire encapsulée dans un dispositif conçu pour protéger les cellules greffées de la réponse immunitaire. Ce dispositif permet la croissance vasculaire, grâce à des membranes poreuses qui favorisent la croissance de capillaires, apportant oxygène et nutriments aux cellules implantées. Cet essai de phase 1/2 est toujours en cours de recrutement [8, 10].
En 2024, les premiers résultats d’un essai clinique de phase 1 de transplantation autologue (provenant du patient) d’îlots dérivés de cellules souches pluripotentes pour le traitement du DT1 ont été publiés [12, 13]. La patiente a acquis 75 jours après la transplantation, une indépendance à l’insuline exogène qui s’est maintenue pendant la période de suivi de 1 an. Ces résultats prometteurs en termes d’innocuité et d’efficacité encouragent à mener d’autres études cliniques avec ce type de cellules permettant la thérapie cellulaire personnalisée. Cependant, les effets à plus long terme de cette greffe restent à évaluer. De plus, la patiente prenait déjà des immunosuppresseurs à la suite d’une greffe de foie antérieure empêchant une évaluation de la réponse auto-immune potentielle [12, 13].
Des essais cliniques utilisant des dispositifs implantés, constitués de membranes semi-perméables isolant physiquement les cellules greffées du système immunitaire tout en laissant diffuser nutriments et insuline, ainsi que sur le développement de cellules hypoimmunes, génétiquement modifiées afin d’échapper au système immunitaire, sont actuellement en cours [7-10].
Perspectives
Les thérapies cellulaires contre le DT1 présentent un fort potentiel, mais plusieurs défis restent à surmonter [5].
Il est primordial d’améliorer les protocoles de différenciation pour garantir une production fonctionnelle, à grande échelle, de cellules β. De plus, la protection immunitaire est un défi majeur. En effet, pour ne plus avoir besoin d’un traitement immunosuppresseur à long terme, il est nécessaire de développer des méthodes d’encapsulation efficaces ou de thérapies géniques pour moduler la réponse immunitaire. Un autre défi est l’accessibilité financière, avec la nécessité de réduire les coûts pour rendre ces traitements accessibles à un large public [6, 7].
Les progrès technologiques et la collaboration entre chercheurs, entreprises et cliniciens joueront un rôle clé pour transformer ces approches en réalités cliniques.
Conflits d’intérêt
Les auteures déclarent qu’elles n’ont aucun conflit d’intérêt.
Références
- Drucker DJ. Transforming type 1 diabetes: the next wave of innovation. Diabetologia 2021 ; 64 : 1059–1065. [Google Scholar]
- Klerk E de, Hebrok M. Stem Cell-Based Clinical Trials for Diabetes Mellitus. Front Endocrinol (Lausanne) 2021 ; 12 : 631463. [Google Scholar]
- Memon B, Abdelalim EM. Stem Cell Therapy for Diabetes: Beta Cells versus Pancreatic Progenitors. Cells 2020 ; 9 : 283. [Google Scholar]
- Loretelli C, Assi E, Seelam AJ, et al. Cell therapy for type 1 diabetes. Expert Opin Biol Ther 2020 ; 20 : 887–897. [Google Scholar]
- Sneddon JB, Tang Q, Stock P, et al. Stem Cell Therapies for Treating Diabetes: Progress and Remaining Challenges. Cell Stem Cell 2018 ; 22 : 810–823. [Google Scholar]
- Marfil-Garza BA, Imes S, Verhoeff K, et al. Pancreatic islet transplantation in type 1 diabetes: 20-year experience from a single-centre cohort in Canada. Lancet Diabetes Endocrinol 2022 ; 10 : 519–532. [Google Scholar]
- Hogrebe NJ, Ishahak M, Millman JR. Developments in stem cell-derived islet replacement therapy for treating type 1 diabetes. Cell Stem Cell 2023 ; 30 : 530–548. [Google Scholar]
- Calafiore R, Luca G, Gaggia F, et al. Human Stem Cell Therapy for the Cure of Type 1 Diabetes Mellitus (T1D): A Hurdle Course between Lights and Shadows. Endocrines 2024 ; 5 : 465–477. [Google Scholar]
- Christiansen JR, Kirkeby A. Clinical translation of pluripotent stem cell-based therapies: successes and challenges. Development 2024 ; 151 : dev202067. [Google Scholar]
- Kirkeby A, Main H, Carpenter M. Pluripotent stem-cell-derived therapies in clinical trial: A 2025 update. Cell Stem Cell 2025 ; 32 : 10–37. [Google Scholar]
- Ghoneim MA, Gabr MM, El-Halawani SM, et al. Current status of stem cell therapy for type 1 diabetes: a critique and a prospective consideration. Stem Cell Res Ther 2024 ; 15 : 23. [Google Scholar]
- The Lancet Diabetes Endocrinology null. Stem-cell therapy for diabetes: the hope continues. Lancet Diabetes Endocrinol 2024 ; 12 : 775. [Google Scholar]
- Wang S, Du Y, Zhang B, et al. Transplantation of chemically induced pluripotent stem-cell-derived islets under abdominal anterior rectus sheath in a type 1 diabetes patient. Cell 2024 ; 187 : 6152-6164. e18. [Google Scholar]
- Keymeulen B, De Groot K, Jacobs-Tulleneers-Thevissen D, et al. Encapsulated stem cell-derived β cells exert glucose control in patients with type 1 diabetes. Nat Biotechnol 2024 ; 42 : 1507–1514. [Google Scholar]
- REICHMAN TW, RICORDI C, NAJI A, et al. 836-P: Glucose-Dependent Insulin Production and Insulin-Independence in Type 1 Diabetes from Stem Cell–Derived, Fully Differentiated Islet Cells—Updated Data from the VX-880 Clinical Trial. Diabetes 2023 ; 72 : 836-P. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Génération de cellules bêta dérivées de cellules souches pluripotentes (PSC) pour la transplantation. A. Le pancréas est constitué d’un compartiment exocrine et d’îlots de Langerhans. Ces derniers contiennent les cellules endocrines (notamment les cellules β), des cellules neurales et endothéliales. B. Différenciation dirigée des cellules souches pluripotentes (PSC) en cellules β pancréatiques. Ce processus reproduit in vitro les grandes étapes du développement pancréatique embryonnaire et repose sur une succession progressive de phases définies par l’activation de voies de signalisation spécifiques et l’expression de facteurs de transcription clés. Les PSC sont d’abord engagées vers l’endoderme définitif (SOX17, FOXA2), puis vers l’intestin primitif et l’intestin antérieur postérieur, avant la spécification des progéniteurs pancréatiques (PDX1, NKX6.1). L’activation du programme endocrinien (NGN3) conduit ensuite à la formation de progéniteurs endocriniens, puis de cellules β immatures produisant de l’insuline, qui acquièrent progressivement une maturation fonctionnelle caractérisée par une sécrétion d’insuline dépendante du glucose (MAFA). Figure réalisée sur BioRender. |
| Dans le texte | |
 |
Figure 2 Schéma de différentes thérapies pour le traitement du diabète de type 1, de leurs avantages et inconvénients. Les cellules souches pluripotentes (PSC) peuvent être différenciées en progéniteurs pancréatiques, îlots de Langerhans ou cellules bêta, puis transplantées pour restaurer la production d’insuline. Pompe à insuline/biosimilaires : permettent une administration continue et ajustable de l’insuline en fonction des besoins du patient, améliorant le contrôle glycémique au quotidien ; limites : ne restaurent pas la régulation physiologique par les cellules β, exposent à des pannes techniques et représentent un coût chronique élevé. Pancréas artificiel : combine capteur de glucose, algorithme et pompe pour automatiser partiellement la délivrance d’insuline, réduisant les variations glycémiques ; limites : système encore imparfait (retard de capteur, erreurs algorithmiques), dépendance permanente à un dispositif externe et coût important. Transplantation de pancréas entier : restaure une sécrétion endogène d’insuline physiologique et un contrôle glycémique durable ; limites : chirurgie lourde avec morbidité significative, immunosuppression à vie, risque de rejet et pénurie d’organes. Transplantation d’îlots pancréatiques : procédure moins invasive que la greffe de pancréas, permettant une sécrétion partielle d’insuline et une réduction des hypoglycémies sévères ; limites : perte progressive des îlots, immunosuppression nécessaire, efficacité souvent transitoire et disponibilité limitée des donneurs. Cellules souches différenciées en progéniteurs, îlots ou cellules β : offrent une source potentiellement illimitée de cellules productrices d’insuline et une standardisation des greffons ; limites : différenciation souvent incomplète entraînant une hétérogénéité cellulaire, faible maturité fonctionnelle, risque de rejet immunitaire et risque tumoral en cas de cellules pluripotentes résiduelles. Figure réalisée sur BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




