| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 355 - 364 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2026054 | |
| Published online | 24 April 2026 | |
Les astrocytes, intégrateurs centraux multiéchelles des états de vigilance
Astrocytes and sleep: from genes to networks
Interactions neurogliales dans la physiologie et les maladies cérébrales, Centre de recherche interdisciplinaire en biologie, Collège de France, CNRS UMR 7241, INSERM U1050, Université PSL, PSL-NEURO, Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Les astrocytes sont des cellules gliales du système nerveux central qui jouent un rôle central dans la régulation de l’activité synaptique et du sommeil. Les récentes avancées en génie génétique, en neuro-imagerie et en biologie moléculaire ont apporté une meilleure compréhension des fonctions astrocytaires. Cette revue met en lumière les multiples mécanismes par lesquels les astrocytes régulent le sommeil, impliquant des modifications transcriptomiques et morphologiques ainsi que la gliotransmission. Mieux comprendre les différentes fonctions astrocytaires permet d’approfondir notre compréhension des mécanismes du sommeil et d’ouvrir la voie à de nouveaux traitements favorisant un meilleur sommeil.
Abstract
Astrocytes are glial cells of the central nervous system that play key roles in regulating synaptic activity and sleep. Recent advances in genetic engineering, neuroimaging, and molecular biology have provided new insights into astrocytic functions. This review highlights the various mechanisms through which astrocytes regulate sleep, including transcriptomic and morphological changes, as well as gliotransmission. A better understanding of these astrocyte-dependent processes in sleep physiology will refine current models of sleep regulation and may open new avenues for sleep-targeted therapies.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Décrits pour la première fois en 1858 par Rudolf Virchow1, les astrocytes sont des cellules gliales [1] (→) dont le nom provient du grec astron (étoile) et kytos (cellule), en référence à leur forme en étoile [2]. Longtemps considérés comme de simples éléments de soutien, ils sont aujourd’hui reconnus comme des acteurs essentiels de la communication neuronale. Grâce à leurs longs prolongements, ils peuvent interagir à la fois avec les vaisseaux sanguins et les neurones, ce qui leur confère une position stratégique au sein du tissu cérébral.
(→) Voir m/s n° 3, 2019, page 199
Pendant des décennies, l’étude des astrocytes a été limitée par des contraintes techniques. Leurs très fins prolongements rendaient leur observation difficile en microscopie, et l’absence de signaux électriques rapides, tels que les potentiels d’action des neurones, a longtemps concentré l’attention sur les neurones. De plus, l’absence de marqueurs spécifiques entravait leur identification. Récemment, les progrès en génie génétique, avec le développement de modèles murins transgéniques, et en microscopie, grâce aux microscopes à deux photons et à super-résolution, ont progressivement révélé leurs multiples fonctions.
Ainsi, il est à présent clairement établi que les astrocytes détectent l’activité synaptique grâce à une large gamme de récepteurs, transporteurs et canaux ioniques, et y répondent via des signaux calciques (Ca2+) [3]. Ils peuvent libérer des gliotransmetteurs ou modifier leur couverture synaptique, c’est-à-dire l’étendue avec laquelle leurs prolongements périsynaptiques entourent les synapses, influençant ainsi directement la diffusion et la recapture des neurotransmetteurs. Les astrocytes forment, avec les neurones, la « synapse tripartite2 » [4–6] (→) et remplissent de multiples fonctions : maintien de l’homéostasie ionique et hydrique, soutien métabolique, couplage neurovasculaire, défense contre le stress oxydatif, participation à la formation de la barrière hémato-encéphalique et aux réponses inflammatoires. Reliés entre eux par des jonctions communicantes [7] (→), ils forment des réseaux capables de moduler l’activité neuronale et, par conséquent, des fonctions intégrées telles que le sommeil [8].
(→) Voir m/s n° 6-7, 2012, page 582
(→) Voir m/s n° 2, 2021, page 127
(→) Voir m/s n° 1, 2009, page 102
Dès la fin du xixe siècle, Santiago Ramón y Cajal3 suggérait déjà que les astrocytes puissent réguler le sommeil en modulant l’efficacité synaptique de manière différentielle entre la veille et le sommeil [9]. Un siècle plus tard, les découvertes en neurobiologie ont révolutionné notre compréhension du rôle des astrocytes dans la régulation du sommeil. Ces cellules émergent à présent comme des intégrateurs du rythme circadien, du métabolisme énergétique, et de l’activité synaptique, agissant à l’échelle moléculaire, cellulaire et du réseau astrocytaire, pour réguler les états de vigilance.
Expression génique astrocytaire : une orchestration du rythme circadien et de la régulation du sommeil
Les astrocytes jouent un rôle central dans la régulation du rythme circadien, essentiel à l’alternance veille-sommeil. Dans le noyau suprachiasmatique4 (SCN), la principale horloge circadienne du cerveau, ils possèdent une horloge moléculaire autonome reposant sur une boucle de rétroaction transcriptionnelle et traductionnelle. Les facteurs de transcription CLOCK (circadian locomotor output cycles kaput) et BMAL1 (brain and muscle ARNT-like protein) exprimés par ces astrocytes, forment un hétérodimère qui active l’expression des gènes Per (period) et Cry (cryptochrome), dont les produits inhibent à leur tour le complexe CLOCK-BMAL1. Ce mécanisme, présent aussi dans les neurones, suffit chez la souris à générer des oscillations circadiennes et à moduler les comportements rythmiques [10], démontrant le rôle déterminant des astrocytes du noyau suprachiasmatique dans la coordination circadienne (Figure 1).
 |
Figure 1 Schéma récapitulatif de différents mécanismes de régulation du sommeil par les astrocytes. Les astrocytes du noyau suprachiasmatique modulent des rythmes circadiens grâce à leur horloge moléculaire, via une boucle de rétroaction négative de transcription-traduction (TTFL). Au niveau cortical, ils peuvent également réguler différentiellement la transcription de gènes, modulant ainsi la couverture synaptique ainsi que la taille du réseau astrocytaire dépendante de l’expression de la connexine 30 (Cx30). Les variations d’expression d’aquaporine-4 (AQP4) permettent aussi une circulation du liquide céphalorachidien et un nettoyage du cerveau pendant le sommeil lent. Les variations de calcium intracellulaire des astrocytes du cortex sont moins prononcées pendant le sommeil, comparées à l’éveil, ainsi que les stocks de glycogène qui participeraient aussi à la régulation du sommeil. Les astrocytes participent aussi à la recapture et à la libération de neurotransmetteurs, ce qui régule le réseau neuronal voisin. Enfin, les astrocytes sont impliqués dans la régulation des poids synaptiques, en les diminuant au cours du sommeil lent. |
La régulation circadienne du transporteur astrocytaire GAT3 (GABA transporter 3), en constitue un exemple typique : son expression rythmique module différentiellement l’absorption de GABA (acide γ-aminobutyrique) dans le noyau suprachiasmatique [11]. Le jour, l’augmentation de GAT3 favorise la clairance du GABA, réduisant son niveau extracellulaire et stimulant l’activité neuronale. La nuit, la diminution de GAT3 entraîne l’accumulation de GABA, renforçant l’inhibition neuronale. Cette oscillation circadienne de GAT3 illustre comment les astrocytes modulent les oscillations GABAergiques et l’inhibition des neurones du noyau suprachiasmatique, contribuant plus largement à la régulation des rythmes circadiens, dont fait partie l’alternance veille-sommeil.
Les analyses transcriptomiques d’astrocytes corticaux et striataux5 montrent que 1,4 % de leurs transcrits varient selon l’état de vigilance [12]. Ainsi, cinquante-cinq gènes sont surexprimés durant le sommeil, dont Cirp (cold-inducible RNA-binding protein), codant pour une protéine liant l’ARN, qui favorise la traduction et la survie cellulaire, et Uba1 (ubiquitin-activating enzyme E1), codant pour une enzyme d’ubiquitination, impliquée dans l’homéostasie synaptique. À l’inverse, près de 400 transcrits, dont Gjb6 (gap junction protein beta 6), codant pour la connexine 30 (Cx30), sont davantage exprimés pendant l’éveil, favorisant la formation du cytosquelette et l’allongement des prolongements astrocytaires périsynaptiques. Ces modifications structurales rapprocheraient les prolongements astrocytaires des synapses pour optimiser la recapture du glutamate pendant l’éveil, tandis que leur retrait durant le sommeil favoriserait la diffusion du glutamate et la synchronisation neuronale du sommeil lent [12].
L’expression circadienne du gène FABP7 (fatty acid binding protein 7), qui code une protéine de liaison aux acides gras spécifiquement exprimée dans les astrocytes, établit également un lien fonctionnel entre le métabolisme lipidique et la régulation du sommeil. Une mutation ponctuelle (T61M) de FABP7 entraîne une fragmentation du sommeil chez l’être humain, un phénomène également observé chez la souris après délétion de ce gène [13]. Enfin, l’augmentation du transporteur MCT1 (monocarboxylate transporter 1) pendant le sommeil suggère une intensification de la navette lactate astrocyte-neurone, mécanisme par lequel le lactate produit par les astrocytes contribue au soutien énergétique des neurones. Cette adaptation participerait aux processus de restauration métabolique cérébrale associés au sommeil. Dans le noyau préoptique ventrolatéral, une région essentielle à la régulation du sommeil, la réponse métabolique des astrocytes au glucose dépend, elle aussi, du moment circadien [14], ce qui souligne la capacité des astrocytes à ajuster l’apport énergétique en fonction de l’état de vigilance. Par ailleurs, il a été montré que la privation de sommeil modifie l’expression des gènes impliqués dans la navette lactate astrocyte-neurone, suggérant que les astrocytes adaptent dynamiquement leur activité métabolique et le transport du lactate en réponse aux besoins fluctuants de l’éveil et du sommeil [15]. Ces ajustements métaboliques contribuent ainsi au maintien de la fonction neuronale et à l’homéostasie du sommeil.
L’ensemble de ces travaux démontre que les astrocytes adaptent dynamiquement leur profil transcriptionnel, leur modulation de l’inhibition neuronale ainsi que leur soutien métabolique en fonction des états de vigilance. Ces ajustements illustrent leur contribution intégrée à la régulation des rythmes circadiens et à l’alternance veille-sommeil.
Modulations morphologiques des astrocytes : de la couverture synaptique au réseau astrocytaire
Modulation de la couverture synaptique
Dans le système nerveux central, environ la moitié des synapses sont entourées par des prolongements astrocytaires, les PAP (perisynaptic astrocytic processes). Ces fines extensions, riches en canaux ioniques, en récepteurs et en transporteurs, permettent aux astrocytes de détecter et de moduler l’activité neuronale [4]. Des travaux récents, notamment ceux de Bellesi et collaborateurs, ont confirmé la plasticité de ces prolongements dans le cortex, en mettant en évidence leur allongement pendant l’éveil et leur rétraction durant le sommeil, modifiant ainsi la couverture synaptique et la diffusion du glutamate. À l’aide d’imagerie tridimensionnelle et d’analyses transcriptomiques, ces auteurs ont montré que ces changements morphologiques s’accompagnent de variations d’expression génétique affectant notamment le cytosquelette d’actine et la matrice extracellulaire [12].
Sur le plan moléculaire, des protéines telles que l’ezrine, la radixine et la connexine 30 soutiennent cette plasticité morphologique. En effet, leurs variations d’expression modulent le cytosquelette des astrocytes et la distance des PAP aux synapses. Cette plasticité structurelle permet aux astrocytes de réguler la transmission synaptique : en se rapprochant ou en s’éloignant des synapses, les PAP modifient la diffusion et/ou la recapture des neurotransmetteurs (Figure 1). Des études en microscopie électronique 3D ont montré qu’un court épisode de privation de sommeil suffit à induire un rapprochement des prolongements astrocytaires de la fente synaptique, renforçant l’idée que la morphologie des PAP varie de manière dynamique, en fonction des rythmes de veille et de sommeil [16].
Modulation du réseau astrocytaire
Les astrocytes forment entre eux un réseau interconnecté par des jonctions communicantes composées de connexines 30 et 43 (Cx30 et Cx43). Ce couplage permet l’échange direct de petites molécules et crée un réseau fonctionnel dont la dimension s’ajuste de manière dynamique. Les fluctuations d’expression des connexines peuvent élargir ou réduire ce réseau, modulant ainsi différentiellement l’excitabilité neuronale [17] et le sommeil [18]. Ainsi, une déficience conditionnelle en Cx43 induit une réduction du couplage astrocytaire et une hypersomnolence nocturne [19]. De même, l’γ-hydroxybutyrate et l’oléamide, qui favorisent le sommeil, réduisent cette connectivité [20]. Inversement, le modafinil6 augmente sélectivement l’expression de Cx30 et le couplage astrocytaire [21], tout en stimulant l’éveil. Ces résultats suggèrent une expansion du réseau astrocytaire pendant l’éveil et sa réduction pendant le sommeil.
De plus, il a été démontré que l’absence de Cx30 réduit la taille du réseau astrocytaire ainsi que l’activité neuronale [22, 23], tandis que sa surexpression étend ce réseau tout en diminuant paradoxalement l’excitabilité des neurones [17]. Ainsi, les astrocytes régulent finement la communication intercellulaire pour équilibrer l’activité neuronale et assurer la transition entre veille et sommeil. L’ensemble de ces observations suggère que le réseau astrocytaire est physiologiquement optimisé pour maintenir l’homéostasie cérébrale. Une diminution ou une expansion de ce réseau altère les fonctions neuronales et la dynamique veille/sommeil.
Rôles des astrocytes dans l’élimination des métabolites et le stockage du glycogène
Élimination des métabolites cérébraux
Le sommeil joue un rôle essentiel dans l’évacuation des déchets métaboliques accumulés dans le cerveau pendant l’éveil [24] (→).
(→) Voir m/s n° 12, 2021, page 1183
Il a été mis en évidence que les taux de peptide β-amyloïde (Aβ) sont plus élevés durant l’éveil que pendant le sommeil, ce qui suggère que le repos favorise sa clairance. Un dysfonctionnement ou un ralentissement de ce processus d’élimination pourrait donc contribuer à la progression de maladies neurodégénératives, telles que la maladie d’Alzheimer. Ainsi, une réduction de la durée ou de la qualité du sommeil augmente le risque de développer des troubles neurodégénératifs, notamment des démences [24]. Ce mécanisme repose sur le système glymphatique, un réseau de circulation du liquide interstitiel dépendant des astrocytes, qui contribue à la clairance des métabolites [25] (→).
(→) Voir m/s n° 1, 2019, page 55
L’aquaporine-4 (AQP4), un canal hydrique fortement exprimé au niveau des pieds astrocytaires périvasculaires, permet les échanges d’eau entre les espaces périvasculaires et le parenchyme, favorisant ainsi ce flux glymphatique [25]. La suppression de l’expression d’AQP4 altère ce flux, soulignant le rôle fondamental des astrocytes dans le nettoyage du parenchyme cérébral (Figure 1).
De plus, il a récemment été démontré que les contractions rythmées des vaisseaux sanguins, régulées par des libérations de noradrénaline pendant le sommeil lent, permettent la circulation du liquide cérébrospinal dans le parenchyme et en permettent l’élimination des déchets. Cependant, sous zolpidem, un somnifère fréquemment prescrit, ces contractions vasculaires sont fortement altérées, ce qui pourrait avoir des répercussions sur le nettoyage glymphatique et soulève des inquiétudes quant à son usage à long terme ainsi que quant à son impact potentiel sur la progression des maladies neurodégénératives [26].
Rôle du glycogène astrocytaire dans la régulation du cycle veille-sommeil
Les astrocytes stockent le glycogène, qu’ils dégradent en glucose et en lactate afin de soutenir le métabolisme neuronal lors de périodes d’éveil, souvent associées à une activité neuronale accrue. Durant le sommeil lent, ces réserves astrocytaires sont restaurées. Certaines études suggèrent que la synthèse et la consommation du glycogène coexistent durant l’éveil, mais que la synthèse est plus difficilement observable, en raison de la forte consommation associée à cette période.
L’enzyme GSK-3β (glycogène synthase kinase-3β), impliquée dans la régulation de la synthèse du glycogène, joue un rôle dans la stabilité des états de vigilance. Sa surexpression fragmente le sommeil lent et le sommeil paradoxal en augmentant le nombre d’épisodes tout en réduisant leur durée, sans altérer la durée totale du sommeil [27]. Ces observations indiquent que le métabolisme astrocytaire ne se limite pas à la restauration énergétique, mais participe activement à la régulation et à la stabilité des états de veille et de sommeil (Figure 1).
Signalisation calcique astrocytaire et régulation veille-sommeil
Fluctuations physiologiques du calcium astrocytaire
Les astrocytes présentent des variations intracellulaires de calcium (Ca2+) qui suivent les différents états de vigilance. Dans le cortex frontal, les niveaux de Ca2+ sont élevés durant l’éveil et diminuent pendant le sommeil lent et le sommeil paradoxal (Figure 2), avec des variations particulièrement marquées dans les prolongements astrocytaires [28]. De plus, dans cette région cérébrale, ces fluctuations, ne reflètent pas simplement l’activité neuronale, mais elles précèdent les transitions entre états de vigilance, suggérant un rôle causal des astrocytes dans la régulation du sommeil [28]. Ainsi, il a été démontré que l’augmentation de la fréquence des événements calciques précède l’apparition des ondes lentes du sommeil lent et les transitions vers le sommeil paradoxal ou l’éveil [8]. De plus, l’activité des astrocytes serait plus synchronisée pendant l’éveil, lorsque l’activité neuronale est plus désynchronisée, et inversement, pendant le sommeil lent [28] (Figure 2).
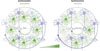 |
Figure 2 Schéma illustrant les variations corticales de Ca2+ intracellulaire dans les astrocytes en fonction des niveaux de vigilance. Pendant l’éveil, les niveaux de Ca2+ sont plus élevés et synchronisés que pendant le sommeil lent au niveau cortical, surtout avant la transition vers le sommeil. Adapté de [28] avec BioRender. |
Le récepteur de l’inositol 1,4,5-trisphosphate de type 2 (IP3 R2), exprimé spécifiquement par les astrocytes, est un acteur clé de la libération du Ca2+ à partir des réserves intracellulaires en réponse à l’activation des voies métabotropiques7. Il a été montré que l’absence du gène codant ce récepteur perturbe les signaux calciques dans les astrocytes corticaux et entraîne une fragmentation du sommeil lent, ainsi qu’une diminution de la puissance delta8 [29], reflet de la qualité du sommeil.
De même, l’inactivation ubiquitaire de la protéine STIM1 (stromal interaction molecule 1), essentielle à l’entrée de Ca2+ dans la cellule, réduit la durée de récupération du sommeil après une privation [28]. Ces résultats renforcent l’idée que la signalisation calcique astrocytaire soutient l’homéostasie du sommeil, bien que ses dynamiques varient selon les régions cérébrales. En effet, pendant le sommeil lent, les niveaux de Ca2+ diminuent fortement dans le cortex et l’hippocampe, tandis qu’ils demeurent relativement stables dans l’hypothalamus et le tronc cérébral. Ainsi, le rôle physiologique des astrocytes dans la régulation du cycle veille/sommeil dépendrait des régions cérébrales [30] (→).
(→) Voir m/s n° 3, 2018, page 199
Stimulation optogénétique ou chimique des astrocytes
Les approches optogénétiques9 et DREADD10 (designer receptors exclusively activated by designer drugs) ont démontré que l’activation des astrocytes module le sommeil de manière région-spécifique. Dans l’hypothalamus postérieur, la stimulation astrocytaire augmente transitoirement le sommeil lent et le sommeil paradoxal, tandis qu’au niveau hippocampique, elle réduit le temps d’éveil sans altérer les oscillations corticales [31]. Dans le pont cérébral, elle diminue la durée du sommeil paradoxal et renforce l’activité delta du sommeil lent. À l’inverse, dans le noyau préoptique ventrolatéral, l’activation astrocytaire prolonge le sommeil, probablement par l’intermédiaire d’une libération locale d’adénosine qui inhibe les interneurones locaux et active les neurones promoteurs du sommeil [32].
Au niveau cortical, les signaux Ca2+ astrocytaires précèdent les ondes lentes, suggérant un rôle proactif des astrocytes dans la synchronisation neuronale [29, 33]. De plus, leur stimulation induit cette synchronisation en favorisant la libération de glutamate [34] (→).
(→) Voir m/s n° 2, 2013, page 142
Durant l’éveil, l’activité Ca2+ élevée des astrocytes soutient la désynchronisation neuronale nécessaire au maintien de la vigilance et aux fonctions cognitives (Figure 2).
Enfin, l’activation sélective de deux voies de signalisation différentes (Gi ou Gq) avec des DREADD induit des effets distincts qui dépendent de la région ciblée : selon le site d’activation, la voie Gi peut augmenter l’intensité des ondes lentes, et donc la qualité du sommeil sans modifier sa durée, tandis que la voie Gq allonge la durée du sommeil lent, ou, au contraire, favoriser un éveil prolongé sans compensation homéostatique. Dans l’ensemble, la signalisation calcique astrocytaire apparaît donc comme un mécanisme actif du contrôle veille-sommeil (Figure 2) : elle module la synchronisation, la transmission synaptique et la stabilité des états de vigilance, selon des dynamiques spatio-temporelles spécifiques à chaque région cérébrale, renforçant ainsi les fonctions propres aux structures où les astrocytes sont situés.
Modulation astrocytaire du sommeil par la libération de gliotransmetteurs et de substances régulatrices
Gliotransmission et mécanismes de libération
La gliotransmission désigne la libération, par les cellules gliales, de molécules actives capables de moduler l’activité neuronale et synaptique [34]. Pour les astrocytes, cette libération peut se faire par exocytose dépendante du Ca2+, impliquant le complexe SNARE (soluble N-ethylmaleimide-sensitive-factor attachment protein receptor), un ensemble de protéines membranaires qui assurent la fusion des vésicules avec la membrane plasmique et la libération régulée de gliotransmetteurs. Elle peut également emprunter d’autres voies, comme l’ouverture de canaux hémi-jonctionnels (connexines, pannexines) ou l’inversion fonctionnelle du flux de certains transporteurs, permettant la libération de médiateurs en fonction des gradients de concentration. Ces mécanismes permettent aux astrocytes d’influencer la neurotransmission synaptique et de moduler les cycles veille-sommeil [35] (→).
(→) Voir m/s n° 10, 2016, page 820
L’adénosine : signal clé de la pression de sommeil
Parmi les molécules libérées, l’adénosine joue un rôle central dans l’homéostasie du sommeil [14, 36]. Son accumulation extracellulaire est le reflet de la dégradation d’ATP durant l’éveil, notamment dans le cortex, l’hippocampe et l’hypothalamus, constituant une pression de sommeil. Chez des souris exprimant une forme mutée du complexe SNARE11 astrocytaire, il a été montré que la suppression de l’exocytose altère le rebond12 de sommeil après privation. Ces résultats suggèrent l’importance de la libération astrocytaire d’adénosine par exocytose dans l’homéostasie du sommeil. Cependant, des travaux plus récents ont remis en question ce résultat : des mesures directes d’adénosine indiquent que les neurones du prosencéphale basal pourraient représenter une source majeure d’adénosine, tandis que les astrocytes interviendraient principalement en modulant sa production extracellulaire via la dégradation de l’ATP libéré par des hémicanaux.
Dans le noyau préoptique ventrolatéral, la libération d’ATP astrocytaire suivie de sa conversion en adénosine par les interneurones locaux augmente la pression de sommeil [14]. L’adénosine exerce ensuite son action inhibitrice sur les récepteurs A113 et, excitatrice, sur les récepteurs A2A. Elle favorise alors le sommeil en inhibant les interneurones locaux et en activant les neurones promoteurs de sommeil [37, 38] (Figure 3).
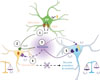 |
Figure 3 Représentation schématique de l’origine et du mode d’action de l’adénosine dans le noyau préoptique ventrolatéral. Après une activation astrocytaire, l’élévation du Ca2+ intracellulaire entraîne la libération d’ATP par les hémicanaux ou les récepteurs P2X7 (purinergic receptor) (1). Cet ATP est ensuite hydrolysé en adénosine par la phosphatase alcaline non spécifique des tissus (TNAP) au niveau des interneurones (2). L’adénosine (3) agit alors sur les récepteurs A1R de ces interneurones, réduisant leur inhibition sur les neurones promoteurs de sommeil (4). Parallèlement, elle exerce un double effet sur ces neurones : elle induit une inhibition neuronale via l’activation des A1R et elle induit une activation des récepteurs A2AR, (5) dont l’effet dépolarisant l’emporte sur l’inhibition via l’activation des A1R. |
Les prostaglandines : un relais astrocytaire dans la régulation du sommeil
Les astrocytes libèrent également des prostaglandines, en particulier la prostaglandine D2 (PGD2), considérée comme l’un des plus puissants inducteurs endogènes du sommeil. Sa concentration dans le liquide cérébrospinal présente une variation circadienne, augmentant pendant l’éveil. La PGD2 agit alors en se liant à son récepteur DP1, exprimé par les astrocytes, ce qui élève les niveaux extracellulaires d’adénosine et module alors à la fois l’activité neuronale et le flux sanguin dans le noyau préoptique ventrolatéral [37, 38].
Ainsi, par la libération coordonnée d’adénosine et de prostaglandines, les astrocytes se placent au cœur du dialogue neurone-astrocyte. Par l’intermédiaire de la gliotransmission, ils assurent une interface dynamique entre le métabolisme, l’activité neuronale et la régulation du cycle veille/sommeil [38].
Le lactate
Les astrocytes libèrent du lactate, dont la concentration varie au cours du cycle veille/sommeil. Les astrocytes métabolisent le glucose en lactate, un processus stimulé par la capture du glutamate issu de l’activité neuronale. Grâce à la navette astrocyte-neurone du lactate, ce lactate est ensuite transféré aux neurones afin de subvenir à leurs besoins énergétiques [39] (→).
(→) Voir m/s n° 4, 2006, page 356
Des travaux récents suggèrent que le lactate astrocytaire pourrait également contribuer à la régulation de l’endormissement en ralentissant la décharge neuronale corticale [40]. Cependant, ce rôle reste discuté et semble dépendre des régions cérébrales considérées. Le lactate exercerait toutefois une fonction neuromodulatrice en stimulant l’expression de gènes liés à la plasticité synaptique, tels que les gènes Arc (activity regulated cytoskeleton associated protein) et Zif268 (zinc finger protein 268), via l’activation des récepteurs NMDA (récepteur au N-méthyl-D-aspartate) et de la voie de signalisation Erk1/2 (extracellular signal-regulated kinase 1 et 2) [41]. Ainsi, le lactate soutiendrait à la fois le métabolisme et la plasticité neuronale, contribuant aux processus de consolidation mnésique associés au sommeil.
Les neurotransmetteurs
Les astrocytes peuvent libérer du glutamate de manière dépendante du Ca2+, ce qui favorise la synchronisation des réseaux corticaux et l’activité à ondes lentes du sommeil [42, 43]. Ils participent aussi à la régulation du GABA, un neurotransmetteur inhibiteur majeur des circuits neuronaux sous-tendant le sommeil. En modulant sa concentration extracellulaire grâce au transporteur GAT-1 (GABA transporter 1), les astrocytes ajustent le tonus inhibiteur nécessaire à l’initiation et au maintien du sommeil. Ainsi, il a été démontré que l’inhibition pharmacologique de GAT-1 raccourcit la latence d’endormissement et prolonge la durée du sommeil lent, confirmant le rôle central du contrôle astrocytaire du GABA dans la dynamique du sommeil. Ce mécanisme semble conservé au cours de l’évolution, puisqu’un rôle comparable du GABA d’origine gliale a été mis en évidence chez la drosophile [44].
Les cytokines
Les astrocytes libèrent diverses cytokines impliquées dans la régulation du sommeil, notamment l’interleukine-1β (IL-1β) et l’interleukine-33 (IL-33), toutes deux issues de la famille des IL-1. L’expression d’IL-1β dans le cortex, l’hippocampe et l’hypothalamus suit un rythme circadien. Il a été démontré que son injection accroît la durée du sommeil lent, tandis que son inhibition la réduit. Chez les souris transgéniques exprimant le récepteur à l’IL-1β spécifiquement dans les astrocytes, on observe une fragmentation du sommeil associée à une diminution de la puissance delta, ce qui suggère l’existence d’un lien entre immunité et homéostasie du sommeil.
Par ailleurs, l’IL-33, agit comme un signal d’alarme glial favorisant l’élagage synaptique grâce à l’activation des cellules microgliales [45] (→).
(→) Voir m/s n° 11, 2018, page 913
Son absence entraîne une augmentation du nombre de synapses excitatrices et une hyperexcitabilité neuronale, soulignant son rôle dans le remodelage des circuits neuronaux.
Ainsi, les cytokines astrocytaires, en particulier IL-1β et IL-33, participent activement à la régulation neuroimmunitaire du sommeil et à la plasticité cérébrale.
Le BDNF
Le facteur BDNF (brain-derived neurotrophic factor), principalement synthétisé par les neurones puis maturé et libéré par les astrocytes, joue un rôle clé dans la croissance cellulaire, la potentialisation à long terme et l’homéostasie du sommeil. Chez la souris, l’injection intracorticale de BDNF au début de la phase d’éveil intensifie le sommeil à ondes lentes, tandis qu’une réduction de 50 % des niveaux de BDNF diminue la durée des épisodes de sommeil profond [46]. Une perte d’expression du BDNF dépendante du promoteur IV, l’un des promoteurs alternatifs de ce gène, est également associée à une réduction de cette activité [47] suggérant un déséquilibre de l’homéostasie du sommeil.
Le BDNF agit via son récepteur TrkB (tropomyosin receptor kinase B), qui existe sous deux isoformes : TrkB.FL (neuronale) et TrkB.T1 (astrocytaire et tronquée). L’inactivation génétique de TrkB.T1 chez la souris n’affecte pas le sommeil lent, mais génère des perturbations similaires aux troubles de l’humeur, avec une augmentation du sommeil paradoxal, une latence réduite de celui-ci, et une fragmentation du sommeil [8]. Ces résultats suggèrent que le BDNF astrocytaire constituerait un lien entre la régulation du sommeil et la santé mentale.
Régulation synaptique par les astrocytes : élagage et plasticité
Les astrocytes assurent l’homéostasie synaptique du cerveau adulte en éliminant les synapses inutiles par phagocytose. Dans l’hippocampe, ils ciblent préférentiellement les synapses excitatrices via le récepteur phagocytaire MEGF10 (multiple epidermal growth factor-like domains 10) [48], tandis que dans le cervelet, les cellules gliales de Bergmann régulent la taille synaptique grâce au transporteur ABCA1 (ATP-binding cassette A1) [49]. Dans le cortex, la privation de sommeil augmente l’expression du récepteur MERTK (Mer tyrosine kinase), un récepteur tyrosine-kinase impliqué dans la phagocytose, ainsi que des marqueurs de peroxydation lipidique, reflet des dommages membranaires associés à une activité synaptique soutenue. Ces observations suggèrent une activation accrue des mécanismes phagocytaires visant à éliminer des composants synaptiques altérés des synapses sursollicitées, en particulier des éléments présynaptiques tels que les boutons axonaux [16]. Ces ajustements constituent probablement une réponse adaptative à la charge synaptique de l’éveil prolongé. Les astrocytes participent également à la plasticité synaptique à long terme grâce à leur capacité à moduler la couverture synaptique, la concentration extracellulaire de glutamate et de potassium, ainsi que l’étendue de leur réseau. Ils pourraient aussi contribuer à la réduction des poids synaptiques associés au sommeil via la libération de TNFα (tumor necrosis factor α) [50]. Toutefois, les effets du TNFα observés in vitro sur les synapses glutamatergiques et GABAergiques étant hétérogènes [51, 52], il reste difficile de conclure que le TNFα d’origine gliale constitue, à lui seul, un mécanisme moléculaire robuste impliqué dans l’ajustement de la force synaptique pendant le sommeil.
Durant le sommeil lent profond, un processus essentiel de réduction des forces synaptiques est impliqué dans le maintien de la plasticité cérébrale. Selon l’hypothèse de l’homéostasie synaptique proposée par Tononi et Cirelli, l’activité de l’éveil induirait une potentialisation progressive des synapses, tandis que le sommeil permettrait leur renormalisation. Ce mécanisme viserait à prévenir la saturation des circuits neuronaux, ce qui compromettrait la plasticité synaptique et la capacité du cerveau à encoder de nouvelles informations [53]. Certaines connexions, associées à des traces mnésiques14 jugées pertinentes, seraient cependant préservées, permettant la consolidation des souvenirs.
Ainsi, le sommeil agirait comme une période de rééquilibrage synaptique. Les astrocytes, en coordination étroite avec les neurones, joueraient un rôle central dans cette régulation en modulant l’environnement synaptique et métabolique, favorisant ainsi le maintien des fonctions cognitives et de l’homéostasie cérébrale.
Conclusion
Longtemps sous-estimés, les astrocytes apparaissent aujourd’hui comme des acteurs centraux de la régulation du sommeil. Véritables intégrateurs métaboliques et temporels, ils coordonnent l’activité neuronale et le cycle veille-sommeil grâce à la régulation de la transcription génique, à la modulation des signaux calciques, à leurs fonctions énergétiques, à la plasticité de leur couverture synaptique et aux mécanismes de gliotransmission.
Défis méthodologiques
Malgré des avancées techniques considérables, l’étude des astrocytes souffre encore d’un manque de spécificité cellulaire. Les outils génétiques actuels, tels que les systèmes Cre-loxP, les approches optogénétiques et chimiogénétiques, ne permettent pas toujours de distinguer les effets propres aux astrocytes de ceux des neurones. Les limites de résolution spatiale et temporelle de l’imagerie représentent aussi un frein majeur à l’analyse des interactions astrocyte-neurone. Le développement de techniques de pointe, telles que la transcriptomique unicellulaire, la microscopie à super-résolution ou encore la protéomique spatiale, devrait permettre de mieux caractériser l’hétérogénéité fonctionnelle des cellules gliales et leurs contributions spécifiques, qui varient souvent selon les régions cérébrales considérées.
Perspectives cliniques
Bien que cette revue n’aborde pas spécifiquement le rôle des astrocytes dans les maladies du sommeil, il convient de souligner leur implication dans des processus tels que la neuroinflammation, la phagocytose et la gliose réactive15, qui sont intimement impliqués dans les troubles du sommeil et les maladies neurodégénératives [54]. Leur capacité à moduler les cascades inflammatoires suggère un rôle déterminant dans diverses perturbations pathologiques du sommeil, comme l’insomnie, l’hypersomnie ou la fragmentation du sommeil, observées dans ces affections [54, 55]. Étant donné que les troubles du sommeil affectent plus d’un tiers de la population et représentent un enjeu majeur de santé publique, il est primordial de mieux comprendre la contribution des astrocytes à la régulation du sommeil. À l’avenir, les approches expérimentales devront mieux cibler ces cellules tout en tenant compte de leurs interactions avec les autres cellules gliales et les circuits neuronaux, afin d’ouvrir la voie à de nouvelles stratégies thérapeutiques.
Conflits d’intérêt
L’auteure déclare qu’elle n’a aucun conflit d’intérêt.
Références
- Agid Y, Fan X. L’autre moitié du cerveau ; les cellules gliales. Med Sci (Paris) 2019 ; 35 : 199–200. [Google Scholar]
- Lenhossek M von. der feinere bau des nervensystems im lichte neuester forchungen. Berlin: Fischer’s Medicinische Buchhandlung H. Kornfiel 1895 ; 177–245. [Google Scholar]
- Cornell-Bell AH, Finkbeiner SM, Cooper MS, et al. Glutamate induces calcium waves in cultured astrocytes: Long-range glial signaling. Science 1990 ; 247 : 470–3. [Google Scholar]
- Panatier A, Robitaille R. L’astrocyte, un partenaire clé des neurones au cours de la transmission synaptique de base. Med sci (Paris) 2012 ; 28 : 582–4. [Google Scholar]
- Araque A, Parpura V, Sanzgiri RP, et al. Tripartite synapses: glia, the unacknowledged partner. Trends Neurosci 1999 ; 22 : 208–15. [Google Scholar]
- Arizono M, Idziak A, Nägerl UV. Il faut être trois pour danser le tango - Illuminer les signaux Ca2+ des synapses tripartites. Med Sci (Paris) 2021 ; 37 : 127–9. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Rouach N. Les connexines astrocytaires nourrissent les synapses. Med Sci (Paris) 2009 ; 25 : 102–4. [Google Scholar]
- Bellier F, Walter A, Lecoin L, et al. Astrocytes at the heart of sleep: from genes to network dynamics. Cell Mol Life Sci 2025 ; 82 : 207. [Google Scholar]
- Ramon y Cajal S. Contribucion al conocimiento de la neuroglia del cerebro humano. Trabajos del Laboratorio de Investigaciones Biologicas de la Universidad de Madrid. 1899. [Google Scholar]
- Brancaccio M, Patton AP, Chesham JE, et al. Astrocytes control circadian timekeeping in the suprachiasmatic nucleus via glutamatergic signaling. Neuron 2017 ; 93 : 1420–35.e5. [Google Scholar]
- Patton AP, Morris EL, McManus D, et al. Astrocytic control of extracellular GABA drives circadian timekeeping in the suprachiasmatic nucleus. Proc Nat Acad Sci USA 2023 ; 120 : e2301330120. [Google Scholar]
- Bellesi M, Vivo L de, Tononi G, et al. Effects of sleep and wake on astrocytes: clues from molecular and ultrastructural studies. BMC Biol 2015 ; 13 : 66. [Google Scholar]
- Gerstner JR, Flores CC, Lefton M, et al. FABP7: a glial integrator of sleep, circadian rhythms, plasticity, and metabolic function. Front Syst Neurosci 2023 ; 17 : 1212213. [Google Scholar]
- Scharbarg E, Daenens M, Lemaître F, et al. Astrocyte-derived adenosine is central to the hypnogenic effect of glucose. Sci Rep 2016 ; 6 : 19107. [Google Scholar]
- Petit J-M, Gyger J, Burlet-Godinot S, et al. genes involved in the astrocyte-neuron lactate shuttle (ANLS) are specifically regulated in cortical astrocytes following sleep deprivation in mice. Sleep 2013 ; 36 : 1445–58. [Google Scholar]
- Bellesi M, Vivo L De, Chini M, et al. Sleep loss promotes astrocytic phagocytosis and microglial activation in mouse cerebral cortex. J Neurosci 2017 ; 37 : 5263–73. [Google Scholar]
- Hardy E, Moulard J, Walter A, et al. Upregulation of astroglial connexin 30 impairs hippocampal synaptic activity and recognition memory. PLoS Biol 2023 ; 21 : e3002075. [Google Scholar]
- Yang S, Kong X-Y, Hu T, et al. Aquaporin-4, Connexin-30, and Connexin-43 as biomarkers for decreased objective sleep quality and/or cognition dysfunction in patients with chronic insomnia disorder. Front Psychiatry 2022 ; 13 : 1–9. [Google Scholar]
- Clasadonte J, Scemes E, Wang Z, et al. Connexin 43-mediated astroglial metabolic networks contribute to the regulation of the sleep-wake cycle. Neuron 2017 ; 95 : 1365–80.e5. [Google Scholar]
- Guan X, Cravatt BF, Ehring GR, et al. The sleep-inducing lipid oleamide deconvolutes gap junction communication and calcium wave transmission in glial cells. J Cell Biol 1997 ; 139 : 1785–92. [Google Scholar]
- Liu X, Petit J-M, Ezan P, et al. The psychostimulant modafinil enhances gap junctional communication in cortical astrocytes. Neuropharmacology 2013 ; 75 : 533–8. [Google Scholar]
- Hardy E, Cohen-Salmon M, Rouach N, et al. Astroglial Cx30 differentially impacts synaptic activity from hippocampal principal cells and interneurons. Glia 2021 ; 69 : 2178–98. [Google Scholar]
- Pannasch U, Freche D, Dallérac G, et al. Connexin 30 sets synaptic strength by controlling astroglial synapse invasion. Nat Neurosci 2014 ; 17 : 549–58. [CrossRef] [PubMed] [Google Scholar]
- Sabia S, Dumurgier J. Relation entre durée du sommeil chez l’adulte et risque de démence. Med Sci (Paris) 2021 ; 37 : 1183–5. [Google Scholar]
- Thomas J-L, Jacob L, Boisserand L. Système lymphatique et cerveau. Med Sci (Paris) 2019 ; 35 : 55–61. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Hauglund NL, Andersen M, Tokarska K, et al. Norepinephrine-mediated slow vasomotion drives glymphatic clearance during sleep. Cell 2025 ; 188 : 606–22.e17. [Google Scholar]
- Ahnaou A, Drinkenburg WHIM. Disruption of glycogen synthase kinase-3-beta activity leads to abnormalities in physiological measures in mice. Behav Brain Res 2011 ; 221 : 246–52. [Google Scholar]
- Ingiosi AM, Hayworth CR, Harvey DO, et al. A Role for astroglial calcium in mammalian sleep and sleep regulation. Curr Biol 2020 ; 30 : 4373–83.e7. [Google Scholar]
- Bojarskaite L, Bjørnstad DM, Pettersen KH, et al. Astrocytic Ca2+ signaling is reduced during sleep and is involved in the regulation of slow wave sleep. Nat Commun 2020 ; 11 : 3240. [Google Scholar]
- Clasadonte J. Rôle des réseaux astrocytaires métaboliques dans le maintien de l’éveil. Med Sci (Paris) 2018 ; 34 : 199–202. [Google Scholar]
- Pelluru D, Konadhode RR, Bhat NR, et al. Optogenetic stimulation of astrocytes in the posterior hypothalamus increases sleep at night in C57BL/6J mice. Eur J Neurosci 2016 ; 43 : 1298–306. [Google Scholar]
- Choi I, Kim J, Jeong J, et al. Astrocyte-derived adenosine excites sleep-promoting neurons in the ventrolateral preoptic nucleus: Astrocyte-neuron interactions in the regulation of sleep. Glia 2022 ; 70 : 1864–85. [Google Scholar]
- Vaidyanathan T V, Collard M, Yokoyama S, et al. Cortical astrocytes independently regulate sleep depth and duration via separate GPCR pathways. Elife 2021 ; 10 : 1–55. [Google Scholar]
- Pfrieger FW, Reber M. Un nouvel aperçu des mécanismes de la communication neurone-glie. Med Sci (Paris) 2013 ; 29 : 142–4. [Google Scholar]
- Chever O, Dossi E, Rouach N. Contrôle astroglial de la synchronisation neuronale. Med Sci (Paris) 2016 ; 32 : 820–2. [Google Scholar]
- Porkka-Heiskanen T, Kalinchuk A V. Adenosine, energy metabolism and sleep homeostasis. Sleep Med Rev 2011 ; 15 : 123–35. [Google Scholar]
- Scharbarg E, Walter A, Lecoin L, et al. Prostaglandin d2 controls local blood flow and sleep-promoting neurons in the vlpo via astrocyte-derived adenosine. ACS Chem Neurosci 2023 ; 14 : 1063–70. [Google Scholar]
- Walter A, Rancillac A. Les astrocytes du VLPO, acteurs clés de la régulation du sommeil. Médecine du Sommeil 2024 ; 21 : 198–206. [Google Scholar]
- Costalat R, Aubert A, Magistretti PJ, et al. Le lactate est-il un substrat énergétique majeur pour les neurones ? Med Sci (Paris) 2006 ; 22 : 356–7. [Google Scholar]
- Bozzo L, Puyal J, Chatton J-Y. Lactate modulates the activity of primary cortical neurons through a receptor-mediated pathway. PLoS One 2013 ; 8 : e71721. [Google Scholar]
- Yang J, Ruchti E, Petit J-M, et al. Lactate promotes plasticity gene expression by potentiating NMDA signaling in neurons. Proc Nat Acad SciUSA 2014 ; 111 : 12228–33. [Google Scholar]
- Poskanzer KE, Yuste R. Astrocytic regulation of cortical UP states. Proc Nat Acad Sci USA 2011 ; 108 : 18453–8. [Google Scholar]
- Poskanzer KE, Yuste R. Astrocytes regulate cortical state switching in vivo. Proc Nat Acad Sci USA 2016 ; 113 : 1–10. [Google Scholar]
- Chaturvedi R, Stork T, Yuan C, et al. Astrocytic GABA transporter controls sleep by modulating GABAergic signaling in Drosophila circadian neurons. Curr Biol 2022 ; 1–14. [Google Scholar]
- Dalmas E. Une nouvelle mission pour l’IL-33 - L’élagage synaptique. Med Sci (Paris) 2018 ; 34 : 913–5. [Google Scholar]
- Garner JM, Chambers J, Barnes AK, et al. Changes in brain-derived neurotrophic factor expression influence sleep-wake activity and homeostatic regulation of rapid eye movement sleep. Sleep 2018 ; 41 : 1–14. [Google Scholar]
- Hill JL, Hardy NF, Jimenez D V, et al. Loss of promoter IV-driven BDNF expression impacts oscillatory activity during sleep, sensory information processing and fear regulation. Transl Psychiatry 2016 ; 6 : e873. [Google Scholar]
- Lee J-H, Kim J, Noh S, et al. Astrocytes phagocytose adult hippocampal synapses for circuit homeostasis. Nature 2021 ; 590 : 612–7. [Google Scholar]
- Morizawa YM, Matsumoto M, Nakashima Y, et al. Synaptic pruning through glial synapse engulfment upon motor learning. Nat Neurosci 2022 ; 25 : 1458–69. [Google Scholar]
- Puentes-Mestril C, Aton SJ. Linking Network Activity to Synaptic Plasticity during Sleep: Hypotheses and Recent Data. Front Neural Circuits 2017 ; 11 : 61. [Google Scholar]
- Stellwagen D, Beattie EC, Seo JY, et al. Differential regulation of ampa receptor and GABA receptor trafficking by tumor necrosis factor-α. J Neurosci2005 ; 25 : 3219–28. [Google Scholar]
- Olmos G, Lladó J. Tumor necrosis factor alpha: a link between neuroinflammation and excitotoxicity. Mediators Inflamm 2014 ; 2014 : 1–12. [Google Scholar]
- Tononi G, Cirelli C. Sleep and the price of plasticity: from synaptic and cellular homeostasis to memory consolidation and integration. Neuron 2014 ; 81 : 12–34. [CrossRef] [PubMed] [Google Scholar]
- Li Y, Que M, Wang X, et al. Exploring astrocyte-mediated mechanisms in sleep disorders and comorbidity. Biomedicines 2023 ; 11 : 2476. [Google Scholar]
- Sofroniew M V. Multiple Roles for Astrocytes as Effectors of cytokines and inflammatory mediators. The Neuroscientist 2014 ; 20 : 160–72. [Google Scholar]
Rudolf Ludwig Karl Virchow (1821-1902) est un médecin pathologiste et homme politique prussien, considéré comme l’un des fondateurs de l’anatomie pathologique moderne. Il effectua l’essentiel de sa carrière à l’hôpital de la Charité de Berlin, se faisant le promoteur d’une médecine strictement orientée vers les sciences naturelles. En tant qu’homme politique, il fut l’un des représentants du Parti progressiste allemand (ndlr).
La synapse tripartite désigne l’élément pré- et postsynaptique, ainsi que leur association fonctionnelle étroite avec les prolongements des astrocytes (des cellules gliales environnantes) présentent dans le système nerveux central (ndlr).
Santiago Ramón y Cajal (1852-1934) est un histologiste et neuroscientifique espagnol, colauréat du prix Nobel de physiologie ou médecine en 1906 avec Camillo Golgi « en reconnaissance de leurs travaux sur la structure du système nerveux » (ndlr).
Le noyau suprachiasmatique est une structure comprenant environ 20 000 cellules et située à la base de l’hypothalamus, au-dessus du chiasma optique (d’où leur nom). Il est responsable du contrôle des rythmes circadiens (ndlr).
Le striatum, appelé également le corps strié, est une structure nerveuse subcorticale paire. Il est impliqué dans le mouvement involontaire, la motivation alimentaire ou sexuelle, la gestion de la douleur et la cicatrisation voire la régénérescence de certains tissus cérébraux (ndlr).
Le modafinil est un psychostimulant favorisant l’éveil, utilisé dans le traitement de la narcolepsie et de l’hypersomnie idiopathique (ndlr).
L’adjectif métabotrope qualifie une classe de récepteurs transmembranaires qui, lorsqu’ils ont fixé leur ligand, changent de conformation et activent une cascade d’évènements intracellulaires par l’intermédiaire de protéines transductrices du signal appelées protéines G (ndlr).
Les ondes cérébrales Delta ont une fréquence de 0 à 4 Hz, et sont émises pendant le sommeil profond. Lorsqu’elle est dans cet état, la personne dort profondément (ndlr).
L’optogénétique est une approche qui permet de contrôler l’activité des cellules grâce à l’introduction ciblée de protéines cannal sensibles à la lumière (ndlr).
DREADD désigne une classe de récepteurs protéiques artificiellement conçus utilisés dans le domaine de la chémogénétique qui sont activés sélectivement par certains ligands (ndlr).
Les protéines SNAREs sont les principales responsables de la fusion membranaire et du trafic membranaire au sein des cellules eucaryotes (ndlr).
Lorsqu’une personne est privée de sommeil, le corps réagit en prolongeant la durée de sommeil la nuit suivante (ndlr).
Le récepteur A1 est un récepteur couplé aux protéines G ayant pour ligand endogène l’adénosine. Il peut être couplé à des protéines Gi, qui inhibent l’activité de l’adénylate cyclase, ou à des protéines G qui interfèrent avec l’ouverture de canaux ioniques (ndlr).
La trace mnésique correspond aux modifications physiques et chimiques qui se produisent au sein des connexions neuronales à la suite d’un stimulus ou d’une expérience. Lorsqu’une information est captée par nos sens, elle est encodée sous forme d’activation neuronale. Cette activation entraîne des changements structurels durables au niveau synaptique, créant ainsi une trace qui servira de base au rappel ultérieur de l’information (ndlr).
La gliose réactive est une réaction inflammatoire du tissu nerveux central, où les astrocytes et les microglies prolifèrent et migrent vers la zone lésée pour former une cicatrice gliale, isolant et protégeant les tissus endommagés, mais pouvant aussi entraîner des changements structurels et influencer la progression de maladies neurodégénératives (ndlr).
Liste des figures
 |
Figure 1 Schéma récapitulatif de différents mécanismes de régulation du sommeil par les astrocytes. Les astrocytes du noyau suprachiasmatique modulent des rythmes circadiens grâce à leur horloge moléculaire, via une boucle de rétroaction négative de transcription-traduction (TTFL). Au niveau cortical, ils peuvent également réguler différentiellement la transcription de gènes, modulant ainsi la couverture synaptique ainsi que la taille du réseau astrocytaire dépendante de l’expression de la connexine 30 (Cx30). Les variations d’expression d’aquaporine-4 (AQP4) permettent aussi une circulation du liquide céphalorachidien et un nettoyage du cerveau pendant le sommeil lent. Les variations de calcium intracellulaire des astrocytes du cortex sont moins prononcées pendant le sommeil, comparées à l’éveil, ainsi que les stocks de glycogène qui participeraient aussi à la régulation du sommeil. Les astrocytes participent aussi à la recapture et à la libération de neurotransmetteurs, ce qui régule le réseau neuronal voisin. Enfin, les astrocytes sont impliqués dans la régulation des poids synaptiques, en les diminuant au cours du sommeil lent. |
| Dans le texte | |
 |
Figure 2 Schéma illustrant les variations corticales de Ca2+ intracellulaire dans les astrocytes en fonction des niveaux de vigilance. Pendant l’éveil, les niveaux de Ca2+ sont plus élevés et synchronisés que pendant le sommeil lent au niveau cortical, surtout avant la transition vers le sommeil. Adapté de [28] avec BioRender. |
| Dans le texte | |
 |
Figure 3 Représentation schématique de l’origine et du mode d’action de l’adénosine dans le noyau préoptique ventrolatéral. Après une activation astrocytaire, l’élévation du Ca2+ intracellulaire entraîne la libération d’ATP par les hémicanaux ou les récepteurs P2X7 (purinergic receptor) (1). Cet ATP est ensuite hydrolysé en adénosine par la phosphatase alcaline non spécifique des tissus (TNAP) au niveau des interneurones (2). L’adénosine (3) agit alors sur les récepteurs A1R de ces interneurones, réduisant leur inhibition sur les neurones promoteurs de sommeil (4). Parallèlement, elle exerce un double effet sur ces neurones : elle induit une inhibition neuronale via l’activation des A1R et elle induit une activation des récepteurs A2AR, (5) dont l’effet dépolarisant l’emporte sur l’inhibition via l’activation des A1R. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




