| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 352 - 353 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026053 | |
| Published online | 24 April 2026 | |
Vers une production in vivo de cellules CAR-T
Une révolution annoncée ?
Towards in vivo production of CAR-T cells: an announced revolution?
Inserm UMR 1356, unité d’immuno-oncologie de nouvelle génération – cancers pédiatriques et de l’adulte, institut Gustave Roussy, faculté de médecine, université Paris-Saclay, Villejuif, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les thérapies fondées sur les lymphocytes T exprimant un récepteur antigénique chimérique (chimeric antigen receptor T lymphocytes [CAR-T]) ont transformé la prise en charge de certaines hémopathies lymphoïdes B [1]. Leur capacité à induire des rémissions complètes, parfois durables, constitue l’une des avancées majeures de l’immuno-oncologie moderne. Toutefois, leur diffusion reste limitée par un processus de fabrication complexe, long et coûteux, reposant sur la modification ex vivo de lymphocytes T autologues, une chimiothérapie préparatoire pour obtenir une lymphodéplétion, et des infrastructures hautement spécialisées. Ces contraintes freinent l’accès au traitement par lymphocytes CAR-T, et limitent son déploiement à grande échelle, notamment contre les tumeurs solides et les maladies auto-immunes [2].
Produire des lymphocytes CAR-T directement dans l’organisme
Hunter et al. décrivent une approche conceptuellement novatrice permettant de produire des lymphocytes CAR-T directement in vivo [3]. Ce travail est issu d’une collaboration entre la société américaine de biotechnologie Capstan Therapeutics et l’université de Pennsylvanie (États-Unis). Le principe repose sur l’utilisation de nanoparticules lipidiques ciblant spécifiquement les lymphocytes T et encapsulant un ARN messager (ARNm) codant un CAR dirigé contre CD19 ou CD20, deux molécules présentes à la surface des lymphocytes B normaux et tumoraux.
Les auteurs ont développé une formulation de nanoparticules lipidiques intégrant un lipide non ionisable (L829) et un anticorps de ciblage (anti-CD5 ou anti-CD8), permettant, après l’injection des nanoparticules par voie intraveineuse, une délivrance préférentielle de l’ARNm aux lymphocytes T. Chez la souris, cette stratégie induit une expression efficace mais transitoire du CAR par ces lymphocytes, associée à une élimination rapide des lymphocytes B tumoraux (Figure 1). L’optimisation des régions non traduites et des codons de l’ARNm améliore l’expression du CAR, la production de cytokines, et l’activité cytotoxique des lymphocytes T humains in vitro.
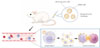 |
Figure 1 Principe de la production in vivo de lymphocytes CAR-T par injection de nanoparticules lipidiques. Après leur injection par voie intraveineuse, des nanoparticules lipidiques (lipid-based nanoparticle [LNP]) ciblant les lymphocytes T leur délivrent un ARN messager (ARNm) codant un récepteur antigénique chimérique (chimeric antigen receptor [CAR]). Les lymphocytes T internalisent les LNP, expriment transitoirement le CAR, et acquièrent une activité cytotoxique dirigée contre les cellules tumorales exprimant l’antigène cible. |
Validation préclinique et premiers succès dans un essai clinique
L’efficacité de cette approche a été confirmée dans des modèles murins humanisés, ainsi que sur des cellules mononucléées du sang provenant de personnes atteintes de maladies autoimmunes. Chez le macaque cynomolgus, deux à trois injections de ces nanoparticules contenant un ARNm codant un CAR dirigé contre CD20 entraînent une déplétion quasi complète des lymphocytes B circulant dans le sang ou présents dans les ganglions lymphatiques. Fait notable, les cellules B réémergentes présentent un phénotype « naïf »1, suggérant un possible « reset » immunologique.
La principale question reste toutefois celle de l’application à la médecine. Lors du congrès annuel de la Société américaine d’hématologie en décembre 2025 ont été présentés des résultats préliminaires d’un essai clinique utilisant une stratégie apparentée de production in vivo de lymphocytes CAR-T (KLN-1010, Kelonia Therapeutics) ciblant l’antigène de maturation des lymphocytes B (B-cell maturation antigen [BCMA]). Chez les quatre premiers patients traités, atteints de myélome multiple, une franche réduction de la masse tumorale a été constatée, sans recours à une chimiothérapie préalable de déplétion lymphocytaire, et avec un profil de tolérance du traitement jugé acceptable. Même s’il convient d’attendre la confirmation de cette efficacité sur un plus grand nombre de patients, ces premiers résultats témoignent de la faisabilité clinique de cette approche.
Enjeux industriels et perspectives thérapeutiques
Les lymphocytes CAR-T produits in vivo représentent aujourd’hui un champ en forte expansion, porté par de gros investissements industriels. Cette dynamique reflète le potentiel thérapeutique d’une telle approche, susceptible de lever plusieurs obstacles associés à la production ex vivo de ces cellules. Les bénéfices attendus incluent, outre la suppression des étapes de manipulation des cellules ex vivo, une simplification des modalités d’administration aux patients, potentiellement en ambulatoire, ainsi qu’une réduction des coûts et une meilleure accessibilité du traitement pour un plus grand nombre de patients. Si leur efficacité et leur sécurité sont confirmées, les lymphocytes CAR-T produits in vivo pourraient, à terme, remplacer certaines thérapies « classiques », en particulier dans des indications nécessitant des traitements rapides ou répétés.
Questions ouvertes et conclusion
Malgré ces avancées prometteuses, plusieurs questions demeurent. Elles concernent notamment la durée d’expression du CAR par les lymphocytes T modifiés, le contrôle fin de l’activation immunitaire, l’immunogénicité des nanoparticules lipidiques, et le risque d’effets « hors-cible ». La maîtrise spatiale et temporelle de l’expression du CAR par les lymphocytes constituera un enjeu central pour garantir la sécurité de cette thérapie.
En conclusion, la production in vivo de lymphocytes CAR-T représente un tournant majeur en immunothérapie cellulaire. Soutenue par des résultats précliniques solides, des premiers résultats cliniques encourageants, et un fort engagement industriel, cette stratégie pourrait modifier considérablement le paysage thérapeutique. Seules des études cliniques à plus grande échelle permettront toutefois de déterminer si cette révolution annoncée deviendra la nouvelle norme.
En France, le réseau UNITC – Consortium national de recherche sur les thérapies cellulaires et géniques, labellisé par l’Institut national du cancer (INCa) – a lancé un programme spécifique dédié aux lymphocytes CAR-T produits in vivo. Cette « force opérationnelle » vise à renforcer l’attractivité du territoire français pour les essais cliniques et à fédérer les acteurs académiques autour du développement de cette nouvelle génération de lymphocytes CAR-T.
Conflits d’intérêt
L’auteur déclare qu’il n’a aucun conflit d’intérêt.
Références
- June CH, Sadelain M. Chimeric antigen receptor therapy. N Engl J Med 2018 ; 379 : 64-73. [CrossRef] [PubMed] [Google Scholar]
- Posey AD, Young RM, June CH. Future perspectives on engineered T cells for cancer. Trends Cancer 2024 ; 10 : 687-95. [Google Scholar]
- Hunter TL, Bao Y, Zhang Y, et al. In vivo CAR T cell generation to treat cancer and autoimmune disease. Science 2025 ; 388 : 1311-17. [Google Scholar]
Phénotype caractéristique des lymphocytes B nouvellement produits, n’ayant pas encore rencontré d’antigène et dépourvus de marqueurs de mémoire immunitaire.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Principe de la production in vivo de lymphocytes CAR-T par injection de nanoparticules lipidiques. Après leur injection par voie intraveineuse, des nanoparticules lipidiques (lipid-based nanoparticle [LNP]) ciblant les lymphocytes T leur délivrent un ARN messager (ARNm) codant un récepteur antigénique chimérique (chimeric antigen receptor [CAR]). Les lymphocytes T internalisent les LNP, expriment transitoirement le CAR, et acquièrent une activité cytotoxique dirigée contre les cellules tumorales exprimant l’antigène cible. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




