| Issue |
Med Sci (Paris)
Volume 42, Number 2, Février 2026
|
|
|---|---|---|
| Page(s) | 146 - 149 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026012 | |
| Published online | 24 February 2026 | |
Mélanome et œstrogènes
Une révolution dans la compréhension des mécanismes métastatiques
Melanoma and estrogens: A revolution in understanding metastatic mechanisms
1
Institut Curie, Université Paris Sciences et Lettres, Inserm U1021, Développement normal et pathologique des mélanocytes, Orsay, France
2
Université Paris-Saclay, CNRS UMR 3347, Orsay, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les résultats d’une étude publiée récemment dévoilent un mécanisme métastatique inédit dans le mélanome malin, en lien étroit avec les hormones sexuelles féminines [1]. Cette découverte met en lumière une cascade moléculaire centrée autour de la perte de la E-cadhérine, de l’activation de la β-caténine, de l’induction du récepteur des œstrogènes ERα, et de la surexpression du récepteur du peptide libérant la gastrine. Une boucle qui favorise, plus particulièrement chez les femmes, la dissémination du mélanome cutané vers les poumons.
Le sexe, une variable majeure trop longtemps négligée dans les études scientifiques et cliniques
Alors que le cancer demeure l’une des principales causes de mortalité dans le monde [2], les avancées de la recherche biomédicale ont longtemps été limitées par une sous-représentation marquée des males dans les modèles animaux expérimentaux et des femmes dans les études cliniques. Jusqu’aux années 1990, les essais cliniques incluaient majoritairement des sujets de sexe masculin, ce qui a introduit un biais dans l’interprétation des résultats concernant de nombreuses maladies, y compris les cancers. Cette exclusion n’était pas motivée par une volonté discriminatoire manifeste, mais résultait plutôt d’un ensemble de facteurs : préoccupations éthiques liées à la grossesse, contraintes logistiques, simplification méthodologique, et ancrage dans une vision androcentrique de la médecine. Il en a néanmoins résulté une méconnaissance des réponses thérapeutiques spécifiques des femmes, exposant ces dernières à des effets indésirables potentiels ou à une efficacité moindre des thérapies. Depuis les années 1990, une prise de conscience a conduit à des réformes visant à rendre la recherche biomédicale plus inclusive, en intégrant davantage les spécificités physiologiques liées au sexe.
Aujourd’hui, on sait que le sexe influence non seulement l’incidence et la progression de plusieurs types de cancers, mais également la réponse aux thérapies, même pour les cancers situés en dehors des organes reproducteurs [3–6].
Une analyse globale de l’incidence du cancer, stratifiée par sexe et par tranche d’âge, a révélé une tendance marquante : treize types de cancers, notamment le mélanome ainsi que les cancers de la thyroïde et de l’estomac, sont plus fréquents chez les femmes que chez les hommes, entre la puberté et la ménopause [1]. Un faisceau croissant d’arguments épidémiologiques indique notamment que l’incidence du mélanome cutané, un cancer à fort potentiel métastatique, est plus grande chez les femmes jeunes que chez les hommes du même âge, dans une période caractérisée, pour les femmes, par une intense production d’œstrogènes (Figure 1).
 |
Figure 1. Le risque de mélanome malin diffère selon le sexe. A. Estimation du nombre de nouveaux cas de mélanome cutané en 2020 dans la population mondiale chez les femmes et chez les hommes selon l’âge, d’après les données de GLOBOCAN [2]. B. Rapport femmes/hommes du nombre de cas de mélanome pour chaque tranche d’âge. Les points sont colorés selon la valeur de cette proportion : en rouge lorsque le rapport est supérieur à 1 (incidence plus élevée chez les femmes), en bleu lorsqu’il est inférieur à 1 (incidence plus élevée chez les hommes), et en noir lorsqu’il est proche de 1 (incidence comparable entre les sexes). |
Cette corrélation suggère l’implication, méconnue jusqu’alors, des hormones sexuelles féminines dans des cancers « non hormonodépendants ».
Contrairement à l’idée reçue selon laquelle les œstrogènes n’auraient d’effet que sur les tissus du système reproducteur, ces recherches montrent qu’ils peuvent également influer sur la plasticité, la migration et l’invasion cellulaires, des éléments clés dans le processus de métastase.
CDH1 : un gène impliqué dans l’adhérence intercellulaire, aux multiples rôles
Au cœur du mécanisme découvert se trouve la E-cadhérine, une molécule d’adhérence entre cellules codée par le gène CDH1. Classiquement considérée comme un « gardien » de l’architecture des épithéliums, sa perte est un évènement primordial dans la transition épithélio-mésenchymateuse, un processus par lequel les cellules cancéreuses acquièrent une capacité migratoire, condition nécessaire à la formation des métastases [7, 8]. Or, l’expression de CDH1 est réduite chez les jeunes femmes atteintes de mélanome, un phénomène corrélé à une surexpression du gène ESR1 codant le récepteur des œstrogènes ERα, et à l’induction d’une voie de signalisation pro-métastatique impliquant le récepteur du peptide libérant la gastrine (gastrin-releasing peptide receptor, GRPR) et le régulateur transcriptionnel YAP1 (Yes-associated protein 1). Cette voie de signalisation sous régulation hormonale n’avait pas encore été identifiée. L’analyse des données épidémiologiques, des profils d’expression génique et des gènes associés (gènes cibles et régulateurs) à ERa a permis d’identifier CDH1 comme un gène dont ERa réduit l’expression. Toutefois, c’est grâce à des modèles animaux génétiquement modifiés que le rôle de ce gène a pu être précisé. Dans un modèle murin de mélanome produisant une forme mutée de la protéine NRAS (NRASGln61Lys) dans les mélanocytes, les femelles dépourvues spécifiquement de la E-cadhérine dans ces cellules (grâce au système Cre-LoxP, Tyr::Cre/° ; Cdh1flox/flox) présentent une augmentation marquée des métastases pulmonaires par rapport aux mâles porteurs de la même mutation ou aux souris (mâles et femelles) exprimant la E-cadhérine. Il convient d’ajouter que l’initiation des mélanomes, correspondant à la prévalence et au temps de latence, est identique quel que soit le sexe ou le statut génétique de Cdh1, ce qui permet de conclure que l’absence de la E-cad-hérine dans les mélanocytes n’est pas impliquée dans l’initiation tumorale, mais qu’elle est fortement impliquée dans la progression tumorale chez les souris femelles.
GRPR, un nouveau protagoniste de la métastase
Une autre découverte majeure de l’étude réside dans l’identification du récepteur GRPR comme un acteur clé de la formation des métastases du mélanome chez les femmes. Ce récepteur, appartenant à la famille des récepteurs couplés aux protéines G, est surexprimé par les cellules tumorales de souris femelles dépourvues de E-cadhérine, tandis qu’il reste peu ou pas exprimé chez les mâles ou chez les femelles dont les cellules tumorales expriment cette molécule d’adhérence. Les analyses transcriptomiques (RNA-seq) et épigénétiques (ChIP-seq) ont révélé une activation spécifique du promoteur de GRPR dans les mélanomes féminins n’exprimant pas la E-cadhérine. Il convient d’ajouter que GRP, ligand du récepteur GRPR, est particulièrement abondant dans le poumon, site privilégié des métastases du mélanome. L’expression de GRPR est corrélée avec une survie tumorale plus faible chez les femmes atteintes de mélanome, soulignant sa valeur pronostique.
Une boucle de régulation ECAD-ESR1-GRPR–YAP1 au cœur du mécanisme
L’équipe a également mis en évidence l’activation de YAP1, un coactivateur transcriptionnel impliqué dans la régulation de CDH1 et connu pour son rôle clé dans la signalisation mécanosensible et oncogénique [9]. L’activation de la voie de signalisation impliquant GRPR déclenche une cascade moléculaire GRPR–YAP1–E-cadhérine–ERa, qui favorise la plasticité cellulaire, la résistance à l’anoïkis1 et l’invasion tumorale, des effets amplifiés par la présence d’œstrogènes [1] (Figure 2).
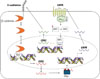 |
Figure 2. Les œstrogènes peuvent activer un mécanisme favorisant la progression métastatique des mélanomes. Dans des conditions physiopathologiques, la perte d’expression de la E-cadhérine entraîne l’activation de la signalisation impliquant la β-caténine, qui induit à son tour la transcription de ESR1 (codant le récepteur des œstrogènes ERα). En présence d’œstrogènes, ce récepteur nucléaire active la transcription de GRPR (codant le récepteur du peptide libérant la gastrine), stimulant ainsi la signalisation pro-métastatique YAP1. Cette voie de signalisation est renforcée par l’action répressive de YAP1 et de ses cofacteurs TEAD (transcriptional enhancer activator domain-containing) sur l’expression de CDH1 (codant la E-cadhérine). Ainsi, une boucle de régulation auto-renforcée s’installe sous contrôle hormonal. Dans des conditions physiologiques, cette boucle peut être directement activée par l’action de l’œstradiol (E2) lié à son récepteur ERα. TCF : T-cell factor/lymphoid enhancer factor. |
Dans les modèles de souris femelles invalidées pour le gène Cdh1, YAP1 apparaît fortement activée dans les cellules de mélanome métastatique, contrairement aux cellules de mélanome métastatique de souris mâles invalidées pour Cdh1 ou de souris, mâles ou femelles, de génotype « sauvage ». L’inhibition de ERβ ou de GRPR entraîne une réduction marquée du potentiel métastatique, confirmant le rôle de ces protéines dans la dissémination des cellules tumorales. Plus généralement, le dysfonctionnement de cette boucle de régulation lorsque ses acteurs principaux présentent des mutations ou des altérations d’expression joue un rôle pathogénique important dans le processus métastatique.
Vers une nouvelle médecine oncologique « sexospécifique »
Ces résultats bouleversent la compréhension du rôle des œstrogènes dans le cancer. Loin de n’être que des stimulateurs de croissance, ils apparaissent ici comme des modulateurs de la plasticité cellulaire et du comportement métastatique des cellules tumorales, ce qui appelle une révision des approches thérapeutiques actuelles.
L’inhibition ciblée de GRPR, ainsi que de la voie de signalisation impliquant également ERα et YAP1, constitue une stratégie thérapeutique prometteuse pour les femmes jeunes atteintes de mélanome métastatique. Des antagonistes de GRPR existent, et ont déjà été évalués dans d’autres contextes pathologiques, notamment pour le traitement du cancer du sein ou de la prostate [10]. Toutefois, l’utilisation thérapeutique de ces molécules présente encore des limitations, tant en termes d’efficacité que de spécificité, et peut avoir des effets indésirables. Le développement de nouveaux antagonistes, plus sélectifs, mieux tolérés et adaptés à une utilisation médicale, apparaît donc nécessaire. Leur repositionnement dans une approche sexospécifique pourrait ouvrir la voie à des traitements personnalisés, mieux ciblés et potentiellement plus efficaces.
Une perspective nouvelle sur les cancers « non hormonodépendants »
Les résultats de cette étude remettent donc en question la distinction traditionnelle entre cancers « hormonodépendants » et « non hormonodépendants », puisqu’ils montrent que les œstrogènes peuvent exercer un effet marqué sur un cancer affectant des tissus n’appartenant pas au système reproducteur, en interagissant avec un réseau moléculaire complexe impliquant la E-cadhérine, GRPR et YAP1.
La mise en lumière d’une vulnérabilité spécifique du sexe féminin dans la progression du mélanome constitue une forte incitation à intégrer systématiquement le sexe comme variable biologique dans la recherche, la conception et les essais cliniques de traitements anticancéreux.
Et maintenant ?
Sans remettre en cause les approches actuelles telles que l’immunothérapie ou les thérapies ciblées, de nouvelles perspectives s’ouvrent désormais en oncologie pour : 1) identifier des biomarqueurs spécifiques au sexe dans les cancers métastatiques ; 2) développer des traitements ciblant GRPR, en synergie avec ERα et YAP1, spécifiquement chez les femmes pour lesquelles la biopsie du mélanome primaire a révélé l'existence de mutations ou la répression de l'expression de CDH1, ou d’une grande quantité d’ARN messagers codant ESR1 ou GRPR (ou de ces protéines ellesmêmes) ; 3) construire une médecine personnalisée intégrant pleinement les spécificités biologiques liées au sexe. Les progrès dans la compréhension des différences biologiques entre les sexes devraient permettre d’améliorer la précision des diagnostics oncologiques, d’ajuster plus finement les traitements anti-cancéreux, et, à terme, d’augmenter les chances de survie des personnes atteintes d’un cancer.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Raymond JH, Aktary Z, Pouteaux M, et al. Targeting GRPR for sex hormone-dependent cancer after loss of E-cadherin. Nature 2025 ; 643 : 801–9. [Google Scholar]
- Sung H, Ferlay J, Siegel RL, et al. Global cancer statistics 2020: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin 2021 ; 71 : 209–49. [CrossRef] [PubMed] [Google Scholar]
- Dong M, Cioffi G, Wang J, et al. Sex differences in cancer incidence and survival: A pan-cancer analysis. Cancer Epidemiol Biomarkers Prev 2020 ; 29 : 1389–97. [Google Scholar]
- Cook MB, Dawsey SM, Freedman ND, et al. Sex disparities in cancer incidence by period and age. Cancer Epidemiol Biomarkers Prev 2009 ; 18 : 1174–82. [Google Scholar]
- Ye Y, Jing Y, Li L, et al. Sex-associated molecular differences for cancer immunotherapy. Nat Commun 2020 ; 11 : 1779. [Google Scholar]
- Vellano CP, White MG, Andrews MC, et al. Androgen receptor blockade promotes response to BRAF/MEK-targeted therapy. Nature 2022 ; 606 : 797. [Google Scholar]
- Larue L, Bellacosa A. Epithelial-mesenchymal transition in development and cancer: role of phosphatidylinositol 3’ kinase/AKT pathways. Oncogene 2005 ; 24 : 7443–54. [Google Scholar]
- Berx G, Van Roy F. The E-cadherin/catenin complex: an important gatekeeper in breast cancer tumorigenesis and malignant progression. Breast Cancer Res 2001 ; 3 : 289–93. [Google Scholar]
- Pobbati AV, Hong W. A combat with the YAP/TAZ-TEAD oncoproteins for cancer therapy. Theranostics 2020 ; 10 : 3622–35. [Google Scholar]
- Meierjohann S. Sex differences in skin-cancer risk are linked to oestrogen levels. Nature 2025 ; 643 : 643–4. [Google Scholar]
Mode d’élimination physiologique des cellules par apoptose consécutive à une rupture des communications entre une cellule et son environnement.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Le risque de mélanome malin diffère selon le sexe. A. Estimation du nombre de nouveaux cas de mélanome cutané en 2020 dans la population mondiale chez les femmes et chez les hommes selon l’âge, d’après les données de GLOBOCAN [2]. B. Rapport femmes/hommes du nombre de cas de mélanome pour chaque tranche d’âge. Les points sont colorés selon la valeur de cette proportion : en rouge lorsque le rapport est supérieur à 1 (incidence plus élevée chez les femmes), en bleu lorsqu’il est inférieur à 1 (incidence plus élevée chez les hommes), et en noir lorsqu’il est proche de 1 (incidence comparable entre les sexes). |
| Dans le texte | |
 |
Figure 2. Les œstrogènes peuvent activer un mécanisme favorisant la progression métastatique des mélanomes. Dans des conditions physiopathologiques, la perte d’expression de la E-cadhérine entraîne l’activation de la signalisation impliquant la β-caténine, qui induit à son tour la transcription de ESR1 (codant le récepteur des œstrogènes ERα). En présence d’œstrogènes, ce récepteur nucléaire active la transcription de GRPR (codant le récepteur du peptide libérant la gastrine), stimulant ainsi la signalisation pro-métastatique YAP1. Cette voie de signalisation est renforcée par l’action répressive de YAP1 et de ses cofacteurs TEAD (transcriptional enhancer activator domain-containing) sur l’expression de CDH1 (codant la E-cadhérine). Ainsi, une boucle de régulation auto-renforcée s’installe sous contrôle hormonal. Dans des conditions physiologiques, cette boucle peut être directement activée par l’action de l’œstradiol (E2) lié à son récepteur ERα. TCF : T-cell factor/lymphoid enhancer factor. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




