| Issue |
Med Sci (Paris)
Volume 42, Number 2, Février 2026
|
|
|---|---|---|
| Page(s) | 143 - 145 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026011 | |
| Published online | 24 February 2026 | |
Les macrophages recyclent les bactéries pour alimenter leurs défenses antimicrobiennes
Macrophages use bacteria as a source of nutrients
Univ. Bordeaux, CNRS, Inserm, Immuno ConcEpT, UMR 5164, ERL 1303, Bordeaux, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Contributions égales.
Les macrophages sont des cellules spécialisées du système immunitaire qui remplissent un ensemble de fonctions contribuant à l’intégrité et à l’homéostasie des organes [1]. Ils possèdent notamment la capacité de détecter les microorganismes potentiellement dangereux grâce à une panoplie de récepteurs leur permettant d’ajuster leur réponse en fonction de la nature des microbes rencontrés [2]. Une fois les microorganismes identifiés, les macrophages les éliminent par phagocytose, un mécanisme par lequel les cellules internalisent et détruisent des microorganismes, des particules nocives, ou des cellules en fin de vie. Les objets phagocytés sont d’abord séquestrés dans des phagosomes, des vésicules hermétiques issues de l’invagination de la membrane cellulaire. Celles-ci forment alors des phagolysosomes en fusionnant avec d’autres vésicules, les lysosomes, qui contiennent un arsenal d’enzymes spécialisées permettant la dégradation des objets phagocytés. Le rôle essentiel des macrophages dans l’élimination des bactéries lors d’une infection est connu [3], mais le devenir des métabolites résultant de la dégradation des bactéries phagocytées ainsi que leur implication dans le fonctionnement des macrophages sont encore mal compris. Notre équipe de recherche a mis en évidence un aspect inédit du fonctionnement des macrophages : leur capacité à recycler les nutriments issus des bactéries ingérées pour soutenir leur activité métabolique et immunitaire [4].
Les bactéries constituent une source alternative de nutriments pour les macrophages
Afin d’élucider le devenir métabolique des bactéries une fois « digérées » par les phagolysosomes des macrophages, il fallait pouvoir tracer les produits de dégradation au sein de la cellule. Nous avons donc développé une approche permettant de marquer des bactéries Escherichia coli au carbone 13 (13C) afin de pouvoir suivre le devenir des molécules bactériennes après l’ingestion de ces microorganismes par des macrophages, in vitro et in vivo, par spectrométrie de masse. Nous avons ainsi montré que les bactéries mortes, une fois dégradées dans les phagolysosomes, fournissent des intermédiaires métaboliques utilisés par les macrophages pour leur propre métabolisme. Ces intermédiaires sont notamment utilisés pour produire de l’énergie dans les mitochondries, constituent une source d’acides aminés pour la synthèse de protéines, ou contribuent à d’autres voies métaboliques majeures des macrophages, telles que la biosynthèse du glutathion, une molécule au fort potentiel antioxydant. Ainsi, les macrophages ont la capacité d’incorporer des éléments essentiels à leur métabolisme par l’ingestion d’une grande variété de bactéries : des bactéries à Gram positif, telles que Staphylococcus aureus ou Listeria innocua, et des bactéries à Gram négatif, comme Citrobacter rodentium ou Pseudomonas aeruginosa.
Les cellules sont pourvues de différents mécanismes leur permettant d’évaluer la présence de nutriments dans leur environnement et d’ajuster leur métabolisme en fonction de l’abondance et de la composition des nutriments à leur disposition [5]. En présence de nutriments, le complexe protéique mTORC1 (mammalian target of rapamicyn complex 1) est assemblé à la surface des lysosomes pour moduler les flux métaboliques intracellulaires [6]. En utilisant des modèles de souris transgéniques dont la voie de signalisation impliquant mTORC1 est constitutivement activée, nous avons pu mettre en évidence la capacité de cette voie à inhiber le recyclage des bactéries mortes par les macrophages. Inversement, l’abolition de la voie mTORC1 promeut l’assimilation de métabolites bactériens par les macrophages.
Le recyclage métabolique des bactéries phagocytées par les macrophages dépend de la viabilité microbienne
Les macrophages ont la capacité d’ajuster leur réponse immunitaire en fonction des récepteurs de l’immunité innée engagés lors de leur rencontre avec un microorganisme pathogène [2]. Ceuxci diffèrent notamment selon la viabilité des bactéries phagocytées [7]. Dans le cas de bactéries vivantes, la réponse des macrophages nécessite une reprogrammation de leur métabolisme bioénergétique, donc du fonctionnement de leurs mitochondries, qui est provoquée par une production accrue d’espèces réactives de l’oxygène (reactive oxygen species, ROS) [8]. Après avoir montré que la dégradation phagolysosomique de bactéries mortes par les macrophages alimente en particulier la voie de biosynthèse du glutathion, un puissant antioxydant endogène, nous avons exploré la possibilité que le recyclage métabolique des bactéries dépende également de leur viabilité. Une analyse comparative, par spectrométrie de masse, des macrophages ayant phagocyté des bactéries vivantes ou mortes et marquées au 13C nous a permis de constater qu’ils assimilent beaucoup mieux les métabolites provenant de bactéries mortes, bien qu’ils phagocytent de manière similaire les bactéries mortes et vivantes. De plus, l’activation expérimentale de la voie de signalisation impliquant mTORC1 permet de diminuer le recyclage métabolique des bactéries mortes pour atteindre un niveau comparable à ceux mesurés pour des bactéries vivantes, ce qui confirme la position clé de mTORC1 dans le contrôle de ce processus.
Nous avons alors entrepris d’identifier les signaux trahissant la viabilité des bactéries et pouvant moduler la reprogrammation métabolique des macrophages. Étonnamment, la comparaison entre les métabolomes de bactéries E. coli vivantes ou mortes a révélé qu’un petit métabolite, l’adénosine monophosphate cyclique (AMPc), est particulièrement abondant dans les bactéries mortes. Nous avons ensuite montré que lors de la phagocytose de bactéries mortes par les macrophages, l’AMPc microbien est métabolisé pour contribuer à la réserve intracellulaire d’AMP, ce qui active l’AMP kinase, une protéine inhibitrice de la voie mTORC1, et stimule ainsi le recyclage de ces bactéries par les macrophages (Figure 1). Ce mécanisme permettant un degré de recyclage des bactéries différent selon leur viabilité pourrait être une manière pour les macrophages de se protéger contre des molécules bactériennes potentiellement dangereuses provenant de bactéries vivantes, tout en utilisant les bactéries mortes, moins dangereuses, comme source de nutriments.
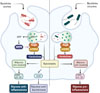 |
Figure 1. Schéma du mécanisme de détection de la viabilité bactérienne contrôlant le recyclage métabolique des bactéries phagocytées par les macrophages et son impact pour les réponses antimicrobiennes. AMP : adénosine monophosphate ; AMPc : AMP cyclique ; AMPK : AMP-activated protein kinase ; RagA : Ras-related GTP-binding protein A (recrute mTORC1 à la surface des lysosomes) ; mTORC1 : mammalian target of rapamycin complex 1 ; ROS : reactive oxygen species ; IL-1β : interleukine 1β (cytokine pro-inflammatoire) ; GSH : glutathion-SH (forme réduite du glutathion). Figure réalisée avec Biorender. |
Le recyclage métabolique des bactéries ingérées permet d’ajuster la réponse immunitaire
Lors d’une infection par des bactéries pathogènes, celles-ci se multiplient le plus souvent beaucoup plus vite que les cellules de l’hôte. Les bactéries, qui s’alimentent également avec les nutriments présents dans le milieu environnant, consomment vraisemblablement une grande proportion des nutriments nécessaires au fonctionnement des cellules de l’hôte, ce qui crée probablement une situation de carence nutritionnelle pour les cellules immunitaires, bien qu’il soit difficile d’en estimer le degré [9]. Les macrophages cultivés dans un milieu pauvre en nutriments meurent rapidement. Or, contrairement à l’ajout de bactéries vivantes, l’ajout de bactéries mortes permet la survie des macrophages dans ce milieu de culture, ce qui témoigne de la capacité des macrophages à puiser les nutriments essentiels à leur survie dans la dégradation de bactéries mortes. Il reste à savoir si cela leur procure un avantage dans la lutte contre les infections microbiennes.
La phagocytose de bactéries mortes ne favorise pas seulement la survie des macrophages, elle permet également d’ajuster la réponse immunitaire. En effet, nous avons montré que la capacité des macrophages à produire différentes molécules, notamment des cytokines ou des espèces réactives de l’oxygène, selon la viabilité des microorganismes rencontrés dépend de leur aptitude à intégrer certains précurseurs métaboliques bactériens nécessaires à la biosynthèse de métabolites capables de moduler la production de ces cytokines [8]. Parmi ces métabolites, le glutathion et l’itaconate empêchent la formation d’espèces réactives de l’oxygène, et diminuent ainsi la production de cytokines pro-inflammatoires, qui sont caractéristiques de la réponse des macrophages aux bactéries vivantes (Figure 1).
Cette remarquable propriété des macrophages, capables de moduler leur métabolisme et d’extraire différents métabolites des phagolysosomes en fonction de la nature des éléments phagocytés, concerne également l’ingestion de cellules apoptotiques [10]. Une telle plasticité pourrait favoriser la survie des macrophages dans des environnements appauvris en nutriments, tels que les foyers infectieux, les tissus hypoxiques, ou les niches tumorales. Un « conditionnement » des macrophages dans de tels environnements pourrait d’ailleurs être mis à profit dans des stratégies thérapeutiques innovantes contre certaines maladies inflammatoires chroniques ou contre des infections bactériennes, ou encore pour la composition de nouveaux vaccins. En effet, les vaccins fondés sur l’utilisation de bactéries vivantes assurent une meilleure réponse vaccinale comparés à ceux composés de simples extraits bactériens, mais présentent certains inconvénients liés à la viabilité des microorganismes. L’utilisation d’adjuvants métaboliques en combinaison avec des bactéries mortes permettrait d’optimiser certaines compositions vaccinales en reproduisant les effets vaccinaux des bactéries vivantes.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Les travaux du laboratoire Biologie mitochondriale et immunité innée ont bénéficié du soutien du CNRS, de l’Inserm, de l’agence nationale de la recherche (ANR-19-CE15-0018, ANR-23-CE14-0044, and ANR-23-CE17-0063-01, ANR-10-IDEX-03-02). Nous remercions nos partenaires étrangers : les laboratoires dirigés par Leif E. Sander (Charité, Berlin, Allemagne), Alejo Efeyan (Centro nacional de investigaciones oncologicas, Madrid, Espagne), et Angelo d’Alessandro (University of Colorado, Denver, États-Unis). Nous remercions également l’ensemble de l’unité ImmunoConcEpT, ainsi que les plateformes d’imagerie (centre d’imagerie de Bordeaux), de cytométrie (FACScility, TBMCore), de métabolomique (SAM, TBMCore) et le personnel de l’animalerie de l’université de Bordeaux.
Références
- Park MD, Silvin A, Ginhoux F, et al. Macrophages in health and disease. Cell 2022 ; 185 : 4259–79. [Google Scholar]
- Underhill DM, Goodridge HS. Information processing during phagocytosis. Nat Rev Immunol 2012 ; 12 : 492–502. [Google Scholar]
- Flannagan RS, Jaumouillé V, Grinstein S. The cell biology of phagocytosis. Annu Rev Pathol 2012 ; 7 : 61–98. [Google Scholar]
- Lesbats J, Brillac A, Reisz JA, et al. Macrophages recycle phagocytosed bacteria to fuel immunometabolic responses. Nature 2025 ; 640 : 524–33. [Google Scholar]
- Palm W, Thompson CB. Nutrient acquisition strategies of mammalian cells. Nature 2017 ; 546 : 234–42. [Google Scholar]
- Zoncu R, Bar-Peled L, Efeyan A, et al. mTORC1 senses lysosomal amino acids through an inside-out mechanism that requires the vacuolar H+-ATPase. Science 2011 ; 334 : 678–83. [Google Scholar]
- Ugolini M, Sander LE. Dead or alive: how the immune system detects microbial viability. Curr Opin Immunol 2019 ; 56 : 60–6. [Google Scholar]
- Garaude J, Acín-Pérez R, Martínez-Cano S, et al. Mitochondrial respiratory-chain adaptations in macrophages contribute to antibacterial host defense. Nat Immunol 2016 ; 17 : 1037–45. [Google Scholar]
- Kedia-Mehta N, Finlay DK. Competition for nutrients and its role in controlling immune responses. Nat Commun 2019 ; 10 : 2123. [Google Scholar]
- Ampomah PB, Cai B, Sukka SR, et al. Macrophages use apoptotic cell-derived methionine and DNMT3A during efferocytosis to promote tissue resolution. Nat Metab 2022 ; 4 : 444–57. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Schéma du mécanisme de détection de la viabilité bactérienne contrôlant le recyclage métabolique des bactéries phagocytées par les macrophages et son impact pour les réponses antimicrobiennes. AMP : adénosine monophosphate ; AMPc : AMP cyclique ; AMPK : AMP-activated protein kinase ; RagA : Ras-related GTP-binding protein A (recrute mTORC1 à la surface des lysosomes) ; mTORC1 : mammalian target of rapamycin complex 1 ; ROS : reactive oxygen species ; IL-1β : interleukine 1β (cytokine pro-inflammatoire) ; GSH : glutathion-SH (forme réduite du glutathion). Figure réalisée avec Biorender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




