| Issue |
Med Sci (Paris)
Volume 42, Number 2, Février 2026
|
|
|---|---|---|
| Page(s) | 131 - 134 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026007 | |
| Published online | 24 February 2026 | |
La lipolyse du tissu adipeux brun est nécessaire à son activité thermogénique
Brown adipose tissue lipolysis, a metabolic pathway crucial for cold-induced thermogenesis
Institut des maladies métaboliques et cardiovasculaires (I2MC) Université de Toulouse, Inserm U1297, Toulouse, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Le tissu adipeux brun est un tissu spécialisé dans la production de chaleur (thermogenèse), caractéristique des mammifères placentaires. Il persiste, en abondance, tout au long de la vie chez les animaux hibernants et chez les rongeurs. Dans l’espèce humaine, il est présent dans la région supraclaviculaire et la partie supérieure de la colonne vertébrale, où son activation dans la période post-natale permet de préserver la température corporelle du nouveau-né. Les dépôts adipeux bruns vont ensuite involuer, du fait d’une meilleure isolation thermique du corps par les vêtements, et de l’apparition d’autres mécanismes de thermorégulation, notamment grâce au développement de la masse musculaire qui permet le frisson. Cependant, à l’âge adulte, ces dépôts adipeux bruns restent activables [1], et leur activité est fortement associée à une meilleure santé cardio-métabolique [2]. Cela explique l’intérêt actuel de la communauté scientifique pour le fonctionnement de ce tissu adipeux particulier chez l’Homme, ainsi que pour l’implication de ses dysfonctionnements dans le développement des maladies métaboliques et cardiovasculaires [3].
Le tissu adipeux brun est très minoritaire en comparaison du tissu adipeux blanc. Ces deux tissus sont constitués majoritairement d’adipocytes. Les adipocytes blancs constituent notre principal réservoir énergétique en stockant les acides gras sous forme de triglycéridesau sein d’une gouttelette lipidique unique et volumineuse [4]. L’adipocyte brun possède le même système enzymatique de stockage des acides gras (par estérification avec le glycérol) et de mobilisation de ces acides gras (par hydrolyse des triglycérides, i.e. lipolyse1) que l’adipocyte blanc. Les étapes limitantes de la lipolyse sont catalysées par les lipases ATGL (adipose triglyceride lipase) et HSL (hormone-sensitive lipase), dont l’activité est contrôlée par le système nerveux sympathique [5]. Malgré ces similitudes, l’adipocyte brun se distingue de l’adipocyte blanc par la présence de multiples petites gouttelettes lipidiques et d’une forte densité de mitochondries à l’origine de la teinte brune caractéristique du tissu. Ces mitochondries possèdent un équipement moléculaire unique : la protéine découplante UCP1 (uncoupling protein 1). Sous l’effet de stimulus environnementaux tels qu’une exposition aigüe au froid, l’activation du système nerveux sympathique induit rapidement l’oxydation mitochondriale de substrats métaboliques, une source énergétique dissipée par UCP1 sous forme de chaleur [6]. La présence de UCP1 confère ainsi au tissu adipeux brun une capacité thermogénique (sans frisson) essentielle au maintien de la température corporelle des nouveaux-nés humains, des animaux hibernants et des rongeurs.
La forte activité métabolique de l’adipocyte brun relative au découplage énergétique mitochondrial incite à rechercher quel(s) substrat(s) alimente(nt) son activité thermogénique [7]. Les acides gras occupent une place essentielle : ils sont à la fois la source énergétique majeure du métabolisme oxydant, et des activateurs directs de la protéine UCP1 [8]. Leur provenance pour soutenir l’activité métabolique de l’adipocyte brun reste cependant débattue : proviennent-ils des stocks intracellulaires de triglycérides, ou sont-ils captés par le tissu adipeux brun dans le sang circulant ?
Des données in vitro [9] et in vivo chez l’homme [10] semblaient indiquer un rôle essentiel de la lipolyse intracellulaire des triglycérides de l’adipocyte brun dans l’induction de la thermogenèse du tissu adipeux brun. Cependant, ce rôle de la lipolyse intracellulaire a été remis en question dans deux articles parus en 2017, au profit de celui d’un flux exclusif d’acides gras provenant de la lipolyse dans le tissu adipeux blanc [11, 12]. Les auteurs de ces articles ont étayé leur hypothèse en bloquant, spécifiquement dans tous les adipocytes ou uniquement dans les adipocytes bruns, la première étape de la lipolyse effectuée par la lipase ATGL. Cependant, la lipolyse est un processus séquentiel qui implique également la lipase HSL. Or, ces deux lipases possèdent chacune la capacité de compenser partiellement la perte d’activité de l’autre [13, 14]. Par ailleurs, le profil fonctionnel de HSL, dont l’activité est à la fois plus restreinte à l’adipocyte et plus pléiotrope (activités hydrolytiques multiples et activité non enzymatique) que celle de ATGL [15, 16] (voir l'article par J. Dufau et D. Langin dans ce numéro), pourrait avoir également entraîné des mécanismes compensatoires quant à la mobilisation des acides gras induite par le froid. L’affirmation selon laquelle la lipolyse intracellulaire du tissu adipeux brun n’était pas impliquée dans la thermogenèse avait ainsi surpris la communauté scientifique, d’autant que les mécanismes compensatoires précités n’avaient pas été pris en compte dans l’interprétation des résultats expérimentaux et qu’aucune mesure directe de l’activité métabolique thermogénique de ce tissu n’avait été effectuée. De plus, depuis 2017, ces résultats expérimentaux n’ont pas été reproduits par d’autres équipes de recherche.
Afin de clarifier cette controverse, notre laboratoire a produit (en utilisant le système Cre-Lox) un nouveau modèle murin inductible privé des deux lipases ATGL et HSL spécifiquement dans les adipocytes bruns à l’âge adulte : le modèle BAHKO (brown adipocyte ATGL and HSL knockout)2 [17]. Pour déterminer la contribution de la lipolyse du tissu adipeux brun sur son activité thermogénique, nous avons soumis les souris témoins et les souris BAHKO à un test classique d’activation de ce tissu, consistant à les exposer au froid quelques heures sans nourriture et à surveiller leur température corporelle.
Nous avons montré que les souris BAHKO exposées au froid ne sont pas capables de maintenir leur température corporelle, quel que soit leur régime alimentaire ou la température d’acclimatation initiale (30 °C, 21 °C ou 4 °C). Grâce à des mesures calorimétriques indirectes, qui permettent, à partir de la consommation d’oxygène des souris, d’évaluer leur activité métabolique globale, nous avons constaté une réduction de la capacité d’activation métabolique des souris BAHKO par rapport aux souris témoins en réponse à une stimulation du système nerveux sympathique. La preuve directe d’une déficience thermogénique du tissu adipeux brun chez les souris BAHKO a été apportée par la mesure de l’activité oxydante de ce tissu in vivo, en utilisant la détection de traceurs (11C-acétate et 11C-palmitate) par tomodensitométrie par émission de positrons. Cette analyse a montré l’absence totale d’ activité oxydante, a fortiori thermogénique, propre du tissu adipeux brun des souris BAHKO exposées au froid (Figure 1A). Nous en avons conclu que la lipolyse intracellulaire impliquant les lipases ATGL et HSL de l’adipocyte brun est nécessaire pour la production de chaleur par ce tissu. De plus, nous avons constaté que l’absence de lipolyse dans le tissu adipeux brun des souris BAHKO entraîne, d’une part, sa transformation morphologique, caractérisée par un changement de teinte, qui devient beige ou blanche, et par une hypertrophie marquée des adipocytes et de leurs gouttelettes lipidiques, qui accumulent des acides gras (Figure 1B), et d’autre part, le développement d’une inflammation locale signalée par un excès de macrophages (Figure 1C). En conclusion, nous avons montré que la capacité thermogénique de l’adipocyte du tissu adipeux brun est dépendante de la mobilisation intracellulaire (par ATGL et HSL) des acides gras contenus dans ses gouttelettes lipidiques (Figure 2). Cette thermogenèse « non frissonnante », spécifique de ce tissu, contribue substantiellement à la tolérance au froid des mammifères placentaires. Ainsi, il conviendra de ne pas restreindre les futures études sur l’adipocyte brun aux seuls mécanismes de régulation transcriptionnelle par des facteurs clés de la biogenèse mitochondriale, et d’inclure notamment des analyses quantitatives des flux métaboliques nécessaires à l’évaluation de l’activité énergétique du tissu. Enfin, dans une perspective d’application médicale, l’activation pharmacologique sélective de la voie lipolytique du tissu adipeux brun pourrait, en augmentant la thermogenèse, contribuer à une stratégie d’accroissement de la dépense énergétique globale de l’individu, et ainsi, à une meilleure santé cardio-métabolique.
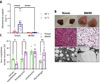 |
Figure 1. Un défaut de lipolyse dans l’adipocyte brun des souris BAHKO conduit à l’involution fonctionnelle, morphologique et inflammatoire du tissu adipeux brun. A. Index d’activité oxydante, i.e. thermogénique, du tissu adipeux brun, issu d’une analyse par imagerie PET-CT (tomodensitométrie par émission de positrons) d’incorporation de [11C]-acétate de souris témoins et BAHKO, déficientes pour ATGL (adipose triglyceride lipase) et HSL (hormone-sensitive lipase) dans les adipocytes de ce tissu, placées à une température de 30 °C (thermoneutralité, en rouge) ou de 10 °C (exposition au froid, en bleu) pendant une semaine. B. En haut : images macroscopiques du tissu adipeux brun interscapulaire d’une souris témoin et d’une souris BAHKO. Au milieu : coloration, par hématoxyline-éosine, de coupes de tissu adipeux brun d’une souris témoin et d’une souris BAHKO (barre d’échelle : 250 mm). En bas : images de microscopie électronique montrant les gouttelettes lipidiques de tissu adipeux brun d’une souris témoin et d’une souris BAHKO (barre d’échelle : 5 mm). C. Proportion des populations cellulaires de la fraction stroma-vasculaire# du tissu adipeux brun chez les souris témoins (en vert) et chez les souris BAHKO (en violet). Les graphiques en A et C indiquent les valeurs moyennes ± s.e.m. (standard error of the mean). * : p < 0,05 ; ** : p < 0,01 ; **** : p < 0,0001. Figure adaptée de [17]. # Le tissu adipeux est composé de plusieurs types cellulaires. Le parenchyme est constitué par les adipocytes. Les autres cellules constituent la « fraction stroma-vasculaire » : cellules progénitrices d’adipocytes (préadipocytes), cellules endothéliales de la paroi des vaisseaux sanguins, cellules du système immunitaire (macrophages, lymphocytes, etc.). |
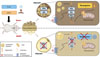 |
Figure 2. La lipolyse du tissu adipeux brun est nécessaire à son activité thermogénique. Lors d’une exposition au froid, les souris BAHKO (en bas), qui sont dépourvues de l’activité des lipases ATGL (adipose triglyceride lipase) et HSL (hormone-sensitive lipase) uniquement dans le tissu adipeux brun, ne peuvent plus fournir les acides gras nécessaires à l’activité métabolique thermogénique propre à ce tissu. Ces souris sont très intolérantes au froid en comparaison des souris témoins (en haut). MGL : monoglyceride lipase. |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- van Marken Lichtenbelt WD, Vanhommerig JW, Smulders NM, et al. Cold-activated brown adipose tissue in healthy men. N Engl J Med 2009 ; 360 : 1500–8. [Google Scholar]
- Becher T, Palanisamy S, Kramer DJ, et al. Brown adipose tissue is associated with cardiometabolic health. Nat Med 2021 ; 27 : 58–65. [Google Scholar]
- Cypess AM, Cannon B, Nedergaard J, et al. Emerging debates and resolutions in brown adipose tissue research. Cell Metab 2025 ; 37 : 12–33. [Google Scholar]
- Morigny P, Boucher J, Arner P, Langin D. Lipid and glucose metabolism in white adipocytes: pathways, dysfunction and therapeutics. Nat Rev Endocrinol 2021 ; 17 : 276–95. [Google Scholar]
- Grabner GF, Xie H, Schweiger M, Zechner R. Lipolysis: cellular mechanisms for lipid mobilization from fat stores. Nat Metab 2021 ; 3 : 1445–65. [Google Scholar]
- Carpentier AC, Blondin DP, Haman F, Richard D. Brown adipose tissue: a translational perspective. Endocr Rev 2023 ; 44 : 143–92. [Google Scholar]
- Bornstein MR, Neinast MD, Zeng X, et al. Comprehensive quantification of metabolic flux during acute cold stress in mice. Cell Metab 2023 ; 35 : 2077–92. [Google Scholar]
- Wojtczak L, Schönfeld P. Effect of fatty acids on energy coupling processes in mitochondria. BiochimBiophys Acta 1993 ; 1183 : 41–57. [Google Scholar]
- Mottillo EP, Bloch AE, Leff T, Granneman JG. Lipolytic products activate peroxisome proliferator-activated receptor (PPAR) α and δ in brown adipocytes to match fatty acid oxidation with supply. J Biol Chem 2012 ; 287 : 25038–48. [Google Scholar]
- Blondin DP, Frisch F, Phoenix S, et al. Inhibition of intracellular triglyceride lipolysis suppresses cold-induced brown adipose tissue metabolism and increases shivering in humans. Cell Metab 2017 ; 25 : 438–47. [Google Scholar]
- Schreiber R, Diwoky C, Schoiswohl G, et al. Cold-induced thermogenesis depends on ATGL-mediated lipolysis in cardiac muscle, but not brown adipose tissue. Cell Metab 2017 ; 26 : 753–63. [Google Scholar]
- Shin H, Ma Y, Chanturiya T, et al. Lipolysis in brown adipocytes is not essential for cold-induced thermogenesis in mice. Cell Metab 2017 ; 26 : 764–77. [Google Scholar]
- Schweiger M, Schreiber R, Haemmerle G, et al. Adipose triglyceride lipase and hormone-sensitive lipase are the major enzymes in adipose tissue triacylglycerol catabolism. J Biol Chem 2006 ; 281 : 40236–41. [Google Scholar]
- Yamada M, Suzuki J, Sato S, et al. Hormone-sensitive lipase protects adipose triglyceride lipase-deficient mice from lethal lipotoxic cardiomyopathy. J Lipid Res 2022 ; 63 : 100194. [Google Scholar]
- Recazens E, Mouisel E, Langin D. Hormone-sensitive lipase: sixty years later. Prog Lipid Res 2021 ; 82 : 101084. [Google Scholar]
- Dufau J, Recazens E, Bottin L, et al. Nuclear hormone-sensitive lipase regulates adipose tissue mass and adipocyte metabolism. Cell Metab 2025 ; 37 : 2250–63 [Google Scholar]
- Mouisel E, Bodon A, Noll C, et al. Cold-induced thermogenesis requires neutral-lipase-mediated intracellular lipolysis in brown adipocytes. Cell Metab 2025 ; 37 : 429–40. [Google Scholar]
En cas de nécessité énergétique (e.g., jeûne, froid), la voie de la lipolyse mobilise les acides gras des stocks de triglycérides (triacylglycérols, constitués de trois acides gras estérifiés sur une molécule de glycérol). Ils seront ensuite catabolisés directement afin de produire de l’énergie, ou libérés dans la circulation sanguine pour fournir de l’énergie au reste de l’organisme. La lipolyse est un processus séquentiel comportant trois étapes et impliquant trois enzymes : 1) la triglycéride lipase (ATGL), qui hydrolyse les triacylglycérols en diacylglycérols, ce qui libère un acide gras, 2) la lipase hormono-sensible (HSL), qui hydrolyse les diacylglycérols en monoacylglycérols, ce qui libère un second acide gras, et 3) la monoglycéride lipase (MGL), qui hydrolyse les monoacylglycérols, ce qui libère le troisième acide gras et la molécule de glycérol. Les deux premières étapes de la lipolyse sont limitantes. Il convient d’ajouter que HSL est capable d’hydrolyser également les triacylglycérols et les monoacylglycérols.
Les souris BAHKO sont issues du croisement de trois lignées murines transgéniques : Pnpla2flox/flox, Lipeflox/flox et Ucp1-icre/ERT2. Les gènes Pnpla2 et Lipe (flanqués des sites flox) codent respectivement ATGL et HSL. La troisième lignée contient le gène codant la recombinase cre (inductible par le tamoxifène) sous le contrôle du promoteur de Ucp1. Ce système permet de supprimer la synthèse des protéines ATGL et HSL uniquement dans les adipocytes bruns produisant UCP1, à partir d’un âge choisi par l’expérimentateur (ici, chez des souris adultes).
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Un défaut de lipolyse dans l’adipocyte brun des souris BAHKO conduit à l’involution fonctionnelle, morphologique et inflammatoire du tissu adipeux brun. A. Index d’activité oxydante, i.e. thermogénique, du tissu adipeux brun, issu d’une analyse par imagerie PET-CT (tomodensitométrie par émission de positrons) d’incorporation de [11C]-acétate de souris témoins et BAHKO, déficientes pour ATGL (adipose triglyceride lipase) et HSL (hormone-sensitive lipase) dans les adipocytes de ce tissu, placées à une température de 30 °C (thermoneutralité, en rouge) ou de 10 °C (exposition au froid, en bleu) pendant une semaine. B. En haut : images macroscopiques du tissu adipeux brun interscapulaire d’une souris témoin et d’une souris BAHKO. Au milieu : coloration, par hématoxyline-éosine, de coupes de tissu adipeux brun d’une souris témoin et d’une souris BAHKO (barre d’échelle : 250 mm). En bas : images de microscopie électronique montrant les gouttelettes lipidiques de tissu adipeux brun d’une souris témoin et d’une souris BAHKO (barre d’échelle : 5 mm). C. Proportion des populations cellulaires de la fraction stroma-vasculaire# du tissu adipeux brun chez les souris témoins (en vert) et chez les souris BAHKO (en violet). Les graphiques en A et C indiquent les valeurs moyennes ± s.e.m. (standard error of the mean). * : p < 0,05 ; ** : p < 0,01 ; **** : p < 0,0001. Figure adaptée de [17]. # Le tissu adipeux est composé de plusieurs types cellulaires. Le parenchyme est constitué par les adipocytes. Les autres cellules constituent la « fraction stroma-vasculaire » : cellules progénitrices d’adipocytes (préadipocytes), cellules endothéliales de la paroi des vaisseaux sanguins, cellules du système immunitaire (macrophages, lymphocytes, etc.). |
| Dans le texte | |
 |
Figure 2. La lipolyse du tissu adipeux brun est nécessaire à son activité thermogénique. Lors d’une exposition au froid, les souris BAHKO (en bas), qui sont dépourvues de l’activité des lipases ATGL (adipose triglyceride lipase) et HSL (hormone-sensitive lipase) uniquement dans le tissu adipeux brun, ne peuvent plus fournir les acides gras nécessaires à l’activité métabolique thermogénique propre à ce tissu. Ces souris sont très intolérantes au froid en comparaison des souris témoins (en haut). MGL : monoglyceride lipase. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




