| Issue |
Med Sci (Paris)
Volume 36, Number 2, Février 2020
Modèles alternatifs
|
|
|---|---|---|
| Page(s) | 147 - 152 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2020012 | |
| Published online | 04 March 2020 | |
Un nouveau paradigme dans le traitement de l’ischémie
L’apport de la drosophile
A new paradigm in the treatment of ischemia. Learning from drosophila
UMR 6097 Université Côte d’Azur, LP2M faculté de Médecine, 28 avenue de Valombrose, 06107 Nice Cedex France
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
L’ischémie est une des préoccupations majeures des cliniciens qui y sont confrontés en permanence, que ce soit aussi bien d’un point de vue chirurgical que pathologique. Les conséquences des stress ischémiques sont dramatiques et peuvent conduire à des incapacités organiques, motrices ou cognitives. Actuellement il n’existe aucune cible moléculaire identifiée dont le ciblage pourrait être bénéfique dans ce domaine. La mouche Drosophila melanogaster, utilisée comme animal modèle, a conduit à une avancée majeure en permettant l’identification d’une toute nouvelle cible pharmacologique dont l’inhibition augmente de façon importante la tolérance à l’hypoxie. Appliqué à un modèle préclinique de transplantation rénale, cette nouvelle approche améliore nettement la reprise fonctionnelle du greffon à long terme. Cette revue retrace les étapes qui ont permis de transférer chez le mammifère supérieur une cible mise en évidence chez la drosophile, ce qui montre clairement, au-delà de la recherche fondamentale, l’apport que peut apporter un organisme modèle à la clinique.
Abstract
Ischemia is one of the major concerns of clinicians who are constantly confronted with it, both in surgical and pathological aspects. The consequences of ischemic stress are dramatic and can lead to organic, motor or cognitive disabilities. Currently, there is no identified specific molecular target whose targeting could be beneficial in this area. The drosophila melanogaster fly, used as a model animal, has made it possible to highlight a major advance by allowing the identification of a completely new pharmacological target whose inhibition significantly increases tolerance to hypoxia. Applied to a preclinical model of renal transplantation, this new approach significantly improves the functional recovery of the graft in the long term. This mini-synthesis retraces the steps that made it possible to transfer to higher mammals a concept highlighted in Drosophila that clearly shows, beyond basic research, the contribution that a model organism can make to the clinic.
© 2020 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Vignette (Photo © Michel Tauc).
La privation d’oxygène est délétère pour l’organisme humain et la recherche clinique est confrontée à un formidable défi face aux troubles physiologiques liés à l’ischémie. Dans tous les cas, c’est l’arrêt de l’apport sanguin aux tissus cibles qui déclenche des processus irréversibles de mort cellulaire pouvant conduire à une dégradation dramatique de l’autonomie cognitive ou motrice des patients. Cet arrêt de l’approvisionnement des tissus peut être programmé, comme dans le cas de la greffe d’organes et de chirurgie aortique, ou physiopathologique, comme lors de la survenue d’un accident vasculaire cérébral (AVC) ou d’un infarctus coronarien. Malgré un nombre élevé d’essais cliniques, il s’avère que, jusqu’à présent, aucun traitement pharmacologique ne s’est révélé réellement efficace. Si l’on prend le cas de l’AVC, qui est une des causes majeure de mortalité, le seul traitement appliqué reste la thrombolyse, avec des fenêtres d’utilisation temporelle très étroites associées à des risques hémorragiques importants.
Si l’on considère le cas de la transplantation, qui est un standard en cas d’insuffisance organique terminale, elle a pris un tel essor que l’on bascule inexorablement vers un contexte de pénurie nécessitant d’élargir la fenêtre de choix en sélectionnant des greffons à critères élargis. Ces organes, considérés comme « limites », sont plus sensibles à l’ischémie et leur reprise fonctionnelle dépend de leur préservation ex vivo. Si la réhabilitation ex vivo des organes [1] peut pallier parfois ce problème d’utilisation de greffons normalement exclus, il n’existe aucun protocole pharmacologique à ciblage précis capable d’augmenter le temps de survie de ceux-ci malgré les progrès effectués sur les liquides de préservation. On peut malgré tout citer la technique qui consiste à pré-conditionner les organes par des ischémies courtes, capables de stimuler des voies endogènes de résistance [2]. Mais si l’on a obtenu des résultats positifs, cette technique reste difficile à appliquer chez le patient. Devant ce blocage conceptuel, il était pertinent de rechercher un nouveau paradigme sur la résistance à l’hypoxie et l’ischémie afin d’identifier de nouvelles cibles situées très en amont et capables de bloquer très tôt les processus conduisant à la mort cellulaire et organique.
Pour contourner cette impasse, le retour à des organismes modèles peut, de par leur relative simplicité d’utilisation et leur moindre complexité, apporter des réponses innovantes. Cet abord réductionniste a, par le passé, permis l’élaboration de nouveaux concepts biologiques. Si l’on remonte dans le temps, et si l’on prend l’exemple du cerveau, le mollusque gastéropode marin Aplysia californica, pourtant très éloigné de la physiologie des mammifères, pris comme animal modèle par Ladislav Tauc [3], a une histoire vénérable en tant que modèle de fonctionnement du système nerveux et plus spécialement de la transmission synaptique [4], avec une importance particulière dans les études sur l’apprentissage et la mémoire. D’ailleurs en 2000, Eric Richard Kandel, un neurophysiologiste, a partagé avec Arvid Carlsson, Paul Greengard et Eric Kandel1, le prix Nobel de physiologie ou médecine pour ses travaux sur les bases moléculaires de la mémoire à court terme et de la mémoire à long terme qu’il avait conduits sur l’aplysie.
En ce qui concerne l’ischémie, le retour à un organisme modèle a récemment permis un progrès prometteur : il était raisonnable d’émettre l’hypothèse que, comme l’oxygène est nécessaire à tous les organismes aérobies sur terre, du plus simple au plus complexe, des mécanismes de défense contre son appauvrissement au sein des cellules se sont mis en place très tôt et sont restés conservés au cours de l’évolution. En 2006, Vigne et Frelin [5] ont développé une nouvelle approche physiologique de l’hypoxie chez la drosophile, un insecte qui partage nombre de processus biologiques avec les vertébrés. Sa relative simplicité et son cycle biologique court, associés à de grandes facilités d’élevage, dénuées de tout risque d’agressivité ou de transmission de maladies, en ont fait un incontournable outil pour la communauté scientifique dans les domaines du développement, du vieillissement, de la mémoire et de l’apprentissage, des rythmes circadiens ou encore du cancer.
On savait qu’une restriction alimentaire augmentait la durée de vie des drosophiles [6,7]. Aussi, y a-t-il une relation entre régime alimentaire et résistance à l’hypoxie chez la drosophile ? C’est la question que se sont posés Vigne et Frelin. Dans une atmosphère appauvrie en oxygène (5 % O2), les drosophiles nourries avec un régime équilibré en protéines (10 % de levures ou 10 % de caséine) et en carbohydrates (10 % de sucrose), ont une durée de vie moyenne de 6 jours (Figure 1). Ces mêmes mouches, nourries uniquement avec une solution de sucrose, voient leur durée de vie moyenne passer à plus de 16 jours. Il apparaît donc clairement que les protéines sont toxiques pour les drosophiles maintenues en hypoxie chronique, et que ce n’est pas l’apport calorique qui est en cause, mais bien la nature protéique de leur régime alimentaire [7].
 |
Figure 1. Indice de survie des mouches en hypoxie en fonction du régime alimentaire. Les mouches ont été nourries avec un régime à 10 % de sucrose supplémenté avec des acides aminés (10 mM) représentatifs de leur classe et les courbes de survie ont été déterminées dans des conditions hypoxiques chroniques (5 % d’O2). L’histogramme représente les longévités moyennes. Les barres noires montrent les situations de contrôle qui correspondent à un régime équilibré en protéines et sucre, un régime en pur sucrose et des conditions de jeûne. Des codes de couleur ont été utilisés pour étiqueter les acides aminés basiques (bleu), les acides aminés hydrophobes (vert) les acides aminés acides (rouge) et les acides aminés hydrophiles neutres (jaune). |
Les mouches ont ensuite été alimentées par un régime constitué de 10 % de sucrose complémenté par 10 mM de n’importe quel acide aminé contenu dans un hydrolysat de caséine. Dans ces conditions, quel que soit l’acide aminé ajouté, celui-ci réduit la tolérance hypoxique des drosophiles (Figure 1). Tous les acides aminés testés nécessitent une atmosphère hypoxique pour que leur toxicité soit observée ; ils restent sans effet en condition normoxique. Ces données ne permettent malheureusement pas de relier l’effet de raccourcissement de la durée de vie induit par ces acides aminés à une quelconque structure spécifique, charge ou hydrophobicité. Aussi, leur effet négatif nécessite d’être relié à une voie métabolique qui leur soit commune. Le cycle de l’urée (Figure 2A) est ainsi potentiellement un bon candidat : c’est la voie catabolique qu’empruntent tous les acides aminés et dont un des rôles est l’élimination de l’azote excédentaire sous forme d’urée [8]. Ce cycle est aussi à l’origine de la biosynthèse des polyamines, molécules essentielles pour la vie, la croissance et la division cellulaire. Une des hypothèses émises est donc que ces polyamines interviendraient dans le mécanisme de toxicité induite par les protéines. Cette hypothèse a été confirmée. En effet, en ajoutant des polyamines (spermine ou spermidine) à un régime uniquement sucré, la longévité des drosophiles maintenues en hypoxie diminue [9] (Figure 2B).
 |
Figure 2. Représentation schématique du nouveau concept pharmacologique de protection de l’ischémie et effets des inhibiteurs DFMO et GC7. A. Le cycle de l’urée génère des polyamines à partir de l’ornithine via l’ornithine décarboxylase (5) qui est inhibée par le DFMO (α-difluorométhylornithine). La voie des polyamines passe par la spermidine qui est à l’origine de la synthèse du facteur d’initiation de la traduction 5A (eIF5A). L’activation de eIF5A nécessite l’action successive de la DHS (10) et de la DOHH (11). L’action du GC7, inhibiteur compétitif de la DHS et donc de l’activation de eIF5A, induit la tolérance hypoxique et ischémique. B. Effets des intermédiaires du cycle de l’urée et des polyamines ajoutés à un régime uniquement sucré sur l’indice de survie de drosophiles maintenues en hypoxie chronique (5 % d’O2). C. Effet du DFMO sur la survie moyenne des drosophiles maintenues en hypoxie et dont le régime sucré contient les éléments cités. D. Effet du GC7 sur la survie moyenne des drosophiles maintenues en hypoxie et dont le régime sucré contient les éléments cités. |
Dans la voie de biosynthèse des polyamines, l’ornithine décarboxylase est une enzyme clé. Elle est située très en amont de la voie de biosynthèse des polyamines et l’α-difluorométhylornithine (DFMO) en est un inhibiteur sélectif (Figure 2A). L’ajout de DFMO à un régime protéiné protège les drosophiles des effets néfastes de l’hypoxie. Inversement, l’ajout de putrescine ou de spermidine en présence de DFMO abolit son effet protecteur (Figure 2C). Le découplage du cycle de l’urée de la synthèse des polyamines est donc bien, ici, impliqué dans la tolérance hypoxique.
Une des branches de la voie des polyamines fournit de la spermidine pour l’hypusination (une modification post-traductionnelle2) du facteur d’initiation de la traduction 5A (eIF5A) (Figure 1A). eIF5A est la seule protéine connue pour contenir l’acide aminé hypusine qui y est incorporé par l’intermédiaire de 2 réactions enzymatiques successives : la déoxyhypusine synthase qui transfère le résidu 4-aminobutyl de la spermidine sur le groupe aminé d’une lysine spécifique de la forme inactive de eIF5A, et la déoxyhypusine hydroxylase qui hydroxyle la forme déoxyhypusinée de eIF5A pour donner sa forme active hypusinée [10]. Cette chaîne enzymatique peut être bloquée spécifiquement dans sa première étape par un dérivé guanylé du 1,7 diaminoheptane : le GC7 (Figure 1) [11]. Or, le GC7 ajouté à une alimentation protéique, ou une alimentation sucrée additionnée avec de la spermidine ou de la spermine, augmente la longévité moyenne des mouches maintenues en hypoxie (Figure 2D) [9].
Le blocage spécifique de l’activation de eIF5A induit donc une importante tolérance hypoxique chez la drosophile. Ce nouveau concept donne un éclairage nouveau sur les voies moléculaires potentielles impliquées dans la gestion de l’oxygène par les eucaryotes.
La transposition chez le mammifère
Cette stratégie qui peut apparaître réductionniste, prend une toute autre dimension si elle peut avoir des répercussions chez le mammifère et, in fine, en clinique humaine. Les organes les plus sensibles à un stress ischémique sont le cerveau, le cœur et le rein, en raison de leur faible, voire inexistante, capacité à se régénérer. Si les deux premiers sont complexes à analyser d’un point de vue fonctionnel, les paramètres rénaux sont, quant à eux, plus simples à quantifier. Nous avons donc appliqué le concept de protection mis en évidence chez la drosophile sur un modèle d’ischémie rénale unilatérale chez le rongeur [12], dans un protocole de pré-conditionnement.
Le pré-conditionnement a été appliqué à des rats par injection intrapéritonéale de l’inhibiteur de la déoxyhypusine synthase, GC7, deux jours avant un acte chirurgical, qui consiste à bloquer le flux artériel du rein gauche pendant 40 minutes et à le rétablir pendant 24 heures avant de réaliser une analyse fonctionnelle indépendante des 2 reins par la technique des clairances. Le rein droit laissé intact sert alors de contrôle interne pour chaque animal (Figure 3A). L’ischémie ainsi réalisée induit une augmentation de l’excrétion fractionnelle de sodium (Figure 3B), de phosphate et de glucose [13], ainsi que l’apparition dans les urines du marqueur de l’atteinte tubulaire NGAL (neutrophil gelatinase-associated lipocalin) (Figure 3C) L’altération de ces paramètres reflète une atteinte drastique du tubule proximal, qui est majoritairement en charge de la gestion de ces ions et des métabolites. Le traitement préalable au GC7 empêche de façon importante la dégradation de ces paramètres, indiquant un effet protecteur vis-à-vis de la privation d’oxygène (Figure 3B, C) [13]. Ce résultat fondamental démontre donc que la translation vers le mammifère du concept mis en évidence chez la drosophile est possible et que les voies mises en jeu semblent très conservées entre ces deux espèces. Un des faits marquants observés chez les animaux traités par le GC7 est la baisse globale de leur consommation en oxygène à l’état de veille. Cette baisse de consommation a pu être reliée, sur un modèle de cellules rénales en culture, à une baisse de la phosphorylation oxydative, avec pour conséquence une diminution de la production de radicaux libres qui sont, à partir d’un certain seuil, extrêmement toxiques pour la cellule [13]. La voie ainsi mise en évidence semble, de plus, indépendante de la classique réponse à l’hypoxie, qui est contrôlée par le facteur de transcription HIF (hypoxia-inducible factor) [14] (→)
(→) Voir la Synthèse de E. Gothié et J. Pouysségur, m/s n° 1, janvier 2002, page 70
 |
Figure 3. Protocole de validation de la protection ischémique sur un modèle d’ischémie rénale. A. Les rats sont prétraités avec du GC7 (3 mg/Kg) 24 heures et 1 heure avant le clampage chirurgical de l’artère rénale gauche pendant 40 min. 24 heures après la reperfusion, la fonction rénale des animaux est évaluée par la méthode des clairances. B. Effet du GC7 sur le marqueur de l’atteinte tubulaire NGAL en unité arbitraire ramenée à la créatinine. C. Effet du GC7 sur l’excrétion fractionnelle du sodium. |
L’application à un modèle préclinique
La transplantation d’organes est un des meilleurs cas de figure pour l’application du concept mis en évidence avec la drosophile et appliqué sur les cellules de mammifère, puisque, dans ce cas, l’ischémie est prévisible et l’acte chirurgical planifié. Dans le cas du rein, la dialyse péritonéale ou l’hémodialyse peut compenser le dysfonctionnement rénal, mais la qualité de vie du patient reste fortement impactée et les coûts engendrés sont considérables pour la société puisqu’il s’agit d’un traitement récurrent, à vie. La greffe rénale est, de ce fait, en plein essor mais un tel engouement reste tributaire de protocoles pharmacologiques capables d’améliorer la résistance des greffons à l’ischémie et à leur reprise fonctionnelle.
L’un des modèles classiquement utilisés pour valider un concept au niveau préclinique est le cochon, et toutes les techniques chirurgicales utilisées sont celles appliquées chez l’homme (Figure 4A) [15]. Les animaux ont été traités par injection intraveineuse de GC7 24 heures et 3 heures avant l’ischémie chaude, induite par clampage du pédicule rénal. Ce type d’ischémie chaude, associée à la préservation du greffon à 4 °C pendant 24 h dans la solution de préservation élaborée par Folkert Belzer de l’Université du Wisconsin (UW)3, reproduit les lésions ischémiques qui sont constatées sur les organes provenant de patient décédés par arrêt cardiaque. Le rein a été greffé sur l’animal sur lequel une néphrectomie contralatérale avait été pratiquée. Les paramètres physiologiques ont été suivis sur une période de 3 mois. Chez les animaux témoins, l’ischémie reperfusion a provoqué à court et long terme une altération de la fonction rénale de l’organe greffé, comme l’indique le temps de récupération de la diurèse, l’excrétion fractionnelle de sodium, l’osmolarité de l’urine ou encore l’excrétion d’alanine aminopeptidase [13]. Chez les animaux préalablement traités au GC7, l’ultrastructure du rein est restée nettement mieux préservée (Figure 4B), le taux de cellules apoptotiques a été diminué, le stress oxydatif (Figure 4C) et la peroxydation des lipides se sont maintenus à un bas niveau et le développement de la fibrose interstitielle, à 3 mois, a été également diminué (Figure 4D). Le GC7 a aussi montré un effet protecteur à long terme contre l’inhibition de la fibrinolyse des vaisseaux connue pour déclencher la fibrose [13]. L’augmentation de la créatinine plasmatique, un marqueur essentiel de l’état de la fonction rénale, est également moindre chez les animaux traités et retrouve un niveau identique au témoin à un mois post-greffe (Figure 4E).
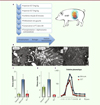 |
Figure 4. Validation du concept dans un modèle préclinique de transplantation rénale chez le cochon. A. Représentation schématique du protocole de transplantation rénale chez le cochon. B. Ultrastructure de la bordure en brosse du tubule proximal 30 min après la reperfusion, la bordure en brosse est préservée chez les animaux traités au GC7 (barre d’échelle = 0,5 μm). C. Effet du GC7 sur le niveau de stress oxydatif 30 min après reperfusion et mesuré par le marquage CellROX® (unité arbitraire). D. Effet du GC7 sur le niveau de fibrose du greffon, 3 mois après transplantation et mesuré sur coupes colorées au rouge Sirius (unité abitraire). E.x Effet du GC7 sur l’évolution de la créatinine plasmatique pendant 3 mois chez les animaux greffés (unité = μmol/L). Ces résultats sont les moyennes obtenues à partir de 6 animaux dans chaque groupe |
Conclusion
Depuis plus d’un siècle, Drosophila melanogaster est l’un des organismes modèles les plus utilisés pour la recherche en génétique. Les scientifiques ont essayé de comprendre sa biologie et de la relier aux processus biologiques humains. Malgré cela, très peu d’études ont pu être transférées à la physiologie des mammifères supérieurs, comme cela a été réalisé dans les études que nous décrivons. Une nouvelle approche mise en évidence dans la tolérance ischémique, montre que nous avons plus en commun avec cette minuscule mouche qu’on ne le pense. Cette découverte a un fort potentiel qui pourrait être utilisé pour développer de nouvelles approches pour les cliniciens pour toutes les pathologies dans lesquelles le manque temporaire d’oxygène est concerné et est source de conséquences dramatiques. Cette approche est d’ailleurs actuellement testée dans un modèle d’AVC chez la souris. Elle montre que le GC7 est capable d’améliorer considérablement la récupération motrice et cognitive des animaux [16].
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Pour leurs découvertes concernant la transmission du signal dans le système nerveux.
Consiste en la transfert d’un groupement 4-aminobutyl de la spermidine sur un acide aminé tel que la lysine.
Références
- Ciubotaru A, Haverich A. Ex vivo approach to treat failing organs: expanding the limits. ESR 2015 ; 54 : 64–74. [Google Scholar]
- Veighey K, MacAllister R. Ischemic conditioning in kidney transplantation. J Cardiovasc Pharmacol Ther 2017 ; 22 : 330–336. [CrossRef] [PubMed] [Google Scholar]
- Tauc L. Studies on elementary activity of cells of the abdominal ganglion of Aplysia. J Physiol (Paris) 1955 ; 47 : 769–792. [Google Scholar]
- Kandel ER, Tauc L. Mechanism of prolonged heterosynaptic facilitation. Nature 1964 ; 202 : 145–147. [Google Scholar]
- Arquier N, Vigne P, Duplan E, et al. Analysis of the hypoxia-sensing pathway in Drosophila melanogaster. Biochem J 2006 ; 393 : 471–480. [CrossRef] [PubMed] [Google Scholar]
- Vigne P, Tauc M, Frelin C. Strong dietary restrictions protect Drosophila against anoxia/reoxygenation injuries. PLoS One 2009 ; 4 : e5422. [CrossRef] [PubMed] [Google Scholar]
- Vigne P, Frelin C. A low protein diet increases the hypoxic tolerance in Drosophila. PLoS One 2006 ; 1 : e56. [CrossRef] [PubMed] [Google Scholar]
- Barmore W, Stone WL Physiology, urea cycle 2019 ; Treasure Island (FL) StatPearls Publishing [Google Scholar]
- Vigne P, Frelin C. The role of polyamines in protein-dependent hypoxic tolerance of Drosophila. BMC Physiol 2008 ; 8 : 22. [Google Scholar]
- Park MH, Nishimura K, Zanelli CF, et al. Functional significance of eIF5A and its hypusine modification in eukaryotes. Amino Acids 2010 ; 38 : 491–500. [CrossRef] [PubMed] [Google Scholar]
- Lee YB, Folk JE. Branched-chain and unsaturated 1,7-diaminoheptane derivatives as deoxyhypusine synthase inhibitors. Bioorg Med Chem 1998 ; 6 : 253–270. [CrossRef] [PubMed] [Google Scholar]
- Kato J, Nakayama M, Zhu WJ, et al. Ischemia/reperfusion of unilateral kidney exaggerates aging-induced damage to the heart and contralateral kidney. Nephron Exp Nephrol 2014 ; 126 : 183–190. [CrossRef] [PubMed] [Google Scholar]
- Melis N, Rubera I, Cougnon M, et al. Targeting eIF5A hypusination prevents anoxic cell death through mitochondrial silencing and improves kidney transplant outcome. J Am Soc Nephrol 2017 ; 28 : 811–822. [Google Scholar]
- Gothié E, Pouysségur J. HIF-1: régulateur central de l’hypoxie. Med Sci (Paris) 2002 ; 18 : 70–78. [CrossRef] [EDP Sciences] [Google Scholar]
- Rossard L, Favreau F, Giraud S, et al. Role of warm ischemia on innate and adaptive responses in a preclinical renal auto-transplanted porcine model. J Transl Med 2013 ; 11 : 129. [CrossRef] [PubMed] [Google Scholar]
- Blondeau N, Bourourou M, Gouix E, et al. By the demonstration of its anti-ischemic potential, the spermidine analog GC7 identifies a new targetable pathway against stroke. J Cereb Blood Flow Metab 2019 ; 39 : 374–375. [Google Scholar]
Liste des figures
 |
Figure 1. Indice de survie des mouches en hypoxie en fonction du régime alimentaire. Les mouches ont été nourries avec un régime à 10 % de sucrose supplémenté avec des acides aminés (10 mM) représentatifs de leur classe et les courbes de survie ont été déterminées dans des conditions hypoxiques chroniques (5 % d’O2). L’histogramme représente les longévités moyennes. Les barres noires montrent les situations de contrôle qui correspondent à un régime équilibré en protéines et sucre, un régime en pur sucrose et des conditions de jeûne. Des codes de couleur ont été utilisés pour étiqueter les acides aminés basiques (bleu), les acides aminés hydrophobes (vert) les acides aminés acides (rouge) et les acides aminés hydrophiles neutres (jaune). |
| Dans le texte | |
 |
Figure 2. Représentation schématique du nouveau concept pharmacologique de protection de l’ischémie et effets des inhibiteurs DFMO et GC7. A. Le cycle de l’urée génère des polyamines à partir de l’ornithine via l’ornithine décarboxylase (5) qui est inhibée par le DFMO (α-difluorométhylornithine). La voie des polyamines passe par la spermidine qui est à l’origine de la synthèse du facteur d’initiation de la traduction 5A (eIF5A). L’activation de eIF5A nécessite l’action successive de la DHS (10) et de la DOHH (11). L’action du GC7, inhibiteur compétitif de la DHS et donc de l’activation de eIF5A, induit la tolérance hypoxique et ischémique. B. Effets des intermédiaires du cycle de l’urée et des polyamines ajoutés à un régime uniquement sucré sur l’indice de survie de drosophiles maintenues en hypoxie chronique (5 % d’O2). C. Effet du DFMO sur la survie moyenne des drosophiles maintenues en hypoxie et dont le régime sucré contient les éléments cités. D. Effet du GC7 sur la survie moyenne des drosophiles maintenues en hypoxie et dont le régime sucré contient les éléments cités. |
| Dans le texte | |
 |
Figure 3. Protocole de validation de la protection ischémique sur un modèle d’ischémie rénale. A. Les rats sont prétraités avec du GC7 (3 mg/Kg) 24 heures et 1 heure avant le clampage chirurgical de l’artère rénale gauche pendant 40 min. 24 heures après la reperfusion, la fonction rénale des animaux est évaluée par la méthode des clairances. B. Effet du GC7 sur le marqueur de l’atteinte tubulaire NGAL en unité arbitraire ramenée à la créatinine. C. Effet du GC7 sur l’excrétion fractionnelle du sodium. |
| Dans le texte | |
 |
Figure 4. Validation du concept dans un modèle préclinique de transplantation rénale chez le cochon. A. Représentation schématique du protocole de transplantation rénale chez le cochon. B. Ultrastructure de la bordure en brosse du tubule proximal 30 min après la reperfusion, la bordure en brosse est préservée chez les animaux traités au GC7 (barre d’échelle = 0,5 μm). C. Effet du GC7 sur le niveau de stress oxydatif 30 min après reperfusion et mesuré par le marquage CellROX® (unité arbitraire). D. Effet du GC7 sur le niveau de fibrose du greffon, 3 mois après transplantation et mesuré sur coupes colorées au rouge Sirius (unité abitraire). E.x Effet du GC7 sur l’évolution de la créatinine plasmatique pendant 3 mois chez les animaux greffés (unité = μmol/L). Ces résultats sont les moyennes obtenues à partir de 6 animaux dans chaque groupe |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




