| Issue |
Med Sci (Paris)
Volume 35, Number 12, Décembre 2019
Anticorps monoclonaux en thérapeutique
|
|
|---|---|---|
| Page(s) | 975 - 981 | |
| Section | La révolution des anticorps modulateurs de la réponse immunitaire en oncologie | |
| DOI | https://doi.org/10.1051/medsci/2019241 | |
| Published online | 06 January 2020 | |
Quelles chaînes lourdes d’immunoglobulines pour quels anticorps d’immunostimulation ?
Which immunoglobulin heavy chains for which immunostimulatory antibodies?
1
Équipe Fc receptors, antibodies and microenvironment, EA7501 GICC, Université de Tours, Tours, France
2
Laboratoire d’immunologie, CHU de Tours, Tours, France
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
En cancérologie, les anticorps conduisant à une immunostimulation, ou anticorps d’immunostimulation, relèvent de différents mécanismes d’action: simple blocage de récepteurs agissant comme points de contrôle de l’immunité, élimination des lymphocytes T régulateurs infiltrant les tumeurs, action agoniste sur des récepteurs activateurs des lymphocytes, etc. Dans la mesure où ces propriétés font parfois intervenir la région Fc et la région charnière, le choix du bon isotype de chaîne lourde ou de variants de cette chaîne lourde obtenus par ingénierie peut s’avérer déterminant pour l’efficacité thérapeutique. Cette brève revue tente de tirer les premières leçons de l’expérience clinique.
Abstract
Immunostimulatory antibodies in cancer rely on different mechanisms of action, simple blocking of immune checkpoints, depletion of tumour-infiltrating regulatory T cells, agonistic action on lymphocyte activatory receptors, etc. Choosing the relevant heavy chain isotype or the adequate engineering variant of this heavy chain is critical for the therapeutic efficacy, since the aforementioned properties sometimes bring into play the Fc region and the hinge region. This short review tries to learn the lessons from the clinical experience.
© 2019 médecine/sciences – Inserm
Le formidable succès en cancérologie des anticorps inhibiteurs des points de contrôle de l’immunité (immune checkpoint inhibitors) (IPCI) s’ajoute à tous les autres succès des anticorps anticancéreux, qu’il s’agisse d’anticorps cytotoxiques antitumoraux, d’antiprolifératifs, d’antiangiogéniques, d’antibody-drug conjugates ou d’anticorps bispécifiques engageant les lymphocytes T. Comme précédemment discuté [1] (→), nous manquons de termes pour englober tout ou partie de ces concepts thérapeutiques, le terme d’immunothérapie étant particulièrement difficile à manier, y compris pour les IPCI. En effet, ces derniers déterminent une immunothérapie active non spécifique, alors que les anticorps déterminent habituellement une immunothérapie passive spécifique [1], même si ce dernier point peut être nuancé par le fait que différents travaux utilisant des modèles murins et différentes données cliniques ont montré l’induction d’une réponse T mémoire par des anticorps dirigés contre la tumeur [32] (→).
(→) Voir le Forum de H. Watier, m/s n° 5, mai 2014, page 567
(→) Voir la Nouvelle de M. Pelegrin et al., m/s n° 5, mai 2013, page 457
Nous préférons donc le terme d’anticorps d’immunostimulation pour englober les anticorps conçus pour réveiller le système immunitaire et déclencher une immunité antitumorale, d’autant que ces derniers ne vont pas se limiter aux IPCI. En effet, les anticorps d’immunostimulation entrent a priori dans deux catégories, les IPCI qui sont des antagonistes de récepteurs inhibiteurs (anti-CTLA-4 [cytotoxic T-lymphocyte-associated protein 4], anti-PD-1 [programmed cell death 1], etc.) ou de leurs ligands membranaires (anti-PD-L1 [programmed death-ligand 1]), et les anticorps agonistes de récepteurs d’activation (anti-CD40, anti-CD137, etc.). Les premiers sont déjà sur le marché alors que les seconds sont encore au stade des essais cliniques.
Bien faire la distinction entre toutes les catégories d’anticorps n’est pas qu’un simple exercice conceptuel ou sémantique. Les effets pharmacologiques attendus diffèrent en effet d’une catégorie à l’autre, non seulement du fait de la cible, mais aussi du choix de la chaîne lourde d’IgG qui détermine les propriétés de la région Fc et celles de la charnière (Figure 1). En cancérologie, il est classique de choisir l’isotype γ1 et donc la sous-classe IgG1 afin de renforcer le potentiel de destruction tumorale, par recrutement des effecteurs de l’immunité, humoraux (complément) et cellulaires (cellules exprimant des récepteurs pour la région Fc des IgG ou RFcγ). Les IgG2 (isotype γ2) et les IgG4 (isotype γ4), beaucoup moins cytolytiques, sont donc habituellement écartées. Les anticorps antagonistes de l’EGFR (epidermal growth factor receptor) dont l’un est une IgG1 (cétuximab) et l’autre une IgG2 (panitumumab) constituent un exemple assez éloquent. Les deux sont efficaces dans le cancer colorectal sans mutation du gène KRAS, laissant penser que l’antagonisation de l’EGFR suffit à obtenir l’effet thérapeutique. En revanche, seul le cétuximab s’est révélé efficace dans les cancers de la sphère ORL (oto-rhino-laryngologiques) ; dans ce cas, l’antagonisation de l’EGFR ne suffit sans doute pas et l’action cytolytique de l’IgG1 apparaît déterminante pour obtenir l’effet antitumoral.
 |
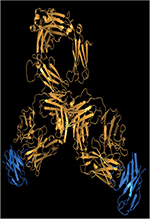
Figure 1. Différences entre sous-classes d’IgG humaines au niveau de la région charnière. A et B. Structure d’une IgG1 (A) et d’une IgG4 (B), les deux seules sous-classes d’IgG humaines ayant été cristallisées dans leur intégralité. Les chaînes lourdes sont en noir, les chaînes légères en gris ; les N-glycanes de la région Fc sont indiqués en rouge. Les figures ont été réalisées en utilisant PyMOL Molecular Graphics System, version 1.7.4 (Schrödinger) à partir du fichier PDB 1HZH représentant l’unique IgG1 humaine cristallisée, nommée B12 et dirigée contre la gp120 du VIH (virus de l’immunodéficience humaine) et à partir du fichier PDB 5DK3 représentant le pembrolizumab, l’unique IgG4 humaine cristallisée (variant G4e1). La grande flexibilité de la région charnière des IgG1 donne de la liberté aux bras Fab et provoque une forte asymétrie. Il n’existe malheureusement pas de structure d’une IgG2 humaine entière. C. Alignement de la région charnière des chaînes lourdes g 1, g 2 et g 4 humaines. Les acides aminés (selon la numérotation EU) et les nucléotides qui diffèrent de la séquence des IgG1 sont indiqués en rouge. Les cystéines engagées dans des ponts disulfures sont indiquées en gras. Les différences notables apparaissent en fond orangé: délétion de 3 acides aminés dans l’IgG2 et l’IgG4, cystéines 219 et 220 de l’IgG2, et sérine 228 de l’IgG4 (voir texte). |
La simple distinction entre IgG1 cytolytiques et IgG2/IgG4 non cytolytiques est en réalité bien plus complexe. D’une part, les IgG2 et les IgG4 ne sont pas totalement silencieuses du point de vue de l’activation du complément ou du recrutement des cellules RFcγ+. D’autre part, les IgG1 ne se révèlent pas forcément cytolytiques chez le patient, à l’image de quelques anticorps antagonistes tels que l’éfalizumab (anti-intégrine LFA-1 [lymphocyte function-associated antigen 1]) ou le basiliximab (anti-IL[interleukine]-2Rα/CD25) qui ne provoquent pas de lymphopénie. Par ailleurs, les progrès de l’ingénierie moléculaire permettent maintenant d’obtenir des IgG1 dont l’effet cytotoxique est dopé, ou au contraire aboli (IgG1 à Fc silencieux), ou des IgG2 et des IgG4 ayant des régions Fc totalement silencieuses. Comme nous allons le voir, d’autres variations peuvent être introduites pour améliorer la stabilité des anticorps in vitro (stockage préadministration) ou in vivo. Ces variants d’ingénierie, de plus en plus nombreux, élargissent considérablement l’éventail des possibilités pharmacologiques. Pour les repérer plus facilement, nous avons proposé un nouveau système de nomenclature dénommé Ge (IgG engineered), décliné en G1e, G2e et G4e selon la sous-classe, inspiré du système de nomenclature des allotypes Gm (IgG marker) [2]. Les Tableaux I (variants G1e des IgG1) et II (variants G4e des IgG4) donnent une version actualisée des variants d’anticorps ou de protéines de fusion contenant une région Fc, au fur et à mesure de leur mise sur le marché.
La diversité des cibles des anticorps d’immunostimulation jointe à la diversité des sous-classes d’IgG et de leurs variants provoque un paysage complexe, mais qui finit par être assez informatif sur la pharmacologie de ces anticorps chez l’homme. C’est ce que nous allons décrire, en considérant chaque cible ou type de cible.
Antagonistes des points de contrôle de l’immunité
Anticorps anti-CTLA-4
Avec le recul, le cas des anticorps anti-CTLA-4 (CD152) est très instructif et illustre toute la difficulté à prédire l’activité d’une sous-classe d’anticorps chez l’homme. En 2007, deux anticorps étaient en compétition, l’ipilimumab, qui est une IgG1κ (chaîne lourde γ1 non mutée G1e0, allotype rare G1m3,1) et le trémélimumab qui est une IgG2κ (chaîne lourde γ2 non mutée G2e0, allotype G2m-23). Le choix de l’IgG2 rassurait [3], car il correspondait mieux au profil pharmacologique attendu d’un anticorps purement antagoniste, peu susceptible de détruire les cellules exprimant CTLA-4. à l’inverse, le choix d’une IgG1 inquiétait, car susceptible d’induire des effets non recherchés, à commencer par la destruction des lymphocytes que l’on souhaitait réveiller, même si les essais précliniques n’étaient pas source d’inquiétude [4].
La suite est maintenant connue… De façon a priori paradoxale, l’ipilimumab a obtenu une AMM dans le traitement du mélanome dès 2007, tandis que le trémélimumab n’a toujours pas été approuvé, malgré de multiples essais de phase III dont aucun ne s’est révélé concluant. Rien ne prouve évidemment que l’incapacité des IgG2 à recruter les effecteurs du système immunitaire soit la cause de l’échec du trémélimumab, mais l’hypothèse mérite sérieusement d’être soulevée. Autrement formulé, comment expliquer qu’un IPCI doublé d’une activité déplétante soit plus actif qu’un anticorps simplement antagoniste de CTLA-4 ? Un premier élément d’explication est venu d’expériences pratiquées chez la souris, avec un anticorps anti-CTLA-4 décliné en plusieurs sous-classes d’IgG de souris [5]. Dans ces modèles, l’anticorps de sous-classe murine IgG2a (avec activité déplétante) a montré une activité antitumorale, au contraire du même anticorps avec la sous-classe murine IgG1 connue pour sa faible activité cytotoxique [5]. La différence d’efficacité semble s’expliquer par la capacité de l’IgG2a anti-CTLA-4 à éliminer rapidement les lymphocytes T régulateurs (Treg) intratumoraux, à la différence de l’IgG1 murine anti-CTLA-4 [5]. Il faut évidemment se garder de toute transposition hâtive avec la situation clinique (ipilimumab vs trémélimumab), tant les sous-classes d’IgG et les mécanismes effecteurs divergent entre espèces. De fait, comme souvent, les données cliniques peinent à confirmer l’hypothèse. Ainsi, après des premières observations encourageantes [6], un article récent a montré que les tumeurs de patients traités par ipilimumab ne montraient pas d’infiltration moindre de Treg par rapport aux tumeurs de patients traités par trémélimumab [7]. Cette étude présente néanmoins un certain nombre de limites qui ont été discutées [8] et qui empêchent d’en tirer des conclusions définitives. Un autre élément dont il faut tenir compte est la très grande variabilité de réponse à l’ipilimumab, avec une faible proportion de patients répondeurs. Or les tumeurs des patients répondeurs à l’ipilimumab montrent avant traitement une plus forte infiltration de macrophage CD68+ [6] et de lymphocytes CD56+ [9] que les non-répondeurs. Ces effecteurs cellulaires expriment le RFcγIIIa/CD16a, un des récepteurs Fc des IgG dont nous avons révélé l’importance pour l’activité clinique des anticorps cytotoxiques, par le biais de l’analyse du polymorphisme de son gène et la mise en évidence d’une relation génotype/phénotype [10]. Avec le recul de plusieurs cohortes de patients traités par différents anticorps cytotoxiques, les patients qui répondent le mieux sont les homozygotes pour la forme 158-valine (158V) du RFcγIIIa (RFcγIIIa-158VV), qui constituent entre 15 et 20 % de la population. Or il apparaît que, sous traitement par ipilimumab, les patients RFcγIIIa-158VV dont la tumeur présente une forte charge néoantigénique ont une meilleure survie que les patients porteurs de l’allotype 158-phénylalanine (158F) de ce même récepteur (à l’état hétérozygote ou homozygote) avec une forte charge néoantigénique tumorale, et que tous les patients ayant une faible charge néoantigénique, quel que soit l’allotype RFcγIIIa dont ils sont porteurs [11]. Ces résultats montrent que le recrutement des effecteurs par la région Fc de l’ipilimumab est déterminante pour l’efficacité thérapeutique, et que l’efficacité des anticorps anti-CTLA-4 peut sans doute être optimisée, au moins chez les patients présentant une forte charge antigénique, afin de leur permettre de répondre même quand ils sont porteurs de l’allotype RFcγIIIa-158F. Des données précliniques montrent d’ores et déjà que des anticorps dont la région Fc a fait l’objet d’une ingénierie afin d’accroître la capacité à recruter les cellules RFcγ+ ont une meilleure activité thérapeutique [12]. Des essais cliniques ont maintenant été lancés par Agenus, avec l’AGEN1181, une IgG1 mutée anti-CTLA-4 dont l’ingénierie protéique portant sur la chaîne lourde n’a malheureusement pas encore été divulguée [13].
Dans tous les cas, il apparaît que les anticorps anti-CTLA-4 efficaces ne sont pas que de simples IPCI, ce qui justifie d’autant le terme plus général d’anticorps d’immunostimulation. S’il se confirme que leur principal mécanisme d’action est la déplétion des lymphocytes Treg, c’est même un changement de paradigme qui s’opère, et qui ouvre la voie au développement d’anticorps cytotoxiques dirigés contre les lymphocytes Treg, tels que des anticorps anti-CD25 [14] ou des anticorps anti-OX40 (CD134) [15] qui ne sont pas des IPCI, ou des anticorps anti-TIGIT [16] qui le sont.
Anticorps anti-PD-1
Contrairement aux anticorps anti-CTLA-4, les anticorps anti-PD-1 satisfont sans doute mieux à la définition stricte d’IPCI, puisqu’il s’agit réellement d’antagoniser un récepteur inhibiteur exprimé par des lymphocytes effecteurs de l’immunité anticancéreuse. Les modèles murins confirment d’ailleurs qu’une IgG2a anti-PD-1 (déplétante) ne présente pas d’activité antitumorale, au contraire d’une IgG1 murine anti-PD-1, voire d’une IgG1 murine dont les fonctions effectrices ont été totalement abolies [17]. L’emploi de souris humanisées pour les RFcγ a montré que les anticorps anti-PD-1 de sous-classe humaine IgG4 ou IgG1 aglycosylée (mutation N297A supprimant le site de N-glycosylation et abolissant les fonctions effectrices) ont également une bonne activité antitumorale. De fait, avec une belle unanimité, tous les anticorps anti-PD-1 sur le marché sont des IgG4κ (pembrolizumab, nivolumab, cémiplimab, ainsi que toripalimab et sintilimab en Chine), et le seul anticorps anti-PD-1 d’une autre sous-classe (pidilizumab, IgG1κ) n’a jamais dépassé la phase II, probablement du fait d’une réactivité restreinte à certaines glycoformes de PD-1 et d’une réactivité croisée avec DLL-1 (delta-like canonical Notch ligand 1).
Ces cinq IgG4 (pembrolizumab, nivolumab, cémiplimab, toripalimab, sintilimab) ne sont pas pour autant des IgG4 bona fide (IgG4 G4e0), mais des IgG4 ayant fait l’objet d’une ingénierie, à savoir l’introduction d’une mutation ponctuelle S228P dans la région charnière (G4e1, Tableau II et Figure 1 ). Il en va de même d’autres IPCI purement antagonistes, comme le lirilumab qui cible les KIR2DL1/-L2/-L3 des lymphocytes NK. Cette mutation n’affecte pas les propriétés de la région Fc, mais abolit la capacité des IgG4 à former des hémi-IgG et à se réassocier avec d’autres hémi-IgG4 pour former des anticorps bispécifiques (Fab-arm exchange) (Figure 2) [18]. Ce phénomène a été mis en évidence in vivo avec le natalizumab, une IgG4 non mutée (G4e0) anti-intégrine α4 [19]. Dans la mesure où cette mutation G4e1 n’est pas protégée par un brevet [18] et qu’elle est employée de longue date (Tableau II), elle peut être facilement utilisée pour éviter d’éventuels inconvénients dus à ce phénomène de Fab-arm exchange, même si aucun ne lui a été associé jusqu’à présent. Porteuses ou non de la mutation S228P, les IgG4 gardent la propriété de se lier au RFcγI et au RFcγIIIa-158V et ne sont donc pas dénuées de toute propriété cytolytique [20]. Les modèles précliniques suggèrent même que l’on gagnerait en efficacité en abolissant totalement la capacité des IgG4 anti-PD-1 à recruter des cellules RFcγ+ [20]. Le tislélizumab est d’ailleurs une IgG4 anti-PD-1 actuellement en phase III, dont la région Fc a fait l’objet d’une ingénierie complexe renforçant la stabilité de la molécule (double mutation S228P et R409K) et abolissant les fonctions Fc (Fc silencieux, via une quadruple mutation E233P, F234V, L235A et D265A).
 |
Figure 2. Phénomène de Fab-arm exchange, ou de dissociation/réassociation d’hémi-IgG4. Chaque IgG4 a tendance à se dissocier en deux au niveau de la région charnière et de la région Fc conduisant à la formation d’un dimère chaîne lourde (H)/chaîne légère (L), HL. Les deux hémi-IgG qui en résultent peuvent se réassocier avec d’autres hémi-IgG4, formant des anticorps bispécifiques, moins avides et moins susceptibles de former des complexes immuns. Cette propriété est naturelle chez les IgG4, mais le plus souvent, elle n’est pas souhaitable pour un anticorps thérapeutique. |
Système G1e des variants d’IgG1.
Système G4e des variants d’IgG4.
En attendant de connaître les résultats cliniques du tislélizumab, on peut se demander quels inconvénients les actuels anticorps IgG4 G4e1 anti-PD-1 pourraient avoir, en particulier chez les patients homozygotes pour le RFcγIIIa-158V, les plus sensibles aux effets cytotoxiques des anticorps. Il n’y a malheureusement pas de données actuellement disponibles, mais l’hypothèse selon laquelle certains patients hyperprogresseurs sous anti-PD-1 soient de ce génotype mériterait d’être étudiée, car cette situation favoriserait une destruction de leurs lymphocytes T antitumoraux.
Anticorps anti-PD-L1
PD-L1, le principal ligand de PD-1, étant exprimé à la fois sur les cellules tumorales et sur les cellules présentatrices d’antigènes, on peut se demander s’il faut se contenter de l’antagoniser, ou si l’on a intérêt à doubler son activité antagoniste d’une activité cytolytique, directement antitumorale. Les modèles précliniques sont plutôt en faveur de la seconde hypothèse [17]. Traduisant cette incertitude, trois anticorps anti-PD-L1 ayant des chaînes différentes sont sur le marché. Curieusement, toutes sont dérivées de la chaîne γ1, sans aucune ingénierie (G1e0) pour l’avélumab, avec une mutation N297A abolissant le site de N-glycosylation (G1e7) pour l’atézolizumab, et avec une triple mutation L234F/L235E/P331S (G1e8) pour le durvalumab. Les variants G1e7 et G1e8 ont des Fc silencieux, ne recrutant pas les effecteurs de l’immunité. Il serait assez instructif de comparer l’avélumab (IgG1 à Fc compétent) à l’un ou l’autre des deux autres anticorps (IgG1 à Fc silencieux), mais ces données ne sont malheureusement pas disponibles. L’avélumab n’est en effet indiqué que dans le carcinome à cellules de Merkel, où son activité cytotoxique est sans doute essentielle [21], et on ne sait pas s’il est efficace dans les cancers où les deux autres anticorps sont indiqués. Des résultats récents suggèrent aussi qu’un anticorps anti-PD-L1 hypofucosylé (G1e4), dont la liaison de sa région Fc au RFcγIIIa est accrue, est plus efficace in vitro pour activer les lymphocytes T CD8+ cytotoxiques ; il est cependant difficile de prédire si cet avantage se traduira par une plus forte efficacité clinique [22]. Des questionnements similaires vont se poser pour les anticorps ciblant CD47 sur les cellules cancéreuses, anticorps destinés à empêcher la reconnaissance de CD47 par SIRPα et à restaurer la capacité phagocytaire des macrophages. L’anticorps anti-CD47 le plus avancé en clinique, le magrolimab, est une IgG4 G4e1, variant dont les propriétés cytotoxiques ont été discutées plus haut, à propos des anti-PD-1.
Agonistes de récepteurs activateurs des lymphocytes
Utiliser des anticorps agonistes de récepteurs de la famille des récepteurs du TNF-a en cancérologie est une idée ancienne, qui a été tentée pour l’instant sans succès vis-à-vis des récepteurs de mort, notamment les récepteurs de TRAIL (tumor-necrosis-factor-related apoptosis-inducing ligand), DR4 (mapatumumab) et DR5 (lexatumumab, tigatuzumab, conatumumab, drozitumab). Tous étaient des IgG1 pour potentialiser l’effet cytolytique, et certains travaux ont montré que le coengagement des RFcγ était nécessaire à leur effet proapoptotique [23]. Dans un but d’immunostimulation, sont recherchés des anticorps agonistes de récepteurs d’activation leucocytaire, évidemment dénués d’effet cytolytique sur les cellules les exprimant. Plusieurs cibles ont été identifiées, CD40 et 4-1BB (CD137), mais aussi OX40 (CD134), CD27, GITR (CD357, glucocorticoid-induced TNFR family-related gene), etc. L’induction d’un signal agoniste dépend évidemment de l’épitope reconnu sur le récepteur [24], mais aussi de la capacité d’un anticorps par définition divalent à agréger deux molécules de récepteur, et même de la capacité de l’anticorps à coengager des RFcg, non pas pour stimuler des fonctions effectrices mais pour provoquer un niveau supplémentaire d’agrégation (clustering) des récepteurs ciblés et accroître ainsi la force du signal agoniste. Les modèles murins ont notamment mis en avant l’intérêt d’utiliser des IgG1 murines plutôt que des IgG2a, et ont souligné l’importance du RFcg inhibiteur, le RFcγIIb. Malgré tout, la transposition en clinique est loin d’être simple ; aucun anticorps d’immuno-stimulation de type agoniste n’est encore approuvé et aucun n’a d’ailleurs encore atteint la phase III. Dans tous les cas, la plus grande prudence est de mise du fait du risque d’induction de réponses cytokiniques massives lors des perfusions. Ce fut notamment le cas avec le TGN1412, une IgG4 anti-CD28 superagoniste qui a déclenché un orage cytokinique chez des volontaires sains. Cet essai désastreux a néanmoins permis de pousser plus loin les analyses mécanistiques, révélant que l’agrégation de CD28 provoquée par le TGN1412 a sans doute été facilitée par le coengagement du RFcγIIb humain, bien qu’il s’agisse d’une IgG4 [25].
Anticorps anti-CD40
Le sélicrélumab (CP-870,893) fut le premier anticorps anti-CD40 agoniste testé en clinique et a donné quelques résultats encourageants, notamment dans le cancer du pancréas [26]. Cette IgG2 ne relevait pas d’un choix délibéré d’un isotype de chaîne lourde car l’anticorps ne faisait que dériver de souris transgéniques productrices d’IgG2 humaines ; il avait juste été sélectionné pour sa forte activité agoniste. Il est en réalité apparu secondairement que le choix de la sous-classe IgG2 favorisait l’effet agoniste [27]. En effet, la région charnière de l’IgG2 est plus courte que celle des IgG1 et comprend deux cystéines supplémentaires permettant la formation de deux autres ponts disulfures (Figure 1), rendant l’IgG2 très rigide, surtout quand elle adopte l’isoforme IgG2B [27]. Cette rigidité accentue l’agrégation du récepteur et, en conséquence, l’effet agoniste. Dans des modèles de souris transgéniques exprimant CD40 et les RFcγ humains, un variant du sélicrélimab dont la région Fc a une affinité accrue pour le RFcγIIb, mais pas pour le RFcγIIa, a montré un effet antitumoral plus puissant encore, mais au prix d’une toxicité accrue [28]. En effet, l’utilisation du sélicrélumab s’est accompagnée du syndrome de libération de cytokines, ainsi que de toxicités plaquettaires et hépatiques. Hormis l’anticorps CDX-1140, qui est aussi une IgG2, les autres compagnies pharmaceutiques développant des anticorps anti-CD40 agonistes ont fait d’autres choix, notamment celui d’une IgG1 G1e0 non mutée pour le dacétuzumab et le mitazalimab. Quant aux compagnies qui développent des anticorps anti-CD40 antagonistes à visée immunosuppressive, l’une a fait le choix d’une IgG4 G4e1 (blésélumab), une autre celui d’une IgG1 à Fc silencieux et à liaison augmentée au récepteur Fc néonatal, FcRn, pour obtenir un accroissement de demi-vie plasmatique (ravagalimab), et une autre celui d’une IgG1 à Fc silencieux et présentant la mutation ponctuelle S131A (iscalimab), mutation dont on ignore la raison d’être et les conséquences pharmacologiques ! Autant dire qu’il y en a pour tous les goûts, ce qui traduit l’incertitude quant au choix de la meilleure chaîne lourde…
Anticorps anti-4-1BB (CD137)
L’urélumab et l’utomilumab sont deux anticorps agonistes de la molécule activatrice 4-1BB. Ils se distinguent à la fois par leur liaison au 4-1BB [29] et par leur chaîne lourde, ce qui rend difficile leur comparaison. L’urélumab est une IgG4 G4e1 (S228P) purement agoniste (ne bloquant pas la liaison du ligand) tandis que l’utomilumab est une IgG2 agoniste et antagoniste, bloquant la liaison du ligand endogène mais activant néanmoins les cellules exprimant 4-1BB. Lors des essais cliniques, l’urélumab (agoniste fort, IgG4 G4e1) s’est montré nettement plus toxique (toxicité hépatique) que l’utomilumab (agoniste faible, IgG2), qui ne s’est pas révélé très efficace. L’observation ne milite donc pas dans le sens d’IgG2 qui seraient toujours plus agonistes et plus à risque de toxicité ; il y a cependant trop de différences entre les deux produits pour en tirer une conclusion solide. Le LVGN6051 est un nouvel anticorps anti-4-1BB conçu comme un agoniste faible (comme l’utomilumab), mais dont la région Fc a fait l’objet d’une ingénierie pour accroître sa liaison au RFcγIIb, sans que ni l’isotype de chaîne lourde, ni l’ingénierie Fc ne soient divulgués [30]. Pour les autres cibles, comme pour CD40 et 4-1BB, la plus grande perplexité règne sur le choix de l’isotype de chaîne lourde, tel qu’illustré pour les anticorps anti-OX-40 [31].
Conclusion
De toute évidence, le rationnel qui sous-tend le choix des sous-classes d’IgG ou de leurs variants pour les anticorps d’immunomodulation se construit au fur et à mesure des résultats des développements cliniques. Les modèles animaux s’avèrent en effet peu prédictifs des résultats thérapeutiques et des mécanismes d’action chez les patients. S’il est plutôt facile de concevoir un IPCI purement antagoniste, à l’image des anti-PD-1, la situation se complique si ces IPCI ciblent des antigènes exprimés par les cellules tumorales (anti-PD-L1) ou des lymphocytes Treg (anti-CTLA-4), où il peut y avoir intérêt à avoir des anticorps capables de recruter des RFcγ. La situation est encore plus complexe pour les anticorps agonistes, pour lesquels le choix de l’épitope, de la région charnière et de la région Fc vont intervenir, afin de tenter d’obtenir un délicat équilibre entre efficacité et effets indésirables. Pour ces derniers, seul l’avenir nous apprendra quel devait être le meilleur choix !
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Ce travail est soutenu par le Ministère de l’Enseignement Supérieur et de la Recherche, programme « Investissements d’Avenir », LabEx MAbImprove ANR-10-LABX-53-01.
Références
- Watier H.. Biothérapies, immunothérapies, thérapies ciblées, biomédicaments. De quoi faut-il parler ?. Med Sci (Paris) 2014 ; 30: 567–575. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Pottier J, Chastang R, Dumet C, Watier H. Rethinking the INN system for therapeutic antibodies. MAbs 2017 ; 9: 5–11. [CrossRef] [PubMed] [Google Scholar]
- Ribas A.. Anti-CTLA4 antibody clinical trials in melanoma. Update Cancer Ther 2007 ; 2: 133–191. [CrossRef] [PubMed] [Google Scholar]
- Keler T, Halk E, Vitale L, et al. Activity and safety of CTLA-4 blockade combined with vaccines in cynomolgus macaques. J Immunol 2003 ; 171: 6251–6259. [CrossRef] [PubMed] [Google Scholar]
- Selby MJ, Engelhardt JJ, Quigley M, et al. Anti-CTLA-4 antibodies of IgG2a isotype enhance antitumor activity through reduction of intratumoral regulatory T cells. Cancer Immunol Res 2013 ; 1: 32–42. [CrossRef] [PubMed] [Google Scholar]
- Romano E, Kusio-Kobialka M, Foukas PG, et al. Ipilimumab-dependent cell-mediated cytotoxicity of regulatory T cells ex vivo by nonclassical monocytes in melanoma patients. Proc Natl Acad Sci USA 2015 ; 112: 6140–6145. [CrossRef] [Google Scholar]
- Sharma A, Subudhi SK, Blando J, et al. Anti-CTLA-4 immunotherapy does not deplete FOXP3+ regulatory T cells (Tregs) in human cancers. Clin Cancer Res 2019 ; 25: 1233–1238. [CrossRef] [PubMed] [Google Scholar]
- Quezada SA, Peggs KS. Lost in translation: deciphering the mechanism of action of anti-human CTLA-4. Clin Cancer Res 2019 ; 25: 1130–1132. [CrossRef] [PubMed] [Google Scholar]
- Sanseviero E, O’Brien EM, Karras JR, et al. Anti-CTLA-4 activates intratumoral NK cells and combined with IL15/IL15Rα complexes enhances tumor control. Cancer Immunol Res 2019 ; 7: 1371–1380. [CrossRef] [PubMed] [Google Scholar]
- Cartron G, Dacheux L, Salles G, et al. Therapeutic activity of humanized anti-CD20 monoclonal antibody and polymorphism in IgG Fc receptor FcγRIIIa gene. Blood 2002 ; 99: 754–758. [Google Scholar]
- Arce Vargas F, Furness AJS, Litchfield K, et al. Fc effector function contributes to the activity of human anti-CTLA-4 antibodies. Cancer Cell 2018; 33: 649–63. [CrossRef] [PubMed] [Google Scholar]
- Ha D, Tanaka A, Kibayashi T, et al. Differential control of human Treg and effector T cells in tumor immunity by Fc-engineered anti-CTLA-4 antibody. Proc Natl Acad Sci USA 2019 ; 116: 609–618. [CrossRef] [Google Scholar]
- Waight J, Manrique M, Gombos R, et al. Preclinical functional characterization of AGEN1181, a clinical stage Fc-engineered anti-CTLA-4 antibody for the treatment of patients with early and advanced malignancies. J Clin Oncol 2019 ; 37: 15 suppl e14126. [Google Scholar]
- Arce Vargas F, Furness AJS, Solomon I, et al. Fc-optimized anti-CD25 depletes tumor-infiltrating regulatory T cells and synergizes with PD-1 blockade to eradicate established tumors. Immunity 2017; 46: 577–86. [CrossRef] [PubMed] [Google Scholar]
- Bulliard Y, Jolicoeur R, Zhang J, et al. OX40 engagement depletes intratumoral Tregs via activating FcγRs, leading to antitumor efficacy. Immunol Cell Biol 2014 ; 92: 475–480. [CrossRef] [PubMed] [Google Scholar]
- Leroy X, Hoofd C, Cuende J, et al. A-TIGIT antagonist antibody EOS884448 shows dual mechanism of action by restoration of T cell effector functions and preferential depletion of Treg. Cancer Res 2018; 78 (13 suppl): LB–114. [Google Scholar]
- Dahan R, Sega E, Engelhardt J, et al. FcγRs modulate the anti-tumor activity of antibodies targeting the PD-1/PD-L1 axis. Cancer Cell 2015 ; 28: 285–295. [CrossRef] [PubMed] [Google Scholar]
- Dumet C, Pottier J, Gouilleux-Gruart V, Watier H. Insights into the IgG heavy chain engineering patent landscape as applied to IgG4 antibody development. Mabs 2019 (sous presse). [Google Scholar]
- Labrijn AF, Buijsse AO, van den Bremer ET, et al. Therapeutic IgG4 antibodies engage in Fab-arm exchange with endogenous human IgG4 in vivo. Nat Biotechnol 2009 ; 27: 767–771. [CrossRef] [PubMed] [Google Scholar]
- Zhang T, Song X, Xu L, et al. The binding of an anti-PD-1 antibody to FcγRI has a profound impact on its biological functions. Cancer Immunol Immunother 2018 ; 67: 1079–1090. [CrossRef] [PubMed] [Google Scholar]
- Boyerinas B, Jochems C, Fantini M, et al. Antibody-dependent cellular cytotoxicity activity of a novel anti-PD-L1 antibody avelumab (MSB0010718C) on human tumor cells. Cancer Immunol Res 2015 ; 3: 1148–1157. [CrossRef] [PubMed] [Google Scholar]
- Goletz C, Lischke T, Harnack U, et al. Glyco-engineered anti-human programmed death-ligand 1 antibody mediates stronger CD8 T cell activation than its normal glycosylated and non-glycosylated counterparts. Front Immunol 2018 ; 9: 1614. [CrossRef] [PubMed] [Google Scholar]
- Wilson NS, Yang B, Yang A, et al. An Fcγ receptor-dependent mechanism drives antibody-mediated target-receptor signaling in cancer cells. Cancer Cell 2011 ; 19: 101–113. [CrossRef] [PubMed] [Google Scholar]
- Yu X, Chan HTC, Orr CM, et al. Complex interplay between epitope specificity and isotype dictates the biological activity of anti-human CD40 antibodies. Cancer Cell 2018 ; 33: 664–675. [CrossRef] [PubMed] [Google Scholar]
- Bartholomaeus P, Semmler LY, Bukur T, et al. Cell contact–dependent priming and Fc interaction with CD32+ immune cells contribute to the TGN1412-triggered cytokine response. J Immunol 2014 ; 192: 2091–2098. [CrossRef] [PubMed] [Google Scholar]
- Beatty GL, Chiorean EG, Fishman MP, et al. CD40 agonists alter tumor stroma and show efficacy against pancreatic carcinoma in mice and humans. Science 2011 ; 331: 1612–1616. [Google Scholar]
- White AL, Chan HT, French RR, et al. Conformation of the human immunoglobulin G2 hinge imparts superagonistic properties to immunostimulatory anticancer antibodies. Cancer Cell 2015 ; 27: 138–148. [CrossRef] [PubMed] [Google Scholar]
- Dahan R, Barnhart BC, Li F, et al. Therapeutic activity of agonistic, human anti-CD40 monoclonal antibodies requires selective FcγR engagement. Cancer Cell 2016 ; 29: 820–831. [CrossRef] [PubMed] [Google Scholar]
- Chin SM, Kimberlin CR, Roe-Zurz Z, et al. Structure of the 4–1BB/4-1BBL complex and distinct binding and functional properties of utomilumab and urelumab. Nat Commun 2018 ; 9: 4679. [PubMed] [Google Scholar]
- Qi X, Li F, Wu Y, et al. Optimization of 4–1BB antibody for cancer immunotherapy by balancing agonistic strength with FcγR affinity. Nat Commun 2019 ; 10: 2141. [PubMed] [Google Scholar]
- Zhang D, Goldberg MV, Chiu ML. Fc Engineering approaches to enhance the agonism and effector functions of an anti-OX40 antibody. J Biol Chem 2016 ; 291: 27134–27146. [CrossRef] [PubMed] [Google Scholar]
- Pelegrin M, Gros L, Piechaczyk M. Des effets vaccinaux pour les anticorps monoclonaux antiviraux: une nouvelle perspective thérapeutique ?. Med Sci (Paris) 2013 ; 29: 457–460. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1. Différences entre sous-classes d’IgG humaines au niveau de la région charnière. A et B. Structure d’une IgG1 (A) et d’une IgG4 (B), les deux seules sous-classes d’IgG humaines ayant été cristallisées dans leur intégralité. Les chaînes lourdes sont en noir, les chaînes légères en gris ; les N-glycanes de la région Fc sont indiqués en rouge. Les figures ont été réalisées en utilisant PyMOL Molecular Graphics System, version 1.7.4 (Schrödinger) à partir du fichier PDB 1HZH représentant l’unique IgG1 humaine cristallisée, nommée B12 et dirigée contre la gp120 du VIH (virus de l’immunodéficience humaine) et à partir du fichier PDB 5DK3 représentant le pembrolizumab, l’unique IgG4 humaine cristallisée (variant G4e1). La grande flexibilité de la région charnière des IgG1 donne de la liberté aux bras Fab et provoque une forte asymétrie. Il n’existe malheureusement pas de structure d’une IgG2 humaine entière. C. Alignement de la région charnière des chaînes lourdes g 1, g 2 et g 4 humaines. Les acides aminés (selon la numérotation EU) et les nucléotides qui diffèrent de la séquence des IgG1 sont indiqués en rouge. Les cystéines engagées dans des ponts disulfures sont indiquées en gras. Les différences notables apparaissent en fond orangé: délétion de 3 acides aminés dans l’IgG2 et l’IgG4, cystéines 219 et 220 de l’IgG2, et sérine 228 de l’IgG4 (voir texte). |
| Dans le texte | |
 |
Figure 2. Phénomène de Fab-arm exchange, ou de dissociation/réassociation d’hémi-IgG4. Chaque IgG4 a tendance à se dissocier en deux au niveau de la région charnière et de la région Fc conduisant à la formation d’un dimère chaîne lourde (H)/chaîne légère (L), HL. Les deux hémi-IgG qui en résultent peuvent se réassocier avec d’autres hémi-IgG4, formant des anticorps bispécifiques, moins avides et moins susceptibles de former des complexes immuns. Cette propriété est naturelle chez les IgG4, mais le plus souvent, elle n’est pas souhaitable pour un anticorps thérapeutique. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




