| Issue |
Med Sci (Paris)
Volume 28, Number 6-7, Juin–Juillet 2012
|
|
|---|---|---|
| Page(s) | 584 - 587 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2012286010 | |
| Published online | 16 juillet 2012 | |
Protection des vaisseaux sanguins contre l’athérosclérose
Le rôle des miARN sécrétés par l’endothélium
miRNA secreted in vesicles allow atheroprotective communication in vessel wall
1
Centre for Molecular Medicine, Institute of Cardiovascular Regeneration, University of Frankfurt Medical School, 60590 Frankfurt am Main, Allemagne
2
Adresse actuelle : UMR CNRS 5164, université Bordeaux 2, 146, rue Léo Saignat, 33076 Bordeaux, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
L’athérosclérose, maladie fréquente correspondant à la modification pathologique des artères, est la cause de nombreuses maladies telles que l’infarctus du myocarde et les accidents vasculaires cérébraux. Dans les pays développés, ces pathologies associées représentent la première cause de mortalité et constituent un enjeu important de santé publique. L’athérosclérose est un phénomène progressif normal au cours de la vie, mais qui peut devenir pathologique s’il s’accélère ou s’amplifie. En effet, les artères sont le siège de dépôts évoluant avec l’âge au niveau de leur paroi : c’est le vieillissement artériel. Ce processus peut être aggravé par les perturbations du flux sanguin perçues par les cellules endothéliales (CE). Dans les zones de turbulences, en général proches des bifurcations artérielles ou d’une plaque d’athérome, le flux sanguin n’est plus laminaire, il est turbulent, ce qui induit une diminution des forces de cisaillement1. Cette information va être transmise aux cellules musculaires lisses (CML) qui entourent les vaisseaux. Les CML vont alors s’activer, se dédifférencier et proliférer, ce qui accélère et aggrave le phénomène d’athérosclérose naturel [1] (Figure 1). Ces dernières années, le facteur de transcription Krüppel-like factor 2 (KLF2) a été identifié comme un senseur jouant un rôle clé dans les effets bénéfiques athéroprotecteurs du flux laminaire dans les vaisseaux [2]. En l’absence de KLF2 dans les CE, les souris meurent au stade embryonnaire E10,5 ; leur phénotype associe une absence de tonus vasculaire, des hémorragies et des dysfonctionnements cardiaques secondaires à des complications vasculaires [3, 4]. De façon intéressante, l’endothélium de ces souris est normal, ce qui n’est pas le cas des CML, dysfonctionnelles et désorganisées. Cette observation indique que l’expression endothéliale de KLF2 exerce un rôle physiologique important sur la couche sous-jacente de CML [5]. Nous nous sommes donc intéressés au mécanisme de cette communication entre les CE et les CML conduisant à l’effet athéroprotecteur relayé par KLF2 [6] (Figure 1).
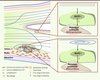 |
Figure 1. Effet du flux dans la mise en place de la plaque d’athérome. Cadre supérieur : le flux laminaire induit l’expression de KLF2 dans les cellules endothéliales (CE). KLF2 est responsable du maintien du phénotype contractile et athéroprotecteur des cellules musculaires lisses (CML) sous-jacentes. Cadre inférieur : lorsque le flux est turbulent, aux abords d’une bifurcation ou d’une plaque d’athérome, l’expression de KLF2 dans les CE diminue et les CML sous-jacentes adoptent un phénotype prolifératif proathérosclérotique. La communication entre les CE et les CML via KLF2 fait l’objet de cette étude. |
Les miARN : un nouveau niveau de régulation de l’expression génique
Des médiateurs de choix de cette communication entre CE et CML seraient les microARN (miARN). Les miARN sont de petits ARN non codants simple brin (22 nucléotides) qui sont transcrits dans le noyau, clivés - notamment par les enzymes Drosha et Dicer -, et incorporés dans un complexe de silencing qui conduit à l’inhibition de la traduction ou à la dégradation des ARNm cibles [7, 17]. Ces molécules sont déjà connues pour leur rôle important dans la vascularisation ainsi que dans différentes pathologies vasculaires [8]. Notre objectif a été de déterminer si KLF2 pouvait réguler l’expression de miARN dans les CE et contribuer à ces effets vasculoprotecteurs.
Les forces de cisaillement régulent l’expression de miARN dans les CE via KLF2
Nous avons tout d’abord déterminé les miARN régulés par KLF2 et par les forces de cisaillement dans les CE. Cette double analyse a permis d’identifier de nouvelles cibles de KLF2 en réponse au flux : le cluster miR-143/145. Nous avons validé ces miARN candidats par l’invalidation de KLF2 in vitro, et nous avons montré qu’en absence de KLF2, ce cluster n’est plus induit par les forces de cisaillement. De plus, KLF2 est capable de se lier au promoteur de ce cluster et d’induire son expression. Les forces de cisaillement induisent donc l’expression de KLF2 dans les CE, et celui-ci, à son tour, induit l’expression de miR-143/145. Ce cluster était jusque là connu pour son action athéroprotectrice au niveau des CML [9].
miARN et communication intercellulaire : entre CE et CML
Nous avons cherché à vérifier si KLF2 pouvait contrôler les CML de façon paracrine via miR-143/145. De récentes études ont mis en évidence la présence de miARN extracellulaires dans les différents fluides de l’organisme [10], miARN circulants qui constituent de véritables traceurs biologiques dans différentes pathologies comme le cancer [11, 18] ou les maladies cardiovasculaires [12]. La fonction biologique des miARN circulants n’est pas encore complètement élucidée, mais il semble qu’ils puissent jouer un rôle dans la communication intercellulaire [13].
Le sang contient de nombreuses ribonucléases et les miARN circulants seraient protégés de la dégradation par des protéines de liaison ou par leur incorporation dans des vésicules [15, 16], ce dernier mécanisme étant privilégié (Figure 2A).
 |
Figure 2. Analyse de la communication intercellulaire. A. Analyse biochimique de la protection des miARN extracellulaires. L’échantillon est traité à la protéinase K ou au détergent pour dégrader les protéines ou les membranes lipidiques, puis les ARN sont dégradés par traitement à la RNase. S’ils sont dégradés, cela indique qu’ils étaient accessibles et révèle le type de protection, protéique ou membranaire. B. Système de coculture permettant d’étudier le transfert de matériel entre les CE et les CML. PBS : phosphate buffer saline. |
Nous avons analysé le surnageant de CE surexprimant KLF2 ou soumises à des contraintes de cisaillement. En utilisant la technique décrite dans la Figure 2 , nous avons pu montrer que ces miARN étaient présents dans le milieu extracellulaire et sont protégés dans une vésicule (Figure 2A). Différents types de vésicules ont été identifiés et classés en fonction de leur taille et de leur mécanisme de formation. Des analyses approfondies (notamment en microscopie électronique) nous ont permis de déterminer que les vésicules contenant miR-143/145 seraient de type microvésicules et/ou exosomes (MV).
Pour vérifier que les CML sont bien capables d’utiliser le contenu des vésicules émises par les CE, nous avons réalisé des cocultures entre des cellules endothéliales exprimant l’eGFP (green fluorescent protein) ou transfectées avec un miARN de C. elegans (cel-miR-39) et des CML sous-jacentes (Figure 2B). L’analyse par immunofluorescence des CML a montré la présence d’eGFP, et l’analyse RT-qPCR a révélé la présence des ARNm codant l’eGFP, démontrant que les CE ont transmis les vésicules d’ARNm aux CML. Par analyse RT-qPCR, nous avons également pu détecter la présence de cel-miR-39 dans les MV ; celles-ci sont transmises également aux CML cocultivées avec les CE transfectées par cel-miR-39. Les MV produites par les CE transportent des ARNm et des miARN et peuvent être incorporées par les CML.
Les miARN contenus dans les MV endothéliales ont un effet athéroprotecteur sur les CML
miR-143/145 étant exprimé par les deux types cellulaires, nous avons ensuite cherché à vérifier si l’apport de ces miARN par les CE agissait sur le phénotype des CML. Nous avons donc inhibé la production endogène de miARN dans les CML en inhibant Drosha (CML KO). Quand ces CML n’exprimant pas de miARN endogènes sont cultivées en présence de CE surexprimant KLF2, on y détecte une augmentation des miR-143/145. Ceci indique que miR-143/145 a été transporté des CE aux CML. Et nous avons montré que ces miARN captés par les CML KO y entraînent une réduction des cibles proathérosclérotiques, telles que ELK1 (E twenty-six like transcription factor I), KLF4 et SSH2 (slingshot-I protein phosphatase) ; les miARN endothéliaux miR-143/145 transmis aux CML sont donc responsables des effets athéroprotecteurs observés au niveau des CML (Figure 3).
 |
Figure 3. Communication entre CE et CML vasculaires. Le flux laminaire induit l’expression de KLF2 dans les CE. KLF2 va induire la transcription des miR-143/145 qui seront transmis aux CML dans des mirovésicules. Dans les CML, miR-143/145 réprime l’expression de ELK1 et KLF4 et inhibe la prolifération, permettant un switch vers le phénotype contractile, athéroprotecteur. |
Nous avons vérifié in vivo l’effet athéroprotecteur de ces MV enrichies en miR-143/145 (produites par des CE surexprimant KLF2). Pour cela, les MV ont été injectées à des souris ayant des prédispositions à développer un processus d’athérosclérose (souris ApoE -/- ) lorsqu’elles sont nourries avec un régime gras, et nous avons quantifié les lésions artérielles. Les souris traitées présentent moins de lésions que les souris contrôles. De plus, l’inhibition de la production des miARN abroge l’effet bénéfique des MV observé in vivo.
Applications thérapeutiques
Ces travaux ont permis de mettre en évidence une communication entre les CE et les CML via les miARN circulants. En réponse au flux sanguin, l’activation de KLF2 permet la production des miR-143/145 qui sont transmis aux CML via des MV. Ces miARN dans les CML vont inhiber l’expression de facteurs proathérogéniques (Figure 3).
Ces résultats encourageants pourraient susciter des applications thérapeutiques intéressantes. Il pourrait être possible, grâce aux MV, de réduire le développement des plaques d’athérome chez les personnes à risque, notamment les personnes obèses. Cette stratégie pourrait s’appliquer à d’autres pathologies où l’expression des miARN est dérégulée (cancer, maladies cardiovasculaires), car les MV constituent un moyen de ciblage des traitements par miARN. Comme nous l’avons montré pour l’athérosclérose, l’administration des miARN via les MV pourrait se faire par voie intraveineuse. Les MV seraient produites in vitro à partir des cellules du patient lui même, réduisant ainsi le risque d’effets secondaires. Le choix du type cellulaire donneur permettrait d’adresser spécifiquement les miARN aux cellules cibles à traiter. De plus, les cellules productrices issues du patient peuvent être manipulées afin de modifier le contenu des MV qui seront délivrées aux cellules ciblées.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Les forces de cisaillement, ou contraintes de cisaillement, sont les forces de friction exercées par le sang sur la paroi du vaisseau. Elles dépendent du débit sanguin, de la viscosité du sang et du diamètre du vaisseau. En l’absence d’obstacle ou de bifurcation, le flux est laminaire et les forces de cisaillement sont maximales.
Références
- Malek AM, Alper SL, Izumo S. Hemodynamic shear stress and its role in atherosclerosis. JAMA 1999 ; 282 : 2035–2042. [Google Scholar]
- Boon RA, Horrevoets AJ. Key transcriptional regulators of the vasoprotective effects of shear stress. Hamostaseologie 2009 ; 29 : 39–40. [PubMed] [Google Scholar]
- Kuo CT, Veselits ML, Barton KP, et al. The LKLF transcription factor is required for normal tunica media formation and blood vessel stabilization during murine embryogenesis. Genes Dev 1997 ; 11 : 2996–3006. [CrossRef] [PubMed] [Google Scholar]
- Lee JS, Yu Q, Shin JT, et al. Klf2 is an essential regulator of vascular hemodynamic forces in vivo. Dev Cell 2006 ; 11 : 845–857. [CrossRef] [PubMed] [Google Scholar]
- Wu J, Bohanan CS, Neumann JC, Lingrel JB. KLF2 transcription factor modulates blood vessel maturation through smooth muscle cell migration. J Biol Chem 2008 ; 283 : 3942–3950. [CrossRef] [PubMed] [Google Scholar]
- Hergenreider E, Heydt S, Treguer K, et al. Atheroprotective communication between endothelial cells and smooth muscle cells through miRNAs. Nat Cell Biol 2012 ; 14 : 249–256. [CrossRef] [PubMed] [Google Scholar]
- Bartel DP. MicroRNAs: target recognition and regulatory functions. Cell 2009 ; 136 : 215–233. [CrossRef] [PubMed] [Google Scholar]
- Bonauer A, Boon RA, Dimmeler S. Vascular microRNAs. Curr Drug Targets 2010 ; 11 : 943–949. [CrossRef] [PubMed] [Google Scholar]
- Rangrez AY, Massy ZA, Metzinger-Le Meuth V, Metzinger L. miR-143 and miR-145: molecular keys to switch the phenotype of vascular smooth muscle cells. Circ Cardiovasc Genet 2011 ; 4 : 197–205. [CrossRef] [PubMed] [Google Scholar]
- Weber JA, Baxter DH, Zhang S, et al. The microRNA spectrum in 12 body fluids. Clin Chem 2010 ; 56 : 1733–1741. [CrossRef] [PubMed] [Google Scholar]
- Schwarzenbach H, Hoon DS, Pantel K. Cell-free nucleic acids as biomarkers in cancer patients. Nat Rev Cancer 2011 ; 11 : 426–437. [CrossRef] [PubMed] [Google Scholar]
- Fichtlscherer S, Zeiher AM, Dimmeler S. Circulating microRNAs: biomarkers or mediators of cardiovascular diseases? Arterioscler Thromb Vasc Biol 2011 ; 31 : 2383–2390. [CrossRef] [PubMed] [Google Scholar]
- Creemers EE, Tijsen AJ, Pinto YM. Circulating microRNAs: novel biomarkers and extracellular communicators in cardiovascular disease? Circ Res 2012 ; 110 : 483–495. [CrossRef] [PubMed] [Google Scholar]
- Weickmann JL, Glitz DG. Human ribonucleases. Quantitation of pancreatic-like enzymes in serum, urine, and organ preparations. J Biol Chem 1982 ; 257 : 8705–8710. [PubMed] [Google Scholar]
- Wang K, Zhang S, Weber J, et al. Export of microRNAs and microRNA-protective protein by mammalian cells. Nucleic Acids Res 2010 ; 38 : 7248–7259. [CrossRef] [PubMed] [Google Scholar]
- Arroyo JD, Chevillet JR, Kroh EM, et al. Argonaute2 complexes carry a population of circulating microRNAs independent of vesicles in human plasma. Proc Natl Acad Sci USA 2011 ; 108 : 5003–5008. [CrossRef] [Google Scholar]
- Dunoyer Patrice. La bataille du silence : mécanisme et inhibition du RNA silencing au cours des interactions plante/virus. Med Sci (Paris) 25 : 5 505–512. [Google Scholar]
- Ladeiro Y, Zucman-Rossi J. Micro-ARN (miARN) et cancer : le cas des tumeurs hépatocellulaires. Med Sci (Paris) 25 : 5 467–472. [Google Scholar]
© 2011 médecine/sciences – Inserm / SRMS
Liste des figures
 |
Figure 1. Effet du flux dans la mise en place de la plaque d’athérome. Cadre supérieur : le flux laminaire induit l’expression de KLF2 dans les cellules endothéliales (CE). KLF2 est responsable du maintien du phénotype contractile et athéroprotecteur des cellules musculaires lisses (CML) sous-jacentes. Cadre inférieur : lorsque le flux est turbulent, aux abords d’une bifurcation ou d’une plaque d’athérome, l’expression de KLF2 dans les CE diminue et les CML sous-jacentes adoptent un phénotype prolifératif proathérosclérotique. La communication entre les CE et les CML via KLF2 fait l’objet de cette étude. |
| Dans le texte | |
 |
Figure 2. Analyse de la communication intercellulaire. A. Analyse biochimique de la protection des miARN extracellulaires. L’échantillon est traité à la protéinase K ou au détergent pour dégrader les protéines ou les membranes lipidiques, puis les ARN sont dégradés par traitement à la RNase. S’ils sont dégradés, cela indique qu’ils étaient accessibles et révèle le type de protection, protéique ou membranaire. B. Système de coculture permettant d’étudier le transfert de matériel entre les CE et les CML. PBS : phosphate buffer saline. |
| Dans le texte | |
 |
Figure 3. Communication entre CE et CML vasculaires. Le flux laminaire induit l’expression de KLF2 dans les CE. KLF2 va induire la transcription des miR-143/145 qui seront transmis aux CML dans des mirovésicules. Dans les CML, miR-143/145 réprime l’expression de ELK1 et KLF4 et inhibe la prolifération, permettant un switch vers le phénotype contractile, athéroprotecteur. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




