| Issue |
Med Sci (Paris)
Volume 26, Number 11, Novembre 2010
|
|
|---|---|---|
| Page(s) | 936 - 942 | |
| Section | Resistance aux antibiotiques : un enjeu international | |
| DOI | https://doi.org/10.1051/medsci/20102611936 | |
| Published online | 15 novembre 2010 | |
Les entérocoques résistants aux glycopeptides
Enterococci resistant to glycopeptides
Centre national de référence de la résistance aux antibiotiques, Laboratoire associé entérocoques, service de microbiologie, CHU de Caen, avenue Côte de Nacre, 14033 Caen, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Enterococcus faecium a développé une multirésistance aux antibiotiques dont les glycopeptides. Les glycopeptides (vancomycine et teicoplanine) agissent sur les entérocoques en se fixant sur les précurseurs de la paroi bactérienne dont ils empêchent ainsi la formation. La résistance est due à l’acquisition d’un opéron de gènes coopérant pour synthétiser des précurseurs sans affinité pour les glycopeptides. Des épidémies sont survenues récemment en milieu hospitalier dues à des souches de E. faecium appartenant à un complexe clonal (CC17) adapté à l’hôpital. Les épidémies peuvent être contrôlées par des mesures appropriées et de nouveaux antibiotiques qui sont disponibles. La dissémination de souches adaptées aux conditions hospitalières nécessite leur surveillance étroite.
Abstract
Enterococci are responsible for various community- and hospital-acquired infections. Glycopeptides (vancomycin and teicoplanin) are active against these microorganisms by inhibiting cell wall synthesis through binding to cell wall precursors. Enterococcus faecium has developed multidrug resistance, including resistance to glycopeptides. Resistance to glycopeptides is due to the acquisition of an operon of genes cooperating to synthesize precursors devoid of affinity for the glycopeptides. Outbreaks were recently reported in hospital settings. These outbreaks were due to E. faecium isolates belonging to an hospital-adapted clonal complex (CC17) characterized by high level resistance to ampicillin and fluoroquinolones and frequently containing virulence factors. Outbreaks may be controlled by appropriate measures and new antibiotics are available in therapy. However, spreading of clonal strains adapted to hospitals require close surveillance.
© 2010 médecine/sciences - Inserm / SRMS
Les entérocoques sont responsables d’infections humaines, principalement dues à Enterococcus faecalis (80 % à 90 % des cas) et à Enterococcus faecium (5 à 10 % des cas) tandis que les autres espèces occasionnellement retrouvées sont Enterococcus gallinarum, Enterococcus casseliflavus, Enterococcus durans, Enterococcus avium et Enterococcus hirae [1]. En 2006, les entérocoques représentaient 6,4 % des micro-organismes isolés au cours d’infections nosocomiales en France et étaient classés au 5e rang après Escherichia coli, Staphylococcus aureus, Pseudomonas aeruginosa et les staphylocoques à coagulase négative [2]. Les infections urinaires sont les plus fréquentes alors que des infections sévères ne sont pas rares, à type de bactériémies, endocardites ou infections intra-abdominales [1].
Alors que les entérocoques sont des bactéries considérées comme peu virulentes, leur multirésistance aux antibiotiques représente le principal problème en pratique clinique ; c’est particulièrement vrai lors des infections dues à E. faecium, souvent résistant à toutes les β-lactamines [3]. La famille des glycopeptides (vancomycine, teicoplanine) constitue une option thérapeutique de choix pour le traitement des infections dues à ces germes. Les entérocoques sont naturellement sensibles à la vancomycine (CMI1 modale de 1 mg/l) et à la teicoplanine (CMI modale de 0,5 mg/l), si on excepte les deux espèces naturellement résistantes à la vancomycine, E. gallinarum et E. casseliflavus [4]. Les premières souches d’entérocoques résistantes aux glycopeptides (ERG) ont été décrites à la fin des années 1980 en France et en Angleterre. Depuis, ces souches ont largement diffusé, notamment aux États-Unis où elles représentent un important problème de santé publique [5].
Mode d’action des glycopeptides
Comme les β-lactamines et la fosfomycine, les glycopeptides sont des inhibiteurs de la synthèse de la paroi bactérienne, plus précisément du constituant majeur de celle-ci, le polymère peptidoglycane (Figure 1) [6, 7]. Le mode d’action de ces antibiotiques repose sur leur forte affinité pour l’extrémité des précurseurs monomériques de la paroi se terminant par un dipeptide D-alanyl-D-alanine à laquelle ils se fixent par l’intermédiaire de cinq liaisons hydrogène (Figure 2) [8]. Les glycopeptides s’y fixent au niveau de la face externe de la membrane cytoplasmique (Figure 1) [6, 7]. Sans pénétrer dans le cytoplasme, ils empêchent ainsi, par encombrement stérique (du fait de leur masse moléculaire élevée d’environ 1 500 Da), les étapes enzymatiques (transglycosylation et transpeptidation) au cours de l’assemblage du peptidoglycane naissant (Figure 1) [6, 7].
 |
Figure 1 Représentation schématique de la biosynthése du peptidoglycane et du mode dșaction desglycopeptides. La synthèse du peptioglycane s’effectue en trois étapes : (1) une étape intra-cytoplasmique (C) avec formation UDP-N-acétyl-muramoyl-pen ta peptide à partir d’UDP-N-acétyl-muramoyl-tripeptide et d’un dipeptide D-Ala-D-Ala ; (2) la translocation via un transporteur lipidique des précurseurs pentapeptidiques (lipide I/lipide II) de la surface interne vers la surface externe de la membrane cytoplasmique (M) ; (3) l’incorporation de ces précurseurs au peptidoglycane issant par transglycosylation et la formation ponts interpeptidiques par transpeptidation au niveau de la paroi (P). La fixation de lșantibiotique au niveau de l’extrémité D-Ala-D-Ala des précurseurs pentapeptidiques inhibe les étapes finales de transglycosylation et de inspeptidation (d’après [6, 7]). |
Mécanismes de résistance aux glycopeptides
La résistance aux glycopeptides est due à la production de précurseurs de la paroi modifiés (terminés par D-alanyl-D-lactate ou D-alanyl-D-sérine) et à l’élimination des précurseurs naturels de haute affinité (terminés par D-Ala-D-Ala) [9]. Cette modification de cible résulte de la coopération de plusieurs gènes organisés en opéron codant pour l’ensemble des enzymes nécessaires à la reprogrammation du peptidoglycane [9, 10]. Le changement porte sur l’extrémité du précurseur et fait disparaître une liaison hydrogène essentielle. Ainsi l’affinité de la vancomycine pour les précurseurs terminés par D-Ala-D-Lac devientelle mille fois moins élevée que celle pour les précurseurs sauvages (terminés en D-Ala-D-Ala) (Figure 2) [8].
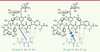 |
Figure 2 Liaison entre la vancomycine et les différentes formes de dipeptide terminal des précurseurs pentapeptidiques. Cinq liaisons hydrogène sont impliquées avec le dipeptide D-Ala-D-Ala, alors que seulement quatre le sont avec le dipeptide D-Ala-D-Lac (d’après [8]). |
Neuf types de résistance aux glycopeptides ont été décrits à ce jour, sur des critères phénotypiques et génotypiques (Tableau I) [6, 11, 12] . Huit correspondent à un mécanisme de résistance acquise (VanA, VanB, VanD, VanE, VanG, VanL, VanM et VanN) tandis qu’un seul est une caractéristique intrinsèque d’espèce (VanC chez E. gallinarum et E. casseliflavus) [3, 9]. Les types VanA et VanB sont les phénotypes les plus fréquemment retrouvés chez les entérocoques (surtout E. faecium) alors que seul VanA a diffusé chez une dizaine de souches de S. aureus rapportées aux États-Unis [9]. Les souches VanA sont hautement résistantes à la vancomycine et à la teicoplanine de façon inductible alors que les souches VanB présentent des niveaux variables de résistance uniquement à la vancomycine, seule inductrice [9].
L’opéron vanA est classiquement porté par un transposon (élément génétique mobile) de type Tn3 (Tn1546) et comprend cinq gènes impliqués dans la résistance aux glycopeptides (vanHAXYZ) et deux gènes de régulation (vanRS) (Figure 3) [10]. Le gène vanH code pour une déshydrogénase qui réduit le pyruvate en D-Lac et fournit un substrat pour la ligase codée par le gène vanA qui catalyse la formation d’un depsipeptide2 D-Ala-D-Lac. Après diverses étapes, ce depsipeptide est finalement incorporé au peptidoglycane en cours d’élongation. Cependant, la résistance ne peut s’exprimer puisque la synthèse bactérienne de précurseurs sauvages persiste et qu’il suffit qu’un petit nombre gagne la surface de la bactérie pour que la vancomycine s’y fixe et interrompe la synthèse de la paroi. L’élimination de ces précurseurs « sensibles » est la tâche du gène vanX qui code pour une D,D-dipeptidase, qui hydrolyse le dipeptide D-Ala-D-Ala formé par la ligase naturelle Ddl, et du gène vanY qui code pour une D,D-carboxypeptidase qui élimine le D-Ala terminal des précurseurs en cas d’élimination incomplète du D-Ala-D-Ala par vanX. Enfin, l’expression de l’opéron vanA est contrôlée par un système de régulation à deux composants, un activateur transcriptionnel et un capteur histidine-kinase, codés respectivement par les gènes vanR et vanS [10].
 |
Figure 3 Résistance de type VanA. Haut : organisation de l’opéron vanA (les flèches indiquent les gènes et la direction de la transcription). Bas : représentation schématique de la synthèse des Précurseurs du peptidoglycane après induction par un glycopeptide. Preg, promoteur des gènes de régulation ; Pres, promoteur des gènes de résistance (d’après [6]). |
Notons qu’il existe des souches résistantes (VanA ou VanB) qui sont dites dépendantes à la vancomycine ou à la teicoplanine (« toxicomanes ») car elles requièrent la présence de l’antibiotique pour leur croissance. Ceci est lié à la présence de mutations dans le gène ddl rendant la ligase naturelle non fonctionnelle. Ces souches dépendent donc entièrement de l’opéron de résistance exprimé après induction pour la synthèse de peptidoglycane [6, 10].
Situation épidémiologique
Comparaison Europe-États-Unis
La fréquence des ERG s’est rapidement accrue aux États-Unis après leur première description en 1990 à New York, alors que leur présence en Europe a été rapportée plus tardivement [13]. Ces souches sont devenues endémo-épidémiques dans les hôpitaux nord-américains avec une proportion de souches résistantes à la vancomycine qui atteint 28 % en 2003 et une place au 3e rang des bactéries multirésistantes dans les unités de soins intensifs [13]. Ces souches ne sont pas restées confinées aux seules unités de soins intensifs et la proportion de souches résistantes est devenue similaire dans les autres unités de soins depuis quelques années.
L’incapacité des équipes américaines à contrôler les épidémies a été attribuée à la diffusion trop tardive des recommandations et à leur application hétérogène selon les établissements, bien que les mesures soient efficaces quand elles sont appliquées [14].
Portage communautaire d’entérocoques résistants aux glycopeptides en Europe
En France et dans divers pays européens, sauf au Royaume-Uni qui connaissait quelques problèmes épidémiques, la proportion de résistance à la vancomycine parmi les entérocoques isolés d’hémocultures est restée stable jusqu’en 2003 à moins de 2 % [15] avec de rares épidémies de diffusion limitée. En contraste avec la situation en milieu hospitalier, plusieurs études européennes ont retrouvé dans les années 1990 une prévalence de portage fécal communautaire des ERG surprenante, allant jusqu’à 28 % en Belgique [16]. En France, 2 % des patients hospitalisés en service de réanimation (essentiellement des entrants) étaient porteurs d’ERG dans leurs selles [17] ; ce portage était de 9 % dans une population de sujets jeunes et en bonne santé [18].
Ce portage communautaire a été relié à l’utilisation en Europe d’un glycopeptide apparenté à la teicoplanine, l’avoparcine, comme additif alimentaire (facteur de croissance) chez les animaux de rente, essentiellement porcs et volailles [29] (→). Voir l’article de Les ERG seraient sélectionnés chez les animaux et transmis à l’homme via la chaîne alimentaire. Ces souches animales ne se sont pas disséminées dans les hôpitaux malgré leur introduction répétée à l’occasion d’admissions de patients porteurs dans ce milieu propice aux épidémies.
(→) Voir l’article de Pascal Sa nders, page 930 de ce numéro
L’utilisation de l’avoparcine en Europe a été proscrite en 1997. En 1999, une étude de l’ANSES (Agence nationale de sécurité sanitaire) réalisée sur des échantillons de caeca de poulets français retrouvait que 5,4 % des isolats de E. faecium étaient résistants à la vancomycine et multirésistants à d’autres antibiotiques [19]. Cette étude a été répétée en 2000, 2001 et 2002, et la proportion de souches résistantes observée était respectivement de 5,6 et 0 %. Le portage humain en communauté n’a pas été réévalué récemment. Cependant, une étude de l’Observatoire national de la résistance aux antibiotiques (ONERBA) réalisée en juin 2006 a permis d’étudier la fréquence de portage digestif d’ERG chez les patients hospitalisés en réanimation et en onco-hématologie et chez ceux présentant des diarrhées suspectées d’être causées par Clostridium difficile [20]. Un total de 76 laboratoires d’hôpitaux, dont la plupart n’avaient pas d’épidémie à ERG, ont reçu des écouvillons rectaux de 4 263 patients dont 0,32 % étaient porteurs d’ERG, dont 9 E. faecium vanA, 3 E. faecium vanB, et un E. hirae vanB. La fréquence du portage est donc considérée actuellement comme faible en dehors d’un contexte épidémique.
L’avoparcine n’a jamais été utilisée aux États-Unis, contrairement à sa diffusion en Europe, et le portage communautaire y est rare.
Changements récents d’épidémiologie en Europe et en France
Malgré la situation initialement rassurante, des changements dans la prévalence des ERG ont été rapportés récemment en Europe (Figure 4) [21]. En 2005, la Grèce et le Portugal rapportent un taux de résistance aux glycopeptides chez les E. faecium isolés d’hémoculture avoisinant 40 %, et l’Allemagne un taux de plus de 10 %, ce qui témoigne d’une évolution de la situation.
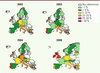 |
Figure 4 Évolution de la proportion de cas de résistance à la vancomycine. Résistance chez les E. faecium isolés d’hémocultures en Europe de 2002 à 2008 [21]. |
En France, les premiers signaux d’alerte ont été les déclarations de cas groupés à l’Institut de veille sanitaire (InVS) dont le nombre a augmenté brutalement depuis 2004 (Figure 5). De plus, des épidémies hospitalières d’ampleur inhabituelle dans trois groupes hospitaliers éloignés géographiquement ont été rapportées en 2004-2005. Entre 62 et 144 patients ont été touchés dans ces établissements sur un total de plus de 400 patients. Ces épidémies sont considérées comme étant contrôlées actuellement [22, 23]. La diffusion des souches par les filières de soins lors de transferts de patients colonisés a joué un rôle important dans l’ampleur des épidémies et les difficultés à les contrôler. Les signalements de cas à ERG, soit nouveaux dans des hôpitaux qui n’en avaient jamais eus, soit épidémiques, se sont multipliés depuis (Figure 5). Parmi les 902 ERG isolés de 2006 à 2008 et reçus au Centre national de référence, 94,8 % étaient des E. faecium et 4,6 % des E. faecalis. Les deux tiers des E. faecium contenaient les gènes vanA (66,7 %) alors que 33,1 % et 0,3 % contenaient respectivement les gènes vanB et vanD. L’analyse des souches par électrophorèse en champ pulsé a montré que, pour un hôpital, un ou plusieurs clones majeurs et quelques clones minoritaires étaient associés à l’épidémie. Les clones majoritaires peuvent diffuser dans les établissements proches mais ils sont différents entre hôpitaux éloignés, hormis de rares exceptions.
 |
Figure 5 Signalement à l’Institut de veille sanitaire (InVS) des cas d’infections/colonisations à entérocoques résistants aux glycopeptides et nombre de souches reçues au CNR et résistantes aux antibiotiques (Laboratoire associé entérocoques) de 2001 à 2008 [Roland Leclercq]. Le nombre de cas signalés annuellement est indiqué par les barres jaunes et le nombre de souches reçues ar les barres violettes. |
Suite aux épidémies de 2004-2005, diverses recommandations ont été émises (voir la fiche opérationnelle3 diffusée par la Direction de l’hospitalisation et de l’organisation des soins du 6 décembre 2006). L’application de ces recommandations a permis le contrôle plus ou moins rapide des épidémies à chaque fois qu’elles étaient signalées. Globalement, de plus en plus d’établissements rapportent des isolements d’ERG, mais les épidémies sont contrôlées plus rapidement et la situation en 2009 n’est pas celle d’une endémo-épidémie « à l’américaine » comme on pouvait le craindre. Les chiffres de résistance à la vancomycine chez les E. faecium isolés d’hémoculture restent très bas pour la France (moins de 2 % en 2008) [21].
Pourquoi l’épidémiologie a-t-elle changé ?
En utilisant diverses méthodes de typage, en particulier des techniques de séquençage comme le Multilocus Sequence Typing (MLST), il est apparu qu’un groupe de clones de E. faecium isolés en milieu hospitalier pouvait être identifié et distingué des clones isolés chez les animaux et les humains porteurs sains en communauté [5, 24]. Ce groupe de clones appelé clonal complex 17 (CC17) est caractérisé par des marqueurs comme la résistance de haut niveau à l’ampicilline, la présence (non constante) des gènes de virulence esp et hly et la résistance aux fluoroquinolones [5]. Les souches CC17 se sont adaptées à l’hôpital depuis plusieurs années mais n’étaient pas initialement résistantes à la vancomycine. i est proposé est celui de la dissémination de souches de E. faecium CC17 adaptées à l’hôpital qui n’ont acquis que récemment des plasmides de résistance à la vancomycine. L’acquisition de ces plasmides par les souches CC17 serait due à leur transfert horizontal à partir des souches communautaires ERG introduites à l’hôpital lors de l’admission de patients porteurs, mais cette hypothèse reste à confirmer.
Il semble donc que l’on soit confronté à une situation nouvelle caractérisée par la présence de souches d’ERG adaptées à l’hôpital qui sont par définition plus difficiles à éradiquer.
Traitement des infections à ERG
Le traitement habituel des infections à entérocoques repose soit sur l’ampicilline (ou l’amoxicilline), soit sur la vancomycine associée à la gentamicine dans les infections sévères. Ces antibiotiques ne sont pas utilisables en présence de E. faecium résistants aux glycopeptides car ils sont presque toujours résistants à l’ampicilline. Face à cette impasse thérapeutique, le développement d’antibiotiques nouveaux a permis d’apporter quelques solutions.
Le premier antibiotique développé a été la quinupristine-dalfopristine, une streptogramine injectable, dérivée de la pristinamycine [25]. La nécessité d’une administration de cet antibiotique par cathéter central, l’apparition de résistance chez E. faecium (environ 10 %) et la résistance naturelle, constante, de E. faecalis en ont limité l’usage.
Le linézolide, seul représentant d’une nouvelle famille, les oxazolidinones, administrable en intra veineux ou per os, est actif contre les ERG (CMI modale 1 mg/l) quelle que soit l’espèce, et a été utilisé dans cette indication [25]. Alors que la fréquence de l’utilisation de cet antibiotique allait croissant, quelques souches d’ERG résistantes au linézolide, parfois épidémiques, ont été rapportées, notamment aux États- Unis [26]. La résistance est due à des mutations ribosomiques au niveau du site de fixation de l’oxazolidinone.
La tigécycline est une glycylcycline qui a l’intérêt par rapport aux tétracyclines classiques d’être active contre les souches résistantes à ces dernières [25]. Les souches cliniques résistantes sont exceptionnelles. Cependant, l’expérience clinique avec la tigécycline dans le traitement des infections à ERG est très limitée.
Ces trois antibiotiques récemment développés sont bactériostatiques contre les entérocoques. Seule la daptomycine, un nouveau lipopeptide cyclique administrable par voie intraveineuse, se montre bactéricide. Cependant, cet antibiotique a surtout été développé contre les staphylocoques et l’expérience clinique, insuffisante dans les infections à entérocoques, ne permet pas son utilisation dans le cadre de l’autorisation de mise sur le marché.
Au total, si plusieurs antibiotiques sont maintenant disponibles, l’efficacité de la plupart d’entre eux dans les infections à ERG reste à valider.
Conclusion
Pour les entérocoques, comme pour d’autres bactéries, la multirésistance aux antibiotiques complique la prise en charge des patients infectés [27, 28]. L’épidémiologie des ERG a récemment changé en France et en Europe avec la survenue d’épidémies hospitalières. Cependant, l’histoire récente nous montre que si les épidémies sont décelées très tôt et si les efforts indispensables sont faits, elles peuvent être contrôlées. Ce contrôle est nécessaire si l’on veut éviter le transfert de la résistance aux glycopeptides aux staphylocoques dorés multirésistants comme cela a été observé aux États-Unis. Ce danger existe d’autant plus que la France, comme d’autres pays européens, connaît un taux encore trop élevé de staphylocoques multirésistants [30] (→).
(→) Voir l’article d’Oana Dumitrescu et al., page 943 de ce numéro
La dissémination de souches appartenant à un complexe clonal considéré comme adapté à l’hôpital fait prédire que les ERG ne pourront être complètement éradiqués des hôpitaux. C’est la surveillance constante de ces bactéries et une réaction rapide pour le contrôle des épidémies débutantes qui permettront d’éviter une situation endémique irréversible.
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun confit d’intérêts concernant les données publiées dans cet article.
La CMI est la plus faible concentration d’antibiotique capable de provoquer une inhibition complète de la croissance d’une bactérie (définition OMS).
Dans un depsipeptide, au moins une liaison amide (-CONHR-) est remplacée par une liaison ester (COOR).
Références
- Murray BE. The life and times of the Enterococcus. Clin Microbiol Rev 1990 ; 3 : 46-65. [Google Scholar]
- Enquête nationale de prévalence des infections nosocomiales, France, juin 2006. www.invs.sante. fr/enp2006 [Google Scholar]
- Cetinkaya Y, Falk P, Mayhall CG. Vancomycin-resistant enterococci. Clin Microbiol Rev 2000 ; 13 : 686-707. [Google Scholar]
- Murray BE. Vancomycin-resistant enterococcal infections. N Engl J Med 2000 ; 342 : 710-21. [Google Scholar]
- Willems RJ, Bonten MJ. Glycopeptide-resistant enterococci : deciphering virulence, resistance and epidemicity. Curr Opin Infect Dis 2007 ; 20 : 384-90. [Google Scholar]
- Courvalin P. Glycopeptide and enterococci. In : Courvalin R, Leclercq R, Rice L, eds. Antibiogram. Paris : ESKA, 2009 : 285-94. [Google Scholar]
- Mainardi JL, Villet R, Bugg TD, et al. Evolution of peptidoglycan biosynthesis under the selective pressure of antibiotics in Gram-positive bacteria. FEMS Microbiol Rev 2008 ; 32 : 386-408. [Google Scholar]
- Walsh C. Molecular mechanisms that confer antibacterial drug resistance. Nature 2000 ; 406 : 775-81. [Google Scholar]
- Courvalin P. Vancomycin resistance in gram-positive cocci. Clin Infect Dis 2006 ; 42 (suppl 1) : S25-34. [Google Scholar]
- Depardieu F, Podglajen I, Leclercq R, et al. Modes and modulations of antibiotic resistance gene expression. Clin Microbiol Rev 2007 ; 20 : 79-114. [Google Scholar]
- Xu X, Lin D, Guo Y, et al. vanM gene cluster: a new glycopeptide resistance gene cluster found in a clinical isolate of Enterococcus faecium. Vienne : European Congress of Clinical Microbiology and Infectious Diseases, 10-13 avril 2010 : abstract 925. [Google Scholar]
- Lebreton F, Depardieu F, Bourdon N, et al. VanN, a novel type of transferable vancomycin resistance in Enterococcus faecium 08-174. Vienne : European Congress of Clinical Microbiology and Infectious Diseases, 10-13 avril 2010 : abstract 926. [Google Scholar]
- National Nosocomial Infections Surveillance System. National nosocomial infections surveillance (NNIS) system report. Résumé des données de janvier 1992 à juin 2004. Am J Infect Control 2004 ; 32 : 470-85. [Google Scholar]
- Ostrowsky BE, Trick WE, Sohn AH, et al. Control of vancomycin-resistant enterococcus in health care facilities in a region. N Engl J Med 2001 ; 344 : 1427-33. [Google Scholar]
- Trystram D, Varon E, Péan Y, et al. Réseau européen de surveillance de la résistance bactérienne aux antibiotiques (EARSS) : résultats 2002, place de la France. BEH 2004 ; 32-33 : 142-4. [Google Scholar]
- Van der Auwera P, Pensart N, Korten V, et al. Influence of oral glycopeptides on the fecal flora of human volunteers : selection of highly glycopeptide-resistant enterococci. J Infect Dis 1996 ; 173 : 1129-36. [Google Scholar]
- Boisivon A, Thibault M, Leclercq R, Collège de bactériologie, virologie, hygiène des hôpitaux généraux français. Colonization by vancomycin-resistant enterococci of the intestinal tract of patients in intensive care units from French general hospitals. Clin Microbiol Infect 1997 ; 3 : 175-9. [Google Scholar]
- Guerin F, Perrier-Gros-Claude JD, Foissaud V, et al. Entérocoques résistants à la vancomycine en France : haute prévalence dans une population ambulatoire de sujets jeunes. Presse Med 1998 ; 27 : 1427-9. [Google Scholar]
- Petsaris O, Miszczak F, Gicquel-Bruneau M, et al. Combined antimicrobial resistance in Enterococcus faecium isolated from chickens. Appl Environ Microbiol 2005 ; 71 : 2796-9. [Google Scholar]
- Observatoire national de l’épidémiologie de la résistance bactérienne aux antibiotiques. http://www.onerba.org [Google Scholar]
- European Antimicrobial Resistance Surveillance System. http://www.rivm.nl/earss [Google Scholar]
- Aumeran C, Baud O, Lesens O, et al. Successful control of a hospital-wide vancomycin-resistant Enterococcus faecium outbreak in France. Eur J Clin Microbiol Infect Dis 2008 ; 27 : 1061-4. [Google Scholar]
- Lucet JC, Armand-Lefevre L, Laurichesse JJ, et al. Rapid control of an outbreak of vancomycin-resistant enterococci in a French university hospital. J Hosp Infect 2007 ; 67 : 42-8. [Google Scholar]
- Willems RJ, Top J, van Santen M, et al. Global spread of vancomycin-resistant Enterococcus faecium from distinct nosocomial genetic complex. Emerg Infect Dis 2005 ; 11 : 821-8. [Google Scholar]
- Cattoir V, Daurel C. Quelles nouveautés en antibiothérapie ? Med Mal Infect 2010 ; 40 : 135-54. [Google Scholar]
- Kainer MA, Devasia RA, Jones TF, et al. Response to emerging infection leading to outbreak of linezolid-resistant enterococci. Emerg Infect Dis 2007 ; 13 : 1024-30. [Google Scholar]
- Labie D. Résistances de Mycobacterium tuberculosis. Med Sci (Paris) 2007 ; 23 : 205-9. [Google Scholar]
- Zahar JR, Bille E, Schnell D, et al. Diffusion communautaire des entérobactéries sécrétrices de bêta-lactamase à spectre élargi (EBLSE). Med Sci (Paris) 2009 ; 25 : 939-44. [Google Scholar]
- Sanders P. Résistance aux antibiotiques chez les bactéries d’origine animale : actions en cours dans le secteur vétérinaire. MedSci (Paris) 2010 ; 26 : 930-5. [Google Scholar]
- Dumitrescu O, Dauwalder O, Boisset S, et al. Résistance aux antibiotiques chez Staphylococcus aureus : les points-clés en 2010. Med Sci (Paris) 2010 ; 26 : 943-9. [Google Scholar]
Liste des tableaux
Liste des figures
 |
Figure 1 Représentation schématique de la biosynthése du peptidoglycane et du mode dșaction desglycopeptides. La synthèse du peptioglycane s’effectue en trois étapes : (1) une étape intra-cytoplasmique (C) avec formation UDP-N-acétyl-muramoyl-pen ta peptide à partir d’UDP-N-acétyl-muramoyl-tripeptide et d’un dipeptide D-Ala-D-Ala ; (2) la translocation via un transporteur lipidique des précurseurs pentapeptidiques (lipide I/lipide II) de la surface interne vers la surface externe de la membrane cytoplasmique (M) ; (3) l’incorporation de ces précurseurs au peptidoglycane issant par transglycosylation et la formation ponts interpeptidiques par transpeptidation au niveau de la paroi (P). La fixation de lșantibiotique au niveau de l’extrémité D-Ala-D-Ala des précurseurs pentapeptidiques inhibe les étapes finales de transglycosylation et de inspeptidation (d’après [6, 7]). |
| Dans le texte | |
 |
Figure 2 Liaison entre la vancomycine et les différentes formes de dipeptide terminal des précurseurs pentapeptidiques. Cinq liaisons hydrogène sont impliquées avec le dipeptide D-Ala-D-Ala, alors que seulement quatre le sont avec le dipeptide D-Ala-D-Lac (d’après [8]). |
| Dans le texte | |
 |
Figure 3 Résistance de type VanA. Haut : organisation de l’opéron vanA (les flèches indiquent les gènes et la direction de la transcription). Bas : représentation schématique de la synthèse des Précurseurs du peptidoglycane après induction par un glycopeptide. Preg, promoteur des gènes de régulation ; Pres, promoteur des gènes de résistance (d’après [6]). |
| Dans le texte | |
 |
Figure 4 Évolution de la proportion de cas de résistance à la vancomycine. Résistance chez les E. faecium isolés d’hémocultures en Europe de 2002 à 2008 [21]. |
| Dans le texte | |
 |
Figure 5 Signalement à l’Institut de veille sanitaire (InVS) des cas d’infections/colonisations à entérocoques résistants aux glycopeptides et nombre de souches reçues au CNR et résistantes aux antibiotiques (Laboratoire associé entérocoques) de 2001 à 2008 [Roland Leclercq]. Le nombre de cas signalés annuellement est indiqué par les barres jaunes et le nombre de souches reçues ar les barres violettes. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




