| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 331 - 334 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026046 | |
| Published online | 24 April 2026 | |
L’enveloppe d’intercinèse
Une découverte qui bouscule notre connaissance de la méiose ovocytaire
The interkinetic envelope: a discovery that challenges our knowledge of oocyte meiosis
1
Université Paris Cité, CNRS UMR 7592, institut Jacques Monod, Paris, France
2
Max Perutz Labs, Vienna Biocenter campus, Vienne, Autriche
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
La division cellulaire : mitose et méiose
La division cellulaire orchestre le développement, le maintien, et la reproduction de tous les organismes vivants. Les cellules eucaryotes se divisent selon deux modalités : la mitose et la méiose. La mitose produit deux cellules filles génétiquement identiques à partir d’une cellule mère. Ce processus assure le renouvellement des tissus, leur croissance, et leur cicatrisation. Pendant la mitose, les chromosomes — préalablement dupliqués lors de la phase S — sont répartis équitablement entre les deux cellules filles. Deux évènements spectaculaires marquent le début de ce ballet chromosomique : la rupture de l’enveloppe nucléaire, qui libère les chromosomes dans le cytoplasme, et leur condensation, qui facilite leur ségrégation. En fin de mitose, les chromosomes se décondensent et une nouvelle enveloppe nucléaire se reforme autour d’eux, restaurant la compartimentation nucléocytoplasmique. La méiose, quant à elle, est un mode de division cellulaire spécialisé pour la reproduction sexuée. Elle produit des gamètes haploïdes (ovocytes et spermatozoïdes) à partir de cellules germinales diploïdes. Contrairement à la mitose, la méiose enchaîne deux divisions successives — méiose I et méiose II — sans réplication de l’ADN entre les deux. La méiose I sépare les chromosomes homologues (division réductionnelle), tandis que la méiose II, semblable à une mitose, sépare les chromatides sœurs (division équationnelle).
Les particularités de la méiose femelle
La méiose ovocytaire possède des caractéristiques uniques qui la distinguent de la méiose mâle et de la mitose. Première spécificité : son extrême asymétrie [1]. Alors que la méiose mâle produit quatre spermatozoïdes fonctionnels de taille égale, la méiose ovocytaire ne produit qu’un seul ovocyte mature, accompagné de l’expulsion de deux globules polaires (Figure 1A). Ces « déchets » cellulaires, formés lors de la méiose I et de la méiose II, contiennent certes un lot complet de chromosomes, mais presque aucun cytoplasme, et ils dégénèrent rapidement. Cette asymétrie des deux divisions méiotiques chez la femelle permet de concentrer l’essentiel des réserves cytoplasmiques dans l’ovocyte mature, pour les besoins des premiers jours du développement embryonnaire. Deuxième particularité : l’absence de centrosomes1 fonctionnels dans les ovocytes de nombreuses espèces, dont les mammifères et le ver Caenorhabditis elegans [2]. Les centrosomes sont normalement situés aux deux pôles du fuseau de division cellulaire. Ils organisent les microtubules de ce fuseau et orchestrent la ségrégation des chromosomes. En l’absence de centrosomes, les ovocytes utilisent des mécanismes alternatifs d’assemblage du fuseau et de ségrégation des chromosomes au cours de la méiose. Chez C. elegans, les chromosomes sont ségrégés par « poussée » plutôt que par « traction », grâce à la polymérisation asymétrique des microtubules du fuseau [3].
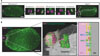 |
Figure 1 L’enveloppe d’intercinèse entoure les chromosomes entre la méiose I et la méiose II dans les ovocytes du nématode C. elegans. A. La méiose femelle produit un ovocyte haploïde et deux globules polaires (GP) à l’issue de deux divisions cellulaires asymétriques successives (méiose I et II), séparées par une courte phase d’intercinèse, au cours de laquelle les chromosomes restent condensés (LEM-2 en vert, ADN en magenta). Barres d’échelle : 5 µm. B. À gauche : image en microscopie confocale d’un ovocyte de C. elegans en intercinèse (LEM-2 en vert, ADN en magenta). Incidemment, le marquage vert hétérogène couvrant le cytoplasme correspond vraisemblablement à la présence de LEM-2 associée à diverses membranes intracellulaires, notamment celle du réticulum endoplasmique. Barre d’échelle : 5 µm. Au milieu : reconstruction tridimensionnelle d’images obtenues par microscopie électronique (technique SBF-SEM) des chromosomes en cours de ségrégation dans un ovocyte de C. elegans (enveloppe d’intercinèse en vert, ADN en magenta). Barre d’échelle : 1 µm. À droite : schéma de la composition protéique de l’enveloppe d’intercinèse, interposée entre les chromosomes (ADN) et le cytoplasme (Cyto). Barre d’échelle : 5 µm. LEM-2 : LEM domain-containing protein 2 ; BAF-1 : barrier-to-autointegration factor 1 ; NPP : protéine du pore nucléaire ; LMN-1 : lamine 1 ; SUN-1 : SUN domain-containing protein 1 ; EMR-1 : emerin homolog 1. |
L’intercinèse : un intervalle de temps énigmatique entre deux divisions méiotiques
Un court intervalle de temps, l’intercinèse, sépare les deux divisions méiotiques (Figure 1A). L’intercinèse diffère de l’interphase qui sépare deux mitoses successives car pendant l’intercinèse, les chromosomes restent condensés et l’ADN ne se réplique pas. L’intercinèse a donc longtemps été considérée comme une simple pause entre méiose I et méiose II, durant laquelle aucune enveloppe nucléaire ne se reforme, laissant les chromosomes exposés dans le cytoplasme.
Découverte de l’enveloppe d’intercinèse
Nos travaux sur les ovocytes de C. elegans ont bousculé ce dogme. En combinant vidéomicroscopie sur cellules vivantes et microscopie électronique de haute résolution, nous avons découvert une double membrane qui entoure les chromosomes condensés pendant l’intercinèse [4]. Bien qu’elle rappelle l’enveloppe nucléaire classique, cette « enveloppe d’intercinèse » s’en distingue par sa composition moléculaire ainsi que par le mécanisme de son assemblage (Figure 1B). L’assemblage de cette structure transitoire débute dès l’anaphase de méiose I, à la surface des chromosomes en cours de ségrégation. Sa formation est asymétrique : elle entoure préférentiellement le lot de chromosomes retenu dans l’ovocyte, tandis que l’autre lot, destiné au premier globule polaire, en est largement dépourvu. L’enveloppe persiste pendant toute l’intercinèse avant de se désintégrer lors de l’entrée en méiose II.
En utilisant la microscopie électronique SBF-SEM (serial block-face scanning electron microscopy), qui permet l’imagerie 3D de volumes cellulaires entiers, et la tomographie électronique, qui offre une résolution nanométrique, nous avons montré que cette enveloppe comporte deux bicouches lipidiques. D’abord fragmentée, elle devient progressivement continue (Figure 1B). Mais elle ne forme jamais une barrière hermétique : de larges perforations persistent, maintenant une communication entre l’intérieur de l’enveloppe et le cytoplasme. L’enveloppe d’intercinèse est donc une double membrane perméable qui compartimente les chromosomes entre l’anaphase de méiose I et le début de la méiose II.
Une composition moléculaire différente de celle de l’enveloppe nucléaire
L’enveloppe nucléaire comporte deux membranes superposées : une membrane interne de composition protéique spécifique et tapissée de lamines sur sa face interne, et une membrane externe, en continuité avec le réticulum endoplasmique. À certains endroits, ces deux membranes fusionnent pour former des pores nucléaires (où s’assemblent les complexes macromoléculaires des pores), essentiels aux échanges nucléocytoplasmiques [5].
Pour caractériser l’enveloppe d’intercinèse, nous avons suivi, par vidéomicroscopie, le déroulement de la méiose d’ovocytes de C. elegans produisant des protéines de l’enveloppe nucléaire fusionnées à des marqueurs fluorescents. Nous avons ainsi constaté que les protéines de la membrane nucléaire interne analysées étaient toutes recrutées à l’enveloppe d’intercinèse, tandis que les protéines typiques de la membrane nucléaire externe et provenant du réticulum endoplasmique étaient totalement absentes de cette enveloppe. Ce résultat témoigne d’une discontinuité entre l’enveloppe d’intercinèse et le réticulum endoplasmique, que nous avons d’ailleurs confirmée par microscopie électronique. Contrairement à l’enveloppe nucléaire, l’enveloppe d’intercinèse se compose exclusivement de protéines de la membrane nucléaire interne, sans aucune connexion avec le réticulum endoplasmique.
Des nucléoporines sans pores nucléaires
Les pores nucléaires sont des structures macromoléculaires complexes qui, chez C. elegans, regroupent 28 nucléoporines organisées en six sous-complexes. Étonnamment, malgré l’absence de pores nucléaires dans l’enveloppe d’intercinèse, certaines nucléoporines sont présentes à la surface des chromosomes pendant l’intercinèse (Figure 1B) [4, 6, 7]. Une analyse cartographique de 17 nucléoporines appartenant à différents sous-complexes a conduit à deux constats assez inattendus : des nucléoporines d’un même sous-complexe ne sont pas nécessairement recrutées ensemble à l’enveloppe d’intercinèse, et certaines nucléoporines coexistent dans cette enveloppe sans former de pore nucléaire complet, ni même de « pré-pore ». Ces constats indiquent que le mécanisme de la formation de l’enveloppe d’intercinèse diffère de celui qui régit l’assemblage de l’enveloppe nucléaire.
Mécanismes moléculaires de formation de l’enveloppe d’intercinèse
Rôle de la protéine BAF-1 dans le recrutement des membranes et l’intégrité structurale
Lors de la reformation de l’enveloppe nucléaire en fin de mitose, la protéine BAF-1 (barrier-to-autointegration factor 1) joue un rôle central. Elle se lie à la chromatine, maintient les chromosomes groupés, puis recrute les protéines de la membrane nucléaire interne et favorise l’ancrage des membranes dérivées du réticulum endoplasmique [5].
Pour explorer son rôle dans la formation de l’enveloppe d’intercinèse, nous avons analysé, par microscopie SBF-SEM, des ovocytes de C. elegans privés de BAF-1. Sans cette protéine, des membranes sont encore recrutées à la surface des chromosomes, mais elles sont moins nombreuses, plus fragmentées et mal distribuées autour des deux lots de chromosomes. Parallèlement, le recrutement des protéines de la membrane interne est perturbé. Autre défaut notable : l’accélération et l’amplification de la ségrégation des chromosomes. La distance entre les deux lots de chromosomes au cours de l’anaphase de méiose I est en effet significativement plus grande en absence de BAF-1 que dans les ovocytes témoins. Ainsi, l’intégrité de l’enveloppe d’intercinèse, qui nécessite la présence de BAF-1, influe directement sur la cinétique et l’amplitude de la ségrégation des chromosomes pendant la première division de la méiose.
Rôle de la protéine MEL-28 dans l’assemblage des membranes et le recrutement des nucléoporines
La protéine MEL-28, ou ELYS (embryonic large molecule derived from yolk sac) chez les vertébrés, est un autre acteur majeur de la reformation de l’enveloppe nucléaire en fin de mitose. Elle se lie précocement à la chromatine et recrute les nucléoporines nécessaires à la formation de pores nucléaires fonctionnels. Dans les ovocytes de C. elegans privés de MEL-28, nous avons constaté une quasi-absence de membranes à la surface des chromosomes en intercinèse. Cette protéine joue donc un rôle essentiel et précoce dans l’assemblage des membranes nécessaires à la formation de l’enveloppe d’intercinèse.
Rôle des nucléoporines à domaine membranaire
L’absence de pores nucléaires fonctionnels dans l’enveloppe d’intercinèse indique un mécanisme atypique de recrutement des nucléoporines. L’analyse de la séquence peptidique de la plupart des nucléoporines de l’enveloppe d’intercinèse prédit l’existence d’un domaine d’ancrage membranaire [8]. Cette propriété pourrait expliquer leur capacité d’ancrage autonome dans les membranes, indépendamment de leur association connue aux pores nucléaires. Par ailleurs, les observations réalisées après déplétion individuelle ou combinée de ces nucléoporines indiquent qu’elles participent activement au recrutement ou à la stabilisation des membranes de l’enveloppe d’intercinèse.
Perspectives
Ainsi, la formation de l’enveloppe d’intercinèse mobilise une machinerie dont la composition moléculaire recoupe partiellement celle de l’enveloppe nucléaire, notamment par la présence des protéines MEL-28 et BAF-1, et de certaines nucléoporines. Cette enveloppe transitoire entourant les chromosomes condensés joue un rôle dans leur ségrégation pendant la première division de méiose des ovocytes de C. elegans. Sa découverte vient s’ajouter à d’autres découvertes récentes pour suggérer que la compartimentation des chromosomes par des membranes, indépendamment de la reformation d’un noyau, pourrait être plus fréquente qu’on ne le pensait. Des travaux récents ont en effet permis d’identifier d’autres structures membranaires transitoires associées aux chromosomes dans différents contextes cellulaires [9].
Une question majeure demeure sans réponse : l’enveloppe d’intercinèse est-elle une particularité des ovocytes de C. elegans, avec leur mode atypique de ségrégation des chromosomes par poussée microtubulaire, ou représente-t-elle un mécanisme conservé dans d’autres espèces ? Des investigations chez les mammifères et d’autres organismes modèles permettront de déterminer si cette structure est universelle, ou au contraire restreinte à certains types cellulaires ou modes de division. Par ailleurs, la fonction précise de cette enveloppe reste à élucider. Protège-t-elle les chromosomes ? Permet-elle de contrôler leur environnement local ? Coordonne-t-elle les évènements de la méiose I et de la méiose II ? La compréhension des mécanismes moléculaires sous-jacents pourrait révéler de nouveaux principes fondamentaux de l’organisation cellulaire et de la dynamique des membranes.
Conflits d’intérêt
Les auteurs déclarent qu’ils n’ont aucun conflit d’intérêt.
Références
- Verlhac M-H, Dumont J. Interactions between chromosomes, microfilaments and microtubules revealed by the study of small GTPases in a big cell, the vertebrate oocyte. Mol Cell Endocrinol 2008 ; 282 : 12-7. [Google Scholar]
- Dumont J, Desai A. Acentrosomal spindle assembly and chromosome segregation during oocyte meiosis. Trends Cell Biol 2012 ; 22 : 241-9. [Google Scholar]
- Laband K, Le Borgne R, Edwards F, et al. Chromosome segregation occurs by microtubule pushing in oocytes. Nat Commun 2017 ; 8 : 1499. [Google Scholar]
- El Mossadeq L, Bellutti L, Le Borgne R, et al. An interkinetic envelope surrounds chromosomes between meiosis I and II in C. elegans oocytes. J Cell Biol 2025 ; 224 : e202403125. [Google Scholar]
- Cohen-Fix O, Askjaer P. Cell biology of the Caenorhabditis elegans nucleus. Genetics 2017 ; 205 : 25-59. [Google Scholar]
- Penfield L, Shankar R, Szentgyorgyi E, et al. Regulated lipid synthesis and LEM2/CHMP7 jointly control nuclear envelope closure. J Cell Biol 2020 ; 219 : e201908179. [Google Scholar]
- Hattersley N, Cheerambathur D, Moyle M, et al. A nucleoporin docks protein phosphatase 1 to direct meiotic chromosome segregation and nuclear assembly. Dev Cell 2016 ; 38 : 463-77. [Google Scholar]
- Hamed M, Antonin W. Dunking into the lipid bilayer: How direct membrane binding of nucleoporins can contribute to nuclear pore complex structure and assembly. Cells 2021 ; 10 : 3601. [Google Scholar]
- Schenkel L, Wang X, Le N, et al. A dedicated cytoplasmic container collects extrachromosomal DNA away from the mammalian nucleus. Mol Biol Cell 2023 ; 34 : ar105. [Google Scholar]
Le centrosome est le centre organisateur des microtubules dans les cellules animales.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 L’enveloppe d’intercinèse entoure les chromosomes entre la méiose I et la méiose II dans les ovocytes du nématode C. elegans. A. La méiose femelle produit un ovocyte haploïde et deux globules polaires (GP) à l’issue de deux divisions cellulaires asymétriques successives (méiose I et II), séparées par une courte phase d’intercinèse, au cours de laquelle les chromosomes restent condensés (LEM-2 en vert, ADN en magenta). Barres d’échelle : 5 µm. B. À gauche : image en microscopie confocale d’un ovocyte de C. elegans en intercinèse (LEM-2 en vert, ADN en magenta). Incidemment, le marquage vert hétérogène couvrant le cytoplasme correspond vraisemblablement à la présence de LEM-2 associée à diverses membranes intracellulaires, notamment celle du réticulum endoplasmique. Barre d’échelle : 5 µm. Au milieu : reconstruction tridimensionnelle d’images obtenues par microscopie électronique (technique SBF-SEM) des chromosomes en cours de ségrégation dans un ovocyte de C. elegans (enveloppe d’intercinèse en vert, ADN en magenta). Barre d’échelle : 1 µm. À droite : schéma de la composition protéique de l’enveloppe d’intercinèse, interposée entre les chromosomes (ADN) et le cytoplasme (Cyto). Barre d’échelle : 5 µm. LEM-2 : LEM domain-containing protein 2 ; BAF-1 : barrier-to-autointegration factor 1 ; NPP : protéine du pore nucléaire ; LMN-1 : lamine 1 ; SUN-1 : SUN domain-containing protein 1 ; EMR-1 : emerin homolog 1. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




