| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 328 - 330 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026045 | |
| Published online | 24 April 2026 | |
Obésité maternelle et stéatose du foie dans la descendance
Les macrophages coupables
Maternal obesity and hepatic steatosis in the offspring: macrophages are guilty
Centre de recherche sur l’inflammation, Inserm UMR 1149, Université Paris Cité, Faculté de médecine Bichat, Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les facteurs environnementaux au cours de la grossesse modifient les risques de l’enfant à venir de développer des maladies à l’âge adulte. Cette origine développementale de certaines maladies, souvent désignée par l’acronyme DOHaD (developmental origin of health and disease) [1] (→) est encore mal comprise, mais des modifications épigénétiques y jouent un rôle déterminant. Ainsi, certains stress subis par le fœtus peuvent entraîner des dérégulations géniques, qui s’exprimeront à l’âge adulte sous différentes formes (désordres métaboliques, maladies neurologiques, cancer, etc.). Dans ce cadre, l’obésité maternelle augmente le risque de développer des affections pour l’enfant à naître, une fois devenu adulte : il a par exemple été montré que la transmission d’un microbiote intestinal modifié par l’obésité maternelle augmentait la probabilité de développer un cancer dans la descendance [2]. De même, l’exposition à une obésité maternelle au cours de la vie fœtale peut entraîner, à l’âge adulte, une stéatose hépatique (accumulation de triglycérides dans les hépatocytes) encore appelée MAFLD (metabolic dysfunction-associated fatty liver disease) [3] (→), en dehors de toute transmission du comportement alimentaire ou d’une alimentation postnatale trop riche en sucres rapides et en graisses.
(→) Voir m/s n° 1, 2016
(→) Voir m/s n° 3, 2024, page 231
La MAFLD peut progresser vers une stéatohépatite (metabolic dysfunction-associated steatohepatitis [MASH]) avec fibrose qui, si l’agression chronique du foie induite par la stéatose n’est pas enrayée, peut progresser vers une cirrhose. Un consortium d’équipes de recherche européennes et chinoise a tenté d’identifier les mécanismes mis en œuvre dans cette transmission maternelle d’une maladie chronique du foie. Il vient de montrer que les macrophages résidents du foie (cellules de Kupffer) de l’enfant à naître étaient probablement en cause [4].
Certains arguments pointaient déjà du doigt le macrophage comme médiateur principal de maladies associées à un stress prénatal. En effet, le fonctionnement de la microglie, sous-population spécialisée de macrophages résidents du cerveau, est perturbé chez les enfants ayant subi un stress au cours de la vie fœtale [5, 6]. Par ailleurs, les cellules de Kupffer dérivent de précurseurs ayant colonisé le foie embryonnaire, ce qui les expose très tôt au flux sanguin maternel venant du placenta, dont la composition est modifiée en cas d’obésité maternelle. Enfin, une sous-population de cellules de Kupffer avait été impliquée dans les modifications métaboliques, le stress oxydant et l’inflammation associés à la stéatose hépatique induite par un régime riche en graisses [7] (→).
(→) Voir m/s n° 6-7, 2022, page 532
Pour valider l’hypothèse selon laquelle le macrophage hépatique est bien la pièce manquante du puzzle reliant obésité maternelle et stéatose hépatique chez les descendants à l’âge adulte, les auteurs ont utilisé un modèle murin d’obésité maternelle induite par un régime alimentaire gras chez la femelle gestante. Afin d’éviter que la stéatose retrouvée chez les descendants ne soit en réalité due à une alimentation lactée postnatale trop riche en graisses en raison de l’obésité de leur mère, les souriceaux ont été allaités par des mères nourricières témoins, donc non obèses. La première constatation est une augmentation du nombre de macrophages dans le foie des descendants de mère obèse ayant reçu une alimentation postnatale normale par rapport aux descendants de mère témoin, même si ces derniers reçoivent une alimentation très riche en graisses. Mais surtout, le remplacement des macrophages hépatiques par des monocytes témoins chez les nouveau-nés de mère obèse empêche l’apparition de la stéatose à l’âge adulte (Figure 1A).
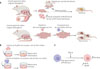 |
Figure 1 L’obésité maternelle induit une stéatose dans la descendance via une reprogrammation métabolique des cellules de Kupffer des souriceaux nouveau-nés. A. Les souriceaux nés de mère obèse présentent une augmentation du nombre de leurs macrophages hépatiques ainsi qu’une signature transcriptomique spécifique orientée vers la glycolyse. Ils présentent un risque de développer une stéatose hépatique à l’âge adulte. Lorsque les macrophages du foie de souriceaux nés de mère obèse sont remplacés par des macrophages témoins, ces souriceaux ne développeront pas de stéatose hépatique à l’âge adulte. B. Les hépatocytes cultivés en présence de cellules de Kupffer provenant de nouveau-nés de mère obèse ont un contenu en triglycérides supérieur à ceux cultivés en présence de cellules de Kupffer provenant de nouveau-nés de mère non obèse. C. Le facteur de transcription HIF1a des macrophages du foie des descendants de mère obèse joue un rôle clé dans leur reprogrammation vers un métabolisme plus « glycolytique » en induisant les apolipoprotéines A1 et E. Figure réalisée avec BioRender. |
Pour comprendre les mécanismes impliqués, les auteurs ont ensuite cherché à savoir si les cellules de Kupffer pouvaient directement induire une accumulation de triglycérides dans les cellules épithéliales hépatiques. Des hépatocytes normaux ont donc été cultivés en présence de cellules de Kupffer provenant du foie de souriceaux nés de mères obèses ou non obèses. De fait, les hépatocytes contenaient plus de lipides lorsque les cellules de Kupffer provenaient de la progéniture de mères obèses, suggérant que des facteurs sécrétés par ces cellules induisent l’accumulation de triglycérides dans les hépatocytes par une signalisation paracrine (Figure 1B). L’analyse comparative du profil transcriptomique des cellules de Kupffer chez les descendants de mères obèses et non obèses a montré l’existence d’une signature spécifique de l’obésité maternelle, en particulier l’induction de gènes impliqués dans la glycolyse et la gluconéogenèse. L’expression du gène Trem2 (Triggering receptor expressed on myeloid cells 2) est également augmentée dans les cellules de Kupffer des foies présentant une stéatose [8]. TREM2 est un récepteur de la famille des immunoglobulines présent dans les cellules myéloïdes et impliqué dans le métabolisme des lipides. Néanmoins, les macrophages TREM2+ semblent avoir un rôle ambivalent : plutôt pro-fibrosant lorsqu’ils sont présents dans les bandes de fibrose du foie (ils sont alors appelés macrophages SAM pour scar-associated macrophages, et expriment d’autres marqueurs comme l’ostéopontine), et plutôt bénéfique en cas de MASH en raison de leur capacité à phagocyter les débris lipidiques, à restreindre l’inflammation, et à aider à la résolution de la fibrose (ils sont alors appelés macrophages LAM pour lipid-associated macrophages) [9-11]. Or, les cellules de Kupffer peuvent adopter un phénotype « LAM-like », ressemblant à celui des macrophages LAM, et jouent alors un rôle réparateur des lésions hépatiques [12]. Ces macrophages LAM sont également présents dans le tissu adipeux de personnes obèses, où ils participent au renouvellement des adipocytes (élimination des adipocytes morts et sécrétion de cytokines modulant le microenvironnement), et dans les lésions d’athérosclérose, où ils permettent l’efflux de cholestérol et l’efférocytose, un processus qui contribue à l’homéostasie tissulaire en favorisant la résolution de l’inflammation. Or, si les macrophages du foie sécrètent des facteurs pro-inflammatoires comme les interleukines IL-1β et IL-6 et le TNF (tumor necrosis factor) en cas de régime gras chez l’adulte, ceux de la descendance de mères obèses allaitée par des mères témoins ont un profil d’expression génique différent, qui rappelle celui des macrophages LAM.
L’analyse spectrale du profil métabolique des cellules de Kupffer du foie de souris nées de mères obèses a confirmé leur reprogrammation métabolique, d’un profil de type « oxydation phosphorylante (OXPHOS) » vers un profil « glycolytique », considéré comme plus fibrogène [10]. En revanche, et bien que ces macrophages acquièrent alors des propriétés pro-inflammatoires, cette reprogrammation n’entraîne pas d’inflammation « systémique » (i.e., avec la présence de marqueurs d’inflammation dans le sang) dans la descendance des souris obèses. La protéine HIF1a (hypoxia inducible factor α) est le principal médiateur de cette reprogrammation au cours du développement. Le facteur de transcription HIF1, dimère composé des sous-unités α et β, joue un rôle clé dans la réponse à l’hypoxie, mais également dans le métabolisme puisque HIF1a est un régulateur de la glycolyse dans les macrophages [13]. Or, la déplétion de HIF1a dans l’ensemble des macrophages des souriceaux nés de mères obèses prévient la stéatose hépatique chez ceux-ci, ainsi que la reprogrammation métabolique de leurs cellules de Kupffer. Pour comprendre comment HIF1a reprogramme les macrophages, les auteurs ont procédé à des analyses transcriptomiques variées (Bulk RNA-Seq, snRNA-Seq et ATAC-Seq, protéomique) des cellules de Kupffer, privées ou non de HIF1a, provenant de nouveau-nés de mères obèses. En condition d’obésité maternelle, l’expression des apolipoprotéines E et A1 est augmentée ainsi que celle des facteurs de transcription PPARa et PPARγ (récepteurs activés par les proliférateurs de peroxysomes) qui contrôlent la synthèse de ces apolipoprotéines (Figure 1C). Ces modifications semblent dépendantes du facteur HIF1a, puisqu’elles ne sont pas retrouvées dans les cellules qui en sont dépourvues.
Les comparaisons du profil d’expression génique ont également révélé des modifications épigénétiques au sein du locus Gpnmb, décrit comme un biomarqueur de la MASH. L’induction de l’expression du gène Gpnmb est limitée à des sous-populations de cellules de Kupffer qui sont plus nombreuses en condition d’obésité maternelle, suggérant que d’autres modifications transcriptionnelles que celles liées à HIF1a existent dans les macrophages de souris nées de mère obèse. Malgré la plasticité connue des macrophages, il convient de noter que toutes ces modifications des cellules de Kupffer induites par l’obésité maternelle sont particulièrement stables dans le temps.
Ainsi, un régime alimentaire gras « obésogène » administré à la mère pendant la gestation induit, chez le fœtus, des changements transcriptionnels et métaboliques des macrophages hépatiques vers un profil « glycolytique » [11]. Ces modifications durables stimulent l’absorption et le stockage des lipides par les hépatocytes avoisinants et contribuent ainsi au développement de la stéatose hépatique. Les macrophages coupables proviennent du sac vitellin, alors que dans les modèles de stéatose hépatique induite par un régime gras chez l’adulte, ce sont des monocytes dérivés de la moelle osseuse qui remplacent progressivement les cellules de Kupffer. Il reste cependant encore à identifier les métabolites ou lipides maternels qui traversent la barrière hématoplacentaire pour reprogrammer les macrophages hépatiques fœtaux vers un métabolisme plus « glycolytique » via HIF1a. L’acide stéarique pourrait être un bon candidat. Il a en effet été montré, dans un contexte très différent d’angiogenèse rétinienne, que cet acide gras à chaîne moyenne remodelait la chromatine de cellules myéloïdes pour induire un programme glycolytique proinflammatoire dans ces cellules [14]. En attendant de mieux comprendre les mécanismes impliqués, serait-il possible de profiter de cette période présymptomatique chez les descendants de mère obèse pour inhiber le facteur HIF1a et empêcher ainsi l’apparition d’une stéatose ultérieure ? Avant de franchir expérimentalement cette nouvelle étape, une validation chez l’homme des constats faits dans le modèle murin, qui intégreraient d’autres facteurs favorisant la stéatose hépatique en particulier les modifications du microbiote intestinal, serait bienvenue.
Conflits d’intérêt
L’auteure déclare qu’elle n’a aucun conflit d’intérêt.
Références
- Origine développementale de la santé et des maladies (DOHaD), environnement et épigénétique. Med Sci (Paris) 2016 ; 32 : 1-130. [Google Scholar]
- Moeckli B, Delaune V, Gilbert B, et al. Maternal obesity increases the risk of hepatocellular carcinoma through the transmission of an altered gut microbiome. J Hep Rep 2024 ; 6 : 101056. [Google Scholar]
- Donné R, Desdouets C. Maladie du foie gras et stress de réplication de l’ADN. Med Sci (Paris) 2024 ; 40 : 231-4. [Google Scholar]
- Huang H, Balzer NR, Seep L, et al. Kupffer cell programming by maternal obesity triggers fatty liver disease. Nature 2025 ; 644 : 790-8. [Google Scholar]
- Block CL. Prenatal environmental stressors impair postnatal microglia function and adult behavior in males Cell Rep 2022 ; 40 : 111161. [Google Scholar]
- Han VX, Patel S, Jones HF, Dale RX. Maternal immune activation and neuroinflammation in human neurodevelopmental disorders. Nat Rev Neurol 2021 ; 17 : 564-79. [CrossRef] [PubMed] [Google Scholar]
- Blériot C, Ginhoux F. Une sous-population de macrophages hépatiques impliquée dans la régulation du métabolisme. Med Sci (Paris) 2022 ; 38 : 532-6. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Remmerie A, Martens L, Thoné T, et al. Osteopontin expression identifies a subset of recruited macrophages distinct from Kupffer cells in the fatty liver. Immunity 2020 ; 53 : 641-57. [Google Scholar]
- Ganguly S, Rosenthal SB, Ishizuka K, et al. Lipid-assoicated macrophages’promotion of fibrosis resolution during MASH regression requires TREM2. Proc Natl Acad Sci USA 2024 ; 121 : e2405746121 [Google Scholar]
- Gilgenkrantz H, Paradis V, Lotersztajn S. Cell metabolism-based therapy for liver fibrosis, repair and hepatocellular carcinoma. Hepatology 2025 ; 81 : 269-87. [Google Scholar]
- Xu R, Vujic N, Bianco V, et al. Lipid-associated macrophages between aggravation and alleviation of metabolic diseases. Trends Endocrinol Metab 2024 ; 35 : 981-95. [Google Scholar]
- De Ponti FF, Bujko A, Liu Z, et al. Spatially restricted and ontogenically distinct hepatic macrophages are required for tissue repair. Immunity 2025 ; 58 : 362-80. [Google Scholar]
- Corcoran SE, O’Neill. HIF1a and metabolic reprogramming in inflammation. J Clin Invest 2016 ; 126 : 3699-707. [Google Scholar]
- Hata M, Andriessen EM, Hata M, et al. Past history of obesity triggers persistent epigenetic changes in innate immunity and exacerbates neuroinflammation. Science 2023 ; 379 : 45-62. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 L’obésité maternelle induit une stéatose dans la descendance via une reprogrammation métabolique des cellules de Kupffer des souriceaux nouveau-nés. A. Les souriceaux nés de mère obèse présentent une augmentation du nombre de leurs macrophages hépatiques ainsi qu’une signature transcriptomique spécifique orientée vers la glycolyse. Ils présentent un risque de développer une stéatose hépatique à l’âge adulte. Lorsque les macrophages du foie de souriceaux nés de mère obèse sont remplacés par des macrophages témoins, ces souriceaux ne développeront pas de stéatose hépatique à l’âge adulte. B. Les hépatocytes cultivés en présence de cellules de Kupffer provenant de nouveau-nés de mère obèse ont un contenu en triglycérides supérieur à ceux cultivés en présence de cellules de Kupffer provenant de nouveau-nés de mère non obèse. C. Le facteur de transcription HIF1a des macrophages du foie des descendants de mère obèse joue un rôle clé dans leur reprogrammation vers un métabolisme plus « glycolytique » en induisant les apolipoprotéines A1 et E. Figure réalisée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




