| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
Chroniques génomiques
|
|
|---|---|---|
| Page(s) | 311 - 314 | |
| Section | Forum | |
| DOI | https://doi.org/10.1051/medsci/2026041 | |
| Published online | 20 March 2026 | |
Thérapies CAR-T in vivo : un progrès décisif
In vivo CAR-Ts, a significant breakthrough
Biologiste, généticien, Président d’Aprogène (association pour la promotion de la génomique), Marseille, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Abstract
Since 2017, the CAR-T ex vivo approach has been very successful for the treatment of B cell malignancies in spite of its complexity and cost. A novel method involves transforming T lymphocytes into CAR-T cells in situ (therefore, in vivo) and promises simplicity, speed and affordability. It also seems applicable to several autoimmune diseases and is currently the object of much activity and interest in academic and corporate environments.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Les cellules CAR-T, une thérapie déjà classique
Les cellules CAR-T (chimeric antigen receptor T cells) ont fait une entrée en scène fracassante en 2017 [1] (→) avec l’autorisation de mise sur le marché par la FDA (Food and Drug Administration) aux États-Unis, et la commercialisation du Kymriah (Tisagenlecleucel, la première formulation de cellules CAR-T) par l’entreprise Novartis, au tarif de 475 000 dollars américains (montant qui a choqué à l’époque, mais depuis on s’est habitué à des tarifs de l’ordre du million de dollars pour des thérapies cellulaires ou géniques). Rappelons qu’il s’agit d’un traitement personnalisé de cancers du sang, reposant sur la modification génique in vitro de cellules T, prélevées chez le patient, pour leur faire exprimer un récepteur transmembranaire chimérique dirigé contre un antigène tumoral, suivie de la réintroduction, après amplification de ces cellules T modifiées qui doivent cibler et détruire les cellules tumorales in vivo. Cette thérapie, qui a fait l’objet de nombreuses améliorations, s’est révélée efficace et s’est largement développée malgré sa complexité logistique et son coût [2] (→) : on compte actuellement sept thérapies CAR-T commercialisées, la dernière fin 20241, et plus de 70 000 patients auraient déjà été traités [3]. Plusieurs de ces traitements sont autorisés en France et pris en charge par l’assurance-maladie. Il s’avère que cette approche est également efficace pour certaines affections auto-immunes, permettant l’élimination durable des Lymphocytes B autoréactifs [4], ce qui ouvre un champ d’application bien plus large que celui des cancers du sang. Mais malgré le succès actuel des thérapies CAR-T, la complexité de la méthode et les difficultés logistiques qu’entraînent le prélèvement, la modification génique, l’expansion et la réinfusion des cellules T modifiées après chimiothérapie (pour « faire de la place » aux cellules T qui vont être infusées), rendent très souhaitable une simplification de cette approche : c’est la perspective qui est ouverte depuis peu par la possibilité d’effectuer la modification génique des cellules non plus ex vivo mais in vivo, directement au sein du patient. Des premiers résultats encourageants ont déclenché un intense intérêt de la part de multiples entreprises, et la perspective de tels traitements devient réaliste [3].
(→) Voir m/s n° 11, 2017, page 1003
(→) Voir m/s n° 11, 2024, page 848
Modifier les lymphocytes T in situ
L’objectif ici est d’effectuer la modification génique des cellules T in vivo, au sein du patient, grâce à l’introduction d’un vecteur dirigé vers ces cellules cibles, véhiculant un ARN messager (ou un plasmide) codant pour l’antigène chimérique et capable de provoquer leur transformation en cellules CAR-T dirigées contre les lymphocytes B que l’on souhaite éliminer. Un tel schéma présente de multiples avantages : il pourrait permettre le traitement du patient en un lieu unique, par la simple infusion d’un réactif (de type viral ou nanoparticule) qui assurerait in situ la transformation de lymphocytes T en cellules CAR-T, éliminant du coup la chimiothérapie préalable, le besoin de centres spécialisés et le transfert de cellules. Cette approche « simplifiée » rendrait les thérapies CAR-T beaucoup plus accessibles du point de vue logistique et financier. Il n’est donc pas étonnant que beaucoup de laboratoires et d’industriels poursuivent cet objectif en dépit des difficultés [3, 5], encouragés par le succès des approches fondées sur le transfert d’ARNm pour les vaccins contre le Covid. Les problèmes sont nombreux : parvenir à un transfert efficace et spécifique du vecteur (viral ou sous forme de nanoparticules lipidiques), obtenir son ciblage spécifique vers les cellules T à modifier, assurer l’expression de l’ARNm ou du plasmide (codant pour le récepteur CAR avec ses domaines d’activation, sa partie transmembranaire et le domaine extracellulaire qui reconnaît l’antigène cible), et s’assurer qu’il n’y a pas d’expression hors cible (off target) dans d’autres cellules ou organes. On estime que plusieurs milliards de dollars ont déjà été investis dans ces travaux
Un travail essentiel, mais encore incomplet
Un article publié en juin 2025 dans la revue Science [6] montre un bel exemple de ces travaux. Il a été réalisé principalement sous l’égide de l’entreprise Capstan, qui compte parmi ses fondateurs Carl June, le « père de la thérapie CAR-T », et qui a été rachetée depuis par la multinationale AbbVie pour 3,1 milliards de dollars. C’est l’approche des nanoparticules lipidiques qui a été choisie (comme pour les vaccins contre la Covid-19), au lieu de vecteurs viraux qui peuvent s’intégrer dans le génome et provoquer une expression durable du récepteur CAR-T : les nanoparticules conduisent, elles, à expression transitoire du transgène, ce qui peut être avantageux pour le traitement d’affections auto-immunes. La nanoparticule (Figure 1) est ciblée vers les lymphocytes T CD5+ ou CD8+ par un anticorps présenté en surface et contient une « charge utile » d’ARNm codant pour un récepteur chimérique dirigé vers un antigène spécifique des cellules B à éliminer comme CD19 ou BMCA (antigène de maturation des lymphocytes B). Dans la pratique, la construction d’un tel système a nécessité un très gros travail de mise au point, essentiel pour assurer l’efficacité du traitement, et incluant de multiples contrôles – ce n’est pas pour rien que cet article comporte quarante auteurs ! La particule nanolipidique, après injection, doit se localiser préférentiellement dans la rate, au contact des cellules du système immunitaire, ce qui est assuré par une composition très particulière en lipides et notamment l’emploi d’un lipide ionisable, appelé L829, qui évite l’accumulation des nanoparticules dans le foie. Il faut ensuite vérifier l’efficacité du ciblage vers les cellules T à modifier, principalement dans cet article les cellules T cytotoxiques CD8+ ; vient ensuite l’optimisation de la séquence de l’ARNm introduit en choisissant les codons les plus adaptés et les promoteurs les plus efficaces, afin d’assurer une synthèse optimale du CAR une fois la nanoparticule introduite dans la cellule T ciblée. Après toutes ces mises au point, on obtient des nanoparticules lipidiques, appelées par exemple CD8-L829-tLNP-CD19 (nanoparticules (tLNP, targeted lipid nanoparticle), contenant le lipide 829, ciblant les cellules T CD8+ et transportant un CAR dirigé contre les cellules B CD19+). Reste à voir comment tout cela fonctionne…
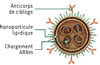 |
Figure 1 Nanoparticule lipidique pour la production de CAR-T in vivo. La particule est dirigée vers les lymphocytes T à modifier par l’anticorps de ciblage présent à sa surface ; elle fusionne avec ces cellules T et y introduit son chargement d’ARN messager qui va diriger la synthèse d’un CAR (chimeric antigen receptor) dirigé vers les cellules B à éliminer (extrait partiel et modifié de la figure 1 de [6]). |
Le premier type de test consiste à incuber in vitro des cellules T primaires humaines avec les nanoparticules lipidiques citées ci-dessus : on observe bien l’expression du CAR (i.e. la transformation de la cellule T en CAR-T). Le second test, plus intéressant, consiste en l’injection des nanoparticules CD8-L829-tLNP-CD19 à des souris humanisées (possédant un système immunitaire humain), ce qui provoque la disparition rapide des cellules B (humaines) ciblées (Figure 2).
 |
Figure 2 Élimination des cellules B humaines dans des souris humanisées après traitement par des nanoparticules CAR ciblant CD19. Le pourcentage de cellules B parmi les leucocytes est représenté au cours du temps. Chaque courbe correspond à un animal ; les nanoparticules CD8-L829-tLNP-mCherry sont utilisées en contrôle, car elles conduisent à l’expression du marqueur Cherry par les CAR-T. Ce marqueur témoin est absent des cellules B, et n’induit donc pas leur destruction (extrait partiel et modifié de la figure 3 de [6]). |
Dans le contexte d’applications visant à traiter des maladies auto-immunes, les auteurs ont également vérifié que le système fonctionne bien sur des prélèvements provenant de patients atteints de telles affections et qu’il provoque l’apparition de cellules CAR-T, capables de lyser les cellules B autologues provenant de ces patients. Dans la dernière partie de l’article, les auteurs se rapprochent d’investigations in vivo en traitant des primates non humains, des macaques crabiers (Macaca fascicularis). L’anticorps anti-CD8 déjà utilisé pour le ciblage vers les cellules T réagit avec la forme présente chez cette espèce, par contre l’anti-CD19 humain (qui permet le ciblage du CAR vers les cellules B humaines) n’est pas utilisable et est remplacé par un anti-CD20, également spécifique des cellules B. Les nanoparticules CD8-L89-tLNP-CD20 injectées par voie intraveineuse à ces macaques provoquent effectivement la transformation en CAR-T de 85 % des lymphocytes T CD8, entraînant l’éradication presque complète des cellules B, et notamment des cellules B mémoire, qui expriment fortement CD20. Après une vingtaine de jours, de nouvelles cellules B apparaissent et atteignent progressivement le niveau d’origine, mais elles ont un phénotype de cellules B naïves, ce qui suggère qu’il y a eu un « reset immunitaire », une remise à zéro du système immunitaire avec élimination des cellules B mémoire. Cet effet a déjà été observé pour plusieurs affections auto-immunes lors de traitements ex vivo par des cellules CAR-T anti CD19, traitements qui ont été couronnés de succès sur le plan clinique [7]. Des effets secondaires notables sont observés (comme l’élévation du niveau des cytokines et d’enzyme hépatiques), mais ce premier résultat in vivo est néanmoins très encourageant, même si l’on est encore loin d’une véritable preuve de concept clinique.
Une vraie révolution en perspective
Même si elles ont connu un grand succès avec le traitement de nombreux patients, les thérapies CAR-T ex vivo restent très complexes, avec une logistique lourde et des coûts extrêmement élevés. La perspective de pouvoir réaliser ces thérapies CAR-T in vivo change complètement la donne : elle fait entrevoir un traitement injecté directement au patient et provoquant in situ la transformation de ses propres cellules T en CAR-T dirigées contre les cellules tumorales ou auto-immunes que l’on souhaite éliminer [8] (Figure 3). Les thérapies CAR-T deviennent alors beaucoup plus accessibles du point de vue pratique, mais aussi financier. Et comme ils ont récemment fait la preuve de leur efficacité pour traiter des maladies auto-immunes [7], un vaste marché s’ouvre à eux, bien plus important que celui des hémopathies B malignes : selon certaines estimations, près de 10 % de la population souffre d’une affection de ce type [6]. Une bonne dizaine d’entreprises se spécialisent dans la mise au point de ces CAR-T in vivo, avec une grande variété d’approches techniques et de vecteurs. À cet égard les vecteurs viraux demeurent les outils les plus utilisés: ils semblent bien adaptés aux applications en cancérologie pour lesquelles une expression durable du CAR peut être avantageuse. Les nanoparticules lipidiques, elles, ont le vent en poupe pour le traitement de maladies auto-immunes. Les grandes firmes pharmaceutiques surveillent de près ce secteur et parfois rachètent (très cher) les start-up les plus prometteuses. Il reste certes bien des étapes à franchir, mais on peut parier qu’à l’échéance de quelques années, les CAR-T in vivo connaîtront un large succès : ce sera là le premier succès à grande échelle (en termes de large champ d’application) de ces thérapies géniques dont on a longtemps attendu l’avènement.
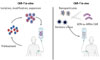 |
Figure 3 Comparaison des deux technologies de CAR-T. CAR-T in vitro (ex vivo) versus in vivo – un processus complexe (à gauche) remplacé par une simple infusion (à droite) de nanoparticules lipidiques ou de vecteurs viraux. Adapté de [8] (licence Creative Commons) |
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Jordan B. Immunothérapie « CAR-T » : une autorisation qui fait date. Med Sci (Paris) 2017 ; 33 : 1003–6. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Messaoudi D, Perez F, Gouveia Z. Les nouvelles générations de cellules CAR-T. Med Sci (Paris) 2024 ; 40 : 848–57. [Google Scholar]
- Marshall A. In vivo CAR-Ts captivate big pharma. Nat Biotechnol 2025 ; 43 : 1893–6. [Google Scholar]
- Schett G, Mackensen A, Mougiakakos D. CAR T-cell therapy in autoimmune diseases. Lancet 2023 ; 402 : 2034–44. [Google Scholar]
- Bui TA, Mei H, Sang R, et al. Advancements and challenges in developing in vivo CAR T cell therapies for cancer treatment. EBioMedicine 2024 ; 106 : 105266. [Google Scholar]
- Hunter TL, Bao Y, Zhang Y, et al. In vivo CAR T cell generation to treat cancer and autoimmune disease. Science 2025 ; 388 : 1311–7. [Google Scholar]
- Müller F, Taubmann J, Bucci L, et al. CD19 CAR T-cell therapy in autoimmune disease – a case series with follow-up. N Engl J Med 2024 ; 390 : 687–700. [CrossRef] [PubMed] [Google Scholar]
- Xin T, Cheng L, Zhou C, et al. In-vivo induced CAR-T cell for the potential breakthrough to overcome the barriers of current CAR-T cell therapy. Front Oncol 2022 : 12 : 809754. [Google Scholar]
Par ordre d’entrée en scène, de 2017 à 2024 : Kymriah (Tisagenlecleucel), Novartis, ciblant CD19 ; Yescarta (Axicabtagene ciloleucel), Kite Pharma (Gilead), ciblant CD19 ; Tecartus (Brexucabtagene autoleucel), Kite Pharma (Gilead), ciblant CD19 ; Breyanzi (Lisocabtagene maraleucel), Bristol Myers Squibb, ciblant CD19 ; Abecma (Idecabtagene vicleucel), Bristol Myers Squibb, ciblant BMCA ; Carvykti (Ciltacabtagene autoleucel), Johnson & Johnson, ciblant BMCA ; Aucatzyl (Obecabtagene autoleucel), Autolus Therapeutics, ciblant CD19.
Liste des figures
 |
Figure 1 Nanoparticule lipidique pour la production de CAR-T in vivo. La particule est dirigée vers les lymphocytes T à modifier par l’anticorps de ciblage présent à sa surface ; elle fusionne avec ces cellules T et y introduit son chargement d’ARN messager qui va diriger la synthèse d’un CAR (chimeric antigen receptor) dirigé vers les cellules B à éliminer (extrait partiel et modifié de la figure 1 de [6]). |
| Dans le texte | |
 |
Figure 2 Élimination des cellules B humaines dans des souris humanisées après traitement par des nanoparticules CAR ciblant CD19. Le pourcentage de cellules B parmi les leucocytes est représenté au cours du temps. Chaque courbe correspond à un animal ; les nanoparticules CD8-L829-tLNP-mCherry sont utilisées en contrôle, car elles conduisent à l’expression du marqueur Cherry par les CAR-T. Ce marqueur témoin est absent des cellules B, et n’induit donc pas leur destruction (extrait partiel et modifié de la figure 3 de [6]). |
| Dans le texte | |
 |
Figure 3 Comparaison des deux technologies de CAR-T. CAR-T in vitro (ex vivo) versus in vivo – un processus complexe (à gauche) remplacé par une simple infusion (à droite) de nanoparticules lipidiques ou de vecteurs viraux. Adapté de [8] (licence Creative Commons) |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




