| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 295 - 305 | |
| Section | Repères | |
| DOI | https://doi.org/10.1051/medsci/2026040 | |
| Published online | 20 March 2026 | |
Évaluer la balance bénéfices-risques des médicaments
Quelques leçons de la Covid-19
Assessing the risk-benefit balance of medicines: Some lessons from Covid-19
1
Université Grenoble Alpes, Inserm U1300, Centre régional de pharmacovigilance de Grenoble, France
2
Université de Bordeaux, France
3
Université Rouen Normandie, Inserm, ENVI UMR1096, CHU de Rouen, département de pharmacologie, Rouen, France
4
Université Grenoble Alpes, Inserm U1300, Centre d’investigation clinique de Grenoble, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
L’efficacité des médicaments est évaluée par les essais cliniques. Cependant, ceux-ci ne sont pas conçus pour identifier les effets indésirables, en particulier lorsqu’ils sont rares. Ceci justifie un système robuste de pharmacovigilance, pour les évaluer après la commercialisation des médicaments, complété au besoin par des études pharmacoépidémiologiques. Les bénéfices des médicaments s’expriment en valeur relative ou absolue, et varient en fonction du risque associé à la maladie (sa sévérité, son risque de complications ou de progression) et de son incidence pour le bénéfice populationnel. Ce n’est pas le cas des effets indésirables, qui dépendent des caractéristiques intrinsèques du médicament et de la population traitée. Dans ce contexte, peut-on réellement mettre en balance les avantages et les risques des médicaments ? L’expérience de la Covid-19 illustre la complexité de cette notion. Elle met clairement en évidence la nécessité d’une analyse conjointe des essais cliniques, du suivi de pharmacovigilance, des études pharmacoépidémiologiques et de la détection des interactions médicamenteuses potentielles. Enfin, l’acculturation du grand public à l’évaluation de l’efficacité et de la sécurité des médicaments est indispensable pour permettre à chacun d’interpréter correctement cette notion complexe de balance bénéfices-risques, d’éviter les simplifications, et de lutter contre la désinformation.
Abstract
The efficacy of medications is evaluated by clinical trials. However, such trials are not designed to assess adverse effects, particularly when those are rare. A robust pharmacovigilance system is therefore required to assess risks, supplemented as requested by pharmacoepidemiology studies. The benefits of medications are expressed in either relative or absolute terms and they vary depending on the baseline risk of the disease (its severity, potential complications, progression, and its incidence for the population-level benefits). This is not the case for adverse effects, which are influenced by the drug characteristics and the population receiving the treatment. In this context, can we truly balance the benefits and risks of medications? The experience of Covid-19 illustrates the complexity of this concept. It clearly highlights the need for a comprehensive approach, integrating analysis of clinical trials, pharmacovigilance monitoring, pharmacoepidemiology studies, and the detection of potential drug interactions. Finally, it is essential to inform and educate the general public about medications. This empowers individuals to accurately understand the complex concept of benefit-risk balance, prevents misleading over simplifications, and helps effectively counter misinformation.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Vignette (© Jean-Luc Cracowski).
Les bénéfices associés à la prise d’un médicament peuvent être évalués par deux types d’études : les essais cliniques contrôlés et randomisés, qui permettent de mesurer son efficacité thérapeutique1, ou les études observationnelles, qui ont un objectif plus modeste, et qui sont effectuées principalement lorsque des essais cliniques ne sont pas réalisables, ou pour compléter les connaissances après des essais randomisés contrôlés. Des études observationnelles ont par exemple été réalisées pour confirmer sur des critères durs le bénéfice des vaccins contre le SARS-CoV2, lors de la pandémie de Covid-19, mais également après l’apparition de nouveaux variants pour lesquels il n’était pas envisageable de réaliser de nouveaux essais cliniques vaccinaux. L’évaluation des risques du médicament, réalisée au moment de son autorisation de mise sur le marché2, repose sur les résultats des données de sécurité des essais cliniques. Or, ces essais n’impliquent généralement qu’un nombre de limité de patients, quelques centaines ou au plus quelques milliers. Par conséquent, il existe toujours un risque que certains effets indésirables, qu’ils soient prévisibles ou non, n’aient pas été observés lors de ces essais cliniques.
L’urgence liée à la pandémie de Covid-19 a conduit à une accélération des délais de développement pharmacologique. Pourtant, les procédés d’évaluation de la balance bénéfices-risques des médicaments sont restés similaires à ceux de la période prépandémique. En revanche, un nouveau concept a émergé, celui d’infodémie3. Cet afflux d’informations a considérablement entravé la capacité du public à comprendre l’évaluation des bénéfices et des risques des médicaments. Par exemple, la diffusion massive de faux messages, notamment sur les réseaux sociaux, au sujet de l’efficacité et des risques de certains traitements, comme l’hydroxychloroquine ou les vaccins contre la Covid-19, a semé la confusion et entretenu la méfiance à l’égard des pouvoirs publics [1]. Garantir l’accès à des informations exactes, présentées en temps utile et de manière claire, pour prendre des décisions éclairées et maintenir la confiance du public est un enjeu majeur dans le domaine de la santé [2].
Comment évaluer le bénéfice d’un médicament ?
L’importance des essais cliniques
Les bénéfices d’un médicament sont les effets positifs et cliniquement pertinents qu’il apporte à un patient, en améliorant sa survie, son état de santé ou sa qualité de vie. Pour l’Agence européenne des médicaments, l’efficacité a une définition précise : il s’agit du bénéfice d’une prise en charge thérapeutique observé dans des conditions idéales, c’est-à-dire dans un cadre contrôlé tel qu’un essai clinique [3, 4] (Figure 1). La validité interne4 de l’essai clinique permet de quantifier les bénéfices et de s’assurer qu’ils soient attribuables au médicament, plutôt qu’à des biais dû à un facteur de confusion [5] (→).
(→) Voir m/s n° 4, 2024, page 381
 |
Figure 1 Différences entre les essais cliniques et les études observationnelles pour évaluer le bénéfice des médicaments. Classiquement, on oppose les essais cliniques randomisés contrôlés en double aveugle, réalisés sur de petits effectifs très contrôlés et les études observationnelles larges biaisées. La réalité est beaucoup plus nuancée. L’idée classique selon laquelle les essais contrôlés randomisés ne concernent pas la population réelle est parfois erronée : lors de la pandémie, de nombreux essais cliniques randomisés contrôlés en ouvert, appelés « essais cliniques pragmatiques » incluaient de larges populations, hétérogènes, et donc plus représentatives de la population générale. Le terme d’études observationnelles comme étant des études en vie réelle est également impropre, car de nombreuses études observationnelles sont très sélectives, et sujettes à d’importants biais de confusion. L’exemple ultime, faisant le pont entre les essais cliniques et les études observationnelles, est celui des essais cliniques émulés basés sur des données observationnelles. |
La validité externe5 représente la façon dont les résultats de l’essai clinique peuvent être généralisés à une population plus large [6].
L’évaluation des bénéfices dans le cadre d’un essai contrôlé randomisé est l’unique moyen d’éviter les biais de sélection et de confusion [7]. C’est dans ce cadre que les vaccins à ARNm contre la Covid-19 ont prouvé sans équivoque leur efficacité pour réduire l’incidence des formes symptomatiques de la Covid-19 [8, 9], permettant leur dispensation à grande échelle dans la population générale au début de l’année 2021. À l’inverse, les données recueillies en mars-avril 2020 sur l’utilisation de l’hydroxychloroquine pour traiter la Covid-19 présentaient un risque élevé de biais de confusion, en raison notamment de l’absence de groupe contrôle6 et de randomisation7. Dans ce cas, l’évolution clinique des patients pouvait résulter d’autres facteurs que le médicament testé, ce qui empêchait d’établir un lien de causalité. La présence d’un groupe contrôle, un placebo en général ou un comparateur actif, permet de prendre en compte l’évolution naturelle de la maladie, l’éventuel effet placebo8 et le phénomène de régression à la moyenne9, tandis que la randomisation permet de s’assurer que les individus inclus dans les groupes évalués soient sélectionnés au hasard et soient donc comparables. De fait, une méta-analyse10 publiée en 2021, qui a repris les résultats des essais contrôlés testant l’hydroxychloroquine, a rapporté un résultat opposé à celui de la communication initiale : une augmentation de 11 % de la mortalité chez les patients traités pour la Covid-19 avec de l’hydroxychloroquine. Ceci illustre l’importance absolue de respecter les principes rigoureux d’évaluation des médicaments, y compris en période de crise. Comprendre la nécessité de mener des essais cliniques avec une rigueur méthodologique absolue est un enjeu crucial, et a fait l’objet d’un livre blanc publié par la société française de pharmacologie et de thérapeutique [10].
Idéalement, l’objectif des essais cliniques devrait être l’évaluation de critères robustes, comme la mortalité ou la fréquence d’évènements graves. Pourtant, cette approche s’avère souvent irréalisable, en particulier pour des pathologies qui présentent un faible taux de mortalité ou d’évènements graves, car elle exigerait des délais beaucoup trop longs pour démontrer un effet. Dans ces situations, l’évaluation de l’essai clinique repose sur des critères de substitution11. À titre d’exemple, pour un essai contrôlé randomisé évaluant l’efficacité d’un vaccin contre la Covid-19 sur la base du taux de mortalité, le nombre de participants nécessaires était estimé entre 25 000 à plus de 5 millions, selon l’âge des sujets et le niveau de circulation du virus SARS-CoV-2 [11]. L’appliquer aurait entrainé un retard considérable dans la démonstration de l’efficacité du vaccin et de son bénéfice pour la population. On comprend donc que tous les essais cliniques évaluant l’efficacité des vaccins contre la Covid-19 aient recherché un bénéfice en termes de réduction des formes symptomatiques de Covid-19, plutôt qu’en termes de mortalité directement liée à l’infection [11]. La réduction de l’incidence des formes symptomatiques de Covid-19 a donc servi de critère de substitution pour évaluer le bénéfice du vaccin afin de ne pas retarder son déploiement dans la population. Ce choix repose sur une hypothèse de transitivité12 : les vaccins réduisent l’incidence des formes symptomatiques de Covid-19, ces formes symptomatiques sont corrélées avec les hospitalisations et les décès liés à la maladie, les vaccins réduisent donc les hospitalisations et les décès liés à la Covid-19 avec la même ampleur (Figure 2). Les données des essais cliniques et des études observationnelles montrent que cette hypothèse est vérifiée, l’efficacité des vaccins sur les formes sévères de Covid-19 étant même supérieure à celle sur les formes bénignes. Cependant, dans d’autres domaines médicaux, cette hypothèse de transitivité pour un critère de substitution peut être rejetée. L’un des meilleurs exemples est celui de la densité osseuse et du fluor dans le cas du traitement de l’ostéoporose : le fluor augmente la masse osseuse, mais il augmente aussi la fragilité du squelette et donc le nombre de fractures non vertébrales chez les femmes ménopausées [12]. Dans le cas du fluor, l’augmentation de la densité osseuse ne peut donc pas être utilisée pour évaluer le risque de fracture chez les femmes ménopausées. Il faut préciser que cette notion de critère de substitution est valable pour un médicament donné dans une indication donnée. Cela illustre la nécessité de valider rigoureusement la pertinence d’éventuels critères de substitution, qui peuvent parfois faire débat, comme les variations des taux de cholestérol dans le cas de l’évaluation de médicaments hypolipémiants.
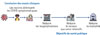 |
Figure 2 Objectifs de la vaccination contre la Covid-19. Les essais cliniques ont clairement montré que les vaccins contre la Covid-19 réduisaient l’incidence des Covid symptomatiques. L’hypothèse initiale au moment de leur mise sur le marché était qu’ils réduiraient également les hospitalisations et les décès dues à la Covid-19, ces deux paramètres étant corrélés à l’incidence des Covid symptomatiques. A posteriori, ceci s’est révélé vrai, toutes les données convergeant vers le fait que les vaccins permettaient de prévenir les formes sévères de Covid-19, avec une efficacité d’ailleurs supérieure à celle mesurée vis-à-vis des formes symptomatiques plus bénignes de la maladie. |
On comprend donc qu’un essai clinique nécessite de se poser au préalable une question clinique concernant le médicament. Ensuite, à partir de cette question, on pourra définir très précisément dans l’essai prévu quelles personnes le recevront, quelles modalités de traitement et de contrôle seront appliquées, comment ce médicament sera évalué, comment seront gérés les évènements survenant pendant l’étude, et quel outil statistique sera utilisé pour estimer l’effet. L’ensemble forme le concept d’estimand13.
La pharmacoépidémiologie
Les résultats d’efficacité obtenus lors des essais cliniques sont parfois complétés par des données issues des registres, des cohortes ou des données médico-administratives [13]. On ne parle alors pas d’efficacité du médicament, mais d’effectivité14 [3]. Cette méthodologie repose idéalement sur une randomisation de patients dans le cadre de leur prise en charge habituelle. On parle alors d’essais cliniques « pragmatiques » qui sont à la frontière entre les essais cliniques randomisés en double aveugle et les études pharmaco-épidémiologiques. Ces essais peuvent être réalisés à distance à l’aide de plateformes web, avec l’envoi des traitements par voie postale, on parle alors d’essais cliniques décentralisés.
Cependant, ces études sont le plus souvent non randomisées, et appelées « observationnelles », ce qui introduit des limites par rapport à la rigueur des essais cliniques randomisés contrôlés [14]. Un autre terme fréquemment employé est « études en vie réelle », qui est un terme impropre, car un essai clinique pragmatique est tout autant, voire plus, en vie réelle qu’une étude observationnelle cas-témoin où les cas sont sélectionnés. Dans tous les cas, les études observationnelles sont sujettes à d’importants biais potentiels, les plus fréquents étant les biais de sélection et de confusion. Voici un exemple simple illustrant ces limites : dans une population donnée, comparer l’évolution des individus vaccinés par rapport à celle des non-vaccinés pose un problème de base, car ces deux groupes ne seront jamais comparables. En effet, les non-vaccinés ont souvent moins accès aux soins médicaux généraux, sont plus jeunes, et surreprésentés dans les populations défavorisées, etc. (Figure 1). Si une différence est observée, elle peut donc résulter d’un facteur autre que le vaccin lui-même. Ce phénomène est contrôlé dans les essais cliniques grâce à la présence d’un groupe de contrôle et à la randomisation. L’essai ouvert non randomisé de mars 2020 sur l’hydroxychloroquine et l’azithromycine dans le traitement de la Covid-19 – dont la publication est aujourd’hui rétractée – est un exemple emblématique de biais de sélection. En effet, les patients ayant refusé le traitement, ceux exclus pour des critères spécifiques ou recrutés hors du centre principal, ont été utilisés comme groupe témoin, ce qui rend biaisée toute comparaison entre les groupes traité et non traité.
En pratique, cela implique qu’il faut tenter de rendre les groupes comparables dans les études observationnelles, en ajustant tous les facteurs susceptibles de modifier la progression de la maladie et sa prise en charge, ce qui est quasiment impossible à accomplir parfaitement. Pour s’en approcher, une des méthodes les plus utilisées consiste à utiliser un score de propension15, qui permet de comparer des patients ayant une probabilité similaire de recevoir le traitement, et qui réduit ainsi les biais de confusion et se rapproche des conditions de comparabilité d’un essai randomisé. Cependant, ce score ne corrige que les facteurs connus et mesurés, et des biais de confusion résiduels persistent inévitablement. L’effectivité d’un médicament doit donc toujours être interprétée à la lumière des résultats d’efficacité obtenus dans les essais cliniques.
Comment quantifier les bénéfices des médicaments ?
L’efficacité et l’effectivité sont des mesures du bénéfice des médicaments qui peuvent être exprimées en pourcentage de réponse au traitement. Par exemple, le premier essai clinique évaluant un vaccin contre la Covid-19 rapportait une protection contre la forme symptomatique de la Covid-19 avec une efficacité de 95 % [8]. Ce chiffre indique la proportion d’évènements évités dans le groupe de sujets vaccinés : ainsi, dans le groupe vacciné, 95 % des participants ont évité une forme symptomatique de Covid-19, ce qui est considérable. Ce paramètre est plus facile à comprendre pour le grand public que le risque relatif, même s’il s’agit d’une autre façon d’exprimer les mêmes données. Il a l’avantage principal de caractériser l’effet du médicament et de ne pas dépendre de l’incidence des maladies, ici l’incidence de la Covid-19, ou d’autres risques, comme l’âge [15].
Une fois le bénéfice relatif démontré, l’impact de ce bénéfice en santé publique peut être évalué par le nombre de sujets à traiter (ou le nombre de sujets à vacciner)16. Celui-ci correspond au nombre moyen de patients qui doivent recevoir le nouveau traitement pendant une période donnée, plutôt que le traitement contrôle, pour qu’un patient supplémentaire en tire un bénéfice. Il s’agit là du bénéfice absolu du traitement [16]. À première vue, le nombre nécessaire de sujets à traiter semble intuitivement très compréhensible : nous devons traiter x patients pour éviter un évènement chez un patient supplémentaire. Cependant, le diable se cache dans les détails : penser qu’on puisse donner un nombre unique est une erreur, car ce nombre ne dépend pas seulement des propriétés intrinsèques du médicament, mais également des caractéristiques de la population traitée [17, 18]. En effet, le nombre de sujets à traiter va représenter le bénéfice absolu du traitement pour une durée donnée chez un public spécifique et dans un contexte de risque précis. Son utilisation doit donc tenir compte de plusieurs problèmes. Il existe tout d’abord un problème mathématique lorsque l’intervalle de confiance de la réduction du risque absolu inclut la valeur zéro17 [19]. Deuxièmement, cette approche néglige souvent la dimension temporelle, c’est-à-dire le fait que le nombre de patients à traiter évolue dans le temps, notamment dans le cas des maladies chroniques, pour lesquelles il doit être défini pour une durée de traitement précise. Troisièmement, pour tous les traitements préventifs, comme c’est le cas des vaccins, le nombre nécessaire de sujets à traiter intègre intrinsèquement l’incidence de la maladie dans son calcul [20]. Ainsi, le nombre de sujets à vacciner pour éviter un évènement supplémentaire est inversement corrélé au taux d’incidence de la Covid-19, et suit une courbe de décroissance exponentielle, on est donc très loin d’un chiffre unique [21]. Inversement, la réduction du risque relatif ne dépend pas de l’incidence de la maladie, il s’agit donc d’une mesure stable du bénéfice relatif du médicament, indépendamment de l’incidence de la Covid-19. Si l’on simplifie, un médicament peut être extrêmement efficace, mais n’aura strictement aucun impact si le risque de développer la maladie est nul, comme c’est le cas avec le vaccin contre la variole.
Prendre en compte le temps pour évaluer le bénéfice d’un médicament
Pour évaluer pleinement le bénéfice d’un médicament, il faut aussi tenir compte d’un facteur : la durée d’exposition à ce médicament et/ou la période de suivi après l’exposition. Dans l’exemple, déjà cité du premier vaccin à ARNm contre la Covid-19, son efficacité contre les formes symptomatiques était de 95 % durant les deux premiers mois [8], mais diminuait à 84 % sur environ 6 mois [22]. Si l’on considère l’ensemble des vaccins contre la Covid-19, on observe une baisse de 20 à 30 % de leur efficacité contre les formes symptomatiques à 6 mois [23]. En revanche, cette baisse d’efficacité est nettement moins marquée, d’environ 10 %, contre les formes graves de Covid-19 (c’est-à-dire celles nécessitant une hospitalisation). Cette perte d’efficacité n’est pas attribuable à l’émergence de variants de SARS-Cov-2, mais à une diminution de la protection vaccinale au cours du temps, ce qui justifie les rappels vaccinaux. Cet exemple montre que l’évaluation du bénéfice d’un médicament dépend étroitement de la durée de suivi et de la période d’exposition pour les traitements chroniques.
Évaluer les risques liés aux médicaments
Évènement indésirable ou effet indésirable ?
Tous les évènements consécutifs à la prise d’un médicament ne sont pas forcément liés à celui-ci. Le terme « évènements indésirables » regroupe ceux consécutifs temporellement à la prise du médicament, sans obligation d’un lien de causalité. Voici un exemple pour illustrer ce propos : le fait de recevoir un grêlon sur la tête en sortant d’une pharmacie juste après une vaccination n’a aucun lien avec le vaccin, bien qu’il existe une association temporelle très claire. Dans ce cas, la réception d’un grêlon sur la tête constitue un évènement indésirable survenu après la vaccination, mais sans lien de causalité. L’imputabilité18 de cet évènement au vaccin est donc peu probable (Figure 3). En pratique, cependant, établir ou écarter un lien de causalité à partir d’un cas isolé s’avère complexe, ce qui souligne toute l’importance de l’expertise en pharmacovigilance19. Aussi, l’évaluation d’un lien de causalité entre un médicament et un évènement indésirable repose sur l’analyse exhaustive de l’ensemble des preuves disponibles, qu’elles soutiennent ou non ce lien. La conclusion d’un lien de causalité est donc la suivante : dès lors qu’il existe au moins une possibilité raisonnable que le médicament soit à l’origine de l’évènement, celui-ci est alors considéré comme un effet indésirable médicamenteux20 [24]. L’évaluation de la causalité des effets indésirables médicamenteux est une mission essentielle de la pharmacovigilance. Pour y parvenir, plusieurs méthodes sont disponibles, basées sur l’appréciation globale par des experts, sur des approches algorithmiques, ou des modèles probabilistes [25, 26].
 |
Figure 3 Comment déterminer l’imputabilité des évènements indésirables associés temporellement à l’administration d’un médicament ? L’évaluation de l’imputabilité est nécessaire pour définir qu’un effet indésirable est dû à la prise d’un médicament. Dans cet exemple, la chute d’un grêlon sur la tête d’un individu après sa vaccination est un évènement indésirable, mais pas un effet indésirable lié à la prise du médicament. En revanche, la survenue d’un érythème au point d’injection dans les jours suivant une vaccination est imputable au médicament basé sur des critères chronologiques et sémiologiques. Cependant, déterminer si un évènement grave survenant à distance de la vaccination est lié au vaccin peut rarement être déterminé à partir d’un cas isolé et nécessite une analyse plus poussée. |
Quantifier les risques liés aux médicaments
Nous avons vu que les essais cliniques sont réalisés pour démontrer les bénéfices des médicaments. Par essence, ces essais permettent d’estimer correctement l’incidence des évènements indésirables observables, donc ceux étant fréquents. Cette estimation est en effet directement liée à la taille du groupe de patients traités dans le cadre de l’essai clinique. On considère qu’un évènement indésirable survenant avec une fréquence de 1/n (n étant le nombre de participants) a 95 % de chances d’être détecté au moins une fois si le groupe traité inclut 3n participants (c’est ce que l’on appelle la règle de trois) [27]. Ceci signifie que, pour détecter un effet indésirable rare comme un évènement survenant avec une fréquence de 1/1000, il faut inclure 3 000 patients dans le groupe traité. Une complexité supplémentaire est que cette règle est valable à la condition que l’évènement ne puisse pas se produire spontanément en l’absence du médicament. Dans tous les cas, l’observation d’un tel évènement ne suffit pas à conclure qu’il s’agit d’un effet indésirable du médicament. Pour établir ce lien, nous devons soit identifier un cas index chez lequel l’imputabilité est très probable, soit démontrer que la fréquence de l’évènement est significativement plus élevée dans le groupe traité que dans le groupe témoin [28]. Par exemple, les vaccins à ARNm contre la Covid-19 ont été évalués dans le cadre d’essais cliniques de grande envergure, incluant plusieurs dizaines de milliers de participants. Ces études ont permis de mettre en évidence rapidement une réactogénicité fréquente, notamment des douleurs locales au point d’injection et des symptômes généraux transitoires (fatigue, maux de tête, fièvre, courbatures), survenant dans les 48 h suivant la vaccination. En revanche, les effets indésirables rares, comme l’anaphylaxie (5 cas/million [29, 30]) ou la myocardite (4,7 cas/100 000 pour les jeunes adultes âgés de 18 à 24 ans [31]) n’ont pas pu être détectés dans les essais cliniques, en raison de leur très faible fréquence. Ceci signifie qu’une fois le médicament approuvé, l’évaluation de sa sécurité repose sur surveillance continue, fondée sur la collecte et l’analyse des notifications spontanées d’effets indésirables, qui est assurée en France par les centres régionaux de pharmacovigilance [32].
La pharmacovigilance génère de nombreux signaux qui nécessitent une évaluation approfondie avant d’envisager un éventuel lien de causalité. Plusieurs situations peuvent se présenter. Dans certains cas, ce lien est établi grâce à des cas index ou « cas marquants », c’est-à-dire lorsqu’un ou plusieurs cas, analysés sur la base d’arguments cliniques et chronologiques solides, suffisent pour confirmer la causalité, en l’absence de diagnostic différentiel plausible. L’exemple emblématique est celui de la thrombose thrombocytopénique induite par le vaccin Vaxzevria® d’AstraZeneca, développé sur une plateforme adénovirale [33]. Le premier cas rapporté de thrombose thrombocytopénique était un évènement grave et rare, caractérisé par une présentation clinique très spécifique, survenue 5 jours après la vaccination. Dès que d’autres cas similaires ont été signalés avec les mêmes caractéristiques, des mesures de minimisation des risques ont pu être mises en place rapidement. Cette approche est valable dans le cas d’évènements très spécifiques, néanmoins très peu d’effets indésirables peuvent être exclusivement attribuables aux médicaments. De plus, lorsqu’un médicament est administré à une large population, toutes les maladies qui auraient pu survenir naturellement dans cette population, même en l’absence du traitement, seront observées pendant la période de suivi. C’est le cas pour tous les médicaments prescrits dans des maladies chroniques, comme les statines ou les inhibiteurs de la pompe à proton. Pour distinguer les effets réels du médicament, il est alors nécessaire de comparer les effets indésirables observés, à ceux attendus en l’absence de traitement pendant la même période. C’est l’objet des études « cas observéscas attendus »21 qui permettent une détection précoce des signaux [34]. Ces études doivent cependant être interprétées avec prudence, car elles sont soumises à un biais de sous-notification, surtout pour des évènements non graves, et à des biais de mesure concernant l’incidence réelle de la maladie dans les cohortes. Ces études sont généralement complétées par des études pharmacoépidémiologiques, qui s’appuient sur des bases de données médico-administratives.
Introduire la notion d’un risque variable selon la population exposée
Les risques liés à un médicament dépendent à la fois du patient (son âge, son sexe, ses comorbidités…) et de la pathologie traitée. Prenons l’exemple de l’hydroxychloroquine, médicament ancien et connu pour allonger l’intervalle QT22 et classé parmi les traitements pouvant conduire à une arythmie ventriculaire par torsade de pointe23. Ce risque était connu bien avant la pandémie de Covid-19, mais considéré comme faible dans la population cible, constituée par les personnes souffrant de lupus érythémateux systémique [35], ce qui a conduit à une extrapolation erronée de sa sécurité cardiaque dans le contexte de la Covid-19. Or, le lupus érythémateux touche principalement des femmes en âge de procréer, et suivies par des médecins internistes formés à repérer les patients à risque, en particulier d’atteinte cardiaque. Dans ce cadre l’iatrogénie24 cardiaque est donc très rare. En revanche, chez des patients présentant des formes symptomatiques de Covid-19, la présence, fréquente, d’une hypokaliémie25 et d’atteintes cardiaques augmente considérablement le risque de troubles du rythme ventriculaire, que la prise d’hydroxychloroquine vient alors aggraver. Ceci explique pourquoi, contrairement à son utilisation dans les cas de lupus, une surmortalité de 11 % a été observée chez les patients Covid-19 traités par hydroxychloroquine [36]. Ceci montre que le risque d’un médicament, établi dans une population et pour une indication donnée, ne peut pas être extrapolé à une autre population et pour une autre indication sans évaluation spécifique.
Gérer les interactions médicamenteuses
La Covid-19 nous fournit aussi un bon exemple de la gestion des interactions médicamenteuses dans le cadre de la balance bénéfices-risques des médicaments26. Le premier traitement antiviral oral efficace contre la Covid-19, comporte du ritonavir, un antiviral qui inhibe une enzyme de biotransformation de nombreux médicaments, le cytochrome P450 3A427. Le ritonavir est utilisé depuis plus de vingt ans dans le cadre de l’infection par le virus de l’immunodéficience humaine (VIH), parce qu’il augmente la demi-vie28 et les concentrations d’autres antiviraux plus puissants. Dans le contexte de la Covid-19, la problématique rencontrée était que les patients à risque de formes graves étaient des personnes âgées prenant de nombreux médicaments, ce qui augmentait le risque d’interactions médicamenteuses. La publication d’un guide de gestion des interactions médicamenteuses par la société française de pharmacologie et de thérapeutique et la mobilisation des pharmacologues cliniciens a permis l’usage encadré et généralisé de ce médicament [37]. Bien que des interactions médicamenteuses se soient produites, leur incidence fut limitée, et principalement liée à une surexposition aux traitements immunosuppresseurs [38].
Équilibrer les bénéfices et les risques des médicaments. Une approche graphique ?
Jusqu’à présent, la quantification des bénéfices et des risques des médicaments a été abordée séparément. La question est de savoir comment les mettre en balance, et donc comment disposer d’une unité de mesure commune pour évaluer le bénéfice et le risque. Une façon simple serait de démontrer qu’un médicament diminue la mortalité. Dans ce cas, le bénéfice (i.e. la réduction de la mortalité grâce au traitement) et le risque (i.e. les décès liés au médicament) sont quantifiés avec la même unité de mesure. Dès lors que la mortalité est réduite, il suffit de décrire quels sont les effets indésirables à gérer pour bénéficier de cette réduction. C’est le cas pour de nombreux anticancéreux, comme les inhibiteurs de point de contrôle immunitaire. Cependant, pour la majorité des médicaments, l’impact sur la mortalité n’est pas disponible au moment de leur mise sur le marché, soit parce que la maladie traitée est peu mortelle, soit parce que le temps nécessaire pour observer une baisse de la mortalité est beaucoup trop long, comme ce fut le cas pour l’évaluation des vaccins contre la Covid-19.
L’Agence européenne des médicaments et la Food and Drug Administration s’appuient sur des évaluations d’experts pour déterminer cette balance des bénéfices et des risques [39, 40], il s’agit donc d’une analyse qualitative. En effet, quantifier cette balance pose problème : le bénéfice absolu d’un médicament préventif dépend à la fois de l’incidence de la maladie et des caractéristiques de la population exposée, alors que le risque lié au médicament, lui, reste constant pour une population donnée, puisqu’il est directement lié à l’exposition au médicament. Pour illustrer le concept de population exposée, prenons l’exemple de l’âge : le bénéfice absolu d’un vaccin contre la Covid-19 sera moins marqué chez le sujet jeune que chez le sujet âgé. Autrement dit, il faudra vacciner moins de sujets âgés pour éviter un évènement. Ce qui rend cette notion complexe est que certains risques dépendront de l’âge, dans un sens ou dans l’autre. Par exemple, les myocardites induites par les vaccins à ARNm contre la Covid-19 sont plus fréquentes chez les jeunes adultes. Cependant, au sein des jeunes adultes, ce risque est prépondérant chez les hommes par rapport aux femmes. Pour évaluer la balance bénéfices-risques, il est donc indispensable de considérer à la fois l’âge et le sexe. Mais la difficulté s’accroît encore, parce qu’il n’y a pas de règle et que chaque médicament a ses propres spécificités. Par exemple, pour le vaccin vivant atténué contre le chikungunya, le risque que le vaccin induise des symptômes semblables à ceux provoqués par la primo-infection par le virus chikungunya est corrélé à l’âge, mais pas au sexe. Ainsi, dans la majorité des cas, il n’est donc pas possible de donner un chiffre unique pour quantifier la balance bénéfices-risques. En conséquence, envisager une balance bénéfices-risques unique relève d’une approche simpliste et erronée et différents scénarios, adaptés à chaque médicament et à chaque population traitée, doivent être envisagés.
Des approches graphiques utilisant des smileys ont été utilisées pour représenter visuellement les avantages et les risques des médicaments, comme pour le traitement par la dexaméthasone utilisé pendant la pandémie de Covid-19 [41]. L’Agence européenne des médicaments a aussi proposé une approche graphique très pédagogique pour représenter la balance bénéfice-risque du vaccin Vaxzevria® contre la Covid-19, vaccin à adénovirus qui n’est plus utilisé [42]. Celle-ci prend justement en compte différentes hypothèses d’incidence de cas de Covid-19 mensuelle : faible (55 cas pour 100 000 personnes), moyenne (401 cas pour 100 000 personnes) et élevée (886 cas pour 100 000 personnes), correspondant à différentes hypothèses de circulation virale. Nous avons combiné et remanié ces données pour proposer une approche graphique condensée (Figure 4), où le bénéfice est décrit à la fois par la baisse des hospitalisations et des décès liés à la Covid-19, et le risque caractérisé par l’incidence de thromboses thrombocytopéniques associées au vaccin. Cette approche permet d’élaborer différents scénarios, en prenant en compte la variation du nombre de cas de Covid-19 et l’âge. Bien qu’imparfaite, cette représentation graphique de la balance bénéfices-risques est précise, car elle introduit la notion de variabilité en fonction des différents scénarios, c’est-à-dire qu’elle montre clairement que la balance bénéfices-risques n’est pas unique, mais va dépendre de l’âge, de la circulation virale et de la gravité de l’effet indésirable. Cette approche a également été utilisée rétrospectivement pour évaluer les bénéfices et les risques des vaccins à ARNm contre la Covid-19. L’énorme avantage de cette analyse rétrospective est qu’elle peut utiliser les incidences réelles de la maladie, donc faire un bilan factuel, cependant elle ne permet pas de prédire la balance bénéfices-risques [43]. D’autres outils ont été proposés pour fournir une évaluation quantitative de la balance bénéfices-risques, tels que le bénéfice net du traitement, en particulier en oncopharmacologie [44], ou dans une moindre mesure le ratio de gains (win ratio) [45].
 |
Figure 4 Illustration graphique de l’approche utilisée pour évaluer les bénéfices et risques du vaccin adénoviral contre la Covid Vaxzevria®. Le bénéfice absolu correspond au nombre d’hospitalisations et de décès, liés à la Covid-19, évités tel qu’estimé sur la base des essais cliniques. Le risque est déterminé par la notification d’un syndrome rare et grave, la thrombose thrombocytopénique, identifié grâce à la pharmacovigilance. Plusieurs scénarios sont décrits, selon un taux d’infection mensuel variant entre un taux élevé (886 Covid pour 100 000 personnes) et un taux faible (55 Covid pour 100 000 personnes). On observe que la balance bénéfices-risques varie fortement selon l’incidence de la maladie et l’âge de population exposée. |
Vers une pharmacologie sociale
L’évaluation de la balance bénéfices-risques des médicaments est donc un processus dynamique. Elle englobe l’analyse continue et concomitante des données des essais cliniques, du suivi de la pharmacovigilance, et des études pharmacoépidémiologiques de sécurité. Ceci signifie qu’au cours de la vie du médicament, l’évaluation de la balance bénéfices-risques est nécessairement associée à un certain niveau d’incertitude, qui décroît avec le temps. Cette incertitude, associée à la génération d’indicateurs multiples, est par essence troublante et complexe à comprendre pour le grand public, et peut être source d’hésitation thérapeutique.
L’évaluation de la balance bénéfices-risques des médicaments doit donc aussi prendre en compte des considérations sociétales. Avant la pandémie de Covid-19, les mesures nécessaires pour lutter contre la désinformation propagée par les réseaux sociaux ont été bien décrites. Elles comprennent l’identification des tendances émergentes et de la prévalence de la désinformation en matière de santé, la compréhension de sa distribution dans la communauté, l’évaluation de son impact sur la santé et le développement de contre-mesures [46]. Dans les premières phases de la crise de la pandémie de Covid-19, il y a eu non seulement une forte augmentation de la recherche d’informations, mais aussi une demande accrue pour des traitements contre la Covid-19 non vérifiés et potentiellement nocifs. Face à cette situation, les autorités sanitaires et les sociétés savantes se sont mobilisées pour produire et diffuser une information publique fiable et accessible sur les médicaments [47].
Alors que la couverture vaccinale se stabilisait et que l’hésitation vaccinale progressait, les autorités de santé de nombreux pays ont envisagé des mesures coercitives, comme les passeports de santé. En France, le 12 juillet 2021, le président de la République a annoncé l’instauration d’un passe sanitaire, obligeant les individus à présenter une preuve de vaccination ou un test négatif pour accéder à diverses activités quotidiennes. Cette politique a permis une augmentation considérable des taux de vaccination, passant de 39 % en juin 2021 à 75 % en octobre 2021 [48] (Figure 5). Cette mesure a en parallèle incité de nombreuses personnes, jusqu’alors réticentes ou inquiètes face à la vaccination, à se faire vacciner. On a alors constaté que plus les personnes étaient hésitantes, plus elles rapportaient des évènements qu’elles jugeaient indésirables, et des impacts négatifs sur leurs activités quotidiennes. Cette observation est troublante, car une fréquence identique d’évènements indésirables ressentis aurait dû être observée dans le temps si ceux-ci étaient liés au vaccin ([49], Figure 5). Deux hypothèses peuvent expliquer ce phénomène : un effet de l’hésitation vaccinale sur la propension à déclarer des effets indésirables réels et/ou une incidence plus élevée des effets nocebo29 chez les personnes réticentes à la vaccination.
 |
Figure 5 Évolution en 2021 du niveau d’adhésion (ligne verte) et d’hésitation (ligne rouge) vis-à-vis du vaccin contre la Covid-19, et proportion des sondés rapportant des effets indésirables (ligne noire). Les doutes sur la vaccination chez les adultes français vaccinés, en fonction du mois au cours duquel ils ont reçu leur première dose, sont exprimés en pourcentage sur un échantillon représentatif de 2015 personnes âgées de plus de 18 ans. En dessous, la ligne noire en pointillés décrit, après la vaccination, les évènements indésirables qu’ils considèrent comme graves. Si ces évènements étaient des effets indésirables dus au médicament, cette ligne devrait être horizontale, avec un pourcentage constant. Cependant, celle-ci augmente au cours du temps en parallèle d’une moindre adhésion à la vaccination, ce qui suggère l’existence d’un effet nocebo. |
En conclusion, l’information et l’éducation du grand public sur les médicaments et l’évaluation de leur balance bénéfices-risques sont impératives. Celles-ci doivent s’appuyer sur les pharmacologues, spécialistes du médicament, qui ont pour mission d’analyser de manière critique et indépendante la balance bénéfices-risques des médicaments, afin de promouvoir la démocratie en santé. Jamais dans l’histoire moderne, les données d’efficacité et de sécurité d’un médicament n’ont été aussi transparentes que celles fournies sur les vaccins contre la Covid-19. Pourtant, leur interprétation est restée confuse par une partie du grand public parce qu’elle est complexe. Par la formation et l’information, notre rôle, essentiel, est donc d’aider le grand public à comprendre et interpréter correctement la balance bénéfices-risques des médicaments et à se prémunir contre la désinformation.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Mackey TK, Purushothaman V, Haupt M, et al. Application of unsupervised machine learning to identify and characterise hydroxychloroquine misinformation on Twitter. Lancet Digit Health 2021 ; 3 : e72–5. [Google Scholar]
- Molimard M, Costagliola D, Maisonneuve H. Information en santé. Bilan des forces et des faiblesses. Recommandations pour une stratégie nationale d’information et de lutte contre la désinformation en santé. 2026 ; https://sante.gouv.fr/IMG/pdf/rapport_information.pdf. [Google Scholar]
- Flay BR. Efficacy and effectiveness trials (and other phases of research) in the development of health promotion programs. Prev Med 1986 ; 15 : 451–74. [Google Scholar]
- Selker HP, Eichler H, Stockbridge NL, et al. Efficacy and effectiveness too trials: clinical trial designs to generate evidence on efficacy and on effectiveness in wide practice. Clin Pharmacol Ther 2019 ; 105 : 857–66. [Google Scholar]
- Hardelin JP. Facteur « confondant » ou de confusion. Med Sci (Paris) 2024 ; 40 : 381–1. [CrossRef] [EDP Sciences] [Google Scholar]
- Sedgwick P. External and internal validity in clinical trials. BMJ 2012 ; 344 : e1004. [Google Scholar]
- Collins R, Bowman L, Landray M, et al. The magic of randomization versus the myth of real-world evidence. N Engl J Med 2020 ; 382 : 674–8. [Google Scholar]
- Polack FP, Thomas SJ, Kitchin N, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine. N Engl J Med 2020 ; 383 : 2603–15. [CrossRef] [PubMed] [Google Scholar]
- Baden LR, Sahly HME, Essink B, et al. Efficacy and safety of the mRNA-1273 SARS-CoV-2 vaccine. N Engl J Med 2020 ; 384 : 403–16. [Google Scholar]
- Société Française de Pharmacologie et de Thérapeutique. Livre blanc. De la nécessité de la méthodologie dans l’évaluation des médicaments. https://sfpt-fr.org/livreblancmethodo/index.htm [Google Scholar]
- Hodgson SH, Mansatta K, Mallett G, et al. What defines an efficacious COVID-19 vaccine? A review of the challenges assessing the clinical efficacy of vaccines against SARS-CoV-2. Lancet Infect Dis 2021 ; 21 : e26–35. [Google Scholar]
- Riggs BL, Hodgson SF, O’Fallon WM, et al. Effect of fluoride treatment on the fracture rate in postmenopausal women with osteoporosis. N Engl J Med 1990 ; 322 : 802–9. [Google Scholar]
- Sarri G, Patorno E, Yuan H, et al. Framework for the synthesis of non-randomised studies and randomised controlled trials: a guidance on conducting a systematic review and meta-analysis for healthcare decision making. BMJ Evid Based Med 2022 ; 27 : 109–19. [Google Scholar]
- Sommet A, Pariente A. Methods in pharmacoepidemiology. Therapie 2019 ; 74 : 187–97. [Google Scholar]
- Furukawa TA, Guyatt GH, Griffith LE. Can we individualize the ‘number needed to treat’? An empirical study of summary effect measures in meta-analyses. Int J Epidemiol 2002 ; 31 : 72–6. [Google Scholar]
- Laupacis A, Sackett DL, Roberts RS. An assessment of clinically useful measures of the consequences of treatment. N Engl J Med 1988 ; 318 : 1728–33. [Google Scholar]
- Correia LCL, Matias D. COVID-19 vaccines: effectiveness and number needed to treat. Lancet Microbe 2021 ; 2 : e281. [Google Scholar]
- Olliaro P, Torreele E, Vaillant M. COVID-19 vaccine efficacy and effectiveness-the elephant (not) in the room. Lancet Microbe 2021 ; 2 : e279–80. [Google Scholar]
- Christensen PM, Kristiansen IS. Number-needed-to-treat (NNT) – needs treatment with care. Basic Clin Pharmacol Toxicol 2006 ; 99 : 12–6. [Google Scholar]
- Montastruc J, Biron P, Sommet A. Efficacy of COVID-19 vaccines: Several modes of expression should be presented in scientific publications. Fundam Clin Pharmacol 2022 ; 36 : 218–20. [Google Scholar]
- Adams K, Riddles JJ, Rowley EAK, et al. Number needed to vaccinate with a COVID-19 booster to prevent a COVID-19-associated hospitalization during SARS-CoV-2 Omicron BA.1 variant predominance, December 2021-February 2022, VISION Network: a retrospective cohort study. Lancet Reg Health Am 2023 ; 23 : 100530. [Google Scholar]
- Thomas SJ, Moreira ED, Kitchin N, et al. Safety and efficacy of the BNT162b2 mRNA Covid-19 vaccine through 6 Months. N Engl J Med 2021 ; 383 :2603–15. [Google Scholar]
- Feikin DR, Higdon MM, Abu-Raddad LJ, et al. Duration of effectiveness of vaccines against SARS-CoV-2 infection and COVID-19 disease: results of a systematic review and meta-regression. Lancet 2022 ; 399 : 924–44. [Google Scholar]
- CIOMS Cumulative Glossary, with a focus on Pharmacovigilance (version 2.1). Counc Int Organ Med Sci https://cioms.ch/wpcontent/uploads/2023/04/CIOMSGlossary_v2.1_1stMay2023.pdf [Google Scholar]
- The use of the WHO-UMC system for standardised case causality assessment https://www.who.int/docs/default-source/medicines/pharmacovigilance/whocausality-assessment.pdf [Google Scholar]
- Miremont-Salamé G, Théophile H, Haramburu F, et al. Causality assessment in pharmacovigilance: the French method and its successive updates. Therapie 2016 ; 71 : 179–86. [Google Scholar]
- Onakpoya IJ. Rare adverse events in clinical trials: understanding the rule of three. BMJ Evid Based Med 2018 ; 23 : 6. [Google Scholar]
- Berlin JA, Glasser SC, Ellenberg SS. Adverse event detection in drug development: recommendations and obligations beyond phase 3. Am J Public Health 2008 ; 98 : 1366–71. [Google Scholar]
- Shimabukuro TT, Cole M, Su JR. Reports of anaphylaxis after receipt of mRNA COVID-19 vaccines in the US-December 14, 2020-January 18, 2021. JAMA 2021 ; 325 : 1101. [CrossRef] [PubMed] [Google Scholar]
- Shimabukuro T, Nair N. Allergic reactions including anaphylaxis after receipt of the first dose of Pfizer-BioNTech COVID-19 Vaccine. JAMA 2021 ; 325 :780–1. [Google Scholar]
- Le Vu S, Bertrand M, Jabagi M-J, et al. Age and sex-specific risks of myocarditis and pericarditis following Covid-19 messenger RNA vaccines. Nat Commun 2022 ; 13 : 3633. [Google Scholar]
- Salmon DA, Chen RT, Black S, et al. Lessons learned from COVID-19, H1N1, and routine vaccine pharmacovigilance in the United States: a path to a more robust vaccine safety program. Expert Opin Drug Saf 2024 ; 23 : 161–75. [Google Scholar]
- Greinacher A, Thiele T, Warkentin TE, et al. Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med 2021 ; 384 : 2092–101. [CrossRef] [PubMed] [Google Scholar]
- Shimabukuro T. COVID-19 Vaccine safety updates. CDC Gov 2021 ; https://stacks.cdc.gov/view/cdc/108329 [Google Scholar]
- Lo CH, Wang YH, Tsai CF, et al. Association of hydroxychloroquine and cardiac arrhythmia in patients with systemic lupus erythematosus: A population-based case control study. PLoS One 2021 ; 16 : e0251918. [Google Scholar]
- Axfors C, Schmitt AM, Janiaud P, et al. Mortality outcomes with hydroxychloroquine and chloroquine in COVID-19 from an international collaborative meta-analysis of randomized trials. Nat Commun 2021 ; 12 : 2349. [Google Scholar]
- Lemaitre F, Grégoire M, Monchaud C, et al. Management of drug-drug interactions with nirmatrelvir/ritonavir in patients treated for Covid-19: Guidelines from the French Society of Pharmacology and Therapeutics (SFPT). Therapie 2022 ; 77 : 509–21. [Google Scholar]
- Bihan K, Lipszyc L, Lemaitre F, et al. Nirmatrelvir/ritonavir (Paxlovid®): French pharmacovigilance survey 2022. Therapie 2023 ; 78 : 531–47. [Google Scholar]
- Benefit-risk methodology – European Medicines Agency. https://www.ema.europa.eu/en/documents/report/benefit-risk-methodology-project-work-package-2-report-applicability-current-tools-and-processes-regulatory-benefit-risk-assessment_en.pdf [Google Scholar]
- Benefit-Risk Assessment for New Drug and Biological Products. 2023. https://www.fda.gov/ regulatory-information/search-fda-guidance-documents/benefit-risk-assessment-new-drug-and-biological-products [Google Scholar]
- Covid-19. Dr Chris Cates’ EBM Website 2020. https://www.nntonline.net/topics/covid-19/ [Google Scholar]
- European Medicines Agency. Annex to Vaxzevria Art.5.3 – Visual risk contextualisation. https://www.ema.europa.eu/en/documents/chmp-annex/annex-vaxzevria-art53-visual-risk-contextualisation_en.pdf [Google Scholar]
- Bozkurt B, Kamat I, Hotez PJ. Myocarditis with COVID-19 mRNA vaccines. Circulation 2021 ; 144 : 471–84. [Google Scholar]
- Buyse M, Saad ED, Peron J, et al. The net benefit of a treatment should take the correlation between benefits and harms into account. J Clin Epidemiol 2021 ; 137 : 148–58. [Google Scholar]
- Pocock SJ, Ariti CA, Collier TJ, et al. The win ratio: a new approach to the analysis of composite endpoints in clinical trials based on clinical priorities. Eur Heart J 2012 ; 33 : 176–82. [Google Scholar]
- Chou WYS, Oh A, Klein WMP. Addressing health-related misinformation on social media. JAMA 2018 ; 320 : 2417–8. [CrossRef] [PubMed] [Google Scholar]
- Larrouquere L, Gabin M, Poingt E, et al. Genesis of an emergency public drug information website by the French society of pharmacology and therapeutics during the COVID-19 pandemic. Fundam Clin Pharmacol 2020 ; 34 : 389–96. [Google Scholar]
- Ward JK, Gauna F, Gagneux-Brunon A, et al. The French health pass holds lessons for mandatory COVID-19 vaccination. Nat Med 2022 ; 28 : 232–5. [Google Scholar]
- Khouri C, Larabi A, Verger P, et al. Impact of vaccine hesitancy on onset, severity and type of self-reported adverse events: a french cross-sectional survey. Drug Saf 2022 ; 45 : 1049–56. [Google Scholar]
L’efficacité correspond au bénéfice d’un médicament observé dans une situation contrôlée et évalué lors d’un essai clinique.
L’autorisation de mise sur le marché (AMM), délivrée par les agences du médicament européenne (EMA : Agence européenne des médicaments) ou américaine (FDA : Food and Drug Administration), est une validation réglementaire fondée sur l’évaluation critique des données précliniques et cliniques. Elle certifie que la balance bénéfices-risques du médicament est favorable pour l’indication thérapeutique revendiquée, et se base sur des normes de qualité pharmaceutique, d’efficacité et de sécurité clinique.
L’infodémie est un mot créé pendant la pandémie de Covid-19. Il désigne une propagation, rapide et à large diffusion, d’un mélange d’informations à la fois exactes et inexactes sur un sujet (ndlr).
La validité interne correspond à l’assurance que les résultats observés sont bien dus au traitement étudié et non à d’autres facteurs, afin de pouvoir conclure à un lien de cause à effet.
La validité externe est la capacité à généraliser les résultats d’une étude menée sur un petit groupe à une population générale.
Un groupe contrôle dans un essai clinique est un groupe de participants ne recevant pas le traitement expérimental, mais un placebo ou un traitement standard.
La randomisation dans un essai clinique, ou tirage au sort, est une méthode qui répartit aléatoirement les participants entre les groupes traitement et contrôle et qui permet d’éviter les biais de sélection.
L’effet placebo est le phénomène observé avec un traitement sans principes actifs, mais qui produit une amélioration de l’état du patient en raison de l’attente ou de la croyance en son efficacité.
La régression à la moyenne est un phénomène statistique où l’estimation ponctuelle d’une variable sélectionnée par un seuil lors d’une première mesure tend à se rapprocher de sa véritable moyenne lors des mesures ultérieures. Par exemple, si un médecin trouve une mesure tensionnelle trop élevée au cabinet, il va demander une automesure tensionnelle. Il disposera alors d’environ 18 mesures à domicile. Ceci évitera que la première mesure, sélectionnée du fait qu’elle est supérieure au seuil de 140/90 mm Hg, soit prise pour la moyenne. Dans ce cas, la répétition des mesures permettra de déterminer la réelle pression artérielle sans sélection du fait d’un seuil.
La méta-analyse est une méthode statistique utilisée pour combiner et analyser les résultats de plusieurs essais cliniques indépendants abordant une question de recherche similaire. L’objectif est d’augmenter la puissance statistique et d’améliorer la précision de l’estimation de l’effet d’un traitement.
Un critère de substitution est un critère biologique ou clinique censé prédire un bénéfice clinique pour le patient, sans être une mesure directe de ce résultat. Par exemple, la tension artérielle est un critère de substitution des évènements cardiovasculaires chez l’hypertendu.
La transitivité est la propriété d’une relation où, si un premier élément est en relation avec un deuxième et que ce deuxième est en relation avec un troisième, alors le premier est aussi en relation avec le troisième.
Le concept complexe d’estimand correspond à une définition très précise de la quantité d’effet du traitement à estimer, qui formalise la question clinique tout en structurant la manière dont cette question sera traduite en une estimation statistique. L’utilisation du concept d’estimand est une avancée importante, car elle améliore la transparence et la pertinence des essais cliniques pour les cliniciens et les décideurs.
L’effectivité est le bénéfice observé d’un médicament dans des conditions aussi proches que possible du soin courant. On peut pour cela recourir à des essais cliniques dits « pragmatiques » ou encore à des études observationnelles.
En pharmacoépidémiologie, le score de propension est la probabilité qu’un individu reçoive un traitement donné. Il est calculé à partir de ses caractéristiques démographiques et cliniques mesurées avant l’initiation du traitement. Il permet de réduire le risque de biais de confusion en équilibrant la distribution des facteurs de confusion mesurés entre les groupes traités et non traités, rendant ainsi les groupes plus comparables et l’estimation de l’effet du traitement moins biaisée.
Le nombre de sujet à traiter est calculé comme l’inverse de la réduction absolue du risque.
Le problème est lié au fait que les estimateurs utilisés dans les essais cliniques sont exprimés en général par une moyenne et un indice de variabilité comme l’intervalle de confiance de la moyenne. Ce n’est pas possible pour le nombre de sujet à traiter dans le cas où l’intervalle de confiance de la réduction absolue du risque englobe zéro, car dans ce cas le nombre de sujets à traité est infini, et ceci pose problème en particulier pour les méta-analyses.
L’imputabilité est l’évaluation du lien de causalité possible entre un évènement indésirable médicamenteux et la prise de ce médicament.
La pharmacovigilance est l’activité de surveillance des effets indésirables des médicaments après leur mise sur le marché
Un effet indésirable médicamenteux est défini par toute réaction nocive et non souhaitée survenant après l’administration d’un médicament, qu’elle soit attendue on non. On évite d’utiliser le terme d’effet secondaire dans ce cadre, ce dernier terme étant moins spécifique, car il inclut aussi les effets bénéfiques non recherchés initialement.
Une étude cas observés-cas attendus en pharmacovigilance repose sur une méthode épidémiologique utilisée pour comparer le nombre de cas d’évènements indésirables observés après l’utilisation d’un médicament, au nombre de cas attendus dans une population non exposée, ce qui permet d’évaluer un éventuel lien de causalité. Les cas observés sont recueillis par la pharmacovigilance, les cas attendus sont estimés à partir de données épidémiologiques historiques.
L’intervalle QT est une mesure importante obtenue à partir d’un électrocardiogramme. Il représente la durée de la dépolarisation et de la repolarisation des ventricules cardiaques. Cette mesure est utilisée comme un indicateur clé pour le diagnostic et le suivi de certaines pathologies cardiaques (ndlr).
L’iatrogénie correspond à l’ensemble des conséquences néfastes pour la santé, qu’elles soient potentielles ou avérées, et qui résultent de l’utilisation d’un produit de santé, d’une intervention médicale ou d’un recours aux soins.
L’hypokaliémie désigne un taux de potassium dans le sang trop faible (ndlr).
Les interactions médicamenteuses se produisent lorsque l’effet d’un médicament est modifié par la présence d’un autre médicament ou d’un aliment, ce qui peut entraîner une augmentation ou une diminution de l’efficacité du médicament testé ou de sa toxicité.
Le cytochrome P450 3A4 (CYP3A4) est une enzyme hépatique du système des cytochromes P450, jouant un rôle majeur dans le métabolisme de nombreux médicaments, en facilitant leur biotransformation et par conséquent leur excrétion.
La demi-vie d’un médicament est le temps nécessaire pour que sa concentration dans le plasma soit diminuée de moitié.
Phénomène négatif survenant lorsqu’une personne ressent des effets indésirables ou une aggravation de ses symptômes en raison d’attentes négatives concernant un traitement ou une prise en charge thérapeutique
Liste des figures
 |
Figure 1 Différences entre les essais cliniques et les études observationnelles pour évaluer le bénéfice des médicaments. Classiquement, on oppose les essais cliniques randomisés contrôlés en double aveugle, réalisés sur de petits effectifs très contrôlés et les études observationnelles larges biaisées. La réalité est beaucoup plus nuancée. L’idée classique selon laquelle les essais contrôlés randomisés ne concernent pas la population réelle est parfois erronée : lors de la pandémie, de nombreux essais cliniques randomisés contrôlés en ouvert, appelés « essais cliniques pragmatiques » incluaient de larges populations, hétérogènes, et donc plus représentatives de la population générale. Le terme d’études observationnelles comme étant des études en vie réelle est également impropre, car de nombreuses études observationnelles sont très sélectives, et sujettes à d’importants biais de confusion. L’exemple ultime, faisant le pont entre les essais cliniques et les études observationnelles, est celui des essais cliniques émulés basés sur des données observationnelles. |
| Dans le texte | |
 |
Figure 2 Objectifs de la vaccination contre la Covid-19. Les essais cliniques ont clairement montré que les vaccins contre la Covid-19 réduisaient l’incidence des Covid symptomatiques. L’hypothèse initiale au moment de leur mise sur le marché était qu’ils réduiraient également les hospitalisations et les décès dues à la Covid-19, ces deux paramètres étant corrélés à l’incidence des Covid symptomatiques. A posteriori, ceci s’est révélé vrai, toutes les données convergeant vers le fait que les vaccins permettaient de prévenir les formes sévères de Covid-19, avec une efficacité d’ailleurs supérieure à celle mesurée vis-à-vis des formes symptomatiques plus bénignes de la maladie. |
| Dans le texte | |
 |
Figure 3 Comment déterminer l’imputabilité des évènements indésirables associés temporellement à l’administration d’un médicament ? L’évaluation de l’imputabilité est nécessaire pour définir qu’un effet indésirable est dû à la prise d’un médicament. Dans cet exemple, la chute d’un grêlon sur la tête d’un individu après sa vaccination est un évènement indésirable, mais pas un effet indésirable lié à la prise du médicament. En revanche, la survenue d’un érythème au point d’injection dans les jours suivant une vaccination est imputable au médicament basé sur des critères chronologiques et sémiologiques. Cependant, déterminer si un évènement grave survenant à distance de la vaccination est lié au vaccin peut rarement être déterminé à partir d’un cas isolé et nécessite une analyse plus poussée. |
| Dans le texte | |
 |
Figure 4 Illustration graphique de l’approche utilisée pour évaluer les bénéfices et risques du vaccin adénoviral contre la Covid Vaxzevria®. Le bénéfice absolu correspond au nombre d’hospitalisations et de décès, liés à la Covid-19, évités tel qu’estimé sur la base des essais cliniques. Le risque est déterminé par la notification d’un syndrome rare et grave, la thrombose thrombocytopénique, identifié grâce à la pharmacovigilance. Plusieurs scénarios sont décrits, selon un taux d’infection mensuel variant entre un taux élevé (886 Covid pour 100 000 personnes) et un taux faible (55 Covid pour 100 000 personnes). On observe que la balance bénéfices-risques varie fortement selon l’incidence de la maladie et l’âge de population exposée. |
| Dans le texte | |
 |
Figure 5 Évolution en 2021 du niveau d’adhésion (ligne verte) et d’hésitation (ligne rouge) vis-à-vis du vaccin contre la Covid-19, et proportion des sondés rapportant des effets indésirables (ligne noire). Les doutes sur la vaccination chez les adultes français vaccinés, en fonction du mois au cours duquel ils ont reçu leur première dose, sont exprimés en pourcentage sur un échantillon représentatif de 2015 personnes âgées de plus de 18 ans. En dessous, la ligne noire en pointillés décrit, après la vaccination, les évènements indésirables qu’ils considèrent comme graves. Si ces évènements étaient des effets indésirables dus au médicament, cette ligne devrait être horizontale, avec un pourcentage constant. Cependant, celle-ci augmente au cours du temps en parallèle d’une moindre adhésion à la vaccination, ce qui suggère l’existence d’un effet nocebo. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




