| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
Nos jeunes pousses ont du talent !
|
|
|---|---|---|
| Page(s) | 943 - 945 | |
| Section | Partenariat médecine/sciences - Écoles doctorales - Masters | |
| DOI | https://doi.org/10.1051/medsci/2025198 | |
| Published online | 12 December 2025 | |
Altération antibio-induite de l’immunité pulmonaire favorisant la surinfection post-grippale
Antibiotic-induced impairment of pulmonary immunity promoting secondary post-influenza infection
Master 2 Infectiologie, Immunité, Vaccinologie et Biomédicaments, Université de Tours, Tours, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
***
This email address is being protected from spambots. You need JavaScript enabled to view it.
La grippe est une infection virale saisonnière qui cause chaque année en France entre 8 000 et 15 000 décès selon Santé Publique France. Une part importante de ces formes graves est liée à des surinfections bactériennes secondaires, qui compliquent l’évolution de la maladie. Parmi les pathogènes impliqués, Staphylococcus aureus joue un rôle majeur, en particulier les souches résistantes à la méticilline (SARM), représentant près de 38 % des isolats identifiés [1, 2]. Pour prévenir ces complications, une antibioprophylaxie est fréquemment administrée aux patients grippés, même en l’absence de documentation bactérienne [1, 3]. Cependant, cette pratique a récemment été remise en question par une étude de Sanches Santos Rizzo Zuttion et al., utilisant un modèle murin d’infection séquentielle grippe-SARM. Les auteurs montrent que l’administration d’antibiotiques dans ce contexte peut paradoxalement affaiblir l’immunité pulmonaire et aggraver le risque d’infection bactérienne secondaire [1]. Les antibiotiques peuvent induire des surinfections en perturbant l’immunité des poumons, une perturbation qui serait liée au microbiote intestinal.
Les antibiotiques favorisent une surinfection bactérienne
Les auteurs ont utilisé un modèle murin de co-infection virale-bactérienne : des souris ont été infectées par le virus de la grippe A (PR8) puis surinfectées 10 jours plus tard par SARM (Figure 1.1). Deux groupes étaient comparés : un recevant une eau contenant un cocktail antibiotique à large spectre (VNAM : vancomycine, néomycine, ampicilline, métronidazole) 7 jours avant et après l’infection virale, l’autre une eau sans antibiotique (Figure 1.2). L’inflammation pulmonaire a été évaluée par histologie et par dosage de cytokines dans le liquide broncho-alvéolaire, en particulier l’interféron gamma (IFN-γ) et l’interleukine 1 bêta (IL-1β). La charge bactérienne a été mesurée par dénombrement des colonies de SARM dans les poumons. La perte de poids a aussi été suivie comme marqueur de sévérité clinique. Les souris ayant reçu un traitement antibiotique présentaient une perte de poids plus importante, une inflammation pulmonaire exacerbée et une charge bactérienne 8 fois plus élevée (Figure 1.4), indiquant une altération substantielle de l’immunité locale. Ces résultats indiquent que les antibiotiques rendent les souris plus sensibles aux infections bactériennes en affaiblissant l’immunité pulmonaire [1].
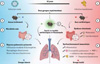 |
Figure 1 Les antibiotiques provoquent une dysbiose intestinale qui altère l’immunité pulmonaire et favorise les surinfections bactériennes. 1. Trois groupes de souris sont infectés par voie intranasale par le virus de la grippe A (PR8), puis surinfectés par Staphylococcus aureus résistant à la méticilline (SARM). 2. Un traitement antibiotique est administré pendant 14 jours à un des groupes (●), tandis qu’aucun traitement n’est administré pour le groupe témoin (●). 3. Les souris ayant reçu le traitement antibiotique développent une dysbiose intestinale avec prolifération fongique (Malassezia, Saccharomyces), absente chez les témoins dont le microbiote reste équilibré. 4. Le traitement antibtiotique est associé à une réponse immunitaire pulmonaire altérée : augmentation de la concentration d’interféron gamma (IFN-γ), infiltration massive d’éosinophiles sécrétant la Major Basic Protein-1 (MBP-1), inhibition des macrophages et augmentation de la charge bactérienne pulmonaire. À l’inverse, les souris témoins présentent des taux stables d’éosinophiles et une clairance efficace du SARM. 5. Un co-traitement antibiotique et antifongique a été administré à un autre groupe (●). Les souris présentent une réduction de l’inflammation, une infiltration modérée d’éosinophiles, une restauration de la fonction macrophagique, et une clairance bactérienne améliorée, proche du profil observé chez les souris témoins. |
Le rôle des éosinophiles dans l’altération de la réponse immunitaire
Cet effet contrintuitif des antibiotiques pourrait être lié aux éosinophiles, des globules blancs souvent associés aux réponses allergiques et inflammatoires [4]. Pour explorer cette piste, les auteurs ont quantifié les populations immunitaires pulmonaires de neutrophiles, macrophages et éosinophiles, par cytométrie en flux. Cette analyse a révélé que les souris traitées par antibiotiques développaient une infiltration pulmonaire trois fois plus importante d’éosinophiles que les souris n’ayant reçu aucun traitement (Figure 1.4). Les éosinophiles interagissent avec les macrophages via la libération de MBP-1, qui inhibe leur activité lorsqu’elle est présente en excès, en rendant les macrophages incapables de phagocyter efficacement les bactéries pathogènes comme le SARM. L’accumulation d’éosinophiles perturbe l’immunité en inhibant les macrophages [5, 6], conduisant ainsi à une prolifération incontrôlée des bactéries dans les poumons [1]. Ainsi, le traitement antibiotique pourrait favoriser la surinfection bactérienne en perturbant l’immunité pulmonaire, notamment en stimulant une infiltration excessive d’éosinophiles qui inhibent l’activité des macrophages [4, 6].
Un microbiote pulmonaire sous l’influence du microbiote intestinal
La réponse immunitaire anormale dans les poumons après traitement antibiotique pourrait être liée à une altération du microbiote intestinal. En effet, des qPCR et séquençage ITS (Internal Transcribed Spacer) sur des échantillons fécaux ont montré les souris traitées par antibiotique présentaient un microbiote fongique intestinal 11 fois plus important que les souris non traitées (Figure 1.3). Cette altération du microbiote intestinal est marquée par une prolifération fongique, notamment Saccharomyces et Malassezia [1,8,9]. Pour étudier le lien entre microbiote intestinal et immunité pulmonaire, les auteurs ont administré du fluconazole, un antifongique, avec le traitement antibiotique (Figure 1.5). Les souris traitées présentaient une meilleure clairance bactérienne, une infiltration d’éosinophiles réduite et un microbiote fongique intestinal plus stable. Ces résultats suggèrent que l’expansion fongique intestinale, favorisée par les antibiotiques, pourrait contribuer à l’inflammation pulmonaire via un axe intestin-poumon à caractériser [1, 7]. L’usage conjoint d’antifongiques pourrait donc représenter une stratégie prometteuse. Ce mécanisme suggère que la surinfection bactérienne induite par les antibiotiques pourrait résulter, au moins en partie, d’une altération du microbiote intestinal conduisant à une accumulation pulmonaire d’éosinophiles, perturbant ainsi l’homéostasie pulmonaire [7].
L’éosinophilie pulmonaire antibioinduite comme facteur pronostic négatif de la grippe
Les auteurs ont ensuite voulu comparer les résultats obtenus sur les modèles murins avec les observations cliniques. Ils ont alors analysé les dossiers médicaux de patients hospitalisés pour des infections respiratoires graves, notamment des grippes sévères. Ils ont observé que les patients ayant reçu des antibiotiques présentaient des niveaux accrus d’éosinophiles dans leur circulation sanguine et dans les poumons, ce qui était corrélé à une inflammation systémique plus marquée et à des séjours hospitaliers prolongés [1]. Par ailleurs, ils ont rapporté pour ces patients un risque plus élevé de développer des infections bactériennes secondaires, en particulier causées par des bactéries résistantes comme le SARM.
Pour d’autres pandémies respiratoires, comme la COVID-19, des études ont également montré que les infections bactériennes secondaires, en particulier chez les patients hospitalisés ayant reçu des doses prophylactiques d’antibiotiques, pouvaient considérablement aggraver l’évolution de la maladie [10]. Ces résultats cliniques confirment les observations faites chez la souris, que l’utilisation prophylactique d’antibiotiques chez les patients atteints de grippe peut compromettre leur réponse immunitaire et augmenter la gravité des infections secondaires. L’accumulation d’éosinophiles pourrait ainsi être un facteur prédictif de complications pulmonaires chez ces patients [1].
Implications cliniques : vers un usage optimisé des antibiotiques
Les résultats obtenus par l’équipe de Sanches Santos Rizzo Zuttion et al. ont des implications majeures pour la pratique clinique. Si les antibiotiques restent essentiels pour traiter les infections bactériennes avérées, leur utilisation prophylactique en cas d’infections virales comme la grippe, sans documentation bactérienne concomitante, doit être reconsidérée [3, 10]. Les auteurs soulignent que les antibiotiques doivent être réservés aux infections bactériennes confirmées. Leur utilisation inappropriée en cas d’infection virale perturbe l’immunité pulmonaire en déséquilibrant le microbiote intestinal, favorisant ainsi des surinfections graves. Les auteurs suggèrent que des traitements complémentaires, comme les antifongiques ou les probiotiques, pourraient atténuer cette dysbiose [1, 9]. Une réévaluation stricte des indications antibiotiques, couplée à des mesures de préservation du microbiote, améliorerait la prise en charge des patients grippés et réduirait les complications respiratoires [3]. L’usage de biomarqueurs spécifiques pourrait jouer un rôle clé dans l’optimisation de la prescription d’antibiotiques, en permettant l’identification des patients réellement à risque de surinfections. Des approches telles que la modulation du microbiote à l’aide de probiotiques ou d’antifongiques pourraient constituer des compléments prometteurs aux traitements actuels.
Vers de nouvelles approches pour renforcer l’immunité pulmonaire
Il devient évident que des mesures visant à protéger et restaurer le microbiote intestinal pourraient jouer un rôle clé dans la prévention des infections bactériennes secondaires [7, 8]. Des approches telles que la modulation du microbiote par l’utilisation de probiotiques ou l’administration d’antifongiques comme le fluconazole pourraient aider à maintenir l’équilibre immunitaire des poumons [1, 8]. Ces interventions ciblées permettraient non seulement de préserver l’intégrité du microbiote intestinal, mais aussi de prévenir l’accumulation excessive d’éosinophiles dans les poumons, réduisant ainsi le risque d’infections graves [7].
L’avenir de la gestion des infections respiratoires pourrait donc résider dans une approche thérapeutique transversale qui tienne compte non seulement des infections bactériennes mais aussi de l’importance du microbiote et de la réponse immunitaire pulmonaire. Ces avancées ouvrent la voie à une médecine plus précise et qui intègre les équilibres immunitaires dans l’établissement de pronostics et la prescription de traitements.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Sanches Santos Rizzo Zuttion M, Parimon T, Bora SA, et al. Antibiotic use during influenza infection augments lung eosinophils that impair immunity against secondary bacterial pneumonia. J. Clin. Invest. 2024 ; 134 : e180986. [Google Scholar]
- Morens DM, Taubenberger JK, Fauci AS. Predominant Role of Bacterial Pneumonia as a Cause of Death in Pandemic Influenza: Implications for Pandemic Influenza Preparedness. J. Infect. Dis. 2008 ; 198 : 962–970. [Google Scholar]
- Ray MJ, Tallman GB, Bearden DT, et al. Antibiotic prescribing without documented indication in ambulatory care clinics: national cross sectional study. BMJ 2019 ; l6461. [Google Scholar]
- Rosenberg HF, Dyer KD, Foster PS. Eosinophils: changing perspectives in health and disease. Nat. Rev. Immunol. 2013 ; 13 : 9–22. [Google Scholar]
- Pidwill GR, Gibson JF, Cole J, et al. The Role of Macrophages in Staphylococcus aureus Infection. Front. Immunol. 2021 ; 11 : 620339. [Google Scholar]
- Wen T, Rothenberg ME. The Regulatory Function of Eosinophils. Microbiol. Spectr. 2016 ; 4 : 4.5.06. [Google Scholar]
- Clemente JC, Ursell LK, Parfrey LW, et al. The Impact of the Gut Microbiota on Human Health: An Integrative View. Cell 2012 ; 148 : 1258–1270. [Google Scholar]
- Schwartz DJ, Langdon AE, Dantas G. Understanding the impact of antibiotic perturbation on the human microbiome. Genome Med. 2020 ; 12 : 82. [Google Scholar]
- Herbst T, Sichelstiel A, Schär C, et al. Dysregulation of Allergic Airway Inflammation in the Absence of Microbial Colonization. Am. J. Respir. Crit. Care Med. 2011 ; 184 : 198–205. [Google Scholar]
- Abelenda-Alonso G, Padullés A, Rombauts A, et al. Antibiotic prescription during the COVID-19 pandemic: A biphasic pattern. Infect. Control HosP. Epidemiol. 2020 ; 41 : 1371–1372. [Google Scholar]
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Les antibiotiques provoquent une dysbiose intestinale qui altère l’immunité pulmonaire et favorise les surinfections bactériennes. 1. Trois groupes de souris sont infectés par voie intranasale par le virus de la grippe A (PR8), puis surinfectés par Staphylococcus aureus résistant à la méticilline (SARM). 2. Un traitement antibiotique est administré pendant 14 jours à un des groupes (●), tandis qu’aucun traitement n’est administré pour le groupe témoin (●). 3. Les souris ayant reçu le traitement antibiotique développent une dysbiose intestinale avec prolifération fongique (Malassezia, Saccharomyces), absente chez les témoins dont le microbiote reste équilibré. 4. Le traitement antibtiotique est associé à une réponse immunitaire pulmonaire altérée : augmentation de la concentration d’interféron gamma (IFN-γ), infiltration massive d’éosinophiles sécrétant la Major Basic Protein-1 (MBP-1), inhibition des macrophages et augmentation de la charge bactérienne pulmonaire. À l’inverse, les souris témoins présentent des taux stables d’éosinophiles et une clairance efficace du SARM. 5. Un co-traitement antibiotique et antifongique a été administré à un autre groupe (●). Les souris présentent une réduction de l’inflammation, une infiltration modérée d’éosinophiles, une restauration de la fonction macrophagique, et une clairance bactérienne améliorée, proche du profil observé chez les souris témoins. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




