| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 855 - 859 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2025216 | |
| Published online | 12 December 2025 | |
Rôle de sous-populations de lymphocytes T résidents mémoires dans la vaccination anti-tumorale et l’immunothérapie des cancers
Role of resident memory T cell subpopulations in anti-tumour vaccination and cancer immunotherapy
1
Université Paris Cité, Inserm U970, Paris centre de recherche cardiovasculaire (PARCC), Paris, France
2
Département d’immunologie, Hôpital européen Georges-Pompidou, Hôpital Necker, Assistance publique-Hôpitaux de Paris (AP-HP), Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Contributions égales
Différentes populations de lymphocytes T mémoires, telles que les lymphocytes T mémoires centraux et les lymphocytes T mémoires effecteurs, sont présentes dans le sang et les ganglions lymphatiques. Plus récemment, une population particulière de lymphocytes T, appelés lymphocytes T résidents mémoires (TRM), a été identifiée dans les tissus. Ces lymphocytes, qui ont une faible capacité à recirculer vers le ganglion lymphatique ou le sang, jouent un rôle dans l’immunosurveillance locale. Leur persistance dans les tissus leur permet de réagir rapidement en cas d’infection ou de tumeur, contrairement aux lymphocytes T mémoires centraux ou effecteurs. Par ailleurs, ils recrutent d’autres cellules immunitaires effectrices par leur sécrétion de chimiokines et de cytokines, ce qui amplifie la réponse immunitaire locale [1].
Hétérogénéité phénotypique des lymphocytes T mémoires résidents
Ces lymphocytes TRM sont définis par l’expression des marqueurs CD69, CD103 et CD49a (molécule favorisant la résidence), combinée à la perte d’expression des marqueurs CD62L, CCR7, S1PR1 (et S1PR5) et KLF2 (marqueur favorisant la sortie des tissus) [2] (Figure 1). Cependant, alors que CD69 est exprimé par la majorité des lymphocytes TRM dans tous les organes, l’expression de CD103 est moins fréquente dans les lymphocytes TRM de certains organes (cerveau, rein), et plus fréquente dans les lymphocytes TRM CD8+ que dans les lymphocytes TRM CD4+ [1].
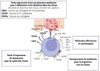 |
Figure 1. Principaux marqueurs des lymphocytes T résidents mémoires CD8+. Les lymphocytes T résidents mémoires CD8+ (CD8 TRM) présentent un phénotype effecteur et sont caractérisés par une forte expression de marqueurs membranaires facilitant leur rétention dans les tissus (CD49a, CD69, CD103), associée à une faible expression des marqueurs favorisant la migration vers le sang ou les ganglions lymphatiques (CCR7, CD62L). Figure créée avec BioRender. |
Les lymphocytes TRM se distinguent des autres lymphocytes T mémoires par l’expression préférentielle des facteurs de transcription Blimp1, Runx3 et Notch, impliqués dans leur différenciation et favorisant leur sortie des tissus. Néanmoins, ce profil de facteurs de transcription peut varier en fonction des tissus. Ainsi, la diminution de l’expression d’Eomes (eomesodermin ou T-box brain protein 2) et de Tbet (T-box expressed in T cells ou TBX21) précède la différenciation des lymphocytes T en lymphocytes TRM dans la peau et les poumons, mais la présence de Tbet est nécessaire pour la formation des lymphocytes TRM dans le foie. Celle de Bhlhe40 (basic helix-loop-helix family, member E40) est également nécessaire pour la différenciation des lymphocytes TRM, surtout dans les poumons.
Chez la souris, on distingue généralement deux populations de lymphocytes TRM : l’une, effectrice à courte durée de vie, exprimant Blimp1, Id3 et CD28, et l’autre, mémoire, exprimant Blimp1 et Id3, mais pas CD28 [3]. Chez l’homme, deux sous-populations de lymphocytes TRM exprimant CD103 co-existent : les lymphocytes TRM1, qui expriment aussi CD49a (CD103+, CD49a+), et les lymphocytes TRM17, qui ne l’expriment pas (CD103+, CD49a-) [4]. Les lymphocytes TRRM1 co-expriment le plus souvent CD122, ce qui explique leur sensibilité à l’interleukine-15, tandis que les lymphocytes TRM17 expriment la molécule ICOS (inducible T-cell costimulator). Une autre population de lymphocytes T mémoires, qui expriment CD49a mais pas CD103 (CD103-, CD49a+, CD69+), a été décrite comme persistant long-temps dans le poumon après un cancer ou une infection virale, mais leur inclusion dans les lymphocytes TRM fait débat [5, 6]. L’analyse transcriptomique a montré que leur profil d’expression génique était proche de celui des lymphocytes TRM CD103+, et ils peuvent, dans certains organes comme le foie, exprimer la molécule d’adhérence LFA1 (lymphocyte function-associated antigen-1), qui est impliquée dans leur rétention tissulaire. Leur différenciation est indépendante du TGF-β, un facteur soluble augmentant l’expression de CD103 à la membrane. L’analyse transcriptomique de cellules uniques a révélé une diversité encore plus grande des lymphocytes TRM, dont la signification reste à préciser. Certaines sous-populations expriment la molécule CD27, qui interagit avec son ligand CD70, présent sur les cellules tumorales. Cette interaction entraîne un dysfonctionnement des lymphocytes TRM, qui deviennent apoptotiques, et le clivage de CD27 membranaire en CD27 soluble. L’augmentation de la concentration de CD27 dans le sang reflète l’infiltration de cette sous-population de lymphocytes dans les tumeurs, et est associée à une résistance à l’immunothérapie chez des personnes atteintes de cancer du rein ou de mélanome [7-9].
Hétérogénéité fonctionnelle des lymphocytes T mémoires résidents
Cette hétérogénéité phénotypique des lymphocytes TRM se traduit également par des fonctionnalités différentes de leurs sous-populations. Ainsi, la sous-population CD103+, CD49a+ produit davantage de cytokines (interleukine-2, interféron γ, TNFα) que la sous-population CD103-, CD49a+, même si paradoxalement, elle exprime plus de récepteurs « inhibiteurs » (PD-1, Tim-3, etc.) [5] (Tableau I).
Hétérogénéité phénotypique et fonctionnelle des sous-populations de lymphocytes T résidents mémoires CD8+ (CD8 TRM) CD103- CD49a+ et CD103+ CD49a+ dans les poumons de personnes atteintes d’un cancer bronchique « non à petites cellules », ou de souris (après vaccination intranasale, infection virale, ou avec un adénocarcinome) [5, 6, 22].
Nous avons montré que la population CD103-, CD49a+ exprimait plus fréquemment le facteur de transcription TCF1 (T-cell factor 1), ce qui suggère un phénotype plus proche de celui d’une cellule progénitrice, c’est-à-dire moins différencié que celui de la population CD103+ [5]. Des deux populations de lymphocytes TRM exprimant CD103, les TRM1 (CD103+, CD49a+) sont les plus cytotoxiques : ils possèdent plus de granules contenant le granzyme et la perforine, et produisent de fortes quantités d’interféron γ [10]. Au contraire, les lymphocytes TRM17 (CD103+, CD49a-) caractérisés par une signature TH17 (RORγt+, CCR6, ICOS) peuvent également coexprimer des gènes associés à un profil TH2 (interleukine-5, interleukine-13) [4]. La population TRM17 aurait aussi une plus grande plasticité phénotypique, répondant finement aux besoins du tissu dans lequel ils se trouvent, que la population TRM1. L’utilisation in vivo d’anticorps neutralisants a notamment permis de montrer le rôle clé des lymphocytes TRM17 en cas de lésion dermique : l’administration d’anticorps anti-interleukine-7R et anti-ICOS-L, qui déplète la peau en lymphocytes TRM17 mais pas en lymphocytes TRM1, freine la réparation tissulaire [1].
Origine des sous-populations de lymphocytes TRM
Deux modèles de production des lymphocytes TRM ont été proposés : dans l’un, les lymphocytes T effecteurs pluripotents pénétreraient dans les tissus et, sous l’influence de signaux du microenvironnement, se différencieraient en lymphocytes TRM à longue durée de vie, tandis que dans l’autre, des lymphocytes T naïfs seraient préconditionnés par le TGFβ produit par des cellules dendritiques dans le ganglion lymphatique pour se différencier préférentiellement en lymphocytes TRM dans les tissus.
Le TGFβ jouerait notamment un rôle important dans la différenciation des lymphocytes TRM CD103+, et l’acide rétinoïque, seul ou en combinaison avec le TGFβ selon les tissus, influencerait la différenciation des lymphocytes TRM [11]. D’autres molécules produites par les cellules dendritiques (interleukine-2, interleukine-15, CD24) influencent également la production de lymphocytes TRM. Leur rôle dépend également du tissu considéré. L’interleukine-15, qui diminue l’expression des signaux de sortie du tissu des lymphocytes T (S1PR1, KLF2, CCR7), est indispensable pour la différenciation des lymphocytes TRM du poumon, de la peau et du foie, mais pas pour celle des lymphocytes TRM de l’intestin. Chez la souris, la différenciation des lymphocytes TRM1 dépend de l’axe Hobit-interleukine-15-Tbet, tandis que celle des lymphocytes TRM17 implique les protéines ICOS, le facteur de transcription c-maf (musculoaponeurotic fibrosarcoma) et l’interleukine-7.
Différents arguments plaident en faveur d’une origine commune des différentes populations de lymphocytes T mémoires, dont les lymphocytes TRM [1]. Les lymphocytes T effecteurs, centraux et mémoires, ainsi que les lymphocytes TRM partagent des séquences hypervariables de leur récepteur T (CDR3) [5]. Les lymphocytes TRM CD103-, CD49a+ pourraient représenter les progéniteurs des lymphocytes TRM CD103+. En effet, l’expression de CD49a apparaît d’abord, dans les ganglions lymphatiques, tandis que celle de CD103 apparaît plus tardivement, dans les tissus [12]. La population TRM1 (CD103+, CD49a+), moins plastique que la population TRM17, correspondrait à une différenciation terminale des lymphocytes TRM.
Rôle des lymphocytes T mémoires résidents dans l’efficacité de la vaccination anti-tumorale
Le rôle crucial des lymphocytes TRM pour l’efficacité de la vaccination antitumorale a été montré par différentes approches expérimentales : déplétion sélective des lymphocytes T circulants, inhibition de la sortie des lymphocytes T du ganglion lymphatique, expérience de parabiose1 [13, 14]. Des conclusions similaires ont été rapportées sur l’importance des lymphocytes TRM pour l’efficacité de vaccins contre des agents infectieux. Néanmoins, dans le cas d’une vaccination thérapeutique contre le cancer, les résultats d’expériences de parabiose ont montré que les lymphocytes T circulants et les lymphocytesTRM permettent de réduire la croissance tumorale, et que la présence de lymphocytes TRM en plus des lymphocytes T circulants augmente le contrôle de la croissance tumorale, suggérant une coopération cellulaire entre ces deux types de lymphocytes [1].
Dans des modèles de cancer du poumon ou des voies aérodigestives supérieures, seul le vaccin administré par voie intranasale a induit des lymphocytes TRM1 (CD103+, CD49a+) dans le poumon, tandis qu’une immunisation avec le même vaccin administré par voie intramusculaire ou sous-cutanée n’a induit que des lymphocytes TRM CD49a+, CD103- [13]. Or, le mécanisme d’action de ces vaccins contre le cancer dépend de leur capacité d’induire des lymphocytes TRM1, coexprimant CD103 et CD49a. Une vaccination par voie intranasale contre les cancers de la sphère ORL ou du poumon s’est d’ailleurs avérée beaucoup plus efficace que la vaccination par la voie intramusculaire pour inhiber la croissance tumorale. Il semble donc que toutes les populations de lymphocytes TRM ne sont pas équivalentes en termes de protection contre le développement du cancer [5, 14].
Ces résultats pourraient être extrapolables à la vaccination anti-infectieuse. Ainsi, il a été montré, chez la souris, qu’une vaccination par de l’ARNm contre le virus influenza A induisait des lymphocytes TRM1 seulement si le vaccin était administré par voie intranasale [15] .
Rôle des lymphocytes T mémoires résidents dans l’immunothérapie du cancer
Pour de très nombreux cancers, l’infiltration de la tumeur par les lymphocyte TRM exprimant CD103 est associée à un bon pronostic [2]. La localisation des lymphocytes TRM en étroite interaction avec les cellules tumorales renforce cet effet favorable sur le pronostic chez des patients atteints de mélanome, de cancer du poumon et de cancer de l’endomètre. Chez des patients atteints d’un cancer du côlon avec métastases hépatiques, seule la sous-population de lymphocytes TRM coexprimant CD103 et CD69 a été associée à une survie prolongée [16].
Plus récemment, il a été rapporté que l’infiltration de la tumeur par les lymphocytes TRM exprimant CD103 avant une immunothérapie par anticorps anti-PD-1 ou anti-PD-L1 était corrélée avec une survie prolongée chez des patients atteints de mélanome, de cancers du poumon, du sein, du foie, de l’œsophage, ou de l’estomac [2]. Nous avons montré la présence de plusieurs sous-populations distinctes de lymphocytes TRM dans les tumeurs provenant de patients atteints de cancer du poumon « non à petites cellules », dont l’une exprimant uniquement CD49a (CD103-) et l’autre exprimant conjointement CD103 et CD49a. Seule la sous-population de TRM coexprimant CD103 et CD49a permettait de prédire la réponse à l’immunothérapie par anticorps anti-PD-1, aussi bien en première ligne qu’en deuxième ligne de traitement. Dans une analyse multivariée incluant PD-L1 et différents paramètres cliniques, la présence de cette souspopulation de lymphocytes TRM restait associée à la prédiction de la réponse clinique à l’immunothérapie [5]. Il semble donc que seule une population particulière de lymphocytes TRM co-exprimant CD103 et CD49 constitue un biomarqueur prédictif de la réponse à l’immunothérapie. Ce résultat renforce les conclusions d’une étude précédente qui avait montré que les lymphocytes TRM proliféraient dans le microenvironnement tumoral après une immunothérapie par des anticorps anti-PD-1 ou anti-PD-L1 chez des patients atteints de mélanome, de cancers du poumon, des voies aérodigestives supérieures, du sein, ou de l’œsophage. La population de lymphocytes TRM qui s’amplifiait le plus après ces traitements était celle exprimant le marqueur CD103, et l’expansion de cette sous-population était associée à un bon pronostic [17].
La population de ces lymphocytes TRM présents dans le microenvironnement tumoral semble également enrichie en lymphocytes T spécifiques de la tumeur. Ainsi, les lymphocytes TRM intratumoraux de femmes atteintes de cancer du sein, isolés in vitro et traités par des anticorps anti-PD-1 ou anti-CTLA-4, prolifèrent au contact de la cellule cancéreuse et produisent des cytokines [18]. Le marqueur CD39 identifie des lymphocytes TRM reconnaissant spécifiquement les cellules tumorales.
Il restait à déterminer si l’expansion de ces lymphocytes TRM provenait de clones préexistant dans le microenvironnement tumoral, ou de nouveaux clones induits par le traitement. Deux études ont montré que les lymphocytes TRM qui proliféraient après le traitement présentaient des récepteurs T communs avec des clones de lymphocytes T présents dans le microenvironnement tumoral avant le traitement [17, 19]. Néanmoins, d’autres études, notamment dans des modèles murins, ont montré que les lymphocytes TRM qui se multiplient dans le microenvironnement tumoral après le traitement peuvent provenir des ganglions lymphatiques, après migration et colonisation de la tumeur [20, 21].
En résumé, les lymphocytes TRM jouent un rôle essentiel dans l’immunosurveillance des tissus, ce qui en fait une première sentinelle de défense de l’organisme contre les infections et les cancers. La population des lymphocytes TRM est en fait hétérogène, et les différentes sous-populations présentent des fonctionnalités différentes. Il semble que seules certaines sous-populations de lymphocytes TRM exprimant CD103 soient associées à un bon pronostic en cas de cancer, et permettent de prédire la réponse à l’immunothérapie. Ces sous-populations de lymphocytes TRM, induites par une vaccination anti-cancéreuse par la voie intranasale, mais pas par les voies intra-musculaire ou sous-cutanée, sont impliquées dans le mécanisme d’action des vaccins anti-cancéreux, et constituent par ailleurs une cible des immunothérapies par anticorps anti-PD-1 ou anti-PD-L1.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Christo SN, Park SL, Mueller SN, et al. The multifaceted role of tissue-resident memory T cells. Annu Rev Immunol 2024 ; 42 : 317-45. [Google Scholar]
- Damei I, Trickovic T, Mami-Chouaib F, et al. Tumor-resident memory T cells as a biomarker of the response to cancer immunotherapy. Front Immunol 2023 ; 14 : 1205984. [Google Scholar]
- Milner JJ, Toma C, He Z, et al. Heterogenous populations of tissue-resident CD8+ T cells are generated in response to infection and malignancy. Immunity 2020 ; 52 : 808-24.e7. [Google Scholar]
- Park SL, Christo SN, Wells AC, et al. Divergent molecular networks program functionally distinct CD8+ skin-resident memory T cells. Science 2023 ; 382 : 1073-9. [Google Scholar]
- Paolini L, Tran T, Corgnac S, et al. Differential predictive value of resident memory CD8+ T cell subpopulations in patients with non-small-cell lung cancer treated by immunotherapy. J Immunother Cancer 2024 ; 12 : e009440. [Google Scholar]
- Reilly EC, Sportiello M, Emo KL, et al. CD49a identifies polyfunctional memory CD8 T cell subsets that persist in the lungs after influenza infection. Front Immunol 2021 ; 12 : 728669. [Google Scholar]
- Benhamouda N, Sam I, Epaillard N, et al. Plasma CD27, a surrogate of the intratumoral CD27–CD70 interaction, correlates with immunotherapy resistance in renal cell carcinoma. Clin Cancer Res 2022 ; 28 : 4983-94. [Google Scholar]
- Sam I, Benhamouda N, Biard L, et al. Soluble CD27 differentially predicts resistance to anti-PD1 alone but not with anti-CTLA-4 in melanoma. EMBO Mol Med 2025 ; 17 : 909-22. [Google Scholar]
- Sam I, Ben Hamouda N, Alkatrib M, et al. The CD70-CD27 axis in cancer immunotherapy: Predictive biomarker and therapeutic target. Clin Cancer Res 2025 ; 31 : 2872-81. [Google Scholar]
- Cheuk S, Schlums H, Gallais Sérézal I, et al. CD49a expression defines tissue-resident CD8+ T cells poised for cytotoxic function in human skin. Immunity 2017 ; 46 : 287-300. [Google Scholar]
- Obers A, Poch T, Rodrigues G, et al. Retinoic acid and TGF-β orchestrate organ-specific programs of tissue residency. Immunity 2024 ; 57 : 2615-33.e10. [Google Scholar]
- Murray T, Fuertes Marraco SA, Baumgaertner P, et al. Very late antigen-1 marks functional tumor-resident CD8 T cells and correlates with survival of melanoma patients. Front Immunol 2016 ; 7 . [Google Scholar]
- Sandoval F, Terme M, Nizard M, et al. Mucosal imprinting of vaccine-induced CD8+ T cells is crucial to inhibit the growth of mucosal tumors. Sci Transl Med 2013 ; 5. [Google Scholar]
- Nizard M, Roussel H, Diniz MO, et al. Induction of resident memory T cells enhances the efficacy of cancer vaccine. Nat Commun 2017 ; 8 : 15221. [Google Scholar]
- Künzli M, O’Flanagan SD, LaRue M, et al. Route of self-amplifying mRNA vaccination modulates the establishment of pulmonary resident memory CD8 and CD4 T cells. Sci Immunol 2022 ; 7 : eadd3075. [Google Scholar]
- Abdeljaoued S, Doussot A, Kroemer M, et al. Liver metastases of colorectal cancer contain different subsets of tissue-resident memory CD8 T cells correlated with a distinct risk of relapse following surgery. OncoImmunology 2025 ; 14 : 2455176. [Google Scholar]
- Luoma AM, Suo S, Wang Y, et al. Tissue-resident memory and circulating T cells are early responders to pre-surgical cancer immunotherapy. Cell 2022 ; 185 : 2918-35.e29. [Google Scholar]
- Lee YJ, Kim JY, Jeon SH, et al. CD39+ tissue-resident memory CD8+ T cells with a clonal overlap across compartments mediate antitumor immunity in breast cancer. Sci Immunol 2022 ; 7 : eabn8390. [Google Scholar]
- Pai JA, Hellmann MD, Sauter JL, et al. Lineage tracing reveals clonal progenitors and long-term persistence of tumor-specific T cells during immune checkpoint blockade. Cancer Cell 2023 ; 41 : 776-90.e7. [Google Scholar]
- Nagasaki J, Inozume T, Sax N, et al. PD-1 blockade therapy promotes infiltration of tumor-attacking exhausted T cell clonotypes. Cell Rep 2022 ; 38 : 110331. [CrossRef] [PubMed] [Google Scholar]
- Connolly KA, Kuchroo M, Venkat A, et al. A reservoir of stem-like CD8+ T cells in the tumor-draining lymph node preserves the ongoing antitumor immune response. Sci Immunol 2021 ; 6 : eabg7836. [Google Scholar]
- Burger ML, Cruz AM, Crossland GE, et al. Antigen dominance hierarchies shape TCF1+ progenitor CD8 T cell phenotypes in tumors. Cell 2021 ; 184 : 4996-5014.e26. [Google Scholar]
Greffe réalisée à des fins expérimentales, par laquelle on soude l’un à l’autre deux organismes pour établir entre eux des échanges physiologiques par voie sanguine.
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des tableaux
Hétérogénéité phénotypique et fonctionnelle des sous-populations de lymphocytes T résidents mémoires CD8+ (CD8 TRM) CD103- CD49a+ et CD103+ CD49a+ dans les poumons de personnes atteintes d’un cancer bronchique « non à petites cellules », ou de souris (après vaccination intranasale, infection virale, ou avec un adénocarcinome) [5, 6, 22].
Liste des figures
 |
Figure 1. Principaux marqueurs des lymphocytes T résidents mémoires CD8+. Les lymphocytes T résidents mémoires CD8+ (CD8 TRM) présentent un phénotype effecteur et sont caractérisés par une forte expression de marqueurs membranaires facilitant leur rétention dans les tissus (CD49a, CD69, CD103), associée à une faible expression des marqueurs favorisant la migration vers le sang ou les ganglions lymphatiques (CCR7, CD62L). Figure créée avec BioRender. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




