| Issue |
Med Sci (Paris)
Volume 41, Number 11, Novembre 2025
|
|
|---|---|---|
| Page(s) | 869 - 876 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2025185 | |
| Published online | 12 December 2025 | |
Le COVID long
Défis et opportunités thérapeutiques face aux séquelles persistantes
Long COVID: therapeutic challenges and opportunities in the face of persistent sequelae
1
CIRI – Centre international de recherche en infectiologie, Equipe GIMAP ; Université Claude Bernard Lyon 1 ; Inserm U1111 ; CNRS UMR5308, ENS-Lyon ; CIC 1408 vaccinologie, Saint-Étienne, France
2
Service d’immunologie, Centre hospitalier universitaire de Saint-Étienne, Saint-Étienne, France
3
CIC 1408 Inserm vaccinologie, Hôpital universitaire de Saint-Etienne, Saint-Étienne, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
La pandémie de COVID-19, causée par le virus SARS-CoV-2, a non seulement entraîné une crise sanitaire et économique mondiale, mais a aussi remis en lumière un phénomène clinique déjà décrit par le passé dans la communauté médicale : la persistance de symptômes après une infection virale, désignée, dans le cas présent, COVID long ou syndrome post-COVID-19. Environ un patient sur huit présente des symptômes persistants d’intensité variable après la phase aiguë de l’infection par le virus SARS-CoV-2. Ce phénomène, associé à la forte transmissibilité du virus et à son taux de mutations rapide, représente un défi majeur pour la santé publique. Cette revue examine différentes approches thérapeutiques actuellement envisagées pour traiter le COVID long, tout en explorant les perspectives futures dans ce domaine.
Abstract
The COVID-19 pandemic, caused by SARS-CoV-2, has not only led to a global health and economic crisis but also renewed attention to a clinical phenomenon of persistent symptoms after viral infection. This phenomenon is defined as long COVID or post-COVID-19 syndrome. Approximately one in eight patients experience persistent symptoms of varying intensity after the acute phase of the infection. This phenomenon, combined with the virus’s high transmissibility and rapid mutation rate, poses a major public health challenge. This review examines various therapeutic approaches currently under consideration for treating long COVID, and explores future prospects in this field.
Co-auteurs
© 2025 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Philippe Roingeard et Sébastien Eymieux, Université de Tours).
Le COVID long : situation globale
Épidémiologie
Selon l’Organisation mondiale de la santé (OMS), le COVID long (CL) désigne un état de santé qui peut survenir après une infection confirmée ou probable par le virus SARS-CoV-2. Cette affection se manifeste généralement dans les trois mois suivant l’apparition des symptômes du COVID-19, avec des symptômes qui durent au moins deux mois et ne peuvent être expliqués par un autre diagnostic. À l’échelle mondiale, la prévalence du CL varie considérablement, non seulement en fonction des critères utilisés pour le définir (durée et sévérité des symptômes, méthode de collecte des données), mais également selon les populations étudiées, le statut vaccinal, la présence de facteurs de risque, l’âge et l’hospitalisation. Ainsi, les études épidémiologiques sur le CL ont estimé que ce syndrome post-viral touchait plus de 400 millions de personnes en 2023 [1,2]. Environ 10 à 30 % des individus non hospitalisés en souffriraient, tandis que parmi les patients hospitalisés, ce chiffre pourrait atteindre 50 à 80 % [3-6]. Plusieurs études menées à travers le monde ont révélé qu’environ la moitié des personnes infectées par le virus SARS-CoV-2 développent des symptômes de CL, avec des taux de prévalence estimés à 51 % en Asie, 44 % en Europe, et 31 % aux États-Unis. Cependant, ces chiffres pourraient être sous-estimés en raison du manque de données complètes et de l’absence de critères diagnostiques standardisés [7]. Dans ce contexte d’incertitude diagnostique, l’analyse de Callard et ses collaborateurs met en lumière un phénomène peu commun dans l’histoire des maladies émergentes : la co-construction du savoir médical par les récits des patients. En l’absence de reconnaissance institutionnelle initiale du CL, ce sont les malades eux-mêmes qui, à travers les réseaux sociaux, les témoignages et le partage d’expériences, ont su faire émerger cliniquement et politiquement cette nouvelle maladie. Santé publique France, quant à elle, estimait en 2022 une prévalence de ces symptômes de 4 % dans la population adulte générale, et de 8 % chez les personnes ayant été infectées par le virus SARS-CoV-2. Parmi les patients hospitalisés, 42 % présentaient un à deux symptômes persistants trois mois après leur sortie, tandis que 27 % en avaient trois ou plus. Il est également important de souligner que la prévalence du CL est probablement sous-estimée dans certaines régions en raison du manque de données complètes, de l’absence de critères diagnostiques standardisés ou de ressources médicales adéquates. De plus, cette maladie demeure encore largement méconnue, particulièrement dans certains pays où les études épidémiologiques sur le CL sont rares.
Les symptômes et les mécanismes sous-jacents
L’impact de l’infection par le virus SARS-CoV-2 sur divers organes et tissus du corps humain explique la diversité des symptômes du CL, dont l’intensité est variable et évolutive (Figure 1). De fait, le CL résulte non pas d’une seule, mais de plusieurs maladies. À ce jour, plus de 200 symptômes sont associés au CL. Une méta-analyse récente portant sur 41 études a identifié la fatigue (23 %), les troubles de la mémoire (14 %), la dyspnée1 (13 %), les troubles du sommeil (11 %), la dépression (8 % à 22 %), les difficultés de concentration (22 % à 28 %), ainsi que les douleurs articulaires (10 %), comme les symptômes majeurs du CL [1]. D’autres symptômes touchant, notamment, les systèmes cardiaque, digestif, respiratoire, reproducteur et dermatologique, peuvent également se manifester. Dans certains cas, ces symptômes sont directement liés à des lésions organiques causées pendant la phase aiguë de l’infection. Les analyses biologiques réalisées chez les patients souffrant de CL révèlent fréquemment des perturbations importantes, telles qu’une élévation des taux de ferritine, de protéine C-réactive, une réduction des concentrations d’hémoglobine et d’albumine, ainsi qu’une augmentation de la vitesse de sédimentation des érythrocytes [8].
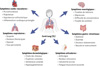 |
Figure 1. Symptômes persistants du COVID long (CL). |
Les mécanismes pouvant expliquer l’apparition de ces symptômes restent encore hypothétiques. Ceux-ci pourraient être liés à un dérèglement immunitaire avec ou sans inflammation, à une persistance virale, à une maladie auto-immune, à une altération du microbiote de type dysbiose, à un dysfonctionnement neurologique ou à un problème de coagulation [9,10]. Une grande variété d’études expérimentales a étudié la physiopathologie du CL. Une étude menée par Wei et al. a mis en évidence un dysfonctionnement des macrophages alvéolaires comme facteur contribuant à la persistance des lésions pulmonaires post-COVID [11]. Chez la souris, la perte de peroxysomes dans ces macrophages, qui survient après l’infection virale, conduit à un défaut de réparation du tissu pulmonaire et au développement d’une fibrose persistante avec un impact négatif sur la fonction respiratoire [12].
Bien que le système respiratoire, notamment les poumons, soit considéré comme la principale cible du virus SARS-CoV-2, plusieurs travaux ont mis en évidence la capacité du virus à infecter également le système nerveux central, entraînant des symptômes neurologiques tels que des vertiges, une anxiété, une altération de l’état de conscience ou encore des atteintes nerveuses crâniennes. Par ailleurs, des altérations cognitives, souvent désignées sous le terme de « brouillard cérébral », figurent parmi les séquelles les plus fréquemment rapportées par les patients souffrant du CL [13]. Une étude réalisée par Zhang et al. en 2024 dans un modèle murin a révélé un lien entre une surexpression du récepteur au virus ACE2 (angiotensin-converting enzyme 2) dans l’hippocampe et l’apparition de troubles cognitifs [14]. Les auteurs ont constaté que la protéine S1 du SARS-CoV-2 induisait cette surexpression, perturbant ainsi la voie de signalisation calcique, offrant ainsi une hypothèse sur les mécanismes par lesquels l’infection par le virus SARS-CoV-2 pourrait entraîner des altérations cognitives.
Une revue narrative récente soutient l’hypothèse que les manifestations neuropsychiatriques liées au COVID-19 pourraient résulter d’une signalisation immuno-inflammatoire excessive, suggérant que l’inflammation systémique pourrait suffire à induire des symptômes psychiatriques, même sans atteinte directe du système nerveux central par le virus [15]. Des études ont par ailleurs montré une corrélation significative entre les concentrations de cytokines inflammatoires (IL-6 [interleukine-6], IL1-β et TNFα [tumor necrosis factor α]) et les modifications cognitives et comportementales chez les patients infectés, soulignant l’existence d’un état de neuroinflammation étendu [16,17].
du COVID-19 [20]. Les microglies de ces patients présentent une défaillance métabolique et une altération de la communication via l’axe CX3CR1–CX3CL1 (C-X3-C motif chemokine receptor 1- chemokine ligand 1), associés à des dommages mitochondriaux au niveau des sites d’inflammation vasculaire, en lien avec la présence d’antigènes viraux. Les auteurs rapportent également une perte des terminaisons nerveuses glutamatergiques, en particulier dans les zones affectées par une inflammation vasculaire sévère, ce qui concorde avec l’observation de modifications au niveau des protéines impliquées dans l’assemblage synaptique, le métabolisme et les marqueurs de souffrance neuronale.
Un autre mécanisme exploré dans l’apparition du COVID long est la persistance des composants viraux. Plusieurs études ont mis en évidence la présence prolongée de protéines virales ou d’ARN messager du virus SARS-CoV-2 dans divers organes, plusieurs mois après l’infection initiale. Cette persistance suggère l’existence de réservoirs viraux tissulaires susceptibles d’entretenir une réponse immunitaire prolongée même en l’absence de réplication virale active, et pourrait expliquer la durée anormalement longue de certains symptômes, notamment ceux touchant le système nerveux central.
Des études récentes soulèvent l’hypothèse d’une implication de l’axe intestin-cerveau dans la physiopathologie du CL [21]. En effet, la persistance virale prolongée au niveau intestinal pourrait provoquer une réponse immunitaire locale et perturber la composition du microbiote, entraînant un état de dysbiose marqué par une diminution de la diversité microbienne associée à une prolifération d’espèces microbiennes potentiellement pathogènes comme Enterococcus et Escherichia coli [22,23]. Une baisse notable de bactéries bénéfiques telles que Faecalibacterium prausnitzii et Bifidobacterium spp et la famille des Verrucomicrobia a également été décrite [24,25]. Ce déséquilibre est associé à une altération de la barrière intestinale, à une inflammation systémique et à une activation immunitaire généralisée [26]. Ces perturbations pourraient indirectement affecter la barrière hémato-encéphalique et favoriser une neuroinflammation [27].
Le dysfonctionnement mitochondrial joue un rôle central dans le CL, contribuant à des symptômes tels que la fatigue et la faiblesse musculaire. Plusieurs études ont démontré que l’infection par le virus SARS-CoV-2 peut altérer le fonctionnement des mitochondries, entraînant une diminution de la production d’ATP, une augmentation du stress oxydatif, un dérèglement de la voie métabolique pyruvate/lactate et la libération de molécules pro-inflammatoires [28,29]. Ces perturbations affectent particulièrement les cellules musculaires, contribuant à la fatigue et à la faiblesse physique souvent signalées chez les personnes atteintes de CL [30]. Dans les cellules endothéliales, le dysfonctionnement mitochondrial se traduit par une réduction de la production de monoxyde d’azote, compromettant la vasodilatation et favorisant l’inflammation vasculaire. Des niveaux élevés d’espèces réactives de l’oxygène d’origine mitochondriale (mtROS) et des dommages à l’ADN mitochondrial ont également été observés, ce qui intensifie le stress cellulaire. Le virus peut également perturber la dynamique des mitochondries (fusion et fission), modifier le potentiel de la membrane mitochondriale et déséquilibrer l’homéostasie calcique. Une étude récente menée sur une cohorte de 358 patients a exploré les mécanismes biologiques pouvant contribuer à la persistance des symptômes du CL [31]. Les analyses effectuées comprenaient l’évaluation de marqueurs sérologiques, de marqueurs inflammatoires plasmatiques, de la longueur des télomères, de la teneur en ADN mitochondrial, ainsi que de la méthylation de l’ADN. Parmi ces marqueurs, la troponine T et le raccourcissement des télomères se sont révélés être les principaux marqueurs prédictifs du CL et des symptômes de malaise post-effort. Une deuxième étude menée par Majima et al., signale la lipidation des protéines, incluant la prénylation, la myristoylation et la palmitoylation, comme un mécanisme physiopathologique potentiel associé au CL [32]. Ces modifications post-traductionnelles permettent l’ancrage des protéines virales aux membranes mitochondriales. Une fois localisées dans ces organites, elles favorisent une production accrue d’espèces réactives de l’oxygène, entraînant un stress oxydatif mitochondrial. Ce phénomène se traduit par des altérations des lipides, des protéines et de l’ADN mitochondrial, contribuant ainsi à la persistance des symptômes cliniques observés chez les patients atteints de CL.
Sur le plan immunologique, une sénescence accrue des lymphocytes T et une activation des monocytes ont été associées à la sévérité du CL (REF). Une revue systématique conduite par Giorghita et al. a montré une diminution prolongée du nombre de cellules T régulatrices (Treg) après une infection par le virus SARS-CoV-2, pouvant persister pendant plusieurs mois. Cette diminution pourrait favoriser le développement de complications respiratoires sévères et du CL. En effet, les Treg régulent à la fois l’immunité adaptative et innée. Ils sécrètent des cytokines immunorégulatrices telles que TGF-β (transforming growth factor- β), IL-10 et IL-35, capables d’inhiber l’activation des cellules T effectrices, notamment les sous-populations Th1 (T helper 1), Th2 et Th17. Ils exercent également un effet direct sur les lymphocytes B et inhibent l’activité des macrophages, soulignant leur rôle central dans le maintien de l’homéostasie immunitaire.
Un déséquilibre quantitatif ou fonctionnel des Treg peut ainsi avoir des conséquences délétères, en limitant l’activité antivirale des cellules T effectrices tout en altérant la réponse immunitaire, notamment chez les patients sévèrement atteints.
Finalement, lors d’une infection par le virus SARS-CoV-2, la coagulation sanguine microvasculaire et la formation de microcaillots peuvent entraîner une hypoxie de différents organes, participer indirectement au maintien de l’état inflammatoire chronique et ainsi expliquer certains symptômes persistants comme le syndrome de tachycardie orthostatique posturale2 [34].
Une étude clinique prospective conduite auprès de 113 patients ayant contracté le COVID-19, et comparés à 39 témoins sains, a permis de mieux caractériser certains mécanismes impliqués dans le CL. L’analyse approfondie de plus de 6 500 biomarqueurs a mis en évidence une activation prolongée du système du complément chez les patients atteints de CL, qui se maintient jusqu’à six mois après l’infection initiale. Par ailleurs, ces patients présentaient des signes de thromboinflammation persistante, caractérisée par une activation endothéliale (notamment du facteur de von Willebrand), une activation continue de la cascade de coagulation, une agrégation plaquettaire accrue, ainsi qu’une stimulation prolongée des lymphocytes T. Ces altérations biologiques pourraient contribuer à la persistance des symptômes observés chez certains individus après la phase aiguë de l’infection.
Les solutions thérapeutiques
Les approches pharmaceutiques
Les traitements anti-inflammatoires
Les anti-inflammatoires constituent une approche thérapeutique prometteuse pour le traitement du CL, en ciblant l’inflammation chronique responsable de nombreux symptômes persistants chez certains patients. L’utilisation de corticoïdes durant la phase aiguë de la COVID-19 est largement documentée [35,36]. Cependant, leur usage prolongé, qu’il s’agisse de corticostéroïdes systémiques ou inhalés, a été associé à un risque accru d’hospitalisation et de mortalité chez les patients atteints de maladies chroniques, rendant difficile l’évaluation précise de leur efficacité [37-39]. Par ailleurs, une étude observationnelle a révélé que les patients traités par de la dexaméthasone durant la phase aiguë de la maladie présentaient un risque réduit de développer des symptômes persistants du CL après un suivi de 8 mois [40]. Les thérapies ciblées, comme les inhibiteurs de cytokines (anti-IL-6, anti-TNF-α), ont démontré un potentiel prometteur contre l’inflammation liée au COVID-19. Les anti-inflammatoires non stéroïdiens, tels que l’aspirine ou l’ibuprofène, peuvent être efficaces pour les symptômes légers, tandis que des approches émergentes, comme les inhibiteurs de la kinase JAK (Janus kinase) et les modulateurs du microbiote, pourraient offrir de nouvelles perspectives pour réduire l’inflammation systémique. Des études cliniques robustes conduites chez des patients présentant un état clinique approprié et des groupes contrôles adaptés sont nécessaires pour valider la possible efficacité de ces traitements anti-inflammatoires.
Les traitements antiviraux
La persistance du virus SARS-CoV-2 chez des patients atteints de CL a été démontrée dans plusieurs études. Proal et al. ont montré que le virus SARS-CoV-2 peut persister dans les tissus gastro-intestinaux, neuronaux ou lymphoïdes, contribuant à une inflammation chronique [41]. Une autre étude a rapporté que l’ARN viral pouvait être détecté dans le cerveau, plusieurs mois après l’infection initiale [42]. Sur le plan thérapeutique, plusieurs essais randomisés ont évalué le bénéfice des antiviraux dans le traitement du CL [43,44]. Plusieurs observations cliniques rapportent également une amélioration chez certains patients à la suite d’une cure de Paxlovid®3 d’une durée de 10 jours [45]. Une étude menée auprès de 4 684 personnes n’a cependant, pas montré d’association significative entre le traitement durant la phase aiguë de l’infection par cet antiviral et l’apparition de symptômes liés à un CL, 90 jours après l’infection [46].
Les traitements anticoagulants
Les anticoagulants sont explorés comme une option thérapeutique potentielle pour traiter certains aspects du CL, en particulier en réponse à l’hypercoagulabilité du sang et à la formation de microthrombus observée chez certains patients. L’utilisation de médicaments comme le rivaroxaban ou l’héparine vise à améliorer la circulation sanguine et à limiter les dommages aux tissus liés à la formation de caillots [48,49]. Cependant, leur prescription nécessite une vigilance particulière pour éviter les complications telles que les hémorragies. Des essais cliniques sont en cours pour évaluer l’efficacité et la sécurité de ces traitements, et déterminer les critères spécifiques permettant d’identifier les patients susceptibles d’en bénéficier [50]. Ces recherches pourraient ouvrir la voie à des thérapies mieux adaptées aux mécanismes physiopathologiques du CL.
Les traitements à base d’anticorps
Les anticorps pourraient être utilisés pour réduire les réponses autoimmunes, atténuer l’inflammation [51,52] ou induire un impact bénéfique sur le microbiome intestinal, notamment en cas de dysbiose [53]. Plusieurs travaux ont mis en lumière une réponse auto-immune dans le contexte du CL, caractérisée notamment par la détection d’auto-anticorps ciblant les cytokines, certaines protéines du tissu conjonctif, ainsi que les récepteurs du système nerveux autonome [29, 54]. Ces altérations immunitaires traduisent un déséquilibre persistant de la réponse immunitaire, susceptible de contribuer à l’émergence ou au maintien de manifestations cliniques du CL, telle que la fatigue chronique. Une étude récente montre que les anticorps jouent un rôle actif dans la régulation du microbiote intestinal, via différents mécanismes tels que la neutralisation microbienne, l’opsonisation4, l’activation du complément ou la régulation de l’inflammation systémique qui perturbe l’homéostasie intestinale [55]. Le traitement par immunoglobulines intraveineuses a démontré une amélioration des symptômes intestinaux dans de petites cohortes de patients [56]. Des bénéfices ont aussi été observés dans des cas isolés de patients traités par des cocktails d’anticorps monoclonaux. Une optimisation des protocoles d’administration et la compréhension des profils symptomatiques et physiopathologiques des patients chez lesquels des bénéfices ont été rapportés restent cruciales afin de pouvoir mettre en place des cohortes robustes pour des essais cliniques. Les nanobodies5 pourraient être une option alternative à tester en clinique (Figure 2). Également appelés anticorps à domaine unique, les nanobodies se distinguent des anticorps conventionnels par l’absence de chaîne légère ainsi que du premier domaine constant de la chaîne lourde (CH1). Cette structure simple, d’une masse d’environ 15 kDa, leur confère une excellente stabilité, une bonne solubilité et une capacité à interagir avec des épitopes difficilement accessibles aux anticorps classiques. Ces propriétés font des nanobodies des outils particulièrement adaptés à des applications thérapeutiques, notamment pour le CL [57]. Une activité immunomodulatrice des nanobodies a notamment été décrite dans le cas d’inflammations neurologiques [58]. Ainsi, grâce à leur capacité à traverser la barrière hémato-encéphalique, ils pourraient, par exemple, cibler la neuro inflammation observée chez certains patients atteints de CL. Des études ont démontré l’efficacité des nanobodies dirigés contre des cytokines pro-inflammatoires (TNF-α ou IL-6), impliquées dans les réponses immunitaires exacerbées au niveau neuronal [59]. Les bases de données talles que la Nanobody library pourraient faciliter la recherche et accélérer les essais cliniques dans le cadre du CL. Malgré leur faible toxicité décrite jusqu’à présent [60,61], des recherches supplémentaires sont nécessaires pour évaluer les voies d’administration, les doses optimales et l’impact de leur utilisation prolongée dans le cadre de maladies chroniques. Ces travaux permettront de maximiser leur potentiel dans les thérapies ciblées.
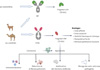 |
Figure 2. Fragments d’anticorps (nanobodies ou VHH) issus des anticorps chaine lourde (HCAb). Avantages et applications potentielles pour lutter contre le COVID long (CL). IgG : immunoglobuline de classe G ; scFv : fragment variable à chaîne unique |
Les approches non pharmaceutiques
Le reconditionnement physique
Le reconditionnement, qui peut inclure de la physiothérapie, une thérapie basée sur des exercices adaptés, et parfois de la relaxation, a été l’une des premières approches mises en avant dès les premiers cas de fatigue chronique observés dans le CL. Quelques études ont démontré un certain bénéfice chez un petit nombre de patients ; cependant d’autres n’ont pas observé de différences significatives. Certaines études ont aussi attiré l’attention sur le risque de malaise post-exercice et recommandent de combiner ou de remplacer cette approche par le PACING (fractionnement et autogestion du rythme des activités) [62-64]. Bien que cette dernière méthode puisse paraître contre-intuitive face à la faiblesse musculaire associée au CL, elle s’avère essentielle pour prévenir l’aggravation des symptômes. Le PACING repose sur une gestion proactive de l’énergie disponible, en adaptant les efforts physiques et cognitifs pour éviter les « crashes » post-activité, favorisant ainsi une amélioration progressive sans exacerbation des symptômes [65].
Les compléments alimentaires
Les probiotiques comme Bifidobacterium longum, ont démontré une certaine capacité à restaurer un microbiote équilibré et à atténuer les symptômes neuropsychiatriques et inflammatoires associés au CL [66]. Des compléments nutritionnels à base de lactoferrine ont montré des effets positifs sur les symptômes gastro-intestinaux et sur la régulation immunitaire, notamment chez les enfants [67]. Bien que prometteuses, ces interventions nécessitent des essais cliniques plus robustes pour valider leur efficacité. Leur potentiel à moduler les réponses immunitaires et à améliorer la régénération cellulaire nécessite davantage d’études.
Face au dysfonctionnement mitochondrial décrit chez les patients atteints de CL, la coenzyme Q10 (CoQ10), essentielle à la production d’énergie mitochondriale, pourrait constituer un moyen d’améliorer l’état général des patients. En effet, la CoQ10 améliore l’endurance physique, réduit le stress oxydatif et favorise la récupération cognitive. Des essais cliniques ont montré qu’une supplémentation en CoQ10 (200 mg/jour) diminue l’inflammation et améliore la survie des patients septiques, suggérant son potentiel pour traiter les infections [68]. Les stimulateurs de NAD+ et les thérapies réparatrices des mitochondries, ainsi que la photobiomodulation (en stimulant la production d’énergie mitochondriale) pourraient également offrir des pistes prometteuses pour atténuer les symptômes du COVID long.
Les médecines alternatives
Les médecines traditionnelles ou alternatives, grâce à leurs composés phytochimiques actifs, pourraient offrir un soulagement des symptômes du CL. Une étude pilote menée par Kim et al. sur 45 patients a démontré la faisabilité de traiter le CL avec trois traitements à base de plantes pendant 12 semaines [69]. En outre, une revue a identifié 159 remèdes issus de la médecine Yunâni6, qui pourraient potentiellement traiter les complications du CL [70]. Cependant, malgré leur utilisation répandue pendant la pandémie, les effets de ces remèdes sur les séquelles à long terme sont mal documentés. Des études cliniques futures, avec des groupes témoins appropriés et des échantillons suffisamment larges, sont nécessaires pour confirmer leur sécurité et leur efficacité.
L’acupuncture, une thérapie chinoise traditionnelle, est bien connue pour le traitement des affections respiratoires et le soulagement de symptômes tels que l’insomnie, la fatigue, la dyspnée et l’inflammation. Elle a montré des résultats prometteurs dans le traitement du COVID-19 aigu, apportant de l’espoir à certains patients souffrant de CL [71,72]. Des recherches récentes suggèrent que l’acupuncture pourrait avoir des effets thérapeutiques sur le CL en régulant les neurotransmetteurs et les cytokines, et en agissant sur certaines voies de signalisation [73]. Toutefois, ces hypothèses nécessitent une validation expérimentale. En raison de la diversité des symptômes du CL, des traitements individualisés et holistiques sont nécessaires. De futures recherches devraient aussi explorer l’impact de l’acupuncture sur le microbiote intestinal et le système nerveux.
L’acupuncture au laser, moins invasive et indolore, gagne en popularité et montre des résultats prometteurs dans l’atténuation de symptômes tels que la dyspnée et la fatigue dans le contexte du CL [74]. Des recherches supplémentaires sont nécessaires pour optimiser les paramètres de ce traitement et évaluer son impact sur la microcirculation et les dysfonctionnements vasculaires liés au COVID-19, ainsi que son efficacité chez les enfants atteints de CL, dont les symptômes peuvent différer de ceux des adultes.
Études cliniques en cours : inclusion et suivi des patients
De nombreux essais cliniques sont actuellement en cours pour évaluer différentes approches thérapeutiques du CL [75]. Aux États-Unis, l’initiative RECOVER constitue l’un des programmes les plus vastes, avec plusieurs essais de phase 2 en cours, qui évaluent des traitements contre les troubles du sommeil, l’intolérance à l’effort ou le PACING structuré, utilisé pour gérer le malaise post-effort. Par ailleurs, l’essai PAX-LC examine l’efficacité d’un traitement antiviral (nirmatrelvir/ritonavir), sur une période de 15 jours, avec pour objectif une amélioration globale du bien-être des patients [76]. D’autres essais sont focalisés sur les altérations immunitaires, comme l’étude ADDRESS-LC avec le bezisterim, un anti-inflammatoire capable de franchir la barrière hémato-encéphalique. Un nouvel essai en phase 2 s’intéresse également aux inhibiteurs de JAK (abrocitinib dans l’essai CLEAR-LC), pour cibler l’inflammation chronique chez 86 patients atteints du CL. Enfin, l’étude OutSMART-LC explore quant à elle l’efficacité d’un anticorps monoclonal (AER002) contre les antigènes viraux résiduels. Ces études traduisent une volonté croissante de stratifier les patients selon leurs symptômes cliniques, dans une tentative de personnaliser les traitements. Elles intègrent de plus en plus les patients et les associations dans la conception des protocoles, renforçant ainsi la pertinence clinique des critères d’évaluation.
Conclusion
La diversité des essais menés pour essayer de traiter le CL, qui témoigne de l’hétérogénéité des symptômes rend à ce stade difficile une conclusion claire sur l’efficacité des traitements et les mécanismes mis en cause. De plus, les études sont souvent limitées par leur taille, un manque de ciblage précis et l’absence de standardisation des résultats. Pour mieux traiter les millions de cas de CL, il est crucial de développer des essais randomisés multicentriques à grande échelle. L’intelligence artificielle pourrait grandement faciliter ce processus en optimisant l’analyse des données cliniques complexes et en proposant des traitements plus personnalisés.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Chen C, Haupert SR, Zimmermann L, et al. Global prevalence of post-coronavirus disease 2019 (COVID-19) condition or long COVID: a meta-analysis and systematic review. J Infect Dis 2022 ; 226 :1593–607. [Google Scholar]
- Al-Aly Z, Rosen C. J. Long covid and impaired cognition—more evidence and more work to do. N Engl J Med 2024 ; 390 : 858–60. [Google Scholar]
- Scurati R, Papini N, Giussani P, et al. The challenge of Long COVID-19 management: from disease molecular hallmarks to the proposal of exercise as therapy. IJMS 2022 ; 23 : 12311. [Google Scholar]
- Bowe B, Xie Y, Al-Aly Z. Postacute sequelae of COVID-19 at 2 years. Nat Med 2023 ; 29 : 2347–57. [Google Scholar]
- Rahmati M, Udeh R, Yon DK, et al. A systematic review and meta-analysis of long-term sequelae of COVID-19 2-year after SARS-CoV-2 infection: A call to action for neurological, physical, and psychological sciences. J Med Vir 2023 ; 95 : e28852. [Google Scholar]
- Kozłowski P, Leszczyn ΄ska A, Ciepiela O. Long COVID definition, symptoms, risk factors, epidemiology and autoimmunity: a narrative review. AJM Open 2024 ; 11:100068. [Google Scholar]
- Callard F, Perego E. How and why patients made Long Covid. Soc Sci Med 2021 ; 268 : 113426. [Google Scholar]
- Pasini E, Corsetti G, Romano C, et al. Serum Metabolic Profile in Patients With Long-Covid (PASC) Syndrome: Clinical Implications. Front Med 2021; 22 ; 8:714426. [Google Scholar]
- Altmann DM, Whettlock EM, Liu S, et al. The immunology of long COVID. Nat Rev Immunol 2023 ; 3 :618–34. [Google Scholar]
- Davis HE, McCorkell L, Vogel JM, et al. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol 2023 ; 21:133–46. [CrossRef] [PubMed] [Google Scholar]
- Wei X, Qian W, Narasimhan H, et al. Macrophage peroxisomes guide alveolar regeneration and limit SARS-CoV-2 tissue sequelae. Science 2025 ; 387: eadq2509. [Google Scholar]
- Sariol A & Perlman S. Lung inflammation drives Long Covid. Science 2025 ; 387 : 1039–40. [Google Scholar]
- Fekete M, Lehoczki A, Szappanos Á, et al. Cerebromicrovascular mechanisms contributing to long COVID: implications for neurocognitive health. GeroScience 2025 1–35. [Google Scholar]
- Zhang L, Huang T, He H, et al. Unraveling the molecular mechanisms of Ace2-mediated post-COVID-19 cognitive dysfunction through systems genetics approach. Exp Neurol 2024 ; 381: 114921. [Google Scholar]
- Malioukis A, Snead R S, Marczika J, et al. Pathophysiological, neuropsychological, and psychosocial influences on neurological and neuropsychiatric symptoms of post-acute covid-19 syndrome: impacts on recovery and symptom persistence. Biomedicines 2024 ; 12 : 2831. [Google Scholar]
- Titze-de-Almeida R, Lacerda PHA, de Oliveira EP, et al. Sleep and memory complaints in long COVID: An insight into clustered psychological phenotypes. PeerJ 2024. 12, e16669. [Google Scholar]
- Popa E, Popa A E, Poroch M, et al. The molecular mechanisms of cognitive dysfunction in long covid: a narrative Review. Inter J Mol Sci 2025 ; 26: 5102. [Google Scholar]
- Panagea E, Messinis L, Petri M C, et al. Neurocognitive impairment in long COVID: a systematic review. Arch Clin Neuropsy 2025; 40 : 125–49. [Google Scholar]
- Plant AN, Rasheed AZ, Hasan M. Long COVID and the brain: a retrospective study of the neuropsychological manifestations of Long COVID. COVID 2025; 5(5): 65. [Google Scholar]
- Fekete R, Simats A, Bíró E, et al. Microglia dysfunction, neurovascular inflammation and focal neuropathologies are linked to IL-1-and IL-6-related systemic inflammation in COVID-19. Nat Neurosci 2025; 1–19. [Google Scholar]
- Kumar S, Bhatia Z, Seshadri S. Microbiome and mycobiome cross-talk from an immunobiotic perspective in COVID-19 and post-acute COVID-19 syndrome. Exp Immuno 2025 ; 5:1003182. [Google Scholar]
- Zhang D, Zhou Y, Ma Y, et al. Gut microbiota dysbiosis correlates with long COVID-19 at one-year after discharge. Korean Med 2023; 38: e120. [Google Scholar]
- Qiu Y, Mo C, Chen L, et al. Alterations in microbiota of patients with COVID-19: implications for therapeutic interventions. Med Comm 2024; 5: e513. [Google Scholar]
- Piazzesi A, Pane S, Del Chierico F, et al. The pediatric gut bacteriome and virome in response to sars-cov-2 infection. Front Cell Infect Microbiol 2024 ; 14:1335450. [Google Scholar]
- Barichello T, Kluwe-Schiavon B, Borba LA, et al. Alterations in Gut Microbiome Composition and Increased Inflammatory Markers in Post-COVID-19 Individuals. Mol Neurobio 2025; 1–10. [Google Scholar]
- Yousef M, Rob M, Varghese S, et al. The effect of microbiome therapy on COVID-19-induced gut dysbiosis: A narrative and systematic review. Life Sci 2024, 122535. [Google Scholar]
- Lupi L, Vitiello A, Parolin C, et al. The potential role of viral persistence in the post-acute sequelae of SARS-CoV-2 infection (PASC). Pathogens 2024; 13: 388. [Google Scholar]
- Gheorghita R, Soldanescu I, Lobiuc A, et al. The knowns and unknowns of long COVID-19: from mechanisms to therapeutical approaches. Front Immunol 2024 ; 15: 1344086. [Google Scholar]
- Peluso M J, Deeks S G. Mechanisms of long COVID and the path toward therapeutics. Cell 2024; 187: 5500–29. [Google Scholar]
- Molnar T, Lehoczki A, Fekete M, et al. Mitochondrial dysfunction in long COVID: mechanisms, consequences, and potential therapeutic approaches. Geroscience 2024; 46: 5267–86. [Google Scholar]
- Polli A, Godderis L, Martens D S, et al. Exploring DNA methylation, telomere length, mitochondrial DNA, and immune function in patients with Long-COVID. BMC Med 2025 ; 23: 60. [Google Scholar]
- Majima H J, Chatatikun M, Indo H P, et al. Lipidated COVID-19 localizes into mitochondria and causes oxidative damage to mitochondrial dna–pathophysiology of long COVID. Med Res Arch 2025; 13. [Google Scholar]
- Gusev E, Sarapultsev A. Exploring the pathophysiology of Long COVID: the central role of low-grade inflammation and multisystem involvement. Inter J Mol Sci 2024; 25: 6389. [Google Scholar]
- Kell DB, Khan MA, Kane B, et al. Possible role of fibrinaloid microclots in postural orthostatic tachycardia syndrome (POTS): focus on Long COVID. J Pers Med 2024;14. [Google Scholar]
- Beltrán-García J, Osca-Verdegal R, Pallardó FV, et al. Sepsis and coronavirus disease 2019: common features and anti-inflammatory therapeutic approaches. Critical Care Med 2020; 48:1841–4. [Google Scholar]
- Zhang S, Chang W, Xie J, et al. The efficacy, safety, and optimal regimen of corticosteroids in sepsis: a bayesian network meta-analysis. Critical Care Expl 2020 ; 2 :e0094. [Google Scholar]
- Brenner EJ, Ungaro RC, Gearry RB, et al. Corticosteroids, but not TNF antagonists, are associated with adverse covid-19 outcomes in patients with inflammatory bowel diseases: results from an international registry. Gastroenterology 2020 ; 159 :481–91. [Google Scholar]
- Gianfrancesco M, Hyrich KL, Al-Adely S, et al. Characteristics associated with hospitalisation for COVID-19 in people with rheumatic disease: data from the COVID-19 Global Rheumatology Alliance physician-reported registry. Ann Rheum Dis 2020 ;79 :859–66. [Google Scholar]
- Schultze A, Walker AJ, MacKenna B, et al. Risk of COVID-19-related death among patients with chronic obstructive pulmonary disease or asthma prescribed inhaled corticosteroids: an observational cohort study using the OpenSAFELY platform. Lancet Respir Med 2020 ; 8 :1106–20. [Google Scholar]
- Milne, A., Maskell, S., Sharp, C., Hamilton, F. W., & Arnold, D. T. (2021). Impact of dexamethasone on persistent symptoms of COVID-19: an observational study. medRxiv ; 2021-11. [Google Scholar]
- Proal AD, Aleman S, Bomsel M, et al. Targeting the SARS-CoV-2 reservoir in long COVID. Lancet Infec Dis 2025. [Google Scholar]
- Stein SR, Ramelli SC, Grazioli A. et al. SARS-CoV-2 infection and persistence in the human body and brain at autopsy. Nature 2022; 612: 758–63. [Google Scholar]
- Chakraborty C, Bhattacharya M. The current landscape of long COVID clinical trials: NIH’s RECOVER to Stanford Medicine’s STOP-PASC initiative. Mol Ther Nucleic Acids 2023 ; 33:887–9. [Google Scholar]
- Choi YJ, Seo YB, Seo JW, et al. Effectiveness of antiviral therapy on Long COVID: a systematic review and meta-analysis. JCM 2023 ;12:7375. [Google Scholar]
- Catalán I P, Buj A G, Muñoz S G, et al. Nirmatrelvir/ritonavir as a possible treatment for Long-COVID. Rev Esp Quim 2023; 36: 545. [Google Scholar]
- Durstenfeld M S, Peluso MJ, Lin F, et al. Association of nirmatrelvir for acute SARS-CoV-2 infection with subsequent Long COVID symptoms in an observational cohort study. J Med Viro 2024 ; 96: e29333 [Google Scholar]
- Nair M S, Luck M I, Huang Y, et al. Persistence of an infectious form of SARS-CoV-2 post protease inhibitor treatment of permissive cells in vitro. bioRxiv 2023. [Google Scholar]
- Ramacciotti E, Barile Agati L, Calderaro D, et al. Rivaroxaban versus no anticoagulation for post-discharge thromboprophylaxis after hospitalisation for COVID-19 (MICHELLE): an open-label, multicentre, randomised, controlled trial. Lancet 2022 ; 399 : 50–9. [Google Scholar]
- Tang N, Bai H, Chen X, et al. Anticoagulant treatment is associated with decreased mortality in severe coronavirus disease 2019 patients with coagulopathy. J Throm aemostasis 2020 ;18 :1094–9. [Google Scholar]
- Connors JM, Ariëns RAS. Uncertainties about the roles of anticoagulation and microclots in postacute sequelae of severe acute respiratory syndrome coronavirus 2 infection. J Throm Haemo 2023 ; 21 : 2697–701. [Google Scholar]
- McCarthy MW. Intravenous immunoglobulin as a potential treatment for long COVID. Exp Opin Biol Ther 2023 ; 23 :1211–7. [Google Scholar]
- Morse BA, Motovilov K, Michael Brode W, et al. A review of intravenous immunoglobulin in the treatment of neuroimmune conditions, acute COVID-19 infection, and post-acute sequelae of COVID-19 Syndrome. Brain Behav Immun 2025 ;123:725–38. [Google Scholar]
- Svačina MKR, Sprenger-Svačina A, Tsakmaklis A, et al. The gut microbiome in intravenous immunoglobulin-treated chronic inflammatory demyelinating polyneuropathy. Euro J Neuro 2023 ; 30 : 3551–6. [Google Scholar]
- Seibert FS, Stervbo U, Wiemers L, et al. Severity of neurological Long-COVID symptoms correlates with increased level of autoantibodies targeting vasoregulatory and autonomic nervous system receptors. Autoimmun reviews 2023; 22: 103445. [Google Scholar]
- Vitari N, Roy S. Intestinal immunoglobulins under microbial dysbiosis: implications in opioid-induced microbial dysbiosis. Front Microbiol 2025; 16:1580661. [Google Scholar]
- Scheppke KA, Pepe PE, Jui J, et al. Remission of severe forms of long COVID following monoclonal antibody (MCA) infusions: A report of signal index cases and call for targeted research. Amer J Emer Med 2024 ;75:122–7. [Google Scholar]
- Muyldermans S. Nanobodies: natural single-domain antibodies. Ann Rev Biochem 2013 ; 82 : 775–97. [Google Scholar]
- Rissiek, B., Koch-Nolte, F., Magnus, T. Nanobodies as modulators of inflammation: potential applications for acute brain injury. Front Cell Neurosci 2014 ; 8 : 344. [Google Scholar]
- Alexander E, Leong K W. Discovery of nanobodies: a comprehensive review of their applications and potential over the past five years. J Nanobiotech 2024; 22: 661. [Google Scholar]
- Rossotti MA, Bélanger K, Henry KA, et al. Immunogenicity and humanization of single-899 domain antibodies. FEBS J 2022 ; 289: 4304–27. [Google Scholar]
- Yu T, Zheng F, He W, et al. Single domain antibody: Development and application in biotechnology and biopharma. Immunol Rev 2024; 328: 98–112. [Google Scholar]
- Colas C, Le Berre Y, Fanget M, et al. Physical activity in Long COVID: a comparative study of exercise rehabilitation benefits in patients with Long COVID, coronary artery disease and fibromyalgia. IJERPH 2023 ; 20 : 6513. [Google Scholar]
- Gloeckl R, Zwick RH, Fürlinger U, et al. Practical recommendations for exercise training in patients with Long COVID with or without post-exertional malaise: a best practice proposal. Sports Med - Open 2024 ; 10 :47. [Google Scholar]
- Nopp S, Moik F, Klok FA, et al. Outpatient pulmonary rehabilitation in patients with Long COVID improves exercise capacity, functional status, dyspnea, fatigue, and quality of life. Respiration 2022 ; 101:593–601. [Google Scholar]
- Ghali A, Lacombe V, Ravaiau C, et al. The relevance of pacing strategies in managing symptoms of post-COVID-19 syndrome. J Trans Med 2023; 21: 375. [Google Scholar]
- Giovanetti M, Pannella G, Altomare A, et al. Exploring the interplay between COVID-19 and gut health: the potential role of prebiotics and probiotics in immune support. Viruses 2024 ; 16 : 370. [Google Scholar]
- Morello R, De Rose C, Cardinali S, et al. Lactoferrin as possible treatment for chronic gastrointestinal symptoms in children with Long COVID: case series and literature review. Children 2022 ; 9 :1446. [Google Scholar]
- Soltani R, Alikiaie B, Shafiee F, et al. Coenzyme Q10 improves the survival and reduces inflammatory markers in septic patients. BLL 2021;121:154–8. [Google Scholar]
- Kim, T. H., Yoon, J., Kim, S., Kang, B. K., Kang, J. W., Kwon, S. Herbal medicines for long COVID: A phase 2 pilot clinical study. Heliyon 2024 ; 10. [Google Scholar]
- Nikhat S, Fazil M. Shortening the long-COVID: An exploratory review on the potential of Unani medicines in mitigating post-Covid-19 sequelae. Phytomed Plus 2024 ; 4:100570. [Google Scholar]
- Feng BW, Rong PJ. Acupoint stimulation for long COVID: A promising intervention. World J Acupunc - Moxibustion 2023 ; 33 :191–7. [Google Scholar]
- Sum CH, Ching JYL, Song T, et al. Chinese medicine for residual symptoms of COVID-19 recovered patients (long COVID)—A double-blind, randomized, and placebo-controlled clinical trial protocol. Front Med 2023 ; 9 : 990639. [Google Scholar]
- Ying X, Jing Z, Yang Y, et al. Investigation of the potential molecular mechanisms of acupuncture in thetreatment of long COVID: a bioinformatics approach. Cell Mol Biol 2024 ; 70 :193–200. [Google Scholar]
- Algitany S, Fouad S, Nassif A, et al. The effect of laser acupuncture on immunomodulation and dyspnea in post-COVID-19 patients. areh 2023 ; 37:33–9. [Google Scholar]
- Vogel J, Pollack B, Spier E, et al. Designing and optimizing clinical trials for long COVID. Life Sci 2024. 122970. [Google Scholar]
- Krumholz HM, Sawano M, Bhattacharjee B, et al. The PAX LC trial: a decentralized, phase 2, randomized, double-blind study of nirmatrelvir/ritonavir compared with placebo/ritonavir for long COVID. Am J Med 2025 ; 138 : 884–92. [Google Scholar]
La dyspnée, aussi appelée essoufflement, est une sensation de difficulté à respirer. Elle peut être aiguë, c’est-à-dire survenir soudainement, ou chronique, c’est-à-dire durer plusieurs heures, semaines ou mois (ndlr).
Le Syndrome de tachycardie posturale orthostatique est une dysautonomie (dysfonctionnement du système nerveux autonome) pour laquelle un changement de la position provoque une augmentation de la fréquence cardiaque supérieure à 30 bpms, dans les 10 premières minutes après la mise en station debout (ndlr).
Le Paxlovid, est un médicament antiviral actif par voie orale, composé par deux molécules, le nirmatrelvir et le ritonavir, qui inhibent la protéase 3CLpro des coronavirus (ndlr).
Processus par lequel des molécules, appelées opsonines, se fixent sur la membrane externe de cellules cibles (généralement pathogènes ou débris cellulaires) afin de faciliter leur reconnaissance et élimination par les cellules phagocytaires du système immunitaire (ndlr).
Les nanobodies sont de petits fragments d’anticorps recombinants dérivés d’anticorps à chaîne lourde d’alpaga (ndlr).
La médecine yunâni, ou médecine unani, est une médecine traditionnelle arabe dont les origines remontent à la médecine gréco-romaine et qui dérive de la traduction en persan de la forme arabisée du galénisme. Malgré la concurrence de la médecine moderne, la médecine yunani continue d’être pratiquée en Inde, au Pakistan, au Bangladesh et en Iran. Elle a également laissé une influence durable sur d’autres médecines traditionnelles dans les pays musulmans (ndlr).
Liste des figures
 |
Figure 1. Symptômes persistants du COVID long (CL). |
| Dans le texte | |
 |
Figure 2. Fragments d’anticorps (nanobodies ou VHH) issus des anticorps chaine lourde (HCAb). Avantages et applications potentielles pour lutter contre le COVID long (CL). IgG : immunoglobuline de classe G ; scFv : fragment variable à chaîne unique |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




