| Issue |
Med Sci (Paris)
Volume 37, Number 3, Mars 2021
|
|
|---|---|---|
| Page(s) | 265 - 270 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2021012 | |
| Published online | 19 March 2021 | |
Impact du FGF21, une hormone du métabolisme énergétique, sur la reproduction
How a metabolic hormone, FGF21 (fibroblast growth factor 21) impacts reproduction
1
INRAe UMR85 Physiologie de la reproduction et des comportements, Centre INRAE Val-de-Loire, 37380 Nouzilly, France
2
Service d’endocrinologie-diabétologie-nutrition, CHU de Tours, 2 boulevard Tonnellé, 37044 Tours Cedex 9, France
*
ph.ducluzeau@chu-tours.fr
**
pascal.froment@inrae.fr
***
guillaume.bourdon@inrae.fr
L’obésité et l’insulinorésistance sont les principales maladies non infectieuses qui progressent le plus dans le monde. Elles favorisent l’hypertension, les maladies cardio-vasculaires, mais conduisent aussi à une chute de la fertilité dans les deux sexes. Le FGF21, découvert dans les années 2000, est lié au statut énergétique de l’organisme et améliore l’insulinorésistance. Via ses récepteurs (FGFR1c, 3c,et 4), il agit sur le foie et au niveau d'organes régulant le métabolisme glucido-lipidique, mais aussi sur le cerveau et les gonades. Des données récentes sont ainsi en faveur d’un rôle régulateur de FGF21 sur la fertilité, tant féminine que masculine. Mais quel rôle FGF21 peut-il jouer dans la reproduction ? Dans cette revue, nous avons examiné les différentes activités que présente cette hormone sur la reproduction, ouvrant la voie à une éventuelle utilisation thérapeutique en cas d’infertilité.
Abstract
Obesity or insulin resistance are the major non-infectious diseases that continue to progress worldwide. They promote diabetes and cardiovascular diseases, but also lead to a decrease in fertility in both sexes. FGF21, discovered in the 2000s, is a hormone closely linked to the energy status and has the ability to decrease insulin resistance. Its action through the FGFR1c, 3c & 4 receptors modulates tissues involved in energy-related metabolism but also the brain and the gonads. Recent data favor a role of FGF21 in female and male fertility, but raise the question about the role of FGF21 on reproductive function. In this review, we have scanned the different FGF21 actions on the reproductive axis, suggesting a potential therapeutic role in case of infertility.
© 2021 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (Photo © Inserm-Sharif, Ariane).
FGF21 et mécanisme d’action
Le FGF21 (fibroblast growth factor 21) est une hormone peptidique de 209 acides aminés découverte en 2000 (Figure 1A) [1]. Son taux sérique est augmenté dans deux situations métaboliques extrêmes : le déficit calorique et l’excès calorique. Il présente en effet la propriété d’être induit dans le foie, en réponse au jeûne et aux agonistes de PPARα (peroxisome proliferator-activated receptor a) [2, 3]. Mais paradoxalement, ses taux circulants sont également augmentés dans les situations d’obésité ou de diabète de type 2, sans que les mécanismes responsables soient bien identifiés.
 |
Figure 1. A. Structure de la protéine FGF21. B. Schéma résumant l’activation de la voie de signalisation du FGF21 après la fixation de l’hormone sur le récepteur FGFR1/3-bKlotho. KLB : β-Klotho ; SP : peptide signal. |
Le FGF21 appartient à la famille des fibrobrast growth factor, regroupant à ce jour 22 protéines, réparties en 7 sous-familles [4]. Ce peptide est majoritairement synthétisé par le foie, et régule l’homéostasie énergétique, notamment en favorisant l’oxydation des lipides et en accroissant l’insulinorésistance. Il permet également de lutter contre la dyslipidémie et l’obésité, ce qui en fait une cible de choix dans le traitement de l’obésité, de la stéatose hépatique et, potentiellement, du diabète de type 2 au stade précoce. Il agit en se fixant à des récepteurs membranaires exprimés par les adipocytes, les FGFR1-c, 3-c et 4, qui sont associés au cofacteur β-Klotho, ce qui en augmente leur affinité (Figure 1B). La séquence du gène FGF21 est conservée entre les espèces, avec un pourcentage d’identité allant de 75 à 99 % entre la séquence humaine et les séquences de souris, de rat, de bovin, et de chimpanzé. Ce gène semble être apparu tardivement au cours de l’évolution, puisqu’on ne retrouve aucune trace d’un gène ancestral chez les invertébrés. Il est issu d’une duplication du gène FGF19, lui-même issu d’autres phénomènes de duplication [5]. La sous-famille des FGF (fibroblast growth factor) endocrines1, propre aux vertébrés, regroupe plusieurs gènes, FGF19, 21 et 23, qui possèdent une faible homologie de séquences (37-38 %).
Le FGF21 est majoritairement synthétisé par le foie, mais aussi au niveau d’organes ou de tissus régulant le métabolisme glucido-lipidique, tels que le pancréas, le tissu adipeux, le muscle squelettique, et le cerveau. D’importantes variations de concentrations plasmatiques de FGF21 ont été mises en évidence : comprises entre 50 et 5 000 pg.mL-1 chez l’homme [4], et entre 100 et 1 000 pg.mL-1 chez la souris [6]. Sa demi-vie courte, de l’ordre de 1 heure, peut s’expliquer par sa dégradation par la FAP (fibroblast activation protein), une prolyl-endopeptidase, et par sa rapide élimination dans les urines [4]. Ce mécanisme de régulation est aboli en présence des mutations affectant FAP, ce qui s’accompagne d’une augmentation des taux circulants de FGF21 [7].
Le FGF21 se lie à plusieurs récepteurs ayant un seul domaine transmembranaire (R1TM), et à activité tyrosine kinase (TRK) : FGFR1c, 3c et 4 [8], trois isoformes du FGFR, qui nécessitent la présence du cofacteur β-Klotho pour permettre la liaison de cette hormone. Le domaine de liaison du FGF21 à β-Klotho joue un rôle primordial dans la transmission du signal qu’il induit (Figure 1B), puisqu’il permet à cette molécule membranaire de s’associer aux différents récepteurs FGFR exprimés à la surface des cellules des organes cibles (Figure 2). β-Klotho confère ainsi directement la spécificité d’action tissulaire du FGF21. Dans les adipocytes, la fixation de FGF21 à son récepteur initie l’activation de différentes voies, comme la phosphorylation de la voie des MAP kinases (mitogen-activated protein kinases) ERK1/2 (extracellular signal-regulated kinases), mais aussi celle de l’AMPK (AMP-activated protein kinase), une enzyme intervenant dans le métabolisme énergétique. La phosphorylation des molécules ERK1/2 est à l’origine du recrutement de facteurs de transcription, comme le SRF (serum response factor), qui vont induire l’expression de gènes, tels que celui codant le transporteur de glucose GLUT1. Le FGF21 modifie également l’activité du récepteur nucléaire PPARγ, un effecteur clé de la différenciation adipocytaire, et induit ainsi l’expression de l’adiponectine.
 |
Figure 2. Répartition des trois récepteurs FGFR1c, 3c et 4, et du cofacteur b-Klotho dans les principaux organes chez l’homme. X : non exprimé ; ✓ : exprimé. |
FGF21 et pathologies métaboliques
Parmi les tissus cibles du FGF21 (Figure 2), le foie est un organe majeur puisque le FGF21 favorise l’expression du PGC-1α (peroxisome proliferator-activated receptor gamma coactivator protein-1alpha), qui stimule la transcription de gènes impliqués notamment dans la mitogenèse, l’oxydation des acides gras et la néoglucogenèse [9]. Au niveau des adipocytes, le FGF21 active les mécanismes de lipolyse pour limiter l’accumulation de graisse et induit la production de chaleur. Cette activation thermogénique du tissu adipeux qui a été observée in vivo chez la souris [10] assure ainsi un contrôle des niveaux de triglycérides. In vitro, le FGF21 augmente l’absorption de glucose par les cellules adipeuses, indépendamment de l’insuline, via l’activation de la voie ERK1/2 et l’expression des transporteurs de glucose. La finalité de ce processus serait le maintien d’un apport énergétique minimal et constant, en cas de jeûne prolongé ou d’hibernation chez certains animaux, tout en maintenant une lipolyse active.
Dans des maladies métaboliques, dites de surcharge calorique, telles que le diabète de type 2, l’obésité ou la stéatose hépatique, les concentrations sanguines de FGF21 sont significativement augmentées [11]. Comme la production de FGF21 est habituellement stimulée par le jeûne, il a été suggéré que l’augmentation des concentrations sanguines en FGF21 dans ces maladies serait la conséquence d’une résistance à son action (tout comme l’insulino-résistance) ; cependant, à ce jour, ce concept de résistance reste débattu. En effet, plusieurs études réalisées sur des souris obèses ont révélé que le FGF21 permet une correction des troubles métaboliques, tout en diminuant la glycémie et l’insulino-résistance, contredisant ainsi cette hypothèse et suggérant que son utilisation pourrait avoir un bénéfice thérapeutique. C’est également le cas chez des sujets obèses ou diabétiques.
Les troubles du métabolisme, relatifs aux maladies de surcharge, peuvent impacter d’autres fonctions, comme la fertilité. Chez les femmes en âge de procréer, 5 à 10 % d’entre elles présentent une infertilité liée au syndrome des ovaires polykystiques (SOPK). Ce syndrome, qui est un trouble endocrinien courant, est associé à l’obésité, à la résistance à l’insuline, et au diabète de type 2. Chez les hommes, les effets de l’obésité, de la dyslipidémie, et de la résistance à l’insuline sur la fertilité masculine ont été clairement établis, avec une baisse de production de la testostérone et une altération de la production et de la qualité des spermatozoïdes. Du fait de ses effets bénéfiques sur l’insulinorésistance, le FGF21 pourrait représenter un outil thérapeutique permettant d'améliorer la fertilité. Des données récentes sont en faveur de ce rôle du FGF21 sur la fertilité, tant féminine que masculine (bien que ce rôle soit moins étudié chez l’homme que chez la femme).
Effets du FGF21 sur la régulation centrale de la reproduction
La reproduction et son contrôle sont sous la dépendance de deux axes : l’axe central hypothalamo-hypophysaire et l’axe périphérique gonadique. Des études portant sur le rôle du FGF21 au niveau de l'axe hypothalamo-hypophysaire ont révélé sa présence, ainsi que celle de son récepteur FGFR1c et de β-Klotho au niveau du cerveau, dès les stades embryonnaires (E10,52 à E 18,5 chez la souris, et 4 semaines post-conception chez l’homme). Chez la souris adulte, le gène fgf21 est exprimé dans plusieurs régions du cerveau, en particulier dans le mésencéphale. Chez l’homme, FGFR1, le principal récepteur du FGF21, est exprimé majoritairement au niveau du cervelet, mais aussi dans l’hypothalamus et l’hypophyse. L’hypothalamus produit la GnRH (gonadotropin-releasing hormone) qui agit sur l’hypophyse pour induire la décharge de LH, l’hormone lutéinisante, et de la FSH, l’hormone folliculostimulante qui, grâce à la circulation sanguine, régule l’activité gonadique. Chez l’homme et la souris, le cofacteur β-Klotho est également exprimé au niveau de l’hypothalamus, dans le noyau arqué, et au niveau du bulbe rachidien, dans les noyaux du raphé.
Dans des études réalisées chez la souris, l’administration de FGF21 dans l’hypothalamus (au niveau du noyau suprachiasmatique) conduit à l’arrêt, chez la femelle, de la signalisation induite par la GnRH en inhibant la production de la kisspeptine, une hormone qui, elle, module la production de GnRH et régule certains comportements sexuels et émotionnels3 (Figure 3) [12]. Le FGF21 agit également sur la libération de mélatonine par la glande pinéale, le centre de contrôle des cycles circadiens. Une des conséquences de l’administration de FGF21 chez les animaux serait de décaler les périodes de chaleurs et ainsi permettre de déclencher une reproduction dépendante des saisons ; ce centre de contrôle est en effet sensible aux périodes lumineuses.
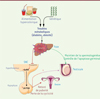 |
Figure 3. Figure schématique des actions du FGF21 sur l’axe hypothalamo-hypophysaire-gonadique. |
Toujours chez la souris, la surexpression du gène fgf21 hépatique induit également la diminution des taux de LH, sans affecter les concentrations de FSH circulantes, qui restent normales. Cette surexpression est ainsi à l’origine d’un retard de puberté, d’une baisse de la libido et de la fertilité, uniquement chez les femelles, les mâles conservant cette dernière [12]. L’impact du FGF21 sur l’ovaire est également important : le cycle ovarien est en effet modifié par le FGF21, avec une anomalie de la folliculogenèse. Ce dernier inhiberait la production de LH. Cette activité négative du FGF21 sur la fertilité est bien connue dans le cas d’un jeûne. Elle pourrait, en partie, reposer alors sur l’augmentation des taux de FGF21, liée à la carence calorique. Étayant cette hypothèse, la correction de l’apport calorique déficient, chez les souris carencées, s’accompagne d’une baisse des taux de FGF21, permettant ainsi de restaurer la fertilité des animaux avec des niveaux de LH et un retour à des cycles ovariens normaux [13]. Une autre méthode permettant de retrouver une fertilité normale chez des souris surexprimant fgf21, est d’inactiver le cofacteur β-Klotho, au niveau du système nerveux central. Cette inactivation permet en effet un retour à la fertilité, avec une réapparition des cycles ovariens et une libido retrouvée, révélant le rôle primordial du cofacteur dans la voie du FGF21 dans le cerveau [12, 13]. De même, l’inactivation du gène fgf21, à l’aide du système CRISPR/Cas9, rend les femelles peu fertiles et réduit la taille des portées, sans que le mécanisme ne soit complètement compris [14]. Chez la femme, dans le cas du syndrome des ovaires polykystiques, les concentrations sanguines de FGF21 ne semblent cependant pas être corrélées au dysfonctionnement ovarien [15]. Une mutation du gène KLB, codant la protéine β-Klotho, chez la souris, résulte en une diminution du nombre de cellules gonadotropes de l’hypophyse, et en une plus faible production de LH et FSH, par rapport aux animaux contrôles [16]. L’absence de β-Klotho n’altère pas le développement normal des neurones producteurs de GnRH, en termes de localisation et de nombre, mais réduit la sécrétion de cette hormone et entraîne une altération de la production de la LH et FSH, ainsi qu’un retard de l’apparition de la puberté [17]. En revanche, des mutations du gène codant le récepteur FGFR1c ont des conséquences néfastes sur la population de neurones producteurs de GnRH [18, 19]. Chez l’homme, il semble que la présence de FGFR1c participe également à la migration et au développement des neurones producteurs de GnRH [18], et des mutations affectant le gène codant ce récepteur conduiraient à un retard de puberté [20].
Effets du FGF21 sur la régulation de la reproduction par les gonades
Le rôle des FGF sur la fonction des gonades est conservé à travers les espèces. Les FGFR et β-Klotho sont en effet exprimés chez les animaux modèles, des invertébrés, tels que Caenorhabditis elegans [21] et la drosophile (Drosophila melanogaster) [22], jusqu’aux mammifères. Leurs mutations chez C. elegans ou chez la souris affectent la fertilité des animaux. Toutefois, peu de données concernent le FGF21. Et bien que cette hormone ne semble pas être exprimée dans l’ovaire et le testicule [23], il reste difficile d’exclure l’existence d’une faible expression à ces niveaux, ou d’un effet direct de l’hormone circulante.
Les gènes codant β-Klotho et les récepteurs FGFR1c, 3c et 4, sont exprimés dans l’ovaire, dès les stades embryonnaires E13,5 à E15,5 chez la souris, et à 4 et 11 semaines post-conception chez l’homme. Après la naissance, β-Klotho est exprimé à tous les stades de la gamétogenèse, du follicule primordial au follicule avec antrum [24]. Les récepteurs FGFR1c, 3c et 4 sont aussi détectés dans le vagin, l’endomètre utérin et l’ovaire [25]. Chez le mâle, ces récepteurs, de même que β-Klotho, sont observés au niveau des gonades, dès les stades embryonnaires (E10,5 chez la souris, et 4 semaines post-conception pour l’homme) [26]. Chez la souris adulte, β-Klotho est exprimé dans l’épididyme, lieu de maturation des spermatozoïdes, et dans le testicule. À ce niveau, ce sont surtout les cellules germinales souches qui l’expriment [27] puis, plus faiblement, les cellules plus matures, comme les spermatocytes et les spermatides. L’expression du gène codant le récepteur FGFR1c suit la même distribution que celle du gène codant β-Klotho. Le gène fgfr3 est exprimé dans l’ensemble des cellules germinales [26]. Chez l’homme, les récepteurs FGFR1c, 3c et 4 sont tous exprimés par les spermatozoïdes [26]. FGFR1c et 4 et β-Klotho sont également exprimés par les cellules de Leydig, les cellules qui produisent les androgènes.
La délétion du gène fgf21, chez la souris mâle, a un impact sur le testicule. Elle se traduit par une augmentation de l’apoptose des cellules germinales par les protéines mitochondriales, comme Bax. La production de spermatozoïdes peut être restaurée par l’administration de FGF21 exogène. Le FGF21 pourrait donc être impliqué dans le maintien d’une spermatogenèse normale et protéger les cellules germinales de la mort cellulaire, notamment dans le cas d’un trouble métabolique comme le diabète (Figure 3) [28]. Chez les animaux chez lesquels KLB est absent, en plus de l’impact que cette absence a sur le système hypothalamo-hypophysaire, les ovaires et l’utérus sont fortement atrophiés, en comparaison à ceux d’individus contrôles, atrophie notamment associée à un hypogonadisme [16]. Un sauvetage phénotypique est possible par l’apport exogène d’un ADN complémentaire (ADNc) codant la protéine β-Klotho, qui limite l’apparition de ces maladies. L’absence de β-Klotho chez la souris mâle conduit également à une atrophie des voies génitales, avec des testicules de taille réduite [16, 17, 27]. Dans l’ovaire, β-Klotho agit sur la maturation des cellules germinales : son absence dans l’ovocyte conduit à l’absence de terminaison de la première division méiotique. Elle mène ainsi à un arrêt de la maturité des follicules (absence des follicules secondaires, des follicules de De Graaf, de corps jaune) [16]. Chez le mâle, malgré une densité mitochondriale réduite, la population de cellules germinales souches (spermatogonies) est plus importante chez les animaux déficients en β-Klotho [27]. Pourtant, dès que les cellules germinales engagent leur maturation, une apoptose au stade « spermatocytes » apparaît [27]. Comme chez la femelle, les cellules germinales mâles sont dans l’incapacité de finir la méiose. Cela se traduit par la présence seulement de spermatocytes au stade pachytène (accompagnée de l’absence de spermatides et de spermatozoïdes) [16].
La voie FGF21/FGFR1c/β-Klotho semble donc être impliquée dans la régulation de la prolifération et l’apoptose des cellules germinales. La question de l’implication de cette voie en cas de dérèglements, tels que le développement de tumeurs des testicules [31] et de l’ovaire [32], peut être posée. Néanmoins, bien qu’aucune étude n’ait montré un lien direct entre cancer gonadique et FGF21, le locus contenant fgf21 fait partie des 6 locus les plus méthylés chez des patientes atteintes d’un cancer de l’ovaire. Cela laisse supposer que ce locus pourrait être un biomarqueur de prédiction de l’évolution de la maladie et de survie. Finalement, nous pouvons nous interroger sur le lien possible entre FGF21 et troubles de la spermatogenèse, des troubles que l’on observe de plus en plus fréquemment chez les individus obèses.
Conclusion
Dans cette revue, nous avons montré que le FGF21, impliqué dans la régulation du métabolisme, régule également la fertilité, au même titre que d’autres molécules, tels que l’insuline, l’IGF-1 (insulin-like growth factor-1), et certaines adipocytokines [29,30] (→).
(→) Voir les Synthèses de M. Reverchon et al., m/s n° 4, avril 2013, page 417 et m/s n° 5, mai 2015, page 493
Le système FGF21/b-Klotho a cette capacité d’informer l’axe gonadotrope sur l’état nutritionnel immédiat et l’état des réserves d’énergie, via l’hypothalamus, mais aussi d’agir sur les cellules germinales et de réguler leur différenciation et leur activité. Cette activité particulière du FGF21 ouvre donc des perspectives de recherche thérapeutique dans le domaine des troubles de la fertilité qui sont liés aux maladies métaboliques.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Nishimura T, Nakatake Y, Konishi M, et al. Identification of a novel FGF, FGF-21, preferentially expressed in the liver. Biochi. Biophys Acta 2000 ; 1492 : 203–206. [Google Scholar]
- Inagaki T, Dutchak P, Zhao G, et al. Endocrine regulation of the fasting response by PPARalpha-mediated induction of fibroblast growth factor 21. Cell Metab 2007 ; 6 : 415–425. [Google Scholar]
- Badman MK, Pissios P, Kennedy AR, et al. Hepatic fibroblast growth factor 21 is regulated by PPARalpha and is a key mediator of hepatic lipid metabolism in ketotic states. Cell Metab 2007 ; 6 : 426–437. [Google Scholar]
- Kilkenny DM, Rocheleau JV. The FGF21 receptor signaling complex: Klothoβ, FGFR1c, and other regulatory interactions. Vitam Horm 2016 ; 101 : 17–58. [PubMed] [Google Scholar]
- Itoh N.. Hormone-like (endocrine) Fgfs: their evolutionary history and roles in development, metabolism, and disease. Cell Tissue Res 2010 ; 342 : 1–11. [Google Scholar]
- Fisher f. M, Chui PC, Antonellis PJ, et al. Obesity is a fibroblast growth factor 21 (FGF21)-resistant state. Diabetes 2010; 59 : 2781–9. [CrossRef] [PubMed] [Google Scholar]
- Dunshee DR, Bainbridge TW, Kljavin NM, et al. Fibroblast activation protein cleaves and inactivates fibroblast growth factor 21. J Biol Chem 2016 ; 291 : 5986–5996. [PubMed] [Google Scholar]
- Ornitz DM, Xu J, Colvin JS, et al. Receptor specificity of the fibroblast growth factor family. J Biol Chem 1996 ; 271 : 15292–15297. [PubMed] [Google Scholar]
- Lin X, Liu YB, Hu H. Metabolic role of fibroblast growth factor 21 in liver, adipose and nervous system tissues. Biomed Rep 2017 ; 6 : 495–502. [PubMed] [Google Scholar]
- Hondares E, Iglesias R, Giralt A, et al. Thermogenic activation induces FGF21 expression and release in brown adipose tissue. J Biol Chem 2011 ; 286 : 12983–12990. [PubMed] [Google Scholar]
- Gao RY, Hsu BG, Wu DA, et al. Serum fibroblast growth factor 21 levels are positively associated with metabolic syndrome in patients with type 2 diabetes. Int J Endocrinol 2019 ; 2019 : 1–8. [Google Scholar]
- Owen BM, Bookout AL, Ding X, et al. FGF21 contributes to neuroendocrine control of female reproduction. Nat Med 2013 ; 19 : 1153–1156. [PubMed] [Google Scholar]
- Singhal G, Douris N, Fish AJ, et al. Fibroblast growth factor 21 has no direct role in regulating fertility in female mice. Mol Metabol 2016 ; 5 : 690–698. [Google Scholar]
- Liu X, Zhang P, Zhang X, et al. Fgf21 knockout mice generated using CRISPR/Cas9 reveal genetic alterations that may affect hair growth. Gene 2020; 733 : 144242. [Google Scholar]
- Olszanecka-Glinianowicz M, Madej P, Wdowczyk M, et al. Circulating FGF21 levels are related to nutritional status and metabolic but not hormonal disturbances in polycystic ovary syndrome. Eur J Endocrinol 2015 ; 172 : 173–179. [PubMed] [Google Scholar]
- Kuro-o M, Matsumura Y, Aizawa H, et al. Mutation of the mouse klotho gene leads to a syndrome resembling ageing. Nature 1997 ; 390 : 45–51. [CrossRef] [PubMed] [Google Scholar]
- Xu C, Messina A, Somm E, et al. KLB, encoding β-Klotho, is mutated in patients with congenital hypogonadotropic hypogonadism. EMBO Mol Med 2017 ; 9 : 1379–1397. [Google Scholar]
- Boehm U, Bouloux PM, Dattani MT, et al. European consensus statement on congenital hypogonadotropic hypogonadism: pathogenesis, diagnosis and treatment. Nat Rev Endocrinol 2015 ; 11 : 547–564. [CrossRef] [PubMed] [Google Scholar]
- Misrahi M.. β-Klotho sustains postnatal Gn RH biology and spins the thread of puberty. EMBO Mol Med 2017 ; 9 : 1334–1337. [Google Scholar]
- Howard SR, Dunkel L. Delayed puberty: phenotypic diversity, molecular genetic mechanisms, and recent discoveries. Endocr Rev 2019 ; 40 : 1285–1317. [CrossRef] [PubMed] [Google Scholar]
- Polanska UM, Edwards E, Fernig DG, et al. The cooperation of FGF receptor and klotho is involved in excretory canal development and regulation of metabolic homeostasis in Caenorhabditis elegans. J Biol Chem 2011 ; 286 : 5657–5666. [PubMed] [Google Scholar]
- Rothenbusch-Fender S, Fritzen K, Bischoff MC, et al. Myotube migration to cover and shape the testis of Drosophila depends on heartless, cadherin/catenin, and myosin II. Biol Open 2017 ; 6 : 1876–1888. [PubMed] [Google Scholar]
- Fon Tacer K, Bookout AL, Ding X, et al. Research resource: comprehensive expression atlas of the fibroblast growth factor system in adult mouse. Mol Endocrinol 2010; 24 : 2050–64. [Google Scholar]
- Pan H, O’Brien MJ, Wigglesworth K, et al. Transcript profiling during mouse oocyte development and the effect of gonadotropin priming and development in vitro. Dev Biol 2005 ; 286 : 493–506. [PubMed] [Google Scholar]
- Ben-Haroush A, Abir R, Ao A, et al. Expression of basic fibroblast growth factor and its receptors in human ovarian follicles from adults and fetuses. Fertil Steril 2005 ; 84(suppl 2): 1257–1268. [Google Scholar]
- Saucedo L, Buffa GN, Rosso M, et al. Fibroblast growth factor receptors (fgfrs) in human sperm: expression, functionality and involvement in motility regulation. PLoS One 2015 ; 10 : e0127297. [Google Scholar]
- Kanatsu-Shinohara M, Yamamoto T, Toh H, et al. Aging of spermatogonial stem cells by Jnk-mediated glycolysis activation. Proc Natl Acad Sci USA 2019 ; 116 : 16404–16409. [Google Scholar]
- Jiang X, Zhang C, Xin Y, et al. Protective effect of FGF21 on type 1 diabetes-induced testicular apoptotic cell death probably via both mitochondrial- and endoplasmic reticulum stress-dependent pathways in the mouse model. Toxicol Lett 2013 ; 219 : 65–76. [PubMed] [Google Scholar]
- Reverchon M, Ramé C, Dupont J. La chémérine : une adipocytokine pro-inflammatoire impliquée dans la fonction de reproduction ?. Med Sci (Paris) 2015 ; 31 : 493–498. [EDP Sciences] [PubMed] [Google Scholar]
- Reverchon M, Maillard V, Froment P, et al. Adiponectine et résistine : un rôle dans les fonctions de reproduction ?. Med Sci (Paris) 2013 ; 29 : 417–424. [EDP Sciences] [PubMed] [Google Scholar]
- Jiang X, Skibba M, Zhang C, et al. The roles of fibroblast growth factors in the testicular development and tumor. J Diabetes Res 2013 ; 2013 : 489095. [Google Scholar]
- Phelps DL, Borley JV, Flower KJ, et al. Methylation of MYLK3 gene promoter region: a biomarker to stratify surgical care in ovarian cancer in a multicentre study. Br J Cancer 2017 ; 116 : 1287–1293. [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. A. Structure de la protéine FGF21. B. Schéma résumant l’activation de la voie de signalisation du FGF21 après la fixation de l’hormone sur le récepteur FGFR1/3-bKlotho. KLB : β-Klotho ; SP : peptide signal. |
| Dans le texte | |
 |
Figure 2. Répartition des trois récepteurs FGFR1c, 3c et 4, et du cofacteur b-Klotho dans les principaux organes chez l’homme. X : non exprimé ; ✓ : exprimé. |
| Dans le texte | |
 |
Figure 3. Figure schématique des actions du FGF21 sur l’axe hypothalamo-hypophysaire-gonadique. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




