| Issue |
Med Sci (Paris)
Volume 36, Décembre 2020
Les Cahiers de Myologie
|
|
|---|---|---|
| Page(s) | 65 - 75 | |
| Section | Mise au point | |
| DOI | https://doi.org/10.1051/medsci/2020271 | |
| Published online | 11 January 2021 | |
La ventilation par embout buccal dans les maladies neuromusculaires
Mouthpiece ventilation in neuromuscular diseases
1
Clinical and Academic Department of Sleep and Breathing, Royal Brompton Hospital, London SW3 6NP, Royaume-Uni
2
Noninvasive Ventilatory Support Unit, Emergency and Intensive Care Medicine Department. Pulmonology Department, São João University Hospital. Faculty of Medicine, University of Porto, Portugal
3
Service de Pneumologie et Réanimation Respiratoire, Hôpital de la Pitié-Salpêtrière, Paris, France
4
Centre for Home Mechanical Ventilation and Specialized Centre for Neuromuscular Diseases, Inkendaal Rehabilitation Hospital, Vlezenbeek, Belgique
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Le document qui suit est la traduction intégrale du compte rendu établi à l’occasion du 252e atelier international ENMC consacré, du 6 ou 8 mars 2020, au « Développement de recommandations pour l’utilisation de la ventilation par embout buccal dans les maladies neuromusculaires », et publié très récemment dans la revue Neuromuscular Disorders (M. Chatwin, M. Gonçalves, J. Gonzalez-Bermejo, M. Toussaint, et al. 252nd ENMC international workshop: Developing best practice guidelines for management of mouthpiece ventilation in neuromuscular disorders. March 6th to 8th 2020, Amsterdam, the Netherlands. Neuromuscular Disorders 2020 ; 30 : 772–81. https://doi.org/10.1016/j.nmd.2020.07.008).
© 2020 médecine/sciences – Inserm
© Michel Toussaint
Introduction
Le Centre Neuromusculaire Européen (ENMC) a toujours fait la promotion de l’assistance ventilatoire dans les maladies neuromusculaires (MNM). Face au manque de prescriptions de la ventilation par embout buccal (ou MPV, abréviation internationale signifiant « mouthpiece ventilation ») et en l’absence de consensus concernant ses modalités et ses indications, l’ENMC a organisé du 6 au 8 mars 2020 à Amsterdam un atelier d’experts internationaux (le 252e) destiné à « Établir des recommandations pratiques pour la ventilation par embout buccal dans les maladies neuromusculaires ». Au total, 22 participants se sont réunis : 20 participants d’Europe accompagnés d’un représentant des États-Unis et un du Canada, représentant un total de 11 pays.
Ce groupe comprenait des pneumologues, infirmières et kinésithérapeutes respiratoires, tous ayant une compétence particulière dans le domaine de la ventilation par embout buccal dans les maladies neuromusculaires. Des représentants des associations de patients étaient également présents. Le programme de la réunion est disponible en ligne (supplément 1). Il faut souligner que l’atelier a eu lieu au début de la pandémie COVID-19. Certaines institutions avaient émis une interdiction de voyager. Dans de telles circonstances, plusieurs participants ont contribué à l’atelier par téléconférence. Les échanges et les discussions ont permis d’aboutir à la création d’un algorithme décisionnel pratique suggérant la mise en route idéale de la MPV chez les malades requérant une assistance ventilatoire diurne (Figure 1).
 |
Figure 1. Algorithme décisionnel précédant la mise en route d’une MPV au long cours. Il existe pour chaque étape une description de l’aide à la fourniture du service. |
Les MNM peuvent affecter les muscles squelettiques, cardiaque et respiratoires. L’importance du déficit des muscles respiratoires dépend de la gravité et de l’évolution de chaque MNM. L’insuffisance respiratoire et les infections pulmonaires sont les principales causes de mortalité et de morbidité dans de nombreuses MNM. L’introduction de l’assistance ventilatoire vise à améliorer l’hypoventilation nocturne. L’assistance ventilatoire est généralement proposée sous la forme de techniques non invasives telles que le port d’un masque nasal pendant le sommeil. Une trachéotomie peut s’avérer nécessaire en cas d’échec de la ventilation non invasive (VNI), en cas d’impossibilité de recourir à la MPV, en cas d’atteinte bulbaire ou d’incapacité à évacuer les sécrétions, ou simplement par choix du patient.
Des études montrent que la ventilation mécanique nocturne améliore les symptômes, les échanges gazeux, la qualité de vie et la survie dans les MNM [1].
À mesure que la maladie progresse et que la dépendance au ventilateur augmente, les patients ont le choix entre l’extension de la VNI durant la journée par masque et l’introduction d’une ventilation mécanique par l’intermédiaire d’une trachéotomie. Si la ventilation invasive (VI) permet de se passer d’un masque fixé sur le visage, un accès direct aux voies respiratoires via une trachéotomie expose à plusieurs types de complications : trachéomalacie, hémorragies trachéales et difficultés d’élocution.
à l’inverse, le port continu d’un masque de VNI expose aux risques d’escarre aux points de contact avec la peau, à l’hypoplasie d’une partie du massif facial, à des difficultés de déglutition et à une faible audibilité de la voix [2].
La VNI par embout buccal (MPV) représente une alternative à la VNI par masque. Elle est également connue sous le nom de MPV en circuit ouvert et se pratique en journée via un respirateur portatif. Elle peut être utilisée pendant de nombreuses activités telles que parler, manger, déglutir ou tousser.
La MPV n’est pas une technique nouvelle. Lors d’un congrès sur le syndrome post-polio en 1953, le Dr Affeldt faisait déjà état d’un appareillage respiratoire capable de réaliser une MPV par le biais d’une pièce buccale habituellement utilisée pour les épreuves fonctionnelles respiratoires [3]. John Bach et ses collaborateurs ont joué un rôle important dans la diffusion mondiale de cette technique de MPV, la rendant de plus en plus populaire [4].
Les objectifs de l’atelier
L’objectif général de l’atelier était de parvenir à :
-
Analyser les résultats de l’enquête sur la MPV réalisée en amont de l’atelier et les publier dans un article à part.
-
Établir des recommandations pratiques concernant la MPV dans les MNM, en abordant, en particulier, les modes de ventilation, les réglages et l’équipement requis, ainsi que les modalités d’un suivi optimal.
-
Établir un algorithme décisionnel concernant l’utilisation de la MPV comme assistance ventilatoire diurne (voir Figure 1).
-
Définir les critères de jugement pour de futures études impliquant la MPV.
Présentations introductives
Après les mots de bienvenue d’Alexandra Breukel (directrice de l’ENMC) et des animateurs de l’atelier, (Michelle Chatwin, Michel Toussaint, Miguel Gonçalves et Jésus Gonzalez-Bermejo), Michelle Chatwin et Michel Toussaint ont présenté le programme de l’atelier et ses objectifs. Ensuite, Jésus Gonzalez-Bermejo a ouvert la première session consacrée à la question de savoir à quel moment il fallait aller au-delà de la ventilation nocturne. Ce moment correspond à l’apparition d’un déficit des muscles respiratoires. Dans un premier temps, ce déficit conduit à une insuffisance respiratoire pendant la phase REM du sommeil du fait de l’inhibition sélective des muscles respiratoires accessoires. à mesure de la progression du déficit, les perturbations ventilatoires apparaissent ensuite pendant toutes les phases du sommeil et conduisent finalement à une insuffisance respiratoire avec hypercapnie en journée. Le traitement par VNI nocturne va améliorer les échanges gazeux et normaliser les gaz du sang [5]. Cependant, certains patients vont développer une hypercapnie diurne et, de ce fait, nécessiter une assistance ventilatoire en journée. Avant de démarrer une MPV, il est recommandé de s’assurer que le patient est correctement ventilé durant toute la nuit. Il faut surveiller le taux de dioxyde de carbone (CO2) [mesuré par différentes méthodes (gazométrie artérielle CO2 en fin d’expiration (EtCO2) ou en transcutané (TcCO2)], l’oxymétrie, et, chaque fois que possible, les données de suivi téléchargeables à partir du respirateur. Des réglages de la machine s’imposent en cas d’hypercapnie persistante. Si les données de suivi indiquent une faible utilisation du respirateur, il faudra en chercher la cause et mettre en place une stratégie pour y remédier. Une fois la capnie contrôlée durant la nuit, un recours à une ventilation diurne pourra être discuté en fonction de plusieurs critères (voir encadré 1). Il est important de signaler que la présence d’une hypercapnie est un signe tardif qu’il ne faut pas attendre avant de proposer une MPV diurne, en particulier dans les maladies rapidement évolutives.
Peter Wijkstra et Laura Verweij ont mis l’accent sur les différences physiologiques, pour un patient donné, entre assistances ventilatoires diurne et nocturne. Les patients en ventilation nocturne sont endormis et en position couchée. Pendant leur sommeil, on note une diminution de la commande respiratoire. En conséquence, l’assistance respiratoire mécanique doit comprendre un système de fréquence respiratoire de rappel répondant aux besoins ventilatoires nocturnes
Durant la journée, les malades sont éveillés, en mouvement, tout occupés qu’ils sont à manger, boire, tousser lorsqu’ils sont encombrés ou à échanger sur le plan social, le tout nécessitant des besoins de ventilation différents comme le montrent les réglages distincts du ventilateur pendant la nuit ou la journée. Le ventilateur utilisé de jour doit être portable et embarquable sur le fauteuil roulant, et doit disposer d’une bonne batterie. Historiquement, l’extension de la ventilation nocturne à la période diurne fait, malheureusement, souvent appel à une trachéostomie comme interface. Les progrès technologiques ont permis d’utiliser des masques nasaux avec ou sans embouts narinaires, laissant libre l’orifice buccal (comme dans la Figure 2). Ceci est de nature à améliorer la communication orale, la déglutition et les interactions sociales.
 |
Figure 2. De gauche à droite : (1) l’image de gauche montre un patient avec un masque nasal de type Dreamwear (© Philips Respironics, Murrysville, PA, USA) ; (2) la deuxième, un patient avec un masque nasal de type AirFit N30i (© ResMed, San Diego, CA, USA) ; (3) celle du milieu, un patient utilisant une interface nasale à coussinets de type Swit Lt (© ResMed, San Diego, CA, USA) ; (4 et 5) les deux photographies de droite correspondant à une pièce buccale (4 à gauche) et une pipette (5 à droite) (© Michelle Chatwin). |
Michel Toussaint et Miguel Gonçalves ont mené les discussions sur le choix entre VNI et assistance ventilatoire diurne par le biais d’une trachéostomie. Le groupe souhaite souligner que la décision d’une trachéotomie dépend parfois des habitudes historiques du centre en la matière, ou si la canule a été mise en place à l’occasion d’un épisode aigu. Dans certains pays, la trachéotomie rend éligible le patient à un remboursement des soins effectués 24 heures sur 24 soit par une infirmière, dans certains cas, ou par un simple soignant. Dans d’autres pays, la mise en œuvre d’une trachéotomie peut imposer une vie en institution plutôt qu’une vie à domicile. Le choix en faveur d’une trachéotomie est parfois dicté par les difficultés d’évacuation des sécrétions, et ce malgré l’emploi de techniques habituellement efficaces dans le drainage (ACTS), ou de l’impossibilité de porter un masque sur le visage. En matière de survie, on ne dispose pas d’études randomisées prouvant une meilleure efficacité d’une technique sur l’autre. Le groupe a conclu, pour ce qui concerne les recommandations pratiques, qu’il était nécessaire de faire un essai de MPV avant d’envisager une trachéotomie. Dans un premier temps, il faut optimiser la VNI nocturne couplée aux techniques de désencombrement proximal (toux assistée) [6, 7]. En cas d’indication d’une trachéotomie au long cours, le choix du patient, lequel doit être suffisamment informé des tenants et des aboutissants de cette technique, reste essentiel face aux conseils du médecin qui ne peut décider seul sans l’avis du malade.
Peter Wijskra a étudié différents types de masque en cas d’impossibilité de MPV et a souligné que l’on peut utiliser alternativement un masque nasal avec ou sans embouts narinaires, lesquels sont plus petits qu’un masque facial entier (voir Figure 2). On peut également utiliser des ventilateurs à pression positive ou une ceinture abdominale de type pneumobelt [8].
Miguel Goncalves et Michelle Chatwin ont présenté les résultats préliminaires de l’enquête consacrée à la MPV. Ils ont relevé une grande disparité dans les indications de MPV selon les pays et à l’intérieur d’un même pays. A chaque endroit où existaient des indications préférentielles de MPV et une méthode d’initiation à la MPV, cette information a été reprise dans l’algorithme décisionnel établi lors de l’atelier (Figure 1) concernant le démarrage d’une MPV chez des patients neuromusculaires. Les présentations faites lors de l’atelier et les discussions autour des trois thématiques suivantes ont également contribué à l’élaboration de la Figure 1.
Première thématique : les aspects techniques de la MPV
Cette thématique a été abordée par le biais d’une discussion menée par Michel Toussaint et Miguel Gonçalves concernant les modalités et réglages de la MPV. Seuls certains centres sont en mesure de proposer une MPV. Classiquement, il s’agit d’une ventilation volumétrique [9], réglée de façon à apporter un volume courant d’au moins 700 ml et allant jusqu’à 1 500 ml [10, 11], sans pression positive expiratoire (PEEP), le tout par l’intermédiaire d’un embout buccal ou d’une pipette maintenus par un support articulé [10, 12]. Pour autant, il arrive que certains patients ne disposent que de ventilateurs barométriques et qu’il faille, dans ce cas, jouer sur les réglages de la pression. Un débat a eu lieu pour savoir lequel des deux modes ventilatoires, celui axé sur le volume [9, 13] ou celui sur la pression [11, 14] était le meilleur, et si l’ajout d’une PEEP apportait une quelconque valeur ajoutée. Certains cliniciens pourraient s’inquiéter, notamment chez les enfants, des effets d’une ventilation volumétrique où un volume fixe d’air est délivré à forte pression. Le groupe a fait remarquer que les cas de pneumothorax restaient rares et que les bénéfices l’emportaient largement sur les inconvénients. La survenue d’un pneumothorax est vraisemblablement multifactorielle mais peut effectivement être en lien avec tout appareil délivrant une pression positive, y compris les relaxateurs de pression (MI-E). En fait, si la MPV est réglée en mode volumétrique et si le volume d’air est jugé trop important par le malade, celui-ci peut simplement ouvrir la bouche et laisser l’air fuir. Certains cliniciens sont amenés à régler la machine afin d’apporter un large volume d’air, le patient étant libre de prendre le volume qu’il souhaite. Le but de cette stratégie d’une inspiration profonde sur base d’un volume courant élevé est de mettre au repos les muscles inspiratoires du patient de sorte qu’il soit capable de respirer sans assistance pendant quelques cycles respiratoires avant de reprendre une nouvelle inspiration profonde par MPV. Une autre stratégie consiste à apporter au patient un volume courant moindre, mais cependant suffisant pour lui permettre un stockage d’air de plusieurs salves inspiratoires (appelé air-stacking) pour atteindre sa MIC (capacité inspiratoire maximale) en seulement trois inspirations. En fonction des réglages et de l’objectif de la MPV, il est possible que le patient soit sous-ventilé lorsqu’il est déconnecté du circuit [15] ce qui impose de surveiller les paramètres en journée et de réévaluer les réglages. Le groupe a néanmoins considéré qu’on pouvait pratiquer la MPV soit en mode volumétrique soit en mode barométrique mais que, chez les enfants, la ventilation barométrique pouvait être considérée. Pour les adultes, l’algorithme décisionnel (Figure 1) donne la préférence à un mode volumétrique lors de la mise en route d’une MPV.
Doug McKim et Michel Toussaint ont rappelé qu’il n’y avait de consensus ni sur le choix de la pièce buccale ni sur les préférences des malades eux-mêmes. Certains centres prônent la fabrication sur mesure des supports [16] tandis que d’autres privilégient les modèles du commerce. La clé pour disposer d’un bras articulé est que ce dernier puisse bouger en même temps que le patient. Ceci signifie qu’il doit toujours être dans une position adéquate lorsque le patient a besoin de reprendre de l’air. Pour faciliter la MPV, le groupe recommande que les centres moins expérimentés, ne disposant d’aucune possibilité de fabrication individuelle de ces supports, utilisent les modèles du commerce. Il faut que les patients essaient d’abord une pipette ou une pièce buccale et qu’on leur laisse le choix de décider ce qui est le meilleur pour eux. Avec la pièce buccale, ils doivent être capables de ventiler convenablement, de ne plus être dyspnéiques, et de faire de l’air-stacking. Un avis complémentaire peut être demandé à un centre spécialisé si nécessaire.
Johan Chaulet et Wendy Hughes ont apporté un éclairage sur ce que les professionnels devraient savoir de la position des malades et des aidants en la matière. Les patients peuvent ressentir de l’anxiété au démarrage de la MPV et un soutien psychologique peut s’avérer nécessaire. Cela peut passer par une psychothérapie, ou par un partage d’expériences et de résolution des problèmes avec d’autres utilisateurs ou avec des représentants d’associations de patients, le tout en toute indépendance. Un suivi régulier par le prescripteur aide à régler les problèmes en amont et avant qu’ils ne deviennent un véritable obstacle au niveau psychosocial. Il est essentiel que le patient et le médecin soient associés au processus décisionnel aboutissant au choix de l’appareillage respiratoire et de ses accessoires. Le timing idéal pour la MPV doit être planifié à l’avance pour optimiser ses chances de succès. Si un centre local ne peut apporter l’aide nécessaire, les patients pourront se retourner, le cas échéant, vers un centre plus spécialisé dans la ventilation à domicile.
Hélène Prigent et Adam Ogna ont exposé les résultats probants d’études sur banc d’essais concernant les ventilateurs et les modalités de la MPV. Les machines de ventilation à domicile sont faites pour fournir une assistance ventilatoire chez des patients dont les conditions respiratoires sont, a priori, stables, et en cas de besoin de ventilation de la part des patients, quand la charge du ventilateur et les résistances du circuit restent stables ou ne se modifient que légèrement avec le temps [17]. La MPV représente un défi pour les ventilateurs utilisés à domicile du fait d’un cycle de ventilation relativement irrégulier et de changements rapides des conditions de charge liés aux déconnexions et reconnexions au circuit de manière intermittente [15]. Ceci a été bien montré dans des études faisant apparaitre un taux élevé de déclenchements de l’alarme pendant la MPV [12].
Les ventilateurs à domicile les plus récents ont un système pneumatique à turbine permettant d’assurer une ventilation volumétrique en se référant à un algorithme destiné à adapter la pression de travail d’un cycle inspiratoire en fonction des cycles précédents. Pendant une MPV volumétrique, la boucle de rétro-action est parfois longue, aboutissant à une lenteur de réaction de la part du ventilateur pour s’adapter aux variations de résistances, conduisant finalement à un mauvais calibrage du volume courant lors des déconnexions/reconnexions au circuit. Ce mauvais calibrage se traduit par une régulation à la baisse de la pression de travail du ventilateur, et, dès lors, par la production d’un volume moins important qu’attendu lors des cycles suivants [13]. Ce phénomène est très variable selon les ventilateurs, 2 à 4 cycles étant nécessaires à la stabilisation du volume courant, particulièrement quand on règle la machine avec une fréquence respiratoire de rappel [14]. De plus, les fuites volontaires, qui sont fréquentes et normales dans la MPV, diminuent la précision des ventilateurs à mesurer le volume courant réellement délivré [18-220] amplifiant ainsi le phénomène. L’utilisation de la MPV en mode barométrique entraine un décalage encore plus grand du volume courant lors d’une déconnexion du circuit, mais diminue la chute de volume courant au moment de la reconnexion au circuit [13]. Ceci peut s’expliquer par une boucle plus courte de rétro-contrôle permettant l’adaptation de la pression de travail du ventilateur au cours du cycle respiratoire en cours. Comme la boucle de rétro-contrôle n’inclut ni le patient ni le circuit, ce mode de ventilation ne garantit pas un volume courant constant en cas de changement de résistance ou de compliance du système respiratoire (par exemple, en cas d’obstruction des voies aériennes par des secrétions), le tout exposant le patient ventilo-dépendant à une assistance respiratoire insuffisante. Les ventilateurs actuellement disponibles ont des capacités adaptatives distinctes quant aux changements brutaux de charge respiratoire qui sont une caractéristique de la MPV. Ainsi, le choix du ventilateur destiné à la MPV chez un patient donné doit prendre en compte les avantages et inconvénients de chacun d’entre eux, et du mode ventilatoire envisagé.
Comme évoqué par Annalisa Carlucci, les alarmes-machines peuvent poser un problème. Une alarme qui se déclenche inopinément peut dissuader un patient d’utiliser cette technique. Il est essentiel de faire la différence entre utilisation constante/continue ou intermittente de la ventilation.
Chez le patient non-ventilo-dépendant, la MPV peut être utilisée à la demande avec une fréquence respiratoire réglée à zéro. Dans ce cas, les alarmes sont inutiles. L’apparition récente d’un mode spécifique à la MPV sur certains ventilateurs permet de régler sur zéro les alarmes de déconnexion et d’apnées, le système de rappel respiratoire aussi sur zéro et de garder une alarme de basse pression de 1 à 5 millibars. En l’absence d’option MPV spécifique ou si celle-ci n’est pas applicable, une combinaison appropriée entre volume courant, temps inspiratoire et type d’embout buccal (en termes de résistance) permet d’éviter un réglage d’alarmes de déconnexion et de basse pression. Pour les patients hautement ventilo-dépendants, différents réglages d’alarmes peuvent s’envisager. Dans ce cas, les alarmes d’apnée et de déconnexion peuvent être utiles, tout comme un back-up chez les malades ventilo-dépendants très affaiblis (Figure 1). Une alarme rappelant le risque de ré-inspirer son propre air (rebreathing) est utile chez le patient ventilo-dépendant. Sur certains ventilateurs, elle est enclenchée par défaut ou a besoin de l’être par un bouton « on » sur d’autres. En l’absence d’alarme de « rebreathing », on peut utiliser un circuit à un seul segment disposant d’une valve expiratoire.
Deuxième thématique : les conditions du succès d’une MPV
L’introduction d’une MPV à un moment propice est la condition de son succès. Josh Benditt a fait une présentation sur la phase initiale de la mise en place de la MPV. D’après la littérature passée en provenance des sociétés scientifiques à propos de l’assistance ventilatoire diurne, la MPV devrait démarrer quand le patient devient, tardivement, hypercapnique dans la journée [21]. La MPV constitue bien un traitement de choix pour la ventilation diurne. Les cliniciens experts estiment qu’au cas où la durée de la ventilation assistée est égale ou supérieure à 12 heures par jour, avec ou sans hypercapnie [15], la MPV doit être proposée chez les patients qui souhaitent conserver une assistance respiratoire non-invasive en journée et qui ont une bonne capacité d’occlusion labiale [22], et/ou chez ceux présentant une dyspnée [23] ou une tachypnée [23-25], même sans hypercapnie.
Les critères pour prescrire une MPV ont été définis par le groupe d’experts :
-
une durée de ventilation par masque égale ou supérieure à 12 heures par jour ;
-
une hypercapnie diurne avec normocapnie nocturne ;
-
une dyspnée disparaissant sous l’effet de l’assistance respiratoire diurne ;
-
la nécessité d’augmenter le volume de la voix ;
-
le besoin d’augmenter l’efficacité de la toux en dehors du lieu de vie (c’est-à-dire quand on ne dispose pas d’une appareil insufflateur-exsufflateur).
Miguel Gonçalves et Jésus Gonzalez-Bermejo ont fait une présentation sur la surveillance au moment de la mise en route de la MPV et à plus long terme. Nardi et al. [15], en étudiant les polygraphies ont mis en évidence que certains patients, sans s’en rendre compte, et sans manifester de symptômes non plus, ne se ventilaient pas suffisamment. La MPV expose au risque d’hypoventilation mais aussi au risque d’hyperventilation. Voir la Figure 3 où un algorithme de surveillance des patients sous MPV est proposé.
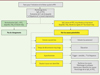 |
Figure 3. Algorithme suggéré pour le monitorage pendant la phase initiale et le suivi des patients avec ventilation de l’embout buccal. Solution suggérée suivant le problème identifié. Dioxyde de carbone (CO2), Saturation pulsée en oxygène (SpO2), fréquence respiratoire (RR), travail respiratoire (WOB). |
Pour ce qui concerne la gestion des risques et la sécurité, plusieurs problèmes ont été signalés par Jésus Gonzalez-Bermejo et Wendy Hugues. Johann Chaulet et Laura Verweij-van den Oudenrijn ont ensuite insisté sur le besoin d’éducation et de formation du patient et de ses aidants. Le manque d’information et de formation ont été identifiés comme des freins à la diffusion de la MPV [9, 10]. Il n’y a pour l’instant aucun protocole spécifique en la matière, des soins individualisés étant pourtant nécessaires au succès de la MPV [26, 27]. Ceci peut représenter un problème pour les centres non spécialisés dans la mise en place de la MPV. Les présentations et les discussions qui ont suivi pendant cette session ont permis d’élaborer trois documents à l’appui du développement de la formation pour les utilisateurs de MPV et leurs aidants, ainsi qu’une check-list destinée aux cliniciens prescripteurs de MPV, et des fiches-types pour la prescription et le descriptif des appareillages (voir les suppléments en ligne S1, S2 et S3). Le groupe a rappelé la nécessité impérieuse de disposer, pour chaque malade, d’un ballon insufflateur de type Ambu®, celui-ci devenant indispensable en cas de panne de l’appareil de ventilation.
Les sécrétions peuvent empêcher le succès de la MPV. Barbara Garabelli a fait une communication sur les techniques de désencombrement (ATC pour Airway Clearance Techniques), l’accent étant mis sur la MPV. La MPV peut être utilisée comme technique de désencombrement proximal pour favoriser la toux [5, 7]. L’air-stacking, technique de stockage d’air, est classiquement réalisé avec un ballon insufflateur type Ambu® ou un ventilateur en mode volumétrique [25]. Rappelons que la MPV peut être réglée en mode assisté-contrôlé pour le volume ou la pression [25]. On peut apprendre au patient à réaliser une inspiration profonde si la MPV est en mode barométrique [28] mais l’air-stacking réalisé en mode volumétrique est à préférer du fait d’un volume plus important d’air avant de tousser. Le groupe en a conclu qu’il fallait impérativement apprendre à aider au désencombrement par une inspiration profonde ou par air-stacking lors d’une MPV, de préférence en mode volumétrique.
Tiago Pinto et Nicolas Audag ont communiqué sur les aspects techniques des fauteuils roulants, les ventilateurs et les batteries externes. Le fauteuil roulant doit disposer d’un système d’arrimage solide et fiable afin d’accueillir le respirateur. Le support du tuyau permettra à l’embout buccal de rester bien en place. Les objectifs principaux sont le confort, la sécurité, l’autonomie sur batterie et la facilité d’utilisation, tant pour les patients que pour leurs soignants.
Les fabricants de respirateurs ont récemment développé un mode MPV spécifique, avec des accessoires tels qu’un bras de support pour les tuyaux ainsi que des circuits sans valve expiratoire permettant au patient de réaliser une expiration en dehors de la pièce buccale [29]. L’autre avantage de ces supports articulés et de ces tuyaux est de pouvoir garder la pièce buccale dans une position idéale et d’être adaptable au fauteuil roulant. De nos jours, les fabricants de respirateurs produisent des machines sauvant des vies et capables de tenir huit heures grâce à une batterie interne, et jusqu’à seize heures avec des batteries auxiliaires.
Au moment du choix du ventilateur, il faut pouvoir l’essayer sur le fauteuil roulant et se demander si ce dernier est toujours capable de basculer en arrière, ventilateur et accessoires compris.
Il est important de discuter avec le patient des questions suivantes. L’embout buccal se fixe-t-il au fauteuil ou sur les épaules du patient lui-même et est-ce que le support bouge avec le patient ? Y-a-t-il un risque d’écrasement ou de détachement des tuyaux ? Est-il possible de brancher le ventilateur ou ses accessoires sur les circuits propres au fauteuil roulant ? On doit aussi se souvenir que le poids de la batterie externe alourdit le fauteuil roulant dans son ensemble. Il existe pour les patients ambulatoires une formule avec sac à dos permettant de préserver à la mobilité.
Troisième thématique : retour d’expérience de la MPV dans les MNM lors de soins aigus et de l’exercice physique
Hélène Prigent et Johan Chaulet ont rapporté leur expérience concernant la MPV dans la dystrophie musculaire de Duchenne (DMD). Dans cette maladie, la MPV a été proposée comme forme alternative de VNI à partir des années 1990 [30]. Au fil des ans, cette technique a été de plus en plus employée pour améliorer la tolérance à la VNI, augmenter sa durée d’utilisation en journée, permettant ainsi son utilisation chez des malades ventilo-dépendants. Cette technique est devenue une indication à part entière dans la prise en charge respiratoire du patient atteint de DMD afin d’éviter complètement une ventilation sur trachéotomie. Les malades rapportent un effet positif de la MPV sur la dyspnée et la fatigue, mais ils soulignent aussi son bénéfice pour l’élocution, la déglutition et la communication [25]. Un des principaux défis posés à la population DMD par la MPV réside dans la sécurisation de l’accès à la pièce buccale surtout chez les patients les plus déficitaires au niveau moteur.
Doug McKim et Jesus Sancho avaient préparé une session sur l’utilisation de la MPV dans la sclérose latérale amyotrophique (SLA). Comme dans beaucoup d’autres maladies neuromusculaires, les patients atteints de SLA souffrent d’un déficit respiratoire évolutif conduisant à une insuffisance respiratoire et à une toux inefficace. Ceci se produit toutefois très rapidement. La VNI est connue pour prolonger la survie, soulager les symptômes, éviter des hospitalisations et améliorer la qualité de vie [22]. Comme dans les autres pathologies neuromusculaires, la VNI est utilisée pendant les heures de sommeil mais, au fur et à mesure de la progression du déficit des muscles respiratoires, les besoins en assistance ventilatoire augmentent. La MPV peut devenir une option chez certains malades atteints de SLA. Une fois mise en place, la MPV peut augmenter la survie, sans trachéotomie, jusqu’à 9,5 mois [22]. Pourtant, 19 % des patients SLA seulement en tirent bénéfice [22]. Deux facteurs déterminent le succès d’une MPV. D’abord, la présence d’un débit expiratoire de pointe à la toux (PCF pour peak cough flow) permettant d’assurer une toux efficace, c’est-à-dire suffisante pour évacuer les sécrétions. Ensuite, la présence d’un minimum de fonction bulbaire pour maintenir l’embout au niveau de la bouche, assurer une occlusion labiale satisfaisante et s’arranger pour atteindre une capacité inspiratoire maximale (MIC). L’atteinte bulbaire s’aggravant avec le temps, la MPV devient inefficace et ceci peut être suspecté lorsque la MIC devient plus petite que la capacité vitale (différence MIC-CV). On devrait permettre aux malades atteints de SLA d’accéder à la MPV plutôt que de limiter leur choix à la trachéotomie et à la VNI continue par masque.
Brit Hov a présenté la MPV dans l’amyotrophie spinale (SMA). Avec l’arrivée de thérapies émergentes (oligonucléotides antisens type nusinersen et thérapie génique), l’histoire naturelle de cette maladie est en train de se modifier. Alors que la MPV a pu être utilisée dans la SMA de type II [31], elle est désormais envisageable dans la SMA de type I à condition d’avoir une fonction bulbaire satisfaisante. Chez les enfants nécessitant aussi une assistance ventilatoire en journée, l’avantage de la MPV par rapport à une VNI par masque nasal réside dans la prévention de la survenue d’une hypoplasie de la moitié du visage, et la prévention ou l’amélioration du pectus excavatum. Il peut y avoir aussi un impact sur l’image de soi avec une augmentation des capacités de communication et de participation, par exemple en classe ou dans d’autres activités sociales. Les enfants seraient possiblement mieux équipés avec un mode de ventilation barométrique, et ceci du fait des risques barotraumatiques liés à de trop gros volumes. Le mode volumétrique peut s’avérer utile pour lutter contre le pectus excavatum. Dans notre expérience, la MPV peut s’envisager chez des enfants dès l’âge de huit ans, mais cela n’empêche pas de l’essayer chez des enfants plus jeunes. La MPV aide à normaliser les gaz du sang [31].
Michelle Chatwin et Wendy Hughes ont abordé les indications de la MPV dans d’autres MNM. La littérature est très pauvre en la matière. Quelques études signalent son utilisation dans le déficit en maltase acide [32], la maladie de Steinert [32], les dystrophies musculaires des ceintures [32], la dystrophie facio-scapulo-humérale [9], les myopathies congénitales [9], la dystrophie musculaire de Becker [9], les myopathies métaboliques [9], le syndrome post-polio [15], l’adhalinopathie primaire, les dystrophies musculaires congénitales [29], la maladie de Pompe [15] ainsi que dans d’autres maladies neuromusculaires [9]. A partir des données de l’enquête conduite par les auteurs, la MPV s’avère être fréquemment utilisée dans les myopathies congénitales (= 60), les lésions médullaires cervicales (n = 46), et la maladie de Steinert (n = 30), un peu moins dans les dystrophies musculaires congénitales et la maladie de Pompe. Le groupe estime que chaque patient devrait être évalué individuellement et ne pas être privé de MPV au motif d’une carence de données de la littérature concernant sa maladie en particulier.
Josh Benditt et Johan Chaulet ont fait une présentation de l’impact de la MPV sur la déglutition. Chez les sujets normaux, le processus de déglutition est hautement synchronisé. La déglutition étant précédée d’une inspiration et suivie d’une expiration. Le volume inspiré avant déglutition entraîne une pression sous-glottique positive, laquelle préviendrait la survenue de fausses routes [33]. Même en l’absence de troubles bulbaires, les personnes ayant perdu cette séquence normale de déglutition et souffrant par ailleurs d’un déficit des muscles respiratoires, peuvent présenter des troubles de déglutition, probablement du fait d’une pression sous-glottique positive insuffisante [34]. Ceci pourrait expliquer pourquoi les fausses routes seraient plus fréquentes avec une trachéotomie. Un manque de coordination des phases pharyngée et laryngée de la déglutition peut également perturber cette déglutition. Lorsque la déglutition est suivie d’une inspiration plutôt que d’une expiration, ceci augmente encore davantage le risque de fausse route.
Garguilo et al. ont montré que la VNI par voie nasale améliorait la déglutition dans la DMD en augmentant le nombre de gorgées après une expiration, réduisant ainsi la fragmentation de la déglutition et améliorant la dyspnée lors d’une déglutition [35]. Lors d’une étude qualitative portant sur la déglutition, des sujets ont rapporté que la MPV améliorait la déglutition comparativement à une respiration spontanée et que la VNI par voie nasale était plus difficile à gérer que la MPV au moment des repas [36].
Cliniquement, les sujets sous MPV sont capables de mieux parler avec des volumes plus grands en construisant des phrases plus longues sans interruption. On manque cependant de preuves pour appuyer cette impression clinique. Une étude qualitative récente a montré que la durée et le volume de la parole étaient améliorées chez les patients. Toutefois, le besoin de reprendre son souffle était ressenti comme une gêne à la fluidité de la parole et posait aussi problème pour les logiciels de reconnaissance vocale [37].
Pour une meilleure pratique, et au moment de la mise en place de la MPV, il faut apprendre au patient à comment mieux déglutir sous MPV. Chez les patients pour lesquels les fausses routes posent un problème, une augmentation du volume d’air délivré avant de déglutir donne plus de temps pour manger et avaler. Ceci peut signifier que les patients ont besoin de deux réglages distincts pour leur MPV, l’un pour manger, l’autre pour respirer.
Miguel Gonçalves a fait une présentation sur l’utilisation de la MPV en soins intensifs. Alors qu’on dispose de très peu de preuves sur son utilisation en soins intensifs, la MPV peut être indiquée pour éviter une intubation en cas de pneumopathie chronique [38]. De façon protocolisée, on peut utiliser la MPV dans la phase qui suit l’extubation mais aussi comme aide au désencombrement [39]. Le groupe recommande clairement que dans un environnement de soins intensifs, on ne prive pas le patient de l’utilisation de la MPV dont il bénéficierait depuis très longtemps. Par ailleurs, un essai avec MPV pourrait éviter d’avoir recours à une trachéotomie chez les malades ayant une très faible capacité vitale.
Miguel Gonçalves a également souligné que la MPV apporte une aide à la ventilation lors de l’exercice physique (comme la marche) dans les MNM. Le bénéfice de la MPV lors de l’exercice a été bien démontré. La MPV a été utilisée comme moyen d’induire une meilleure tolérance à l’effort chez des patients atteints de paralysie diaphragmatique [40]. Une MPV est également envisageable chez des sujets marchants mais il faut s’assurer que l’équipement puisse être arrimé sur un déambulateur, un fauteuil roulant, ou une poussette, ou qu’il puisse être glissé dans un sac à dos. Un des principaux problèmes de portabilité réside dans le poids. Une autre option est d’utiliser un ballon insufflateur. Les malades peuvent aussi avoir besoin d’une pince nasale pour éviter les fuites à ce niveau.
Juan Escarrabill a présenté le retour d’expérience du patient à propos de la MPV. La survie, la qualité de vie en santé, l’activité physique, et les admissions à l’hôpital représentent des outils classiques évaluant principalement l’efficacité et la sécurité. La satisfaction est une construction subjective intimement liée aux attentes de la personne. Le vécu du patient va bien au-delà de la satisfaction. Certains outils disponibles sont plus généralisables (comme des enquêtes) et d’autres sont plus descriptives (interviews en profondeur, groupes ad hoc ou panels de patients). à la fin, et grâce au regard du patient, l’évaluation de l’organisation des soins vise à identifier les besoins non couverts des malades pour améliorer la prise en charge respiratoire. Mesurer le vécu du patient est important non seulement pour guider l’amélioration du service rendu mais aussi parce que l’expérience de l’individu peut être reliée aux résultats cliniques et aux coûts [41].
à partir des discussions autour du choix des patients qui pourraient bénéficier de la MPV, le groupe a conclu que la MPV n’était pas réservée à un diagnostic étiologique particulier mais qu’elle pouvait être indiquée dans beaucoup de pathologies à partir du moment où les prérequis à une MPV étaient réunis. Les conditions de la réussite sont :
-
Être capable de maintenir en place la pièce buccale. On peut l’évaluer en demandant au patient de fermer la bouche et de gonfler les joues ;
-
Être capable de réaliser une capacité inspiratoire maximale qui soit plus grande que la capacité vitale ;
-
Être capable de comprendre le choix possible entre trachéotomie et MPV.
Autres domaines de travail
Le groupe de l’atelier a identifié que les fabricants de respirateurs gagneraient à impliquer des cliniciens et des malades lorsqu’ils développent une nouvelle technologie de MPV. Un plus grand choix pour les supports articulés et les interfaces buccales est nécessaire, notamment pour ceux pour lesquels la customisation reste difficile. Les innovations doivent être testées en laboratoire afin que les appareillages atteignent les objectifs fonctionnels. Un travail complémentaire est nécessaire pour évaluer les effets de la MPV sur la parole, la déglutition et la qualité de vie. La MPV ayant le potentiel de stabiliser les malades pendant des années, un registre des patients sous MPV serait utile. Ceci donnerait des indications supplémentaires sur le timing optimal de la mise en place de la MPV.
Davantage d’éducation est requise pour que les malades puissent, le cas échéant, bénéficier de la MPV en unité de soins intensifs, soit pour éviter une intubation soit pour passer à une VNI après une extubation réussie. Des documents d’information et des parcours individualisés concernant la MPV pourraient aider à mieux diffuser ce traitement en soins intensifs. Enfin, les réseaux sociaux et les médias pourraient favoriser l’entraide entre patients sous MPV.
Conclusion
Le manque d’expérience clinique des équipes de terrain apparait comme le principal obstacle à la diffusion de la MPV auprès des malades. Le fait de disposer d’éléments de preuve constitue un moteur puissant de prescription. Les malades ne bénéficient de thérapies qu’à la condition que des éléments de preuve ou des publications informent la communauté médicale sur les meilleures pratiques. Ceci provient du fait que les cliniciens sont souvent dans l’incertitude concernant les bénéfices attendus pour un patient donné.
Le frein principal à la diffusion de la MPV n’est pas lié au manque d’appareillage disponible ou à l’absence de preuve clinique. D’autres facteurs limitants liés au patient lui-même ont été identifiés : impossibilité d’obtenir une bonne occlusion de la bouche autour de la pièce buccale, le refus de faire un essai avec une MPV, et un manque d’interfaces et d’appareillage.
Le 252e atelier international ENMC apporte ainsi des documents de référence pour les bonnes pratiques concernant la MPV dans les maladies neuromusculaires.
Indications pour démarrer une MPV
-
Capacité vitale inférieure à 30% de la valeur théorique
-
Ventilation au masque d’une durée supérieure ou égale à 12 heures par jour
-
Une dyspnée dont le score est supérieur à 2,5 sur l’échelle de Borg et qui s’améliore sous l’effet de l’assistance ventilatoire
-
Perte de poids
-
Essoufflement lors du repas
-
Essoufflement lors du parler et/ou voix de faible intensité
-
Sevrage de la ventilation invasive
-
Adaptation à aucune forme de VNI
-
Hypercapnie diurne, avec échanges gazeux normalisés la nuit par la VNI.
Liste des participants
Michel Toussaint, Belgique
Michelle Chatwin, Royaume-Uni
Jésus Gonzalez-Bermejo, France
Miguel Gonçalves, Portugal
Joshua O. Benditt, États-Unis
Doug McKim, Canada
Brit Hov, Norvège
Valeria Sansone, Italie
Hélène Prigent, France
Annalisa Carlucci, Italie
Peter Wijkstra, Pays-Bas
Tiina Andersen, Norvège
Barbara Garabelli, Italie
Joan Escarrabill, Espagne
Tiago Pinto, Portugal
Nicolas Audag, Belgique
Laura Verweij-van den Oudenrijn, Pays-Bas
Adam Onga, Suisse
Wendy Hughes, Royaume-Uni
Christian Devaux, France
Johann Chaulet, France
Jesus Sancho, Espagne
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Autorisations
Traduction et reproduction autorisées par Elsevier B.V.
Reproduction des photographies autorisée par Michelle Chatwin.
Matériel Supplémentaire
Du matériel supplémentaire associé à cet article peut être retrouvé dans la version en ligne de l’article original à l’adresse suivante doi: 10.1016/j.nmd.2020.07.008.
Remerciements
à J. Andoni Urtizberea et au département Myoinfo de la Direction des Actions Médicales de l’AFM-Téléthon pour la traduction du texte.
Références
- Shneerson JM, Simonds AK. Noninvasive ventilation for chest wall and neuromuscular disorders. Eur Respir J 2002 ; 20 : 480–487. [CrossRef] [PubMed] [Google Scholar]
- Hull J, Aniapravan R, Chan E, et al. British thoracic society guideline for respiratory management of children with neuromuscular weakness. Thorax 2012; 67 (suppl 1) : I 1–40. [PubMed] [Google Scholar]
- Round table conference on poliomyelitis equipment. Roosevelt Hotel, White Plaines May 1953 ; New York: City National Foundation for Infantile Paralysis-March of Dimes Inc [Google Scholar]
- Bach JR, Alba AS, Saporito LR. Intermittent positive pressure ventilation via the mouth as an alternative to tracheostomy for 257 ventilator users. Chest 1993 ; 103 : 174–182. [PubMed] [Google Scholar]
- Annane D, Orlikowski D, Chevret S. Nocturnal mechanical ventilation for chronic hypoventilation in patients with neuromuscular and chest wall disorders. Cochrane Database Syst Rev 2014; Cd001941. [PubMed] [Google Scholar]
- Toussaint M, Chatwin M, Gonzales J, Berlowitz DJ. 228th ENMC international workshop: airway clearance techniques in neuromuscular disorders, Naarden, The Netherlands, 3–5 March 2017. Neuromuscular Disord 2018 ; 28 : 289–298. [CrossRef] [Google Scholar]
- Chatwin M, Toussaint M, Goncalves MR, et al. Airway clearance techniques in neuromuscular disorders: a state of the art review. Respir Med 2018 ; 136 : 98–110. [CrossRef] [PubMed] [Google Scholar]
- Yang GF, Alba A, Lee M, Khan A. Pneumobelt for sleep in the ventilator user: clinical experience. Arch Phys Med Rehabil 1989 ; 70 : 707–711. [PubMed] [Google Scholar]
- Khirani S, Ramirez A, Delord V, et al. Evaluation of ventilators for mouthpiece ventilation in neuromuscular disease. Respir Care 2014 ; 59 : 1329–1337. [Google Scholar]
- Pinto T, Chatwin M, Banfi P, Winck JC, Nicolini A. Mouthpiece ventilation and complementary techniques in patients with neuromuscular disease: a brief clinical review and update. Chron Respir Dis 2017 ; 14 : 187–193. [CrossRef] [PubMed] [Google Scholar]
- Boitano LJ, Benditt JO. An evaluation of home volume ventilators that support open-circuit mouthpiece ventilation. Respir Care 2005 ; 50 : 1457–1461. [Google Scholar]
- Hess DR. Noninvasive ventilation for neuromuscular disease. Clin Chest Med 2018 ; 39 : 437–447. [CrossRef] [PubMed] [Google Scholar]
- Ogna A, Prigent H, Falaize L, et al. Accuracy of tidal volume delivered by home mechanical ventilation during mouthpiece ventilation: a bench evaluation. Chron Respir Dis 2016 ; 13 : 353–360. [CrossRef] [PubMed] [Google Scholar]
- Fiorentino G, Esquinas AM. Home ventilator performances with mouthpiece ventilation: does resistance change effectiveness?. Clin Respir J 2018 ; 12 : 1765–1766. [PubMed] [Google Scholar]
- Nardi J, Leroux K, Orlikowski D, et al. Home monitoring of daytime mouthpiece ventilation effectiveness in patients with neuromuscular disease. Chron Respir Dis 2016 ; 13 : 67–74. [CrossRef] [PubMed] [Google Scholar]
- Toussaint M, Steens M, Wasteels G, Soudon P. Diurnal ventilation via mouthpiece: survival in end-stage Duchenne patients. Eur Respir J 2006 ; 28 : 549–555. [CrossRef] [PubMed] [Google Scholar]
- Fauroux B, Leroux K, Pepin JL, Lofaso F, Louis B. Are home ventilators able to guarantee a minimal tidal volume?. Intensive Care Med 2010 ; 36 : 1008–1014. [CrossRef] [PubMed] [Google Scholar]
- Khirani S, Louis B, Leroux K, et al. Harms of unintentional leaks during volume targeted pressure support ventilation. Respir Med 2013 ; 107 : 1021–1029. [CrossRef] [PubMed] [Google Scholar]
- Sogo A, Montanya J, Monso E, et al. Effect of dynamic random leaks on the monitoring accuracy of home mechanical ventilators: a bench study. BMC Pulm Med 2013 ; 13 : 75. [CrossRef] [PubMed] [Google Scholar]
- Carlucci A, Schreiber A, Mattei A, et al. The configuration of bi-level ventilator circuits may affect compensation for non-intentional leaks during volume-targeted ventilation. Intensive Care Med 2013 ; 39 : 59–65. [CrossRef] [PubMed] [Google Scholar]
- Finder JD, Birnkrant D, Carl J, et al. Respiratory care of the patient with Duchenne muscular dystrophy: ATS consensus statement. Am J Respir Crit Care Med 2004 ; 170 : 456–465. [CrossRef] [PubMed] [Google Scholar]
- Bedard ME, McKim DA. Daytime mouthpiece for continuous noninvasive ventilation in individuals with amyotrophic lateral sclerosis. Respir Care 2016 ; 61 : 1341–1348. [Google Scholar]
- McKim DA, Griller N, LeBlanc C, et al. Twenty-four hour noninvasive ventilation in Duchenne muscular dystrophy: a safe alternative to tracheostomy. Can Respir J 2013 ; 20 : e5–e9. [CrossRef] [PubMed] [Google Scholar]
- Bach JR. Noninvasive respiratory management of patients with neuromuscular disease. Ann Rehabil Med 2017 ; 41 : 519–538. [CrossRef] [PubMed] [Google Scholar]
- Garuti G, Nicolini A, Grecchi B, et al. Open circuit mouthpiece ventilation: concise clinical review. Rev Port Pneumol 2014 ; 20 : 211–218. [CrossRef] [PubMed] [Google Scholar]
- Fiorentino G, Esquinas AM. Tidal volume during mouthpiece non-invasive home ventilation: when the choice is the right answer. Chron Respir Dis 2016 ; 13 : 383–384. [CrossRef] [PubMed] [Google Scholar]
- Ogna A, Lofaso F. Mouthpiece ventilation: individualized patient care is the key to success. Chron Respir Dis 2016 ; 13 : 385–386. [CrossRef] [PubMed] [Google Scholar]
- Dalziel J.. On sleep and an apparatus for promoting artificial respiration. Br Assoc Advancement Sci 1838 ; 2 : 127. [Google Scholar]
- Toussaint M, Chatwin M, Verhulst S, Reychler G. Preference of neuromuscular patients regarding equipment for daytime mouthpiece ventilation: a randomized crossover study. Clin Respir J 2020; 14 : 214–21. [PubMed] [Google Scholar]
- Bach JR, O’Brien J, Krotenberg R, Alba AS. Management of end stage respiratory failure in Duchenne muscular dystrophy. Muscle Nerve 1987 ; 10 : 177–182. [Google Scholar]
- Ward K, Ford V, Ashcroft H, Parker R. Intermittent daytime mouthpiece ventilation successfully augments nocturnal non-invasive ventilation, controlling ventilatory failure and maintaining patient independence. BMJ Case Rep 2015; 2015. [Google Scholar]
- Garuti G, Nicolini ADR, et al. Mouthpiece ventilation in patients with neuromuscular disease: a brief clinical review. Phys Med Rehab Int 2014 ; 1 : 1–4. [Google Scholar]
- Gross RD, Atwood CW, Jr, Grayhack JP, Shaiman S. Lung volume effects on pharyngeal swallowing physiology. J Appl Physiol (1985) 2003 ; 95 : 2211–2217. [CrossRef] [PubMed] [Google Scholar]
- Terzi N, Orlikowski D, Aegerter P, et al. Breathing-swallowing interaction in neuromuscular patients: a physiological evaluation. Am J Respir Crit Care Med 2007 ; 175 : 269–276. [CrossRef] [PubMed] [Google Scholar]
- Garguilo M, Lejaille M, Vaugier I, et al. Noninvasive mechanical ventilation improves breathing-swallowing interaction of ventilator dependent neuromuscular patients: a prospective crossover study. PLoS One 2016 ; 11 : e0148673. [Google Scholar]
- Britton D, Hoit JD, Benditt JO, et al. Swallowing with noninvasive positive-pressure ventilation (NPPV) in individuals with muscular dystrophy: a qualitative analysis. Dysphagia 2019. [Google Scholar]
- Britton D, Hoit JD, Pullen E, et al. Experiences of speaking with noninvasive positive pressure ventilation: a qualitative investigation. Am J Speech Lang Pathol 2019 ; 28 : 784–792. [CrossRef] [PubMed] [Google Scholar]
- Glerant JC, Rose D, Oltean V, et al. Noninvasive ventilation using a mouthpiece in patients with chronic obstructive pulmonary disease and acute respiratory failure. Respiration 2007 ; 74 : 632–639. [CrossRef] [PubMed] [Google Scholar]
- Bach JR, Gonçalves MR, Hamdani I, Winck JC. Extubation of patients with neuromuscular weakness: a new management paradigm. Chest 2010 ; 137 : 1033–1039. [CrossRef] [PubMed] [Google Scholar]
- Koopman M, Vanfleteren L, Steijns S, et al. Increased exercise tolerance using daytime mouthpiece ventilation for patients with diaphragm paralysis. Breathe (Sheff) 2017 ; 13 : 225–229. [CrossRef] [PubMed] [Google Scholar]
- Manary MP, Boulding W, Staelin R, Glickman SW. The patient experience and health outcomes. N Engl J Med 2013 ; 368 : 201–203. [Google Scholar]
Liste des figures
 |
Figure 1. Algorithme décisionnel précédant la mise en route d’une MPV au long cours. Il existe pour chaque étape une description de l’aide à la fourniture du service. |
| Dans le texte | |
 |
Figure 2. De gauche à droite : (1) l’image de gauche montre un patient avec un masque nasal de type Dreamwear (© Philips Respironics, Murrysville, PA, USA) ; (2) la deuxième, un patient avec un masque nasal de type AirFit N30i (© ResMed, San Diego, CA, USA) ; (3) celle du milieu, un patient utilisant une interface nasale à coussinets de type Swit Lt (© ResMed, San Diego, CA, USA) ; (4 et 5) les deux photographies de droite correspondant à une pièce buccale (4 à gauche) et une pipette (5 à droite) (© Michelle Chatwin). |
| Dans le texte | |
 |
Figure 3. Algorithme suggéré pour le monitorage pendant la phase initiale et le suivi des patients avec ventilation de l’embout buccal. Solution suggérée suivant le problème identifié. Dioxyde de carbone (CO2), Saturation pulsée en oxygène (SpO2), fréquence respiratoire (RR), travail respiratoire (WOB). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




