| Issue |
Med Sci (Paris)
Volume 36, Number 1, Janvier 2020
|
|
|---|---|---|
| Page(s) | 16 - 19 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/2019254 | |
| Published online | 04 February 2020 | |
L’activation des canaux Nav1.9 par le monoxyde d’azote à l’origine des céphalées par abus médicamenteux
Activation of Nav1.9 channels by nitric oxide causes medication-overused headache
SomatoSens, laboratoire de neurosciences cognitives, UMR 7291 CNRS, Aix-Marseille-université, CS80011, 51 boulevard Pierre Dramard, 13344 Marseille, France
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Les céphalées (maux de tête) correspondent à des douleurs locales unilatérales ou généralisées ressenties au niveau de la boîte crânienne ou du visage. Elles constituent une cause fréquente de consultation en médecine générale, et représentent donc un réel problème de santé publique [1]. L’efficacité des analgésiques et des substances anti-migraineuses dites spécifiques est souvent limitée. En conséquence, beaucoup de patients ont recours à une surconsommation de médicaments, qui favorise la survenue d’une céphalée chronique. Dans l’étude que nous avons réalisée [2], nous montrons que ces céphalées par abus médicamenteux (CAM) [3] résultent d’une hypersensibilité des nocicepteurs méningés au monoxyde d’azote (NO), un gaz qui peut être libéré dans certaines situations de stress ou suite à l’ingestion d’aliments riches en nitrates.
Céphalées et abus médicamenteux
Les céphalées primaires surviennent sans aucun lien avec une autre maladie ou un traumatisme identifié. Les principales céphalées primaires sont les céphalées de tension et la migraine. Épisodiques (6 % de la population) ou chroniques (3 % de la population), les céphalées de tension se caractérisent par des maux de tête touchant les deux côtés du crâne, souvent associés à une sensation de pression, alors que la migraine, qui touche environ 7 millions de personnes en France, avec une forte prévalence chez les femmes [4], se manifeste par des douleurs locales unilatérales. Les crises de migraine sont souvent accompagnées de nausées, de vomissements, et d’une hypersensibilité à la lumière (photophobie), au son (phonophobie), ou aux odeurs (osmophobie) [5]. Ces crises peuvent être déclenchées par de nombreux facteurs, aussi bien alimentaires (chocolat, alcool, café), que psychologiques (stress, anxiété, contrariété), hormonaux (règles, pilule contraceptive), ou sensoriels (lumière, bruit, odeurs) [6].
Parmi les médicaments prescrits contre les céphalées, les plus communément utilisés sont les analgésiques simples (paracétamol), les anti-inflammatoires non stéroïdiens (ibuprofène, aspirine, indométacine), mais également les anti-migraineux plus spécifiques, tels que les dérivés ergotés (dihydroergotamine, tartrate d’ergotamine) et les triptans (sumatriptan). Néanmoins, le traitement des douleurs induites par les crises migraineuses reste faiblement efficace sur le long terme, et pris en trop grande quantité ou trop souvent, ces médicaments peuvent entraîner une chronicité des céphalées primaires. Les CAM affectent principalement les femmes souffrant préalablement de céphalées primaires [7], le plus souvent migraineuses, chez lesquelles la prise excessive et régulière d’antalgiques et/ou d’anti-migraineux spécifiques conduit à l’induction et à l’entretien de céphalées chroniques quotidiennes.
La physiopathologie des CAM, un préalable à l’amélioration de leur prise en charge thérapeutique, nécessite d’approfondir nos connaissances sur la contribution du système trigéminal. En effet, l’explication des CAM, bien qu’encore imprécise, réside en partie dans une sensibilisation des fibres nerveuses dévolues à la perception douloureuse dans le cinquième nerf crânien, ou nerf trijumeau. Dans ce cadre, nous avons étudié les mécanismes de contrôle de l’excitabilité des nocicepteurs méningés dans un modèle animal de CAM induites par l’administration chronique de sumatriptan, un anti-migraineux ciblant les récepteurs 5HT1B/1D de la sérotonine (ou 5-hydroxytryptamine, 5HT).
Le canal Nav1.9 est exprimé dans les nocicepteurs méningés
Les fibres nociceptives expriment une large gamme de canaux ioniques spécialisés dans la détection et la propagation du message douloureux. Parmi eux, le canal ionique Nav1.9 (isoforme 9 des canaux ioniques sélectifs pour les ions Na+) revêt un intérêt particulier. Ce canal présente des caractéristiques inhabituelles pour un canal sodique, qui lui confèrent un rôle prépondérant dans les phénomènes d’hyperexcitabilité neuronale et dans la douleur, aussi bien chez l’animal que chez l’homme [8–13] (→).
(→) Voir la Nouvelle de S. Lolignier, m/s n° 2, février 2016, page 115 ; et la Nouvelle de P. Delmas, m/s n° 2, février 2019, page 162
Cela nous a conduits à formuler l’hypothèse selon laquelle le canal Nav1.9 contribuerait à la sensibilisation des nocicepteurs méningés et à l’activation du système trigémino-vasculaire observée pendant la céphalée. Les immunomarquages chez la souris montrent que le canal Nav1.9 est localisé dans les fibres trigéminales méningées exprimant également le CGRP (calcitonin gene-related peptide), une molécule pro-inflammatoire associée aux crises de migraine.
L’invalidation du gène Scn11a chez la souris abolit les symptômes induits par le monoxyde d’azote, un déclencheur de migraine
Afin de reproduire chez des souris les conditions d’une céphalée induite par abus médicamenteux, nous leur avons administré du sumatriptan [14] (ou une solution saline) durant six jours, à l’aide de minipompes osmotiques implantées sous la peau. La sensibilité tactile des animaux a ensuite été évaluée à l’aide des filaments de von Frey1, environ 15 jours après l’arrêt de l’administration du médicament ou de la solution saline. Les animaux traités avec la solution saline développent une allodynie tactile de faible amplitude (allodynie basale) en réponse à l’injection sous-cutanée de nitroprussiate de sodium, un donneur de NO connu pour déclencher la crise migraineuse chez l’homme. Les animaux traités par le sumatriptan ont en revanche une hypersensibilité tactile très marquée suite à l’administration de NO. Ces animaux présentent une allodynie péri-orbitale et extra-céphalique exacerbée, ainsi qu’une hypersensibilité au son et à la lumière, des symptômes observés classiquement pendant la crise migraineuse chez l’homme. Les souris mutantes Scn11a -/- (dépourvues du canal Nav1.9), après l’administration du sumatriptan, ne présentent pas d’allodynie tactile exacerbée, ni de photophobie ou phonophobie en réponse au NO. Ainsi, les animaux soumis à un traitement chronique par le sumatriptan présentent une sensibilisation latente aux déclencheurs de migraine qui dépend de la présence du canal Nav1.9 dans les nocicepteurs méningés.
Le sumatriptan sensibilise les canaux Nav1.9 au NO
Afin d’explorer le rôle des canaux Nav1.9 dans les CAM, nous avons enregistré l’activité de ces canaux dans les neurones trigéminaux qui innervent les méninges, par la technique de patch clamp. Chez les animaux traités par le sumatriptan, le niveau d’expression du gène Scn11a et l’amplitude basale du courant Nav1.9 sont similaires à ceux des animaux non traités (témoins). Cependant, l’application aiguë de NO triple l’amplitude du courant Nav1.9 chez les animaux traités par le sumatriptan, alors qu’elle n’a que peu d’effet sur le courant Nav1.9 dans les nocicepteurs méningés des animaux témoins. Cette augmentation du courant est associée à un déplacement, d’environ –20 mV, de la valeur du potentiel de membrane pour laquelle 50 % de la conductance Nav1.9 est activée (potentiel de « demi-activation »), ce qui traduit une activation facilitée. Parce que la guanosine monophosphate cyclique (GMPc) joue un rôle prépondérant dans la signalisation du NO, nous avons cherché à déterminer l’implication de la guanylate cyclase soluble, l’enzyme de synthèse du GMPc, dans l’activation des canaux Nav1.9. L’ajout de bleu de méthylène (100 μM), un inhibiteur de cette enzyme, abolit l’effet du NO sur le courant Nav1.9. L’ensemble de ces résultats indique que la voie NO-GMPc est anormalement active sur le courant Nav1.9 dans les nocicepteurs méningés des animaux traités par le sumatriptan.
L’activation des canaux Nav1.9 par le NO induit une hyperexcitabilité des nocicepteurs méningés
Nous avons étudié les propriétés d’excitabilité des neurones afférents méningés, identifiés par marquage rétrograde, en réponse à une exposition au NO. L’activation du courant Nav1.9 par le NO convertit les décharges phasiques des neurones en décharges prolongées dans environ 80 % des nocicepteurs de la dure-mère chez les animaux traités par le sumatriptan. En outre, la présence de NO abaisse le seuil de déclenchement du potentiel d’action (PA) dans ces neurones. En revanche, le NO n’a pas d’effet significatif sur la décharge et le seuil de déclenchement du PA des nocicepteurs innervant les méninges de souris témoins traitées par une simple solution saline, ou de souris Scn11a -/- traitées par le sumatriptan.
L’activation des canaux Nav1.9 par le NO provoque la sécrétion de CGRP
Nous avons testé si l’hyperexcitabilité induite par l’activation de Nav1.9 avait un effet sur la sécrétion de CGRP (calcitonin-gene related peptide), un marqueur de la céphalée migraineuse. à de très faibles concentrations, le nitroprussiate de sodium n’a pas d’effet significatif sur le taux de CGRP sécrété par les neurones trigéminaux de souris témoins cultivés in vitro. En revanche, il augmente significativement (+70 %) la sécrétion de CGRP par les neurones trigéminaux de souris traitées par le sumatriptan. Cet effet n’est pas observé avec les neurones trigéminaux des souris Scn11a -/-, ce qui indique que l’activation des canaux Nav1.9 est un prérequis à la libération de CGRP.
La contribution de la libération de CGRP à l’allodynie tactile induite par le NO a été évaluée en injectant un antagoniste de ce peptide (α-CGRP8-37) 30 minutes avant le nitroprussiate de sodium. L’injection d’α-CGRP8-37 inhibe l’allodynie tactile exacerbée des souris traitées par le sumatriptan, indiquant que la libération de CGRP est impliquée dans les phénomènes d’hypersensibilité induits par le NO.
L’activation des canaux Nav1.9 par le NO induit une vasodilatation des artères méningées
Puisque les fibres des nerfs trijumeaux exprimant Nav1.9 et CGPR innervent la paroi des artères méningées, nous avons évalué les effets du NO sur la vasodilatation des artères méningées. Nous avons utilisé la technique d’anémométrie laser Doppler, qui permet de mesurer le débit sanguin, et ainsi d’apprécier indirectement le calibre des vaisseaux sanguins. Le nitroprussiate de sodium, injecté dans la veine jugulaire, provoque une augmentation progressive du débit sanguin des artères méningées chez les souris traitées par le sumatriptan. En revanche, il est sans effet chez les souris Scn11a -/- traitées de façon similaire. L’ensemble de ces résultats indique que l’activité accrue des nocicepteurs méningés consécutive à l’activation des canaux Nav1.9 par le NO déclenche la libération de médiateurs vasoactifs (GCRP, et possiblement substance P) responsables de la vasodilatation des artères méningées. Ce phénomène est particulièrement marqué chez les animaux traités avec le sumatriptan, et sous-tend le passage de substances inflammatoires et algogènes dans les tissus méningés.
L’activation des canaux Nav1.9 par le NO induit une dégranulation des mastocytes
L’hyperexcitabilité des nocicepteurs méningés peut entraîner une dégranulation des mastocytes, avec libération de médiateurs préformés vasoactifs, pro-inflammatoires, et nociceptifs. Nous avons donc examiné si la sécrétion de médiateurs par les nocicepteurs, chez les animaux CAM, pouvait provoquer la dégranulation des mastocytes méningés et amplifier la douleur. Nous montrons que le cromoglycate de sodium, un médicament qui inhibe la dégranulation des mastocytes, réduit considérablement l’intensité de l’allodynie généralisée chez les animaux traités par le sumatriptan lorsqu’il est injecté par voie intra-péritonéale avant le nitroprussiate de sodium. En revanche, ce médicament n’a aucun effet sur l’allodynie basale des souris Scn11a -/- traitées de façon similaire. Ces résultats montrent que, chez les animaux traités par le sumatriptan, l’activation des canaux Nav1.9 induit une dégranulation des mastocytes qui accentue le message douloureux véhiculé par les fibres méningées trigéminales.
Les médiateurs mastocytaires stimulent en retour les canaux Nav1.9
Nous avons recherché si la dégranulation des mastocytes pouvait rétroagir sur les terminaisons nerveuses trigéminales en modulant l’activité des canaux Nav1.9. Les mastocytes se caractérisent par la présence, dans leur cytoplasme, de très nombreux médiateurs chimiques comme la sérotonine, l’histamine, les prostaglandines, la tryptase, ou l’héparine. Les enregistrements électrophysiologiques en patch clamp ont montré que l’histamine et la prostaglandine E2 (PGE2) sont de puissants activateurs du courant Nav1.9 dans les nocicepteurs méningés (amplitude du courant augmentée de 100 ± 25 % ou 233 ± 40 %, respectivement). Ces effets sont observés indépendamment du traitement des souris, ce qui implique que les médiateurs mastocytaires, une fois libérés, vont exciter les fibres sensitives du nerf trijumeau et aggraver la douleur.
En conclusion
Cette étude apporte un éclairage nouveau sur les mécanismes responsables de la CAM induite par l’usage fréquent des triptans. Ces céphalées résultent d’une activation anormale des canaux Nav1.9 par le NO. Ces canaux agissent alors comme une plaque tournante déclenchant une cascade d’évènements (hyperexcitabilité neuronale, inflammation neurogène, vasodilatation artérielle, extravasation plasmatique, dégranulation des mastocytes) qui conduit à une hypersensibilité du système trigémino-vasculaire favorisant le déclenchement de nouvelles crises (Figure 1). Ces résultats ouvrent la voie à de nouvelles approches pour le traitement de la migraine, fondées sur l’association de bloqueurs des canaux Nav1.9 aux médicaments anti-migraineux.
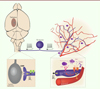 |
Figure 1. Le canal Nav1.9 : plaque tournante des céphalées par abus médicamenteux. Le monoxyde d’azote (NO), qui peut être produit par différentes sources, active les canaux Nav1.9 des nocicepteurs méningés chez les animaux traités par le sumatriptan. L’activation de ces canaux induit un état d’hyperexcitabilité neuronale à l’origine de la libération de médiateurs inflammatoires et vasoactifs qui agissent sur les vaisseaux méningés et les mastocytes. La sécrétion de CGRP, et peut-être d’autres médiateurs, provoque la dégranulation des mastocytes résidents. Les médiateurs libérés par les mastocytes potentialisent en retour l’activation des canaux Nav1.9, renforçant ainsi l’excitation des nocicepteurs méningés, un cercle vicieux qui conduit à un message douloureux exacerbé. Caudalis subnucleus, noyau caudal trigéminal ; SP, substance P ; CGRP, calcitonin-gene related peptide ; Hist, histamine ; NO, monoxyde d’azote ; TG neuron, neurone trigéminal ; PGE, prostaglandine E2 (© Illustration par Nancy Osorio). |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Série de 20 filaments fabriqués en nylon et calibrés pour fléchir à une force connue, la plage proposée allant de 8.10- 5 à 3 N. Ils permettent de tester l’allodynie ou l’hyperalgésie mécanique en délivrant une force d’intensité connue à différents endroits du corps.
Références
- Steiner TJ Stovner LJ Katsarava Z et al. The impact of headache in Europe: principal results of the Eurolight project. J Headache Pain 2014 ; 15 : 31. [CrossRef] [PubMed] [Google Scholar]
- Bonnet C, Hao J, Osorio N, et al. Maladaptive activation of Nav1.9 channels by nitric oxide causes triptan-induced medication overuse headache. Nature Commun 2019; 10 : 4253. [CrossRef] [Google Scholar]
- Diener HC Dodick D Evers S et al. Pathophysiology, prevention, and treatment of medication overuse headache. Lancet Neurol 2019 ; 18 : 891–902. [CrossRef] [PubMed] [Google Scholar]
- Bigal ME Lipton RB Stewart WF The epidemiology and impact of migraine. Curr Neurol Neurosci Rep 2004 ; 4 : 98–104. [CrossRef] [PubMed] [Google Scholar]
- Headache Classification Committee of the International Headache Society IHS). The international classification of headache disorders, 3rd edition (beta version. Cephalalgia 2013 ; 33 : 629–808. [CrossRef] [PubMed] [Google Scholar]
- Marmura MJ Triggers, protectors, and predictors in episodic migraine. Curr Pain Headache Rep 2018 ; 22 : 81. [CrossRef] [PubMed] [Google Scholar]
- Kristoffersen ES Lundqvist C Medication-overuse headache: a review. J Pain Res 2014 ; 7 : 367–368. [CrossRef] [PubMed] [Google Scholar]
- Lolignier S, Bonnet C, Gaudioso C, et al. The Nav1.9 channel is a key determinant of cold pain sensation and cold allodynia. Cell Rep 2015; 11 : 1067–78. [CrossRef] [PubMed] [Google Scholar]
- Maingret F Coste B Padilla F et al. Inflammatory mediators increase Nav1.9 current and excitability in nociceptors through a coincident detection mechanism. J Gen Physiol 2008 ; 131 : 211–225. [CrossRef] [PubMed] [Google Scholar]
- Amsalem M Poilbout C Ferracci G et al. Membrane cholesterol depletion as a trigger of Nav1.9 channel-mediated inflammatory pain. EMBO J 2018 ; 37 : e97349. [PubMed] [Google Scholar]
- Lolignier S Eschalier A Bonnet C et al. Le canal Nav1.9: protéine clé pour la perception du froid et cible thérapeutique potentielle contre la douleur. Med Sci (Paris) 2016 ; 32 : 162–165. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Delmas P Padilla F Poilbout C Le cholestérol cellulaire, un régulateur important de la douleur inflammatoire. Med Sci (Paris) 2019 ; 35 : 115–118. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Dib-Hajj SD Black JA Waxman SG NaV1.9: a sodium channel linked to human pain. Nat Rev Neurosci 2015 ; 16 : 511–519. [CrossRef] [PubMed] [Google Scholar]
- De Felice M Ossipov MH Wang R et al. Triptan-induced enhancement of neuronal nitric oxide synthase in trigeminal ganglion dural afferents underlies increased responsiveness to potential migraine triggers. Brain 2010 ; 133 : 2475–2488. [CrossRef] [PubMed] [Google Scholar]
© 2020 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Le canal Nav1.9 : plaque tournante des céphalées par abus médicamenteux. Le monoxyde d’azote (NO), qui peut être produit par différentes sources, active les canaux Nav1.9 des nocicepteurs méningés chez les animaux traités par le sumatriptan. L’activation de ces canaux induit un état d’hyperexcitabilité neuronale à l’origine de la libération de médiateurs inflammatoires et vasoactifs qui agissent sur les vaisseaux méningés et les mastocytes. La sécrétion de CGRP, et peut-être d’autres médiateurs, provoque la dégranulation des mastocytes résidents. Les médiateurs libérés par les mastocytes potentialisent en retour l’activation des canaux Nav1.9, renforçant ainsi l’excitation des nocicepteurs méningés, un cercle vicieux qui conduit à un message douloureux exacerbé. Caudalis subnucleus, noyau caudal trigéminal ; SP, substance P ; CGRP, calcitonin-gene related peptide ; Hist, histamine ; NO, monoxyde d’azote ; TG neuron, neurone trigéminal ; PGE, prostaglandine E2 (© Illustration par Nancy Osorio). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




