| Issue |
Med Sci (Paris)
Volume 35, Number 11, Novembre 2019
|
|
|---|---|---|
| Page(s) | 825 - 827 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/2019159 | |
| Published online | 17 December 2019 | |
Les nanotubes membranaires des macrophages infectés par le VIH-1
Un moyen pour le virus de se propager plus vite dans un contexte de tuberculose
Tunneling nanotube formation in HIV-1-infected human macrophages: building bridges for efficient HIV-1 dissemination during co-infection with Mycobacterium tuberculosis
1
Institut de pharmacologie et biologie structurale, IPBS, université de Toulouse, CNRS, UPS, 205 route de Narbonne, 31077 Toulouse, France
2
Laboratoire international associé CNRS « IM-TB/HIV » 1167, Toulouse, France
Buenos Aires, Argentine
# This email address is being protected from spambots. You need JavaScript enabled to view it.
Co-auteurs
La co-infection VIH-1/tuberculose
L’infection par le virus de l’immunodéficience humaine (VIH-1), responsable du syndrome de l’immunodéficience acquise (sida), est à l’origine d’une pandémie mondiale. De plus, son association avec d’autres agents pathogènes, notamment Mycobacterium tuberculosis (Mtb), l’agent responsable de la tuberculose, optimise la pathogénie de chacun et complique le diagnostic et le traitement des patients. La co-infection VIH-1/Mtb, qui touche 1,2 million de personnes dans le monde, est donc un problème majeur de santé publique, particulièrement dans les pays en développement. L’association entre ces deux agents pathogènes étant particulièrement meurtrière, il est primordial de mieux comprendre comment VIH-1 et Mtb accélèrent mutuellement leur progression infectieuse. D’une part, les patients infectés par le VIH-1 ont un risque accru de développer une tuberculose dans sa forme active (primo-infection ou réactivation d’une tuberculose latente), qui progressera alors rapidement. D’autre part, chez les patients co-infectés, on observe une forte augmentation de la réplication du VIH-1 dans les poumons, le site infectieux préférentiel de Mtb, ainsi que dans le fluide pleural et le sang. Les mécanismes de réactivation de la tuberculose induite lors d’une infection par le VIH-1 sont largement décrits, notamment à travers la modification de l’organisation des granulomes, structures permettant de maintenir Mtb dans un état de latence asymptomatique [1]. En revanche, les mécanismes par lesquels Mtb exacerbe l’infection par le VIH-1 et accélère la progression du sida restent très mal connus. C’est à cette question que nous nous sommes intéressés dans l’article que nous avons récemment publié dans Cell Reports [2].
Un environnement associé à la tuberculose favorise la production de VIH-1 dans les macrophages
Nos travaux [2] démontrent que les macrophages participent à l’exacerbation de l’infection par le VIH-1 associée à Mtb. Les macrophages sont l’hôte principal de Mtb. En plus des lymphocytes T CD4+, ils sont également une cible majeure pour le VIH-1 : ils permettent une réplication virale productive et contribuent à l’établissement de réservoirs viraux persistants [3]. Dans les poumons, les macrophages alvéolaires sont les cibles principales du VIH-1. Nous nous sommes donc demandé si le micro-environnement créé dans le poumon par les macrophages infectés par la bactérie pourrait être propice à la multiplication du virus dans les macrophages voisins. Pour mimer cet environnement, nous avons développé différents modèles : un modèle in vitro fondé sur la différenciation des macrophages en présence de surnageants de culture de macrophages infectés par Mtb (appelé CmMTB, pour conditionned medium from Mtb-infected macrophages), ainsi qu’un modèle ex vivo utilisant du fluide pleural (PE) de patients tuberculeux (PE-TB). Nos travaux précédents utilisant ces deux modèles avaient permis de montrer que, sous l’action majeure de l’interleukine-10 (IL-10), une cytokine anti–inflammatoire, sécrétée par les macrophages infectés par Mtb et présente dans le PE-TB, les monocytes nouvellement recrutés se différencient préférentiellement en macrophages anti-inflammatoires, appelés M(IL-10). Ces derniers sont caractérisés par une forte expression des récepteurs de surface CD16a (le récepteur des IgG de type IIIa, RFcIIIa), CD163 (un récepteur éboueur ou scavenger), et MerTK (c-mer proto-oncogene tyrosine kinase), ainsi que par l’activation du facteur de transcription STAT3 (signal transducer and activator of transcription 3), et présentent des modifications fonctionnelles, dont un défaut de contrôle de la croissance de Mtb [4]. Dans des poumons de macaques tuberculeux, le nombre de macrophages M(IL-10) est significativement augmenté et est associé à une charge bactérienne élevée [4]. Plus important encore, nos travaux récents montrent que cette accumulation des macrophages M(IL-10) est accentuée chez les macaques co-infectés avec le virus de l’immunodéficience simienne (VIS). De plus, le nombre de monocytes sanguins potentiellement précurseurs de macrophages M(IL-10) est très élevé chez des patients co-infectés, comme le montre la présence de trois fois plus de récepteurs solubles spécifiques des monocytes, sCD163 et sMer (marqueurs des macrophages M[IL- 10]), dans le sérum des patients co-infectés par rapport à des patients mono-infectés ou des donneurs sains. Cela nous a permis de valider in vivo l’importance des macrophages M(IL-10) dans la co-infection. Par la suite, en utilisant nos deux modèles (CmMTB et PE-TB), nous avons montré que le microenvironnement associé à la TB augmente de manière significative (1) la production virale globale par les macrophages, (2) le nombre de macrophages infectés par le VIH-1, (3) la formation des cellules géantes multinucléées (CGM), produites à partir de macrophages infectés par le VIH-1 [5], et (4) la migration des macrophages, un moyen pour le virus de se disséminer dans l’organisme [2]. Ces effets sur l’infection par le VIH-1 sont spécifiques de Mtb puisque qu’ils ne sont pas observés lorsque les macrophages sont traités avec des effusions pleurales de patients ayant des infections non tuberculeuses.
Ainsi, nous avons montré que les macrophages infectés par Mtb génèrent un environnement qui module les macrophages voisins (effet « bystander ») vers un programme d’activation qui les rend très efficaces pour la production du VIH-1.
Les nanotubes membranaires induits par la tuberculose favorisent le transfert du VIH-1 entre les macrophages et augmentent ainsi la production virale
Comment la voie de signalisation IL-10/STAT3 induite dans un contexte tuberculeux agit-elle sur les macrophages pour augmenter la production du virus ? Pour répondre à cette question, différents aspects et étapes de l’infection virale des macrophages ont été analysés. Nous avons montré que ni l’entrée du VIH-1 dans les macrophages, ni l’expression des facteurs de restriction virale ne sont affectés dans les macrophages M(IL-10) in vitro. En revanche, leur capacité à former des nanotubes membranaires est doublée par l’ajout de CmMTB, et est encore doublée lorsqu’ils sont en plus infectés par le VIH-1 [2]. Les nanotubes sont de fines structures tubulaires non adhérentes qui connectent au moins deux cellules entre elles et constituent une nouvelle voie de communication intercellulaire (Figure 1). Ils sont impliqués dans la transmission entre cellules de différents récepteurs, protéines solubles, ARN, mais aussi d’organites (lysosomes, mitochondries, etc.) et d’agents infectieux [6, 7]. L’existence des nanotubes a été révélée dans de nombreux types cellulaires, et leurs caractéristiques morphologiques et structurales sont assez différentes selon la cellule à partir de laquelle ils sont formés [6]. Pour les macrophages, les nanotubes peuvent connecter deux cellules proches (moins de 10 μm) ou éloignées (plus de 200 μm). Ils sont constitués de membrane plasmique, de filaments d’actine, et contiennent parfois des microtubules [7]. Alors que l’infection par le VIH-1 favorise à elle seule la formation des nanotubes dans les macrophages [8], nous avons mis en évidence, pour la première fois, que le micro-environnement associé à la tuberculose induit la formation de nanotubes larges (contenant des microtubules) ainsi que des nanotubes fins (dépourvus de microtubules). Cette augmentation de la formation des nanotubes induite par le traitement des monocytes avec le CmMTB est amplifiée par l’infection par le VIH-1. Elle est responsable de l’augmentation de la production de virus dans les cellules traitées avec du CmMTB par rapport aux cellules contrôles, comme nous l’avons montré grâce à l’utilisation d’un inhibiteur de la formation des nanotubes (TNTi), qui abolit l’exacerbation de l’infection virale induite par le CmMTB. La formation des nanotubes dépend de l’IL-10 produite par les macrophages infectés par Mtb et de l’activation du facteur de transcription STAT3. En effet, l’inhibition de la voie de signalisation IL-10/STAT3 diminue la formation des nanotubes et, par conséquent, la production virale. Enfin, dans des expériences de co-culture effectuées en présence ou en l’absence du TNTi, nous avons observé que le virus est transféré d’un macrophage à un autre, en partie en utilisant les nanotubes. Il est possible que le VIH-1 emprunte majoritairement les nanotubes épais comme des tunnels (Figure 2) [8], en utilisant éventuellement les microtubules comme des rails. Ainsi, ce processus pourrait être différent de celui décrit pour le transfert du VIH-1 entre les lymphocytes T CD4+, qui nécessite une « synapse » à l’extrémité bout des nanotubes [9], ou pour le bacille de Calmette et Guérin (BCG), un autre micro-organisme dérivé du bacille tuberculeux bovin (Mycobacterium bovis), qui semble « surfer » à l’extérieur le long des nanotubes [7]. Enfin, nous avons observé des structures similaires à des nanotubes entre les macrophages M(IL-10) dans les poumons de macaques co-infectés par le VIS et Mtb. Cependant, en raison de l’absence d’un marqueur spécifique des nanotubes et des difficultés techniques pour étudier ces structures in vivo, nous n’avons pas pu poursuivre leur caractérisation.
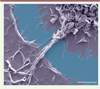 |
Figure 1 Formation de nanotubes membranaires entre les macrophages. Des macrophages humains sont traités par le CmMTB et infectés par le VIH-1, puis fixés et analysés en microscopie électronique à balayage. Les macrophages ont été coloriés en gris et la lamelle de verre en bleu. Barre d’échelle : 5 µm. |
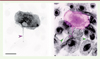 |
Figure 2 Le VIH-1 emprunte les nanotubes. Des macrophages humains sont traités par le CmMTB et infectés par le VIH-1, puis fixés et marqués. Photographie de gauche : immunomarquage de la protéine virale Gag seule (niveaux de gris). Photographie de droite : immunomarquage de Gag (en rose) et marquage des membranes par la lectine wheat germ agglutinin (WGA, en gris). Les têtes de flèches indiquent des nanotubes fins (vert), et un nanotube épais (rose) qui contient la protéine virale Gag. Barre d’échelle : 10 µm. |
Ainsi, l’activation des macrophages par un signal anti-inflammatoire (IL-10) associé à la tuberculose induit la formation de nanotubes qui jouent un rôle essentiel dans la propagation du VIH-1 entre ces cellules et l’augmentation de la production virale.
Conclusion
Nos travaux ont permis d’identifier les mécanismes cellulaires et moléculaires mis en jeu dans un contexte d’infection par Mtb pour favoriser la production du VIH-1 et sa dissémination au sein des macrophages. Ceux-ci pourraient expliquer pourquoi la charge virale est augmentée chez les patients co-infectés par le VIH-1 et Mtb. Ces résultats nous permettent de proposer que la formation des nanotubes membranaires par les macrophages infectés par le VIH-1 dans un environnement tuberculeux est une stratégie du virus pour se propager au sein de l’hôte « sans être vu ». Nos travaux ouvrent de nouvelles perspectives thérapeutiques fondées sur l’inhibition de la formation des nanotubes pour améliorer le traitement des patients co-infectés par le VIH- et Mtb, mais aussi dans d’autres contextes pathologiques tels que les cancers ou les maladies neurodégénératives, pour lesquels un rôle des nanotubes membranaires a été décrit [10].
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Nous remercions nos collègues qui ont participé à cette étude, et présentons nos excuses à ceux dont les travaux n’ont pu être cités faute d’espace. Nous remercions également le laboratoire de niveau 3 de l’IPBS (P3 multi-pathogène) et les plateformes du réseau d’imagerie TRI (Toulouse réseau imagerie, Genotoul). Ces travaux sont financés par le centre national de la recherche scientifique, l’université Paul Sabatier, l’agence nationale de la recherche (ANR 2010-01301, ANR14-CE11-0020-02, ANR16-CE13-0005-01, ANR-11-EQUIPEX-0003), l’agence nationale de recherche sur le sida et les hépatites virales (ANRS2014-CI-2, ANRS2014-049, ANRS 2019), Sidaction, le programme ECOS-Sud (A14S01), la fondation pour la recherche médicale (DEQ2016 0334894, DEQ2016 0334902) et la fondation Bettencourt Schueller.
Références
- Du Bruyn E, Wilkinson RJ, The immune interaction between HIV-1 infection and Mycobacterium tuberculosis. Microbiol Spectr 2016;4. [Google Scholar]
- Souriant S, Balboa L, Dupont M, et al., Tuberculosis exacerbates HIV-1 infection through IL-10/STAT3-dependent tunneling nanotube formation in macrophages. Cell Rep 2019;26:3586–3599. [CrossRef] [PubMed] [Google Scholar]
- Rodrigues V, Ruffin N, San-Roman M, Benaroch P, Myeloid cell interaction with HIV: a complex relationship. Front Immunol 2017;8:1698. [CrossRef] [PubMed] [Google Scholar]
- Lastrucci C, Benard A, Balboa L, et al., Tuberculosis is associated with expansion of a motile, permissive and immunomodulatory CD16+ monocyte population via the IL-10/STAT3 axis. Cell Res 2015;25:1333–1351. [CrossRef] [PubMed] [Google Scholar]
- Verollet C, Souriant S, Bonnaud E, et al., HIV-1 reprograms the migration of macrophages. Blood 2015;125:1611–1622. [Google Scholar]
- Dupont M, Souriant S, Lugo-Villarino G, et al., Tunneling nanotubes: intimate communication between myeloid cells. Front Immunol 2018;9:43. [CrossRef] [PubMed] [Google Scholar]
- Onfelt B, Nedvetzki S, Benninger RK, et al., Structurally distinct membrane nanotubes between human macrophages support long-distance vesicular traffic or surfing of bacteria. J Immunol 2006;177:8476–8483. [CrossRef] [PubMed] [Google Scholar]
- Eugenin EA, Gaskill PJ, Berman JW, Tunneling nanotubes (TNT) are induced by HIV-infection of macrophages: a potential mechanism for intercellular HIV trafficking. Cell Immunol 2009;254:142–148. [Google Scholar]
- Sowinski S, Jolly C, Berninghausen O, et al., Membrane nanotubes physically connect T cells over long distances presenting a novel route for HIV-1 transmission. Nat Cell Biol 2008;10:211–219. [CrossRef] [PubMed] [Google Scholar]
- Ariazi J, Benowitz A, De Biasi V, et al., Tunneling nanotubes and gap junctions. Their role in long-range intercellular communication during development, health, and disease conditions. Front Mol Neurosci 2017;10:333. [CrossRef] [PubMed] [Google Scholar]
© 2019 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Formation de nanotubes membranaires entre les macrophages. Des macrophages humains sont traités par le CmMTB et infectés par le VIH-1, puis fixés et analysés en microscopie électronique à balayage. Les macrophages ont été coloriés en gris et la lamelle de verre en bleu. Barre d’échelle : 5 µm. |
| Dans le texte | |
 |
Figure 2 Le VIH-1 emprunte les nanotubes. Des macrophages humains sont traités par le CmMTB et infectés par le VIH-1, puis fixés et marqués. Photographie de gauche : immunomarquage de la protéine virale Gag seule (niveaux de gris). Photographie de droite : immunomarquage de Gag (en rose) et marquage des membranes par la lectine wheat germ agglutinin (WGA, en gris). Les têtes de flèches indiquent des nanotubes fins (vert), et un nanotube épais (rose) qui contient la protéine virale Gag. Barre d’échelle : 10 µm. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




