| Issue |
Med Sci (Paris)
Volume 35, Number 3, Mars 2019
|
|
|---|---|---|
| Page(s) | 266 - 270 | |
| Section | Repères | |
| DOI | https://doi.org/10.1051/medsci/2019034 | |
| Published online | 01 April 2019 | |
Bébés CRISPR
Anatomie d’une transgression
CRISPR babies: technology and transgression
UMR 7268 ADÉS, Aix-Marseille, Université/EFS/CNRS ; CoReBio PACA, case 901, Parc scientifique de Luminy, 13288 Marseille Cedex 09, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Abstract
Analysing the data recently presented by Jiankui He and assuming that it is authentic shows that the goal of abolishing the expression of CCR5 may have been reached for one of the resulting twins, although this remains to be proven. However, the canonical delta32 mutation has not been achieved. The various preliminary experiments and controls give some confidence that major off-target modifications have not occurred; again, this is difficult to exclude. Clearly, the requirements of perfect technical mastery of the process have not been met, to say nothing of the requirements for complete transparency and full societal approval.
© 2019 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Vignette (Photo © Inserm – Patrick Delapierre).
L’annonce de la naissance de deux enfants dont l’ADN a été modifié par la technique CRISPR [1] a déjà fait couler beaucoup d’encre. Nous y revenons dans ce numéro de médecine/sciences pour, d’une part, faire le point sur ce qui a été fait, et dans quelles conditions (c’est l’objet de cet article) et, d’autre part [2] (→), préciser les conséquences sur le plan de l’éthique et de la régulation de cet évènement assez prévisible – mais que l’on n’attendait pas aussi tôt.
(→) Voir la Chronique bioéthique de H. Chneiweiss, page 263 de ce numéro
Le contexte
Question préalable : faut-il croire à cette annonce, ou s’agit-il d’une nouvelle « bidon » ?, comme cela fut le cas pour le prétendu clonage humain par la secte des Raëliens fin 2002 [3] (→) ou pour les mirifiques résultats de clonage thérapeutique publiés par le chercheur Coréen Hwang en 2005 [4] (→).
(→) Voir Perspective/Horizons de B. Jordan, m/s n° 2, février 2003, page 243
(→) Voir la Chronique bioéthique de H. Chneiweiss, m/s n° 2, février 2006, page 218
Dans le cas présent, il est assez vraisemblable que les expériences présentées par Jiankui He aient été effectivement réalisées. Cela semble cohérent avec l’intense activité déployée dans ce domaine en Chine (d’où proviennent la plupart des travaux appliquant la technique CRISPR à des embryons – non implantés jusqu’ici). De plus, comme on le verra par la suite, les résultats obtenus par He sont en fait assez mitigés et ne constituent pas un franc succès, ce qui incite à les croire véridiques. Cela dit, la seule source d’informations un peu détaillée est constituée par la présentation de He lors du colloque sur l’édition du génome (Human genome editing summit) qui a eu lieu à Hong Kong du 27 au 29 novembre 2018 [5], pour laquelle on peut consulter un diaporama accessible sur Internet [5]. Compte tenu du scandale qu’a suscité ce travail, il est peu probable qu’une revue accepte de le publier, il semble que même le serveur de preprints BioxRiv ait pris une position négative : il faudra donc nous contenter de ces 58 diapositives qui ne remplacent pas une publication mais apportent néanmoins bon nombre d’informations. Avant d’entamer l’analyse des données, quelques précisions sur la trajectoire de Jiankui He : on l’a souvent présenté comme un médecin, mais en réalité il a fait (en Chine) des études de physique, puis a passé plusieurs années aux États-Unis au cours desquelles il s’est intéressé à la génétique et aux techniques d’« édition » du génome, a obtenu un doctorat (PhD) à l’université Rice à Houston et a effectué un stage post-doctoral à l’université de Stanford (Californie). Considéré en Chine comme un élément très prometteur, il a été recruté en 2012 par l’université de Shenzen et a bénéficié de nombreux financements et prix au niveau local et national, tout en fondant plusieurs entreprises dont Direct Genomics, une firme chinoise qui commercialise des séquenceurs d’ADN fondés sur la technologie de feu Helicos 1 [6] (→).
(→) Voir la Chronique génomique de B. Jordan, m/s n° 1, janvier 2019, page 81
Bref, c’est (c’était…) un personnage en vue de la science chinoise, comblé d’honneurs et bénéficiant de soutiens financiers et politiques conséquents.
L’objectif
Le but annoncé par He était d’obtenir des enfants génétiquement modifiés chez lesquels la protéine CCR5 (C-C chemokine receptor type 5, normalement exprimée sur les lymphocytes T CD4+) est absente en raison de l’inactivation du gène correspondant, ce qui doit induire la résistance à l’infection par le virus VIH (virus de l’immunodéficience humaine) qui utilise cette protéine comme co-récepteur pour entrer dans la cellule. Il existe en effet dans les populations d’origine européenne 10 % environ de personnes qui portent une petite délétion (appelée delta32) dans le gène CCR5 et qui sont, de ce fait, résistantes à ce virus, tout en jouissant par ailleurs d’une santé normale2. Nombre de commentateurs se sont étonnés de ce choix, arguant que la correction d’une mutation délétère (liée par exemple à l’hémophilie ou à la mucoviscidose) constituerait un objectif plus défendable [7]. Mais ils oublient, me semble-t-il, que dans presque tous les cas, le diagnostic préimplantatoire apporte une solution bien plus sûre, puisqu’après une fécondation in vitro, on va quasiment toujours trouver quelques embryons non affectés, sauf situation très exceptionnelle (un parent homozygote pour une mutation dominante, par exemple, cas ultra-rare). Le choix de He est donc assez rationnel, d’autant plus qu’il n’est sans doute pas nécessaire d’effectuer une modification très précise et que toute mutation inactivant le gène CCR5 pourrait aboutir au résultat souhaité. Une telle manipulation constitue en fait un premier cas d’amélioration déguisée en prévention, et comme on peut penser que l’objectif réel des modifications germinales sur l’homme est l’obtention d’enfants « améliorés » (enhanced), il va tout à fait dans le sens de l’histoire…
La présentation de Jiankui He : expériences préliminaires…
Rappelons pour commencer que l’introduction de la délétion delta32 dans le gène CCR5 a déjà été réalisée en 2016 par une équipe chinoise [8] utilisant des embryons tripronucléaires3 et donc non viables [9] (→).
Voir la Chronique génomique de B. Jordan, m/s n° 5, mai 2017, page 549
L’analyse montrait que dans quelques embryons (cinq) la modification désirée avait bien eu lieu, mais que dans la majorité des cas (une cinquantaine) il y avait eu jonction aléatoire (NHEJ, non-homologous end joining) après la coupure de l’ADN par la nucléase Cas9, avec addition ou délétion d’un nombre variable de nucléotides. De plus, la plupart des embryons s’avéraient être des mosaïques (mais cela pouvait être lié au fait qu’ils étaient triploïdes dès le départ). En somme ce travail montrait qu’il était possible d’introduire dans le gène CCR5 la mutation désirée, mais que l’on était encore loin de maîtriser la technique et d’effectuer à coup sûr la modification voulue.
La présentation de He [5] détaille un ensemble d’expériences préliminaires. Elle montre d’abord l’édition d’embryons de souris dans le but d’inactiver le gène Ccr5 murin, avec pour résultat l’introduction de diverses délétions dans le gène dont une seule correspond à delta32 à l’état hétérozygote. À partir de cette souris, il a pu obtenir par croisements une souris portant cette mutation à l’état homozygote et vérifié l’absence d’anomalies évidentes au niveau tissulaire ou comportemental4. Il est ensuite passé aux cellules humaines (la lignée HEK293T, lignée dérivée de rein embryonnaire et souvent utilisée pour la production de vecteurs rétroviraux) et a testé l’efficacité de différents ARN guide (sgRNA, ARN dirigeant la nucléase Cas9 vers l’endroit ciblé dans l’ADN) et a choisi le plus efficace, appelé sg4RNA, qui correspond au début de la délétion delta32 dans le gène CCR5. Profitant de la quasi-identité de la séquence d’ADN dans cette région entre l’homme et le singe cynomolgus (appelé aussi macaque crabier), il a alors effectué diverses mises au point sur des embryons de ce singe et a montré que la meilleure efficacité d’édition (80 %) était obtenue en injectant Cas9 et l’ARN guide au moment de la fécondation par ICSI (intra-cytoplasmic sperm injection) de l’ovule, et que cette injection précoce réduisait la proportion de blastocystes mosaïques. La mise au point a été poursuivie sur des embryons humains non viables (tripronucléaires), montrant notamment qu’il est préférable d’injecter la protéine Cas9 plutôt que son ARN. L’établissement de lignées de cellules souches embryonnaires à partir d’embryons « édités » a permis de vérifier qu’après induction, celles-ci expriment les marqueurs de différenciation attendus. La recherche d’éventuelles modifications parasites (off-target) a été menée de manière assez approfondie, impliquant notamment le séquençage de l’ADN des parents (pour détecter tous les sites potentiels) ainsi qu’une approche informatique spécifique permettant de détecter d’éventuelles délétions.
…et passage à l’acte
On en arrive alors, après une bonne quarantaine de diapositives, à la modification d’embryons en vue de leur réimplantation (Figure 1). L’ADN des deux parents est séquencé (afin de permettre une prédiction personnalisée des sites potentiels de modification parasite) ; la protéine Cas9 et l’ARN guide (sg4RNA) sont injectés dans l’ovule en même temps qu’un spermatozoïde. Après développement jusqu’au stade blastocyste, quelques cellules (3 à 5) sont prélevées pour être séquencées : séquençage « génome entier » avec confirmation par la technique de Sanger pour examiner l’édition de CCR5 et d’éventuels effets off-target. À ce stade, quatre blastocystes viables avaient été obtenus ; deux s’avèrent non modifiés, un présente une délétion de 15 paires de bases (dans le gène CCR5) sur un chromosome, l’autre étant non modifié ; le quatrième blastocyste, enfin, porte une insertion d’une paire de bases sur un chromosome et une délétion de quatre sur l’autre (toujours dans le gène CCR5). La mutation désirée (delta32) n’est donc pas présente, et seul l’embryon portant deux modifications est susceptible de ne pas exprimer la protéine CCR5 (mais cela reste à démontrer). De plus, cet embryon semble présenter une mutation parasite dans une région inter génique. Malgré ces résultats en demi-teinte, la décision fut prise (par les parents, indique He) de procéder à l’implantation de ces deux embryons, qui devaient donner naissance à deux filles, Nana (double mutante) et Lulu (mutante hétérozygote). Un suivi en cours de grossesse, effectué par séquençage de l’ADN fœtal isolé du sang maternel avait confirmé l’édition, totale ou partielle, du gène CCR5 et, en parallèle, vérifié l’absence de mutations dans un jeu de 600 gènes liés au cancer. À la naissance, le séquençage à haute redondance du sang de cordon et de l’ADN de placenta confirmait encore l’édition du gène CCR5 ; en revanche, la mutation parasite avait disparu. Une nouvelle recherche de mutations parasites et de délétions ne détecte rien. La présentation se termine en esquissant les futures étapes : essai d’infection de lymphocytes CD4 par le VIH, recherches plus approfondies d’effets off-target et d’un éventuel mosaïcisme… en terminant par un programme de suivi médical des jumelles jusqu’à leur majorité. Compte tenu de la situation de Jiankui He, qui est actuellement assigné à résidence, tout cela reste assez hypothétique.
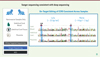 |
Figure 1. Reproduction partielle d’une diapositive présentée par Jiankui He à Hong Kong [6], montrant la confirmation par séquençage Sanger des modifications introduites au début du gène CCR5 des deux enfants. Les mêmes changements sont retrouvés dans les trois tissus étudiés (sang et tissu de cordon, placenta). Le document d’origine est d’assez mauvaise qualité (photographie d’une projection et non fichier de la présentation) ce qui explique le léger flou de cette image. |
Un résultat en demi-teinte, une véritable transgression
En somme cette première manipulation génétique sur l’humain, visant à l’inactivation du gène CCR5 pour conférer la résistance au virus VIH, aboutit à la naissance d’un enfant chez lequel les deux exemplaires du gène sont mutés (mais sans que l’on soit certain que cela assure son inactivation) et d’un deuxième enfant portant un exemplaire muté et un autre normal, donc a priori non protégé. Le but annoncé (reproduire la mutation naturelle delta32) n’est pas atteint, mais il est possible que l’inactivation du gène CCR5 ait réussi. Cela dit, si l’effet de la mutation delta32 est bien connu, celui des mutations introduites chez ces deux enfants ne l’est pas et l’on peut toujours craindre de mauvaises surprises. Par ailleurs des contrôles assez approfondis laissent espérer qu’il n’y a pas de gros problème de modifications parasites ou de délétions, sans que l’on puisse être totalement rassuré à ce niveau5. C’est en somme un résultat que l’on pourrait considérer sur un plan purement technique comme plutôt encourageant, indicatif d’une faisabilité à terme tout en montrant le chemin qui reste à parcourir…… s’il ne s’agissait pas d’une modification irréversible de la lignée germinale humaine. De fait, il constitue une transgression majeure, la première véritable manipulation génétique sur l’humain affectant tant les sujets concernés que leur descendance, dans des conditions de sécurité bien trop approximatives (comme l’indiquent les résultats) et en violation flagrante des conditions éthiques et sociétales énoncées à de multiples reprises [10] (→).
Voir la Chronique génomique de B. Jordan, m/s n° 2, février 2016, page 217
Il n’est donc pas étonnant que la révélation de cette tentative « sauvage » ait suscité une réprobation générale et la disgrâce de Jiankui He ; reste à tirer les conséquences de cette transgression pour l’encadrement de tels travaux et à montrer que, en dépit de cet accroc, la communauté scientifique est capable de se réguler de manière efficace.
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Je remercie Hervé Chneiweiss pour ses remarques ayant permis d’améliorer cet article.
Entreprise nord-américaine qui a fait faillite en 2012.
Avec peut-être une sensibilité accrue au West Nile virus.
Embryons non fertiles, mais capables de se diviser.
La souris n’étant pas sensible à l’infection par le VIH, on ne peut examiner ce paramètre.
Les techniques employées ne permettent pas d’exclure des délétions de grande taille.
Références
- Associated Press, le 26 novembre 2016 https://apnews.com/4997bb7aa36c45449b488e19ac83e86d. [Google Scholar]
- De Chneiweiss H.. retour de Hong-Kong ou l’éthique à l’heure d’une génétique d’augmentation de la personne humaine. Med Sci (Paris) 2019 ; 35 : 263–265. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Jordan B.. L’humanité est au seuil du paradis. Med Sci (Paris) 2003 ; 19 : 243–245. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Chneiweiss H.. Cloningate ? La publication scientifique et le clonage thérapeutique face à la mystification Hwang. Med Sci (Paris) 2006 ; 22 : 218–222. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Liens vers le colloque de Hong Kong (l’accès au deuxième site, plus complet, est parfois aléatoire): http://www.nationalacademies.org/hk/ http://www.nationalacademies.org/gene-editing/2nd_summit/index.htm. Lien vers les diapositives de Jiankui He : https://drive.google.com/drive/folders/1T1zLTtHS2z_cgl29fN_7qJg7fLA4qlrd. [Google Scholar]
- Jordan B.. Actualités du séquençage d’ADN. Med Sci (Paris) 2019 ; 35 : 81–83. [CrossRef] [Google Scholar]
- The blind babymaker. Editorial. Nat Biotechnol 2019 ; 37 : 1. [CrossRef] [PubMed] [Google Scholar]
- Kang X, He W, Huang Y, et al. Introducing precise genetic modifications into human 3PN embryos by CRISPR/Cas-mediated genome editing. J Assist Reprod Genet 2016 ; 33 : 581–588. [CrossRef] [PubMed] [Google Scholar]
- Jordan B.. CRISPR sur embryons humains : une nouvelle étape. Med Sci (Paris) 2017 ; 33 : 549–551. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Jordan B.. Sommet de Washington : feu orange pour la thérapie germinale ?. Med Sci (Paris) 2016 ; 32 : 217–220. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. Reproduction partielle d’une diapositive présentée par Jiankui He à Hong Kong [6], montrant la confirmation par séquençage Sanger des modifications introduites au début du gène CCR5 des deux enfants. Les mêmes changements sont retrouvés dans les trois tissus étudiés (sang et tissu de cordon, placenta). Le document d’origine est d’assez mauvaise qualité (photographie d’une projection et non fichier de la présentation) ce qui explique le léger flou de cette image. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




