| Issue |
Med Sci (Paris)
Volume 34, Novembre 2018
Les Cahiers de Myologie
|
|
|---|---|---|
| Page(s) | 35 - 38 | |
| Section | JSFM 2017 | |
| DOI | https://doi.org/10.1051/medsci/201834s210 | |
| Published online | 12 November 2018 | |
15es JSFM : Prix Master 2017*
Effet de l’interféron-gamma sur la biologie des cellules musculaires squelettiques
The effect of interferon-gamma on skeletal muscle cell biology
1
ED402, Paris Est-Créteil University, Créteil, France
2
Inserm U955 Team 10, Paris Est-Créteil University, Créteil, France
** This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Les myopathies inflammatoires et dysimmunitaires (DIMs) touchent 14/100 000 personnes dans le monde. Ces pathologies sont classées par des critères immunopathologiques en quatre groupes : (1) polymyosites (PM)/ myosites à inclusions (IBM), (2) dermatomyosites, (3) myopathies nécrosantes auto-immunes et (4) myosites de chevauchement comprenant le syndrome anti-synthétase (ASS). Les ASS et PM/IBM sont caractérisées par la présence d’infiltrats inflammatoires mononucléés. Récemment, nous avons mis en évidence une expression myocytaire du complexe majeur d’histocompatibilité de type 2 (CMH2) dans les muscles de patients atteints d’ASS et d’IBM. L’expression du CMH2 est connue pour être induite par l’interféron-gamma (IFNγ) dans les cellules myogéniques. Or, les lymphocytes T CD8 (LTCD8), cellules productrices d’IFNγ sont retrouvés à proximité des fibres musculaires CMH2 positives. Cette cytokine inhibe la différenciation musculaire in vitro par l’interaction CIITA-myogénine (CIITA : major histocompatibility complex class II transactivator). Les mécanismes impliquant une toxicité musculaire médiée par les lymphocytes dans les DIMs restent inconnus. Les objectifs de ce projet sont dans un premier temps de caractériser les effets de l’IFNγ sur la biologie des cellules musculaires par des approches morphologiques, moléculaires et cellulaires. Puis, d’identifier le rôle de l’IFNγ dans ces myopathies et son impact au cours de la régénération musculaire. Des études préliminaires in vitro ont été réalisées sur des myoblastes humains et murins exposés ou non à l’IFNγ. Nos résultats devraient permettre d’obtenir de meilleures connaissances sur la physiopathologie des DIMs et d’identifier de potentielles nouvelles cibles thérapeutiques.
Abstract
Dysimmune and inflammatory myopathies (DIMs) affect around 14/100,000 people worldwide. Based on immupour nopathological criteria, DIMs are divided in four groups: (1) polymyositis (PM)/inclusion body myositis (IBM), (2) dermatomyositis (DM), (3) immune-mediated necrotizing myopathies (IMNM) and (iv) overlapping myositis including anti-synthetase syndrome (ASS). ASS and PM/IBM are characterized by the activation of inflammation with lymphocytic infiltrations. Recently, we showed that an expression of the major histocompatibility complex class 2 (MHC2) was present in myofibers from ASS and IBM muscle biopsies. Interestingly, MHC2 expression is known to be stimulated by Interferon-gamma (IFNγ) in myogenic cells. LTCD8 cells, which are well-known producers of IFNγ, are commonly found in close vicinity to MHC2 positive myofibers. This inflammatory cytokine also inhibits myogenic differentiation in vitro by CIITA-myogenin interaction. The mechanisms involved in the lymphocyte-driven muscle toxicity in DIMs are unclear. The objectives of this project are to characterize IFNγ effects on the biology of human myogenic cells by morphological, molecular and cellular approaches. Then, we aim to investigate the role of IFNγ in these myopathies and its impact during muscular regeneration. In vitro preliminary studies have been performed using human and mouse myoblasts treated or not with IFNγ. Our results should lead to a better understanding of the role of IFNγ in the pathophysiology of DIMs, and would hopefully help identify new therapeutic targets.
Le Prix Master de la Société Française de Myologie (SFM) est une des actions marquantes de cette société savante. Créé depuis 2006, ce prix récompense chaque année un(e) jeune chercheur(euse) pour la qualité de son travail de Master en Biologie en recherche clinique, physiopathologique ou fondamentale dans le domaine de la Myologie.
© 2018 médecine/sciences – Inserm
Contexte et hypothèses
Le muscle squelettique possède de grandes capacités d’adaptation lui permettant de détecter et de s’accommoder aux changements d’activité contractile. Cette plasticité du tissu musculaire répond de manière spécifique à différents changements ou conditions tels que l’exercice physique, les facteurs de croissance, les apports nutritionnels, le stress et certaines pathologies. Cette plasticité est possible par la complémentarité de deux phénomènes : la myogenèse et l’angiogenèse, toutes deux essentielles pour le maintien de l’homéostasie du muscle squelettique [1]. Ce tissu contient en effet une population de progéniteurs musculaires, également nommés cellules satellites, présents dans un microenvironnement particulier, la niche satellitaire [2]. Les cellules satellites sont localisées entre la lame basale et le sarcolemme et sont majoritairement à l’état quiescent dans un muscle sain. A la suite d’une lésion musculaire, les cellules satellites s’activent, prolifèrent puis se différencient et fusionnent pour former de nouvelles fibres musculaires (Figure 1A, 1B). Une partie des cellules satellites activées (i.e. myoblastes) ne se différencient pas mais retournent en position satellite, permettant ainsi de reconstituer le pool de cellules souches [2]. La cellule musculaire et son microenvironnement sont perturbés en cas de pathologies neuromusculaires, qu’elles soient acquises (inflammatoires/dysimmunitaires ou toxiques) ou non-acquises (génétiques). Les myopathies inflammatoires et dysimmunitaires (DIMs) idiopathiques résultant d’un dysfonctionnement du système immunitaire sont classées en quatre groupes selon des critères histopathologiques : (1) polymyosites (PM) / myosites à inclusion (inclusion body myositis, IBM), (2) dermatomyosites (DM), (3) myopathies nécrosantes auto-immunes (immune-mediated necrotizing myopathies, IMNM) et (4) myosites de chevauchement comprenant le syndrome anti-synthétase (antisynthetase myopathy, ASM) (Tableau I) [3].
 |
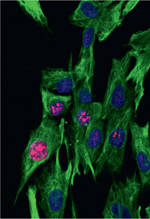
Figure 1. A. Schématisation des principales étapes de la différenciation musculaire et expression des facteurs de transcription myogénique correspondants. B..Immuno-marquages de myotubes (8 jours de culture primaire de cellules musculaires murines issues du modèle murin transgénique Pax7-GFP) in vitro marqués pour les noyaux au Hoesch (bleu), myogénine MyoG (rose) et la myosine (rouge). C. Immuno-marquage de myoblastes humains après un double tri CD56+ (n = 4), desmine (vert), ki67 (rouge) : 96,7 % des cellules triées étaient desmine-positives, ce qui suggère une prépondérance de progéniteurs musculaires dans nos cultures primaires de muscles humains. D. Quantification par qPCR de l’expression de CIITA par les cellules myogéniques humaines suite au traitement d’IFNγ à J0 (n = 1 en triplicat. hTBP utilisé comme gène de référence). |
Principales caractéristiques immuno-histopathologiques des myopathies inflammatoires et dysimmunitaires.
Les signatures interférons dans le sang et dans le muscle permettent de mieux analyser les mécanismes physiopathologiques à l’origine des lésions musculaires au cours des DIMs. Ainsi, la DM se distingue des autres DIMs par une signature interféron (IFN) de type 1 (IFNα et β) corrélée à la sévérité de la maladie [4]. À l’inverse, le syndrome anti-synthétase (ASM) et les myosites à inclusions (IBM) se caractérisent par une signature IFN de type 2 (IFNγ) [5]. Dans le cas des PM/IBM, les complexes majeurs d’histocompatibilité de types 1 et 2 (CMH1 ; CMH2) sont surexprimés dans les fibres musculaires tandis que les fibres musculaires de sujets sains n’expriment pas le CMH [6]. L’IFNγ est un puissant inducteur du CMH2 par l’intermédiaire du transactivateur CIITA via la phosphorylation de STAT1 [7].
Les effets de l’IFNγ sur les cellules musculaires squelettiques sont mal connus, les effets réels sur la régénération musculaire restant encore controversés. Après une lésion musculaire, l’inflammation induite est associée à une production d’IFNγ. L’IFNγ est essentielle pour obtenir une réparation efficace du muscle squelettique grâce à son implication dans la régulation du système immunitaire telle que l’activation des macrophages [8]. In vitro, l’IFNγ stimule la prolifération des cellules myogéniques murines [9] et inhibe leur différenciation [7,9].
Dans les ASM et les IBM, le niveau d’expression d’IFNγ pourrait avoir un effet direct sur les cellules myogéniques, et/ou indirect par l’activation des cellules inflammatoires résidentes, et ainsi contribuer à la physiopathologie de ces maladies.
Caractérisation de l’effet de l’IFNγ dans la physiopathologie musculaire
Mon travail de thèse a pour objectif d’étudier le rôle de l’IFNγ sur la biologie des cellules musculaires à l’état normal et dans les myopathies inflammatoires. La première partie du travail est l’analyse in vitro des effets de l’IFNγ sur la prolifération et la différentiation des myoblastes (Figure 1A, 1B) (cultures primaires humaines et murines).
Des cultures primaires de cellules myogéniques humaines ont été obtenues à partie de biopsies musculaires de patients avec un muscle histologiquement normal ou présentant une DIMs. Après dissociation mécanique, digestion enzymatique et tri sur billes magnétiques, la myogénicité de la population cellulaire isolée a été déterminée par l’expression de desmine (Figure 1C). Les myoblastes isolés ont été exposés à l’IFNγ humain (exposition unique ou répétée) en condition de prolifération ou de différenciation. Nos résultats préliminaires montrent que le traitement par IFNγ active fortement la voie de signalisation de l’IFNγ (Figure 1D). L’exposition à une dose unique d’IFNγ (≥1ng/ml) induit également une réponse cellulaire dès 24 h avec une induction génique encore présente 72 h après traitement pour une dose supérieure à 5ng/mL. Ces protocoles nous permettent de caractériser l’effet sur la prolifération et la différenciation des cellules myogéniques.
La seconde partie de mon travail portera sur l’étude in vivo de différents modèles murins de pathologie musculaire en analysant notamment l’effet de l’IFNγ endogène. En particulier, je réaliserai l’étude qualitative et quantitative des effets de l’IFNγ sur le développement musculaire en analysant notamment les facteurs de régulation myogénique : Pax7 pour les cellules satellites, MyoD pour les myoblastes et myogénine (MyoG) pour les myocytes, puis les deux chaînes lourdes de myosine pour les myotubes (Figure 1A, 1B).
Cette approche vise à caractériser les effets de l’IFNγ sur les myoblastes et les fibres musculaires, en conditions normale et pathologique. Ceci est d’autant plus important que pour certaines myopathies il n’existe pas de thérapie efficace sur le long terme. De plus, le rôle des interférons est de plus en plus étudié dans la physiopathologie des maladies auto-immunes [10] incluant des approches spécifiques basées sur leur neutralisation in vivo.
Prix Master de la Société Française de Myologie
L’objectif du Prix Master de la SFM est double : reconnaître la qualité d’un travail réalisé au sein d’une équipe de recherche en Myologie ; être une force d’incitation à la continuité de ce travail scientifique en doctorat d’État et ainsi faciliter l’orientation de jeunes scientifiques vers la recherche appliquée aux maladies du muscle.
Le prix Master est de 1 000 €. Il est versé directement au récipiendaire en récompense du travail réalisé pendant son Master jugé sur la présentation de son mémoire. Le candidat primé poursuivra ses recherches par une thèse d’université dans le domaine de la Myologie.
Ce prix donne accès au versement d’une subvention de 9 000 € d’1 an, éventuellement renouvelable 1 fois. La subvention est attribuée au laboratoire d’accueil.
Pour tout renseignement sur les conditions de soumission au Prix Master de la SFM, consulter le site www.sfmyologie.org
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Kostallari E Baba-Amer Y Alonso-Martin S et al. Pericytes in the myovascular niche promote post-natal myofiber growth and satellite cell quiescence. Development 2015 ; 142 : 1242–1253. [CrossRef] [PubMed] [Google Scholar]
- Relaix F Zammit PS Satellite cells are essential for skeletal muscle regeneration: the cell on the edge returns centre stage. Development 2012 ; 139 : 2845–2856. [CrossRef] [PubMed] [Google Scholar]
- De Bleecker JL Lundberg IE de Visser M 193rd ENMC international workshop pathology diagnosis of idiopathic inflammatory myopathies 30 November-2 December 2012, Naarden. The Netherlands. Neuromuscul Disord 2013 ; 23 : 945–951. [CrossRef] [Google Scholar]
- Gitiaux C Latroche C Weiss-Gayet M et al. Myogenic progenitor cells exhibit type I interferon-driven proangiogenic properties and molecular signature during juvenile dermatomyositis. Arthritis Rheumatol Hoboken NJ 2018 ; 70 : 134–145. [CrossRef] [Google Scholar]
- Rigolet M, Hou C, Baba Amer Y, et al. Distinct interferon signatures stratify inflammatory and dysimmune myopathies. 2018 (soumis pour publication). [Google Scholar]
- Aouizerate J De Antonio M Bassez G et al. Myofiber HLA-DR expression is a distinctive biomarker for antisynthetase-associated myopathy. Acta Neuropathol Commun 2014 ; 2 : 154. [Google Scholar]
- Londhe P Davie JK Gamma interferon modulates myogenesis through the major histocompatibility complex class II transactivator. CIITA. Mol Cell Biol 2011 ; 31 : 2854–2866. [CrossRef] [Google Scholar]
- Cheng M Nguyen MH Fantuzzi G et al. Endogenous interferon is required for efficient skeletal muscle regeneration. AJP Cell Physiol 2008 ; 294 : C1183–C1191. [CrossRef] [Google Scholar]
- Grzelkowska-Kowalczyk K Wicik Z Majewska A et al. Transcriptional regulation of important cellular processes in skeletal myogenesis through interferon-g. J Interferon Cytokine Res 2015 ; 35 : 89–99. [CrossRef] [PubMed] [Google Scholar]
- Higgs BW Zhu W Morehouse C et al. A phase 1b clinical trial evaluating sifalimumab, an anti-IFN-α monoclonal antibody, shows target neutralisation of a type I IFN signature in blood of dermatomyositis and polymyositis patients. Ann Rheum Dis 2014 ; 73 : 256–262. [CrossRef] [PubMed] [Google Scholar]
Liste des tableaux
Principales caractéristiques immuno-histopathologiques des myopathies inflammatoires et dysimmunitaires.
Liste des figures
 |
Figure 1. A. Schématisation des principales étapes de la différenciation musculaire et expression des facteurs de transcription myogénique correspondants. B..Immuno-marquages de myotubes (8 jours de culture primaire de cellules musculaires murines issues du modèle murin transgénique Pax7-GFP) in vitro marqués pour les noyaux au Hoesch (bleu), myogénine MyoG (rose) et la myosine (rouge). C. Immuno-marquage de myoblastes humains après un double tri CD56+ (n = 4), desmine (vert), ki67 (rouge) : 96,7 % des cellules triées étaient desmine-positives, ce qui suggère une prépondérance de progéniteurs musculaires dans nos cultures primaires de muscles humains. D. Quantification par qPCR de l’expression de CIITA par les cellules myogéniques humaines suite au traitement d’IFNγ à J0 (n = 1 en triplicat. hTBP utilisé comme gène de référence). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




