| Issue |
Med Sci (Paris)
Volume 19, Number 5, Mai 2003
|
|
|---|---|---|
| Page(s) | 601 - 605 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2003195601 | |
| Published online | 15 May 2003 | |
Nouveaux aspects du cholestérol dans le système nerveux central
New views on cholesterol in the central nervous system
Atip Cnrs/Max-Planck, UPR 2356, Centre de Neurochimie, 5, rue Blaise Pascal, 67084 Strasbourg edex, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Le cholestérol est une molécule aux multiples facettes, remplissant des fonctions essentielles pour l’organisme et impliquée dans diverses maladies. Cependant, son rôle dans le système nerveux central reste obscur. Nos travaux réalisés sur des cultures de neurones hautement purifiés à partir du système nerveux central de rongeurs suggèrent que, durant le développement cérébral, les neurones réduisent leur synthèse de cholestérol et l’importent des astrocytes via des lipoprotéines. Les neurones utilisent ce cholestérol d’origine gliale afin de former de nombreuses synapses fonctionnelles. Ces observations conduisent à de nouvelles hypothèses quant au rôle du cholestérol dans le SNC et à la fonction des astrocytes comme producteurs du cholestérol. Afin de vérifier ces hypothèses, de nouvelles études clarifiant les fonctions du cholestérol dans le cerveau et lors de maladies neurodégénératives seront nécessaires.
Abstract
Cholesterol is a multifacetted molecule, which serves as essential membrane component, as cofactor for signaling molecules and as precursor for steroid hormones. Despite intense research on the diverse aspects of cholesterol, the role of cholesterol in the nervous system is still little understood. Our recent studies on primary cultures of highly purified neurons from the rodent central nervous system (CNS) suggest that during development, neurons reduce or even abandon cholesterol synthesis and import cholesterol from astrocytes via lipoproteins. Neurons use the glia-derived cholesterol to form numerous and efficient synapses. This provokes new ideas about the role of astrocytes as cholesterol producers and about the function of cholesterol in the CNS and its involvement in neurodegenerative diseases.
© 2003 médecine/sciences - Inserm / SRMS
Le cholestérol est une molécule multifonctionnelle. Elle détermine les propriétés des membranes cellulaires et de leurs composants de signalisation [1], sert de précurseurs à la synthèse des hormones stéroïdiennes [2] et règle les fonctions des différents signaux cellulaires [3]. Compte tenu de ces multiples fonctions, il n’est pas surprenant que des déficiences du métabolisme du cholestérol soient à l’origine de graves maladies [4–5]. Cependant, et de manière étonnante, peu de données existent sur le rôle du cholestérol dans le système nerveux [6–8].
Deux hypothèses peuvent être formulées quant à la fonction du cholestérol dans le cerveau et au rôle de la glie dans son métabolisme. D’une part, il est probable que, au cours du développement post-natal, les neurones réduisent ou arrêtent la synthèse du cholestérol et l’importent à partir d’un sous-type de cellules gliales, les astrocytes, qui sécrètent le cholestérol dans des particules de lipoprotéines riches en apo-lipoprotéine E (ApoE). D’autre part, les neurones du système nerveux central (SNC) ont besoin de ce cholestérol provenant de la glie afin de former de nombreuses synapses fonctionnelles [9–12]. Les données expérimentales ayant conduit à ces hypothèses sont présentées dans cet article, et leurs implications discutées sur la base des connaissances actuelles sur le métabolisme du cholestérol.
Preuves expérimentales d’une nouvelle interaction neurone-glie
Le lien entre la synaptogenèse et le cholestérol d’origine gliale a été suggéré par une série d’études ayant pour but premier de définir l’implication des cellules gliales dans le développement des synapses [9, 13–15]. En effet, les cellules gliales règlent plusieurs aspects de la différenciation neuronale et, au cours du développement cérébral, la plupart des synapses ne sont formées qu’après la différenciation des astrocytes [16].
Afin d’étudier l’influence de la glie sur la formation et la fonction des synapses, Pfrieger et Barres [13] ont séparé les cellules neuronales (→) et gliales et mesuré ainsi la formation et les propriétés physiologiques des synapses dans des cultures purement neuronales. Cette approche réductionniste a été rendue possible par la mise au point d’une méthode de purification et de culture des cellules ganglionnaires rétiniennes (CGR) de rats en post-natal [17]. En co-culture, les cellules gliales augmentaient de manière drastique la transmission synaptique entre les CGR. Ces effets étaient produits grâce à l’intervention d’un ou plusieurs facteurs solubles libérés par les astrocytes et les oligodendrocytes. Enfin, les changements observés n’étaient pas dus à une augmentation de la survie des neurones ou de leur excitabilité.
(→) m/s 1999, n° 5, p. 750
Les cellules gliales induisent-elles la formation des synapses, ou augmentent-elles l’efficacité des connexions existantes ? Ces deux questions ont été abordées grâce à l’utilisation de micro-cultures dans lesquelles les neurones isolés poussent sur des îlots de substrat [14, 15]. Les analyses en immunocytochimie et en microscopie électronique ont montré que le traitement avec le milieu conditionné glial (MCG) augmentait de près de sept fois le nombre de synapses formées par les CGR [14, 15]. L’augmentation du nombre de synapses n’était pas due à une augmentation du nombre de neurites, ce qui indique bien que les cellules gliales agissent directement sur la formation des synapses [9]. De plus, Nägler et al. [14] ont démontré que les facteurs solubles dérivés de la glie stimulent également l’efficacité de la libération de neurotransmetteurs. L’ensemble de ces résultats démontre qu’un ou plusieurs signaux provenant des cellules gliales augmentent le nombre et l’efficacité des synapses.
Le défi à relever consistait à identifier de ce(s) facteur(s) dérivé(s) de la glie, afin de pouvoir analyser ces interactions in vivo et déterminer les mécanismes moléculaires impliqués. Des preuves solides permettent d’affirmer que la plupart des effets décrits ci-dessus sont induits par le cholestérol [9]. Tout d’abord, les lipoprotéines extraites par chromatographie du MCG reproduisent les effets observés sur l’activité synaptique. Deuxièmement, la réduction de la concentration en cholestérol à l’aide d’un inhibiteur de sa synthèse réduit de façon drastique les effets du MGC sur les neurones. Troisièmement, le blocage de l’entrée des lipoprotéines dans les neurones par un antagoniste compétitif des récepteurs des LDL (low-density lipoproteins) abolit l’effet du MCG sur l’activité synaptique. Quatrièmement, des marquages cytochimiques des CGR avec un composé se liant au cholestérol indiquent que le MCG augmente fortement le cholestérol total dans ces neurones. Enfin, le cholestérol seul mime la plupart des effet induits par le MCG sur le nombre et les capacités fonctionnelles des synapses des CGR [14].
L’ensemble de ces résultats suggère, d’une part, que les neurones réduisent leur synthèse de cholestérol durant le développement et importent ce composé des astrocytes par l’intermédiaire de particules de lipoprotéines. D’autre part, les neurones utilisent ce cholestérol d’origine gliale pour former de nombreuses connexions synaptiques fonctionnelles [11]. Compte tenu du nombre impressionnant d’études sur les cultures primaires de neurones, il est surprenant que cette dépendance soit passée inaperçue. Une explication possible réside dans le fait que les milieux de culture conventionnels contiennent des lipoprotéines riches en cholestérol fournies soit par l’ajout de sérum, soit par la présence de cellules gliales. De plus, la plupart des cultures sont préparées à partir de cerveaux embryonnaires dans lesquels les neurones synthétisent probablement leur propre cholestérol.
Fonctions du cholestérol dans les synapses
Le scénario décrit précédemment soulève la question du mécanisme par lequel le cholestérol glial stimule le développement des synapses. L’explication la plus simple serait que le cholestérol constitue un composant structural essentiel de la machinerie synaptique et que sa disponibilité soit, en conséquence, un facteur limitant l’assemblage des structures synaptiques [12].
Il a récemment été montré que la diminution du cholestérol dans la lignée cellulaire « neuronale » PC12 perturbe l’exocytose et que la machinerie d’exocytose (vésicules et protéines associées) est localisée dans des micro-domaines membranaires riches en cholestérol (Figure 1) [18]. De nombreuses données expérimentales suggèrent l’existence de tels domaines, dénommés rafts (→), dont la fonction est d’organiser les composants de signalisation dans la membrane plasmique des cellules, en général, et des synapses neuronales, en particulier [19]. Ainsi, au niveau présynaptique, une dépendance de l’exocytose des vésicules vis-à-vis du cholestérol pourrait expliquer, au moins partiellement, l’observation selon laquelle le cholestérol augmente l’efficacité de la libération des neurotransmetteurs dans les cultures de CGR [9].
(→) m/s 1999, n° 10, p. 1142
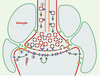 |
Figure 1. Fonctions du cholestérol dans les synapses. Localisation des domaines rafts (domaines membranaires lipidiques) riches en cholestérol (en vert): (1) dans les membranes des vésicules synaptiques (cercle rouge), où ils participent au transport axonal par la kinésine (cercle bleu) le long des microtubules (barre orange); (2) dans les zones pré-synaptiques, au niveau desquelles ils organisent la machinerie d’exocytose (losange bleu); (3) dans les membranes post-synaptiques, où ils agrègent les récepteurs aux neurotransmetteurs (ovale bleu) ou (4) dans les stocks extra-synaptiques, pour une mobilisation de ces récepteurs en fonction de l’activité (flash violet foncé); et, enfin, (5) aux bordures des synapses, favorisant ainsi l’adhérence cellulaire (rectangle jaune). Les synapses importent le cholestérol des astrocytes (membrane verte) par l’intermédiaire de particules de lipoprotéines (cercle vert) et de récepteurs de ces lipoprotéines (hexagone jaune). |
Des études antérieures avaient montré que les vésicules synaptiques possèdent plus de cholestérol que les autres organites intracellulaires [20]. Ainsi, la biogenèse des vésicules pourrait dépendre du taux de cholestérol cellulaire. Cette notion est renforcée par les travaux de Thiele et al. [21] qui ont montré que le taux de cholestérol détermine la disponibilité des vésicules sécrétrices dans les cellules PC12. De plus, une étude récente a démontré que le transport des vésicules le long des microtubules nécessite que leur membrane renferme du cholestérol [22]. Cela suggère que le transport efficace des vésicules synaptiques vers les terminaisons pré-synaptiques (Figure 1) dépendrait de leur composition en cholestérol. La notion que le cholestérol est nécessaire à la formation et au transport des vésicules pourrait expliquer l’observation selon laquelle le cholestérol augmente fortement le nombre de vésicules synaptiques des neurones en culture [9].
Le cholestérol pourrait également favoriser la différenciation post-synaptique. Il a été notamment montré que les récepteurs des neurotransmetteurs, ainsi que d’autres composants post-synaptiques, sont associés aux rafts (Figure 1) [23]. Le cholestérol fourni par les astrocytes pourrait faciliter, via les rafts, l’agrégation des récepteurs post-synaptiques et augmenter ainsi les réponses post-synaptiques [9]. Il est intéressant de noter que les récepteurs associés aux rafts forment une réserve extra-synaptique et que les rafts vont régler la mobilité latérale de ces récepteurs (Figure 1) [24].
Transfert de cholestérol entre astrocytes et neurones
Les astrocytes en culture synthétisent deux à trois fois plus de cholestérol que les neurones ou les fibroblastes [25] et sécrètent des particules de lipoprotéines servant de transporteurs de cholestérol in vitro [26] et in vivo [27]. De telles propriétés sont compatibles avec la notion selon laquelle les neurones dépendent intimement du cholestérol glial (Figure 2) [6].
 |
Figure 2. Transfert du cholestérol des astrocytes aux neurones. Les astrocytes libèrent des lipoprotéines (sphère vert clair) contenant du cholestérol (structures chimiques en vert foncé au coeur des lipoprotéines) et de l’ApoE (trait vert clair dans la membrane des lipoprotéines) à proximité des synapses. Les lipoprotéines sont récupérées par des récepteurs (hexagone jaune) exprimés au niveau des terminaisons pré- et post-synaptiques. L’activité électrique (flash violet foncé) pourrait augmenter le nombre de récepteurs des lipoprotéines ou augmenter la synthèse et la libération de cholestérol et de lipoprotéines par les astrocytes voisins (flèches pourpres). Le cholestérol serait alors utilisé par les neurones pour la synaptogenèse, l’excès de cholestérol étant éliminé par relargage de particules de lipoprotéines ou d’oxystérols. |
La découverte de la dépendance des neurones vis-àvis du cholestérol glial soulève plusieurs questions concernant son métabolisme. Les neurones synthétisent-ils du cholestérol ? Il est clairement établi que la totalité du cholestérol cérébral est synthétisée localement et non puisé dans la circulation sanguine [8], mais il n’est pas démontré que les neurones contribuent à l’élaboration du stock de cholestérol cérébral. Pour quelles raisons les neurones choisiraient-ils d’importer le cholestérol plutôt que de le synthétiser ? Une raison probable pourrait résider dans le coût logistique élevé de la synthèse des stérols, qui nécessite une batterie d’enzymes consommant l’énergie en grande quantité. Il n’est pas déraisonnable de penser que les neurones, qui sont des cellules très spécialisées dans la production de l’activité électrique, abandonnent la synthèse du cholestérol, notamment dans les zones synaptiques éloignées du soma. La dépendance neuronale en cholestérol extérieur pourrait également varier en fonction des régions cérébrales considérées et des différents types de neurones. Le concept selon lequel les cellules gliales sous-traitent la synthèse du cholestérol pour les neurones n’est pas sans rappeler d’autres exemples de coopération métabolique entre ces deux types de cellules [28].
Comment les neurones peuvent-ils récupérer le cholestérol glial ? D’une manière générale, les cellules récupèrent le cholestérol grâce à deux voies différentes, soit par l’endocytose de lipoprotéines se liant à des récepteurs des LDL, soit par le transfert direct des lipoprotéines vers la membrane plasmique via des récepteurs des HDL (high density lipoprotein) [8]. Pour le moment, le mécanisme par lequel les neurones récupèrent ce cholestérol sécrété par les cellules gliales et le mode de régulation de cet échange restent inconnus.
Implication dans les maladies neurodégénératives
Le fait que les neurones dépendent du cholestérol astrocytaire pour la synaptogenèse implique que des interférences dans le transfert du cholestérol conduisent à une neurodégénérescence. Les molécules impliquées dans la maladie d’Alzheimer [29] - peptide β-amyloïde et isoforme ApoE4 de l’apolipoprotéine ε - pourraient diminuer l’efficacité du transfert du cholestérol par l’intermédiaire des lipoprotéines ou perturber son homéostasie dans les neurones [30]. La mutation d’un gène codant pour une protéine impliquée dans l’acquisition du cholestérol dérivé des lipoprotéines induit une maladie neurodégénérative rare, la maladie de Niemann-Pick de type C [4]. Ces observations renforcent l’idée que les neurones dépendent in vivo également de l’apport de cholestérol par une source extérieure. Une rupture de l’homéostasie du cholestérol pourrait également contribuer à d’autres processus neurodégénératifs comme la chorée de Huntington (→) dont les relations avec ce lipide n’ont pas été identifiées pour l’instant.
(→) m/s 2003, n° 5, p. 613
Conclusions et perspectives
Un faisceau de preuves suggère que les neurones réduisent la coûteuse synthèse du cholestérol et qu’ils importent ce lipide des astrocytes afin de l’utiliser lors de la synaptogenèse. En conséquence, les mécanismes liés à la formation, à la fonction et à la plasticité des synapses sont probablement sensibles à des perturbations du métabolisme cérébral du cholestérol. De nouveaux modèles de souris devront être développés, chez lesquels sera modifié le métabolisme du cholestérol dans un type cellulaire précis et de façon spécifique et contrôlée dans le temps. Par ailleurs, il sera nécessaire de mettre au point, chez ces animaux, de nouvelles techniques permettant d’enregistrer le taux de cholestérol de façon localisée, voire cellulaire, afin de définir le rôle du cholestérol dans le dialogue s’établissant entre cellules gliales et neurones. Les réponses apportées par ces travaux contribueront à mieux comprendre les fonctions et l’homéostasie du cholestérol dans le cerveau et son implication lors de processus neurodégénératifs.
Remerciements
Les auteurs remercient M. Muzet pour son aide dans la rédaction de cet article. Notre recherche bénéficie du soutien du Cnrs, de la Société Max-Planck, de la Fondation pour la Recherche Médicale, de la Fondation Électricité de France, de l’ Ara Parseghian medical research foundation, de la Région Alsace et de la Deutsche Forschungsgemeinschaft.
Références
- Burger K, Gimpl G, Fahrenholz F. Regulation of receptor function by cholesterol. Cell Mol Life Sci 2000; 57: 1577–92. [Google Scholar]
- Baulieu EE, Robel P, Schumacher M. Neurosteroids: beginning of the story. Int Rev Neurobiol 2001; 46: 1–32. [Google Scholar]
- Mann RK, Beachy PA. Cholesterol modification of proteins. Biochim Biophys Acta 2000; 1529: 188–202. [Google Scholar]
- Vanier MT. Lipid changes in Niemann-Pick disease type C brain: personal experience and review of the literature. Neurochem Res 1999; 24: 481–9. [Google Scholar]
- McNamara DJ. Dietary cholesterol and atherosclerosis. Biochim Biophys Acta 2000; 1529: 310–20. [Google Scholar]
- Danik M, Champagne D, Petit-Turcotte C, Beffert U, Poirier J. Brain lipoprotein metabolism and its relation to neurodegenerative disease. Crit Rev Neurobiol 1999; 13: 357–407. [Google Scholar]
- Fagan AM, Holtzman DM. Astrocyte lipoproteins, effects of apoE on neuronal function, and role of apoE in amyloid-beta deposition in vivo. Microsc Res Tech 2000; 50: 297–304. [Google Scholar]
- Dietschy JM, Turley SD. Cholesterol metabolism in the brain. Curr Opin Lipidol 2001; 12: 105–12. [Google Scholar]
- Mauch DH, Nägler K, Schumacher S, et al. CNS synaptogenesis promoted by glia-derived cholesterol. Science 2001; 294: 1354–7. [Google Scholar]
- Göritz C, Mauch DH, Nägler K, Pfrieger FW. Role of gliaderived cholesterol in synaptogenesis: new revelations in the synapseglia affair. J Physiol (Paris) 2002; 96: 257–63 [Google Scholar]
- Pfrieger FW. Outsourcing in the brain: do neurons depend on cholesterol delivery by astrocytes ? Bioessays 2003; 25: 72–8. [Google Scholar]
- Pfrieger FW. Role of cholesterol in synapse formation and function. Biochim Biophys Acta 2003; 1610 : 271–80. [Google Scholar]
- Pfrieger FW, Barres BA. Synaptic efficacy enhanced by glial cells. Science 1997; 277: 1684–7. [Google Scholar]
- Nägler K, Mauch DH, Pfrieger FW. Glia-derived signals induce synapse formation in neurones of the rat central nervous system. J Physiol 2001; 533: 665–79. [Google Scholar]
- Ullian EM, Sapperstein SK, Christopherson KS, Barres BA. Control of synapse number by glia. Science 2001; 291: 657–61. [Google Scholar]
- Jacobson M. Developmental neurobiology. New York: Plenum Press, 1991. [Google Scholar]
- Barres BA, Silverstein BE, Corey DP, Chun LLY. Immunological, morphological, and electrophysiological variation among retinal ganglion cells purified by panning. Neuron 1988; 1: 791–803. [Google Scholar]
- Lang T, Bruns D, Wenzel D, et al. SNAREs are concentrated in cholesterol-dependent clusters that define docking and fusion sites for exocytosis. EMBO J 2001; 20: 2202–13. [Google Scholar]
- Simons K, Toomre D. Lipid rafts and signal transduction. Nat Rev Mol Cell Biol 2000; 1:31–9. [Google Scholar]
- Breckenridge WC, Morgan IG, Zanetta JP, Vincendon G. Adult rat brain synaptic vesicles. II. Lipid composition. Biochim Biophys Acta 1973; 320: 681–6. [Google Scholar]
- Thiele C, Hannah MJ, Fahrenholz F, Huttner WB. Cholesterol binds to synaptophysin and is required for biogenesis of synaptic vesicles. Nat Cell Biol 2000; 2:42–9. [Google Scholar]
- Klopfenstein DR, Tomishige M, Stuurman N, Vale RD. Role of phosphatidylinositol (4,5) bisphosphate organization in membrane transport by the Unc104 kinesin motor. Cell 2002; 109: 347–58. [Google Scholar]
- Becher A, White JH, McIlhinney RA. The gammaaminobutyric acid receptor B, but not the metabotropic glutamate receptor type-1, associates with lipid rafts in the rat cerebellum. J Neurochem 2001; 79: 787–95. [Google Scholar]
- Meier J, Vannier C, Serge A, Triller A, Choquet D. Fast and reversible trapping of surface glycine receptors by gephyrin. Nat Neurosci 2001; 4: 253–60. [Google Scholar]
- Saito M, Benson EP, Saito M, Rosenberg A. Metabolism of cholesterol and triacylglycerol in cultured chick neuronal cells, glial cells, and fibroblasts: accumulation of esterified cholesterol in serum-free culture. J Neurosci Res 1987; 18: 319–25. [Google Scholar]
- LaDu MJ, Gilligan SM, Lukens JR, et al. Nascent astrocyte particles differ from lipoproteins in CSF. J Neurochem 1998; 70: 2070–81. [Google Scholar]
- DeMattos RB, Brendza RP, Heuser JE, et al. Purification and characterization of astrocyte-secreted apolipoprotein E and Jcontaining lipoproteins from wild-type and human apoE transgenic mice. Neurochem Int 2001; 39: 415–25. [Google Scholar]
- Magistretti PJ, Pellerin L. Cellular mechanisms of brain energy metabolism and their relevance to functional brain imaging. Philos Trans R Soc Lond B Biol Sci 1999; 354: 1155–63. [Google Scholar]
- Selkoe DJ. Alzheimer’s disease: genes, proteins, and therapy. Physiol Rev 2001; 81: 741–66. [Google Scholar]
- Michikawa M, Gong JS, Fan QW, Sawamura N, Yanagisawa K. A novel action of Alzheimer’s amyloid beta-protein (Abeta): oligomeric Abeta promotes lipid release. J Neurosci 2001; 21: 7226–35. [Google Scholar]
Liste des figures
 |
Figure 1. Fonctions du cholestérol dans les synapses. Localisation des domaines rafts (domaines membranaires lipidiques) riches en cholestérol (en vert): (1) dans les membranes des vésicules synaptiques (cercle rouge), où ils participent au transport axonal par la kinésine (cercle bleu) le long des microtubules (barre orange); (2) dans les zones pré-synaptiques, au niveau desquelles ils organisent la machinerie d’exocytose (losange bleu); (3) dans les membranes post-synaptiques, où ils agrègent les récepteurs aux neurotransmetteurs (ovale bleu) ou (4) dans les stocks extra-synaptiques, pour une mobilisation de ces récepteurs en fonction de l’activité (flash violet foncé); et, enfin, (5) aux bordures des synapses, favorisant ainsi l’adhérence cellulaire (rectangle jaune). Les synapses importent le cholestérol des astrocytes (membrane verte) par l’intermédiaire de particules de lipoprotéines (cercle vert) et de récepteurs de ces lipoprotéines (hexagone jaune). |
| Dans le texte | |
 |
Figure 2. Transfert du cholestérol des astrocytes aux neurones. Les astrocytes libèrent des lipoprotéines (sphère vert clair) contenant du cholestérol (structures chimiques en vert foncé au coeur des lipoprotéines) et de l’ApoE (trait vert clair dans la membrane des lipoprotéines) à proximité des synapses. Les lipoprotéines sont récupérées par des récepteurs (hexagone jaune) exprimés au niveau des terminaisons pré- et post-synaptiques. L’activité électrique (flash violet foncé) pourrait augmenter le nombre de récepteurs des lipoprotéines ou augmenter la synthèse et la libération de cholestérol et de lipoprotéines par les astrocytes voisins (flèches pourpres). Le cholestérol serait alors utilisé par les neurones pour la synaptogenèse, l’excès de cholestérol étant éliminé par relargage de particules de lipoprotéines ou d’oxystérols. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




