| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
|
|
|---|---|---|
| Page(s) | 373 - 381 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2026056 | |
| Published online | 24 April 2026 | |
Trajectoires clonales de l’hématopoïèse post-greffe
Clonal trajectories of post-transplant hematopoiesis
1
Sorbonne Université, Inserm UMR_S938, Centre de recherche Saint Antoine (CRSA), Paris, France
2
EFS Ile-de-France, Unité d’ingénierie et de thérapie cellulaire, Créteil, France
3
Sorbonne Université, CNRS, Inserm, Développement, adaptation et vieillissement, Dev2A, Paris, France
4
Sorbonne Université, CNRS, Inserm, Institut de biologie Paris-Seine, IBPS, Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
**
This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
L’hématopoïèse repose sur des cellules souches multipotentes et des progéniteurs hématopoïétiques ayant une grande capacité d’amplification, et se déroule dans des niches spécialisées des os. Grâce aux progrès réalisés dans le typage HLA (human leucocyte antigen ; en français : complexe majeur d’histocompatibilité ou CMH) et dans le conditionnement des sources cellulaires, la transplantation de cellules souches hématopoïétiques permet de traiter efficacement les hémopathies malignes ainsi que certaines maladies génétiques. Le traçage des cellules révèle une reconstitution temporelle biphasique après greffe : d’abord par des progéniteurs hématopoïétiques, puis par les cellules souches hématopoïétiques multipotentes. L’hématopoïèse reconstituée reste polyclonale, influencée par l’âge du donneur, le contexte pathologique et les antécédents génétiques du donneur et du receveur. La transplantation n’augmente pas le nombre de mutations, mais elle induit une sélection clonale qui réduit la diversité, surtout chez les donneurs âgés. Ces résultats valident les stratégies de thérapie génique fondées sur l’utilisation de cellules souches hématopoïétiques et ouvrent des perspectives d’optimisation pour la sélection des donneurs, le conditionnement des cellules et la prise en charge personnalisée du receveur.
Abstract
Hematopoiesis relies on self-renewing hematopoietic stem and more committed progenitor cells (HSPCs), which occurs in specialized niches. Their transplantation can effectively treat malignant blood disorders and genetic diseases, thanks to advances in HLA typing, cell sources, and conditioning regimens. Clonal tracing reveals a biphasic pattern of hematopoietic reconstitution following transplantation, with initial contribution from short-term progenitors followed by long-term multi-potent hematopoietic stem cells (HSCs). Reconstituted hematopoiesis remains polyclonal, and is influenced by donor age, pathological context, and genetic history. Transplantation does not increase the mutational burden but induces clonal selection, leading to reduced clonal diversity, especially with HSPC from older donors. These results validate HSPC-based gene therapy and open new prospects for optimizing donor selection, conditioning regimens, and personalized patient care.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Hématopoïèse : quelques chiffres
Chez l’être humain, l’hématopoïèse se déroule dans la moelle osseuse des os plats (sternum, côtes, vertèbres, os iliaques) et dans les épiphyses des os longs. On dénombre environ 1,2 × 1012 cellules mononucléées et 2,8 × 1013 cellules sanguines dans la moelle osseuse humaine [1]. Chez une personne adulte, environ 500 milliards de cellules sanguines sont produites chaque jour. Cette production élevée est nécessaire pour compenser la durée de vie courte de certaines cellules sanguines, comme les neutrophiles, qui survivent seulement quelques heures à quelques jours, ou les plaquettes, dont la durée de vie moyenne est de sept à dix jours. Cette production repose sur les cellules souches hématopoïétiques (CSH), dont environ 10 % seulement sont actives, les autres étant en état de quiescence [2]. Les CSH ont la capacité unique de s’autore-nouveler et de se différencier en différents lignages hématopoïétiques. On estime qu’une CSH se divise en moyenne toutes les 40 semaines chez l’être humain [2]. Cette estimation a été obtenue en mesurant, chez des femmes, le pourcentage de cellules sanguines porteuses de l’inactivation du chromosome X soit paternel, soit maternel. Cette mesure de la sélection hémizygote donne une estimation du nombre de divisions cellulaires depuis la naissance, moment où la distribution hémizygote est considérée comme étant de 50 : 50. Des données biologiques ainsi que des simulations computationnelles ont permis d’estimer que la production quotidienne des cellules sanguines repose sur environ 10 000 CSH [2]. Ces chiffres ont récemment été remis en cause par deux études [3, 4] utilisant le séquençage profond du génome entier de CSH amplifiées in vitro. Ces études concluent à un nombre de CSH compris entre 44 000 et 215 000 et à une fréquence de division comprise entre deux et vingt mois. Ces résultats, basés sur la détection de mutations dans des ensembles de gènes préétablis, ont été complétés par des modèles bayésiens1.
Ces chiffres, bien supérieurs à ceux rapportés jusqu’à présent, doivent être confirmés, car, dans les deux études, le nombre de cellules analysées est faible (140 dans [3], et 18 dans [4]), ce qui réduit considérablement la robustesse statistique des données. Cependant, le fonctionnement quotidien du système hématopoïétique repose sur des progéniteurs hématopoïétiques2 à forte capacité de multiplication, ainsi que sur des CSH « activées », et proches de la niche vasculaire, qui vont entrer en cycle et produire de nouveaux progéniteurs hématopoïétiques [5, 6]. De plus, les marqueurs de surface cellulaire couramment utilisés pour isoler les CSH permettent d’obtenir une fraction cellulaire composée de CSH et de progéniteurs hématopoïétiques multipotents. Dans la suite de cette étude, nous appellerons les cellules utilisées pour la thérapie génique ou cellulaire « cellules souches et progéniteurs hématopoïétiques (CSPH) » afin de mieux refléter la diversité populationnelle obtenue et traitée. Les populations cellulaires seront nommées « CSH » dans le cas de greffes à long terme et/ou lorsque leur quiescence est avérée.
La notion de niche hématopoïétique
Chez l’adulte, les CSPH résident dans le microenvironnement unique de la moelle osseuse, appelé niche hématopoïétique. Celle-ci a été particulièrement bien décrite chez la souris adulte, mais elle reste moins bien définie chez l’être humain, malgré quelques avancées récentes [7–9]. Chez la souris comme chez l’être humain, les niches sont définies en fonction de leur localisation anatomique dans la moelle osseuse et du type de vaisseau sanguin qu’elles contiennent : les sinusoïdes ou les artérioles3. Deux niches au moins sont définies sur une base anatomique : la niche endostéale, au contact de l’os, et la niche centrale, localisée au centre de la moelle. La première occupe environ 10 % du volume total et abrite environ 15 % des CSH totales ; elle est composée de cellules dérivées de cellules souches mésenchymateuses, c’est-à-dire d’ostéoblastes, de fibroblastes et d’adipocytes, ainsi que de cellules hématopoïétiques impliquées dans la résorption osseuse. La seconde, qui contient la majorité des sinusoïdes et des artérioles, comprend plus de 90 % du volume de la moelle osseuse et 80 % des CSH. Les deux niches assurent des fonctions différentes. Les CSH actives transitent par la niche centrale, qui assure la production quotidienne de cellules sanguines et est sensible au stress génotoxique et à la myéloablation4. À l’inverse, la niche endostéale est relativement préservée de ces agressions et semble jouer un rôle important dans la reprise hématopoïétique après une déplétion médullaire [10].
La transplantation hématopoïétique : des origines… à nos jours
La transplantation de cellules hématopoïétiques, également appelée greffe de moelle osseuse ou greffe de CSH, a émergé comme une avancée médicale majeure au cours de la seconde moitié du xxe siècle. Historiquement, elle s’inspire des travaux d’Egon Lorenz (1892-1954), médecin germano-américain, publié en 1951 [11], qui ont démontré l’utilité de la greffe de cellules de la moelle osseuse chez des souris et des cobayes pour réduire la mortalité après irradiation. Les premiers essais de greffe de cellules de la moelle osseuse chez l’être humain ont eu lieu en 1957 [12], mais n’ont abouti qu’à une greffe à court terme. Le premier succès thérapeutique a été obtenu avec la première greffe hématopoïétique hétérologue (encore appelée allogénique) après l’accident de l’Institut des sciences nucléaires de Vinča5 [13] en 1958, lorsqu’une prise de greffe temporaire a permis la survie des patients jusqu’à la reconstitution de leur propre moelle. Dans la greffe allogénique, on recherche le donneur le plus compatible par rapport au receveur. Le donneur peut être apparenté ou non apparenté. La première greffe à long terme fut une greffe géno-identique, publiée en 1961, avec la transplantation d’un patient, atteint d’aplasie médullaire, avec des cellules de son frère jumeau [14]. Quelques années plus tard, la première greffe hétérologue à long terme a permis de traiter des patients atteints de leucémie [15]. La méconnaissance des systèmes d’histocompatibilité a cependant posé problème jusqu’aux années 1990, car de nombreux patients décédaient de la maladie du greffon contre l’hôte (GVH, graft-versus-host disease) ou développaient une GVH chronique [16]. La découverte, par le Pr. Jean Dausset6, du rôle crucial des antigènes HLA (human leukocyte antigen) dans la tolérance de la greffe [17], a permis d’améliorer considérablement le taux de succès des greffes de moelle osseuse [18] (→).
(→) Voir m/s n° 5, 2010, page 447
Actuellement, un typage HLA de haute résolution (HLA-A, -B, -C, DRB1 et DQB1) est réalisé dès le diagnostic. En première intention, le typage est effectué au sein de la fratrie du patient. En l’absence de donneur apparenté HLA-identique, la recherche est élargie aux registres internationaux. La compatibilité entre le receveur et le donneur est évaluée à l’aide d’un score, calculé en fonction du degré de correspondance entre les différents HLA typés [19]. La plupart des greffes sont réalisées de manière hétérologue avec un donneur compatible. Cependant, chaque année, plusieurs milliers de patients restent en attente de donneurs compatibles (source : world marrow donor association7, 2021). Aujourd’hui, la greffe de CSH demeure le principal traitement curatif pour de nombreuses hémopathies malignes et des maladies génétiques héréditaires [20], ainsi que pour les thérapies géniques basées sur les CSPH [21].
Les progrès techniques ont permis de diversifier les sources de cellules souches : la moelle osseuse, le sang périphérique et le sang du cordon ombilical. Parallèlement, l’optimisation des traitements de conditionnement et des thérapies post-greffe a permis de réduire les risques de rejet et de complications. Des avancées majeures dans la compréhension du microbiome et du rôle de l’immunité dans la réponse au greffon ont également amélioré les résultats à long terme. Dans ce contexte, il est essentiel de comprendre le rôle de différentes populations de CSPH après la transplantation afin d’améliorer les procédures cliniques visant à établir non seulement le maintien à long terme du greffon, mais aussi la récupération précoce de l’aplasie médullaire8.
Le traçage cellulaire pour étudier l’hématopoïèse
Depuis quelques années, de nouvelles approches basées sur le traçage cellulaire in vivo sont progressivement employées pour étudier le comportement des CSPH après transplantation [22]. Ces techniques ont été utilisées dans deux articles récents parus dans la revue Nature, rapportant respectivement l’utilisation des sites d’insertion virale comme des codes-barres dans le cadre de thérapies géniques [23], et l’utilisation des mutations naturelles acquises au cours du temps comme marqueurs de lignage, permettant de recréer des arbres phylogénétiques après transplantation [24].
Dans de nombreuses thérapies géniques utilisant les CSPH, des copies fonctionnelles du gène défectueux sont délivrées aux cellules à l’aide d’un vecteur viral recombinant qui s’intègre dans le génome. Cette intégration spécifique à chaque couple vecteur viral-cellule, constitue un véritable code-barre unique. Les conditions de transduction sont ajustées pour que chaque cellule reçoive tout au plus un vecteur viral, assurant ainsi l’intégration d’une seule copie du vecteur viral par cellule. Chaque CSPH transduite devient alors un clone dont la descendance héritera du même code-barre. L’analyse par séquençage des sites d’intégration permet de reconstituer l’histoire de différents clones, leur capacité à s’amplifier et à se différencier dans un ou plusieurs lignages.
Ce traçage des sites d’insertion du vecteur viral a permis, dans un premier temps, d’étudier en détail la transplantation hématopoïétique chez des primates non humains dans des conditions très proches de celles de l’être humain [25–27]. Ces trois études ont conclu à une contribution importante de progéniteurs hématopoïétiques à court terme dans les premières phases post-transplantation, suivie par la mise en place d’une hématopoïèse stable assurée par 4 à 10 % des clones, sans doute des CSH. Une étude a, de plus, montré que la dynamique de reconstitution après traitement myéloablatif pouvait impliquer des CSH greffant rapidement et persistant à long terme [28].
Quelques études similaires utilisant les sites d’insertion, cette fois-ci dans le cadre de thérapies géniques chez l’être humain, ont révélé la complexité du fonctionnement du système hématopoïétique [29–34]. Ces études montrent que, durant les six premiers mois postthérapie, l’hématopoïèse est initialement assurée par des clones restreints à un seul lignage cellulaire, avant d’être progressivement relayée par des cellules hématopoïétiques capables de différenciation multilignage, vraisemblablement des CSH. Certaines de ces cellules peuvent rester quiescentes pendant la première phase de la reconstitution, puis s’activer ensuite, indiquant que la transplantation ne s’accompagne pas nécessairement d’une activation hématopoïétique liée au stress de la transplantation [33]. Ces études indiquent également que cette stabilisation de la reconstitution cellulaire au profit des CSH survient entre un et deux ans post-transplantation, et, que, si le nombre de clones observés est important immédiatement après la thérapie génique, il tend à diminuer pour atteindre une moyenne de 2 000 à 50 000 clones de CSPH actifs, en accord avec des chiffres obtenus par d’autres moyens [1] sur des sujets normaux et en étudiant d’autres types de maladies [29, 35].
Dynamiques hématopoïétiques post-greffes
L’insertion virale comme code-barre
L’étude de Calabria et al., s’appuie sur un suivi clonal de la reconstitution hématopoïétique après thérapie génique lentivirale de CSPH chez 53 personnes âgées de 6 mois à 15 ans, atteintes de trois maladies génétiques distinctes : 9 patients atteints de β-thalassémie, une maladie génétique héréditaire qui affecte la production des chaînes ß de l’hémoglobine produites en quantités insuffisantes, ce qui altère la fonctionnalité des globules rouges ; 15 patients atteints du syndrome de Wiskott-Aldrich (WAS), une maladie récessive liée à l’X dont la cause principale est une mutation du gène WAS, fortement exprimé par les cellules hématopoïétiques, et dont la protéine (WASP) est un régulateur majeur de la polymérisation de l’actine, ce qui provoque un déficit en lymphocytes ; et 29 patients atteints de leucodystrophie métachromatique (MLD), une maladie métabolique neurodégénérative causée par une mutation dans le gène ARSA (arylsulfatase A) qui conduit à l’accumulation de sulfatides dans le système nerveux central et périphérique en raison d’un déficit de l’enzyme arylsulfatase A, entraînant une démyélinisation et une accumulation nocive de lipides dans le système nerveux, et provoquant une inflammation locale. Les progrès en thérapie génique et le traitement de la β-thalassémie et du WAS ont fait l’objet d’articles récents dans médecine/sciences [36, 37] (→).
(→) Voir m/s n° 10, 2022, page 768
(→) Voir m/s n° 8-9, 2023, page 589
L’étude a suivi les patients jusqu’à huit années après la greffe, avec des échantillons collectés à 1, 3, 6, 9 et 12 mois post-traitement au cours de la première année, puis une fois par an par la suite. Le suivi a été réalisé sur les CSPH de la moelle osseuse et du sang périphérique, ainsi que sur les cellules myéloïdes, B, T, érythroïdes, précurseurs et progéniteurs CD34+ purifiés, pour un total de plus de 6 700 échantillons séquencés. Plusieurs paramètres ont été étudiés : la dynamique des clones de cellules marquées, la taille des populations souches et progénitrices, la production des cellules CD34+ et l’analyse longitudinale de la différenciation des cellules souches et progénitrices (Figure 1). Dans cette étude, le nombre de CSPH actives au cours de l’hématopoïèse stable varie de 1 800 à 74 000, ce qui représente 0,0007 à 0,03 % des cellules totales inoculées, un chiffre similaire pour les trois maladies, que les cellules soient collectées à partir du sang périphérique ou de la moelle osseuse. Cette étude met également en lumière l’avantage d’utiliser les CSPH mobilisées9 du sang périphérique. Pour les trois maladies, la production de CSPH ayant un potentiel multilignages (dans cette étude, sont considérés comme multilignages les clones qui produisent au moins deux lignages hématopoïétiques différents, ce qui peut introduire un biais dans l’analyse) ne représente que 50 % des clones, tandis que les 50 % restants sont constitués de clones engagés vers un lignage spécifique, avec des différences propres aux programmes cliniques. De manière intéressante, plus de 75 % des sites d’insertion du vecteur viral ont été identifiés au cours des 12 premiers mois post-traitement et ont persisté pendant au moins 10 ans, avec cependant des clones additionnels qui apparaissent au cours du temps. Les sites d’intégration sont majoritairement retrouvés dans des régions riches en gènes, en particulier dans des gènes impliqués dans les modifications de la chromatine et des histones, comme précédemment décrit [29, 35]. Si le nombre de clones actifs est important au début du traitement, il diminue notablement après 24 mois. Ceci reflète la contribution de nombreux progéniteurs engagés au début du traitement, qui vont s’épuiser et être progressivement remplacés à long terme par un plus petit nombre de CSPH actives assurant l’hématopoïèse.
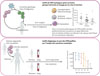 |
Figure 1 Suivi de l’hématopoïèse post-greffe. En haut : greffe de cellules autologues après correction génique par lentivirus et traçage des CSPH ingéniérées grâce aux sites d’insertion des vecteurs viraux. Trois maladies génétiques distinctes affectant l’hématopoïèse ont été ciblées : la leucodystrophie métachromatique, maladie métabolique neurodégénérative ; le syndrome de Wiskott-Aldrich, maladie récessive liée à l’X et la β-thalassémie, maladie génétique héréditaire qui affecte la production des chaines ß de l’hémoglobine. Cette étude révèle le rôle clé du microenvironnement pathologique pour biaiser la production hématopoïétique vers les lignages déficients dans la maladie. CSPH : cellules souches pluripotentes hématopoïétiques ; BTHAL : β-thalassémie ; WAS : syndrome de Wiskott-Aldrich ; MLD : leucodystrophie métachromatique. En bas : greffes allogéniques et suivi des CSPH greffées et résiduelles par l’analyse des mutations somatiques. La liste des mutations présentes dans les cellules hématopoïétiques du donneur est établie et sert de socle pour évaluer l’influence de la greffe sur l’accumulation de mutations post-greffe. Les profils mutationnels hématopoïétiques des donneurs et des receveurs sont suivis longitudinalement. L’influence de la greffe sur le profil mutationnel est établie ainsi que les dynamiques de reconstitution hématopoïétique post-greffe. La conclusion est que l’âge du donneur influence de façon majeure la dynamique de reconstitution hématopoïétique avec, dans le cas de donneurs âgés, une très forte réduction du nombre de CSH contribuant à l’hématopoïèse chez le receveur, accompagnée d’une accumulation plus importante de mutations par rapport aux cellules du donneur n’ayant pas subi de greffe. |
Chez les patients atteints de MLD, de WAS et de β-thalassémie, les clones transduits montrent une production préférentielle et un engagement dans les lignées myéloïde, lymphoïde et érythroïde respectivement, même après plusieurs années de traitement. Les CSPH transplantées répondent donc à l’environnement pathologique en favorisant la production des types cellulaires les plus nécessaires, c’est-à-dire que la maladie oriente la différenciation hématopoïétique des CSPH injectées. Le suivi des cytokines dans ces maladies montre soit une persistance de la production d’érythropoïétine dans la β-thalassémie, soit une diminution tardive de la thrombopoïétine au moins un an après la thérapie pour le WAS. Ceci suggère que la maladie impacte non seulement les cellules hématopoïétiques, mais influence aussi fortement le microenvironnement médullaire et la production des cytokines. Ce biais n’est cependant pas observé dans d’autres maladies telles que la granulomatose chronique ou les leucodystrophies [35, 38–40]. De plus, l’âge affecte également l’engagement hématopoïétique multilignages. Les patients plus âgés atteints de MLD et de β-thalassémie présentent moins de clones multilignages que leurs homologues plus jeunes. Les CSPH génétiquement modifiées, une fois leur stabilité atteinte, contribuent à environ 50 % de l’hématopoïèse, tandis que les clones restants sont engagés dans un lignage donné. Ces observations confortent l’hypothèse selon laquelle, à distance de la transplantation, l’hématopoïèse est maintenue par de nombreuses CSPH engagées dans un lignage et capables de persister pendant plusieurs années, sans qu’aucune preuve de dominance clonale ne soit mise en évidence, même à distance de la greffe.
Cette étude confirme et étend les conclusions des études précédentes [29, 34, 35, 38, 41, 42] (→) concernant l’efficacité à long terme de la thérapie génique par un vecteur rétroviral intégratif dans les maladies du sang. Les conclusions générales sont que le rendement à long terme, l’engagement dans la différenciation des CSPH, ainsi que l’accumulation de mutations somatiques post-traitement, sont fortement modulés par les antécédents génétiques des patients, sans doute pour mieux s’adapter et compenser les exigences posées par l’état clinique spécifique.
(→) Voir m/s n° 11, 2025, page 877
Les mutations somatiques comme traceur de lignage
L’étude de Spencer-Chapman et al. [24] utilise les mutations spontanées qui se produisent au cours de la vie comme codes-barres pour le suivi de la reconstitution cellulaire. À partir de la fécondation, les cellules du corps humain subissent continuellement des dommages génomiques, soit pour des raisons intrinsèques, soit en raison d’une exposition exogène à des mutagènes. Bien que la quasi-totalité des dommages causés à l’ADN soit réparée et que le génome soit répliqué avec une fidélité extrêmement élevée, les cellules acquièrent progressivement des mutations somatiques tout au long de la vie. Si des mutations sont présentes dans une cellule, elles sont partagées avec sa descendance. Comme des mutations identiques surviennent rarement par hasard, les mutations partagées indiquent souvent une histoire développementale commune. Une fois acquises, les mutations sont rarement perdues. Ainsi, les relations développementales passées des phases embryonnaire, fœtale, infantile et adulte de la vie peuvent être identifiées à partir des mutations dans les cellules adultes. C’est ce principe d’accumulation et de traçage des mutations somatiques que Spencer-Chapman et al. ont utilisé, pour étudier la dynamique hématopoïétique après transplantation de CSH. Si la majorité des mutations sont neutres, certaines peuvent aussi conduire des clones possédant une mutation somatique conférant un avantage sélectif à s’amplifier plus que les autres [41].
L’étude de Spencer-Chapman et al., offre une image de la dynamique de la prise de greffe à long terme (9 à 31 ans post-greffe) des CSPH en suivant la phylogénie du système hématopoïétique au sein de paires10 donneur-receveur, frères ou sœurs ayant une compatibilité HLA totale. L’indication la plus fréquente de ces transplantations était la leucémie aiguë myéloïde, et les régimes de préparation étaient soit la myéloablation, soit le conditionnement11. Les sources de cellules souches étaient la moelle osseuse ou le sang périphérique mobilisé, et les receveurs et donneurs étaient d’âge similaire (de 7 à 11 ans). Pour chaque donneur et receveur, des CSPH ont été isolées, leur capacité à produire des colonies hématopoïétiques en milieu semi-solide a été analysée, et ces colonies ont été prélevées et séquencées. Les génomes de 2 824 colonies hématopoïétiques ont ainsi permis d’étudier les mutations somatiques des dix paires (Figure 1).
Pour les greffes provenant de donneurs relativement jeunes (âgés de 18 à 47 ans au moment de la greffe), environ 5 000 à 30 000 CSPH avaient greffé. En revanche, ce nombre était environ dix fois inférieur pour les greffes provenant de donneurs plus âgés (50 à 66 ans). La greffe a considérablement réduit la diversité clonale chez les receveurs, correspondant à 10 à 15 ans de vieillissement supplémentaire par rapport à une personne en bonne santé n’ayant pas bénéficié d’une greffe. Cet effet était encore plus prononcé lorsque la greffe provenait de donneurs plus âgés. Sur les centaines de millions de cellules reçues du donneur, seuls quelques milliers ou dizaines de milliers contribuent encore à l’hématopoïèse 10 ans plus tard, voire au-delà. La diversité clonale observée chez les donneurs les plus âgés repose sans doute sur des CSPH particulièrement bien adaptées à survivre en condition de stress, plus adaptées que les CSPH “normales”. Cela dit, la détérioration de la fonction hématopoïétique liée à l’âge ne se produit pas par un déclin général des CSPH transplantées, mais par l’acquisition de mutations particulières par un petit nombre de CSPH. La contrepartie est que ces clones peuvent présenter un désavantage pour le receveur sur le long terme, tel qu’un biais de lignage, une réponse faible au stress hématopoïétique ou une diversité immunitaire réduite, ce qui explique les moins bons résultats de la transplantation hématopoïétique chez les individus plus âgés. Cette image est à rapprocher de celle fournie par une étude de la hiérarchie hématopoïétique chez 10 individus sains âgés de 0 à 81 ans, sans maladie hématopoïétique connue [42]. L’étude montre que les CSPH accumulent en moyenne 17 mutations par an après la naissance et que l’hématopoïèse chez les adultes de moins de 65 ans est massivement polyclonale, avec une population de 20 000 à 200 000 CSPH contribuant à la production hématopoïétique. En revanche, les individus âgés de plus de 75 ans voient leur diversité clonale diminuer drastiquement, 12 à 18 clones indépendants contribuant entre 30 et 60 % de l’hématopoïèse globale, chacun d’eux y contribuant entre 1 et 34 %. La plupart des clones ont initié leur expansion avant 40 ans, mais seuls 22 % portent une mutation driver12 connue. Ce changement abrupt peut s’expliquer par l’accumulation de mutations (driver et non driver) qui confère un désavantage progressif, devenant délétère autour de 75 ans. En considérant entre 20 000 et 50 000 CSH par individu, autour de 70 ans, le pool de CSH portera entre 350 000 et 1 400 000 mutations [43].
Chez les donneurs, la charge globale des mutations ponctuelles s’accumule tôt avec l’âge, à un taux de 15,8 mutations par CSPH et par an, en accord avec des résultats déjà publiés [4, 42]. En moyenne, les CSPH du receveur présentent 23 mutations de plus que celles du donneur, ce qui équivaut à un an et demi de vieillissement normal. Cependant, cette différence n’est observée que dans la moitié des paires et n’est donc pas significative selon les auteurs. Cette faible différence dans le nombre de mutations entre donneur et receveur corrobore les résultats antérieurs concernant la transplantation de CSPH issues de sang de cordon ombilical et plaide en faveur d’un rôle neutre de la transplantation dans l’apparition de mutations. Soixante et onze mutations indépendantes ont été trouvées dans les 10 paires étudiées. Les gènes mutés les plus fréquents sont DNMT3A [DNA methyl – transferase-3A] (n = 23) et TET2 [ten-eleven-translocation 2] (n = 9). Les mutations dans le gène DNMT3A sont réparties de manière variable entre donneurs et receveurs. La superposition du moment de la transplantation hématopoïétique avec ces phylogénies montre que toutes les mutations partagées entre donneur et receveur datent d’avant la transplantation. Cependant, chez les receveurs, il y a une coalescence13 accrue des arbres phylogénétiques au moment de la greffe ou après, indiquant que le conditionnement et/ou l’acte même de greffe contribuent à un appauvrissement de la diversité cellulaire.
L’estimation du nombre de CSPH ayant greffé à long terme varie de 700 à 25 000 selon les paires. Ce chiffre est supérieur chez les donneurs les plus jeunes, et la diversité clonale est plus importante chez les donneurs que chez les receveurs. Cependant, la trajectoire individuelle des clones est plus variable, avec des clones s’amplifiant davantage chez les receveurs que chez les donneurs. La grande majorité des clones montre un biais vers l’un ou l’autre des lignages, avec une préférence pour le lignage myéloïde, puis vers le lignage lymphoïde B et enfin le lignage T. Si le lignage myéloïde se développe rapidement dans les deux à trois mois suivant la transplantation, les lignages lymphoïdes mettent des années à se rétablir, probablement en raison du traitement immunosuppresseur et de la vitesse plus lente d’établissement de l’immunité adaptative. Il a été établi que la diversité clonale de l’hématopoïèse diminue progressivement avec l’âge, de sorte qu’après 70 ans, une grande partie de la production sanguine repose sur 10 à 20 clones ayant acquis au fil des années des mutations driver. Chez les paires les plus âgées, ce processus est accéléré : les receveurs ont une proportion d’hématopoïèse dérivant de clones mutés plus élevée que leurs donneurs appariés, ce qui entraîne une baisse globale de la diversité clonale. L’analyse phylogénétique indique que cela équivaut à près de 12 années supplémentaires de vieillissement hématopoïétique. Au cours de cette étude, 52 mutations driver connues [44–46] ont été analysées. Sur le long terme, la fréquence post-greffe de la majorité des clones ne change pas significativement : 14 ont augmenté, 5 ont diminué ; il est cependant à noter que les mutations du gène CHEK2 (checkpoint kinase 2) sont systématiquement amplifiées chez les receveurs. Les trajectoires sont comparables dans les monocytes, les cellules B et les cellules T. Les clones cumulant plusieurs mutations driver connues tendent à croître davantage que ceux n’en possédant qu’une seule.
Un modèle bayésien a été développé par cette équipe pour déduire les distributions a posteriori de la fraction clonale de chaque mutation somatique dans chaque type cellulaire. Les différences observées entre les compartiments myéloïdes et lymphoïdes T ne s’expliquent que partiellement par les biais identifiés. L’analyse des mutations embryonnaires précoces montre que, chez les paires donneur-receveur jeunes, les fractions clonales sont similaires entre donneurs et receveurs pour tous les types cellulaires. Pour les paires plus âgées, la composition clonale des lymphocytes des receveurs reste proche de celle des donneurs, sans signe de dérive vers quelques clones dominants induite par la greffe, à l’exception d’une paire, pour laquelle une expansion clonale spécifique apparaît dans les cellules T du receveur (environ 20 %).
La perte de diversité clonale après greffe ne peut pas être expliquée uniquement par la sélection liée à l’âge. L’analyse phylogénétique révèle deux modes distincts de sélection clonale. Le premier, la sélection par élagage, voit certains clones faiblement présents chez le donneur prendre l’ascendant après la greffe, en raison d’avantages intrinsèques favorisant leur survie, leur collecte ou leur implantation. Le second, la sélection par croissance, correspond à l’amplification de certains clones, principalement après la greffe, grâce à une prolifération préférentielle dans la moelle du receveur. Ces deux mécanismes expliquent mieux la perte de diversité clonale observée ; cependant, certains cas suggèrent une combinaison des deux ou l’influence d’autres facteurs spécifiques aux clones. En particulier, il est fortement envisageable que l’environnement inflammatoire associé à la greffe influence les trajectoires clonales et favorise la persistance de certaines mutations.
Une étude parue simultanément [47] confirme les résultats de Spencer-Chapman et al., tout en apportant un éclairage original sur l’hématopoïèse clonale. Cette étude utilise seize paires donneurs-receveurs d’un âge à la transplantation de 6,6 à 45,7 ans. Issue des patients du Fred Hutchinson Cancer Center entre 1971 et 2010, elle inclut les plus anciens patients transplantés au monde. Elle étudie les fréquences relatives de mutation et les schémas d’hématopoïèse clonale en utilisant une technique ultra-sensible de séquençage appelée “séquençage duplex”. Cette technique détecte les variants à faible fréquence que d’autres méthodes de séquençage de l’ADN ne détectent pas, en marquant, copiant et séquençant séparément les brins d’ADN direct et inverse, ce qui élimine presque totalement les artefacts résultant d’erreurs de polymérase ou de dommages de l’ADN. Le taux d’erreur du “séquençage duplex” est inférieur à 1 sur 10 millions, ce qui permet une détection sensible et spécifique de variants à fréquence exceptionnellement faible. Le séquençage est réalisé directement sur les cellules du sang périphérique sans culture, comme dans l’étude de Spencer-Chapman et al. De façon surprenante, des mutations d’hématopoïèse clonale dans des gènes régulièrement mutés dans des maladies myéloïdes sont détectées chez tous les donneurs sains, y compris au cours de leurs vingt premières années de vie. La fréquence des mutations d’hématopoïèse clonale augmente avec l’âge. Les variants les plus fréquents concernent les gènes DNMT3A, TET2 et ASXL1 (additional sex combs-like 1). Cette étude démontre que la transplantation n’induit pas d’augmentation de la charge mutationnelle. Néanmoins, cette conclusion doit être nuancée en raison des limites liées à la composition de la cohorte. En effet, sur les 16 paires, 4 sont des donneurs-receveurs apparentés et non frères et sœurs, et les maladies initiales sont hétérogènes (un syndrome myélodysplasique, trois leucémies aiguës lymphoblastiques, cinq leucémies myéloïdes chroniques, quatre anémies aplasiques et une hémoglobinurie paroxystique nocturne). Ces différences cliniques et génétiques pourraient influencer la dynamique clonale observée après la greffe.
Conclusion
L’étude du devenir des CSPH post-transplantation a considérablement enrichi notre compréhension de l’hématopoïèse humaine. Les approches de traçage clonal, reposant sur l’analyse des sites d’intégration des vecteurs viraux, utilisés en thérapie génique, ou sur l’étude des mutations somatiques, montrent que la reconstitution hématopoïétique s’effectue en deux phases : une contribution initiale massive de progéniteurs à court terme, suivie de l’installation plus durable des CSH à long terme. Ces analyses révèlent également que la diversité clonale persiste à long terme, bien que modulée par l’âge, l’état clinique et les antécédents génétiques des receveurs. Si la greffe ne semble pas accroître significativement la charge mutationnelle, elle s’accompagne néanmoins d’une sélection clonale complexe, mêlant les concepts statistiques d’élagage et d’amplification préférentielle, pouvant ainsi accentuer la perte de la diversité hématopoïétique chez les receveurs plus âgés. La découverte de nombreuses mutations driver jusque-là non répertoriées souligne l’existence de mécanismes sélectifs encore mal compris, potentiellement propres au contexte de la transplantation. Ainsi, l’hématopoïèse post-greffe ne repose pas uniquement sur quelques clones dominants, mais sur un équilibre entre clones multipotents et engagés, capables de contribuer de façon stable à l’hématopoïèse pendant des décennies. Ces travaux éclairent les fondements biologiques de la greffe de CSH et ouvrent des perspectives pour optimiser la sélection des donneurs, affiner les stratégies de conditionnement et améliorer la prise en charge des receveurs, en particulier chez les patients âgés ou porteurs de mutations clonales préexistantes.
Conflits d’intérêt
Les auteurs déclarent qu’ils n’ont aucun conflit d’intérêt.
Références
- Cosgrove J, Hustin LSP, de Boer RJ, Perie L. Hematopoiesis in numbers. Trends Immunol 2021 ; 42 : 1100–12. [Google Scholar]
- Catlin SN, Busque L, Gale RE, et al. The replication rate of human hematopoietic stem cells in vivo. Blood 2011 ; 117 : 4460–6. [Google Scholar]
- Lee-Six H, Obro NF, Shepherd MS, et al. Population dynamics of normal human blood inferred from somatic mutations. Nature 2018 ; 561 : 473–8. [Google Scholar]
- Osorio FG, Rosendahl Huber A, Oka R, et al. Somatic mutations reveal lineage relationships and age-related mutagenesis in human hematopoiesis. Cell Rep 2018 ; 25 : 2308–16 e4. [Google Scholar]
- Olson OC, Kang YA, Passegue E. Normal hematopoiesis is a balancing act of self-renewal and regeneration. Cold Spring Harb Perspect Med 2020 ; 10. [Google Scholar]
- Busch K, Klapproth K, Barile M, et al. Fundamental properties of unperturbed haematopoiesis from stem cells in vivo. Nature 2015 ; 518 : 542–6. [Google Scholar]
- Bandyopadhyay S, Duffy MP, Ahn KJ, et al. Mapping the cellular biogeography of human bone marrow niches using single-cell transcriptomics and proteomic imaging. Cell 2024 ; 187 : 3120–40 e29. [Google Scholar]
- Ayhan S, Nemutlu E, Uckan Cetinkaya D, et al. Characterization of human bone marrow niches with metabolome and transcriptome profiling. J Cell Sci 2021 ; 134. [Google Scholar]
- Desterke C, Petit L, Sella N, et al. Inferring gene networks in bone marrow hematopoietic stem cell-supporting stromal niche populations. iScience 2020 ; 23 : 101222. [CrossRef] [PubMed] [Google Scholar]
- Mendez-Ferrer S, Bonnet D, Steensma DP, et al. Bone marrow niches in haematological malignancies. Nat Rev Cancer 2020 ; 20 : 285–98. [Google Scholar]
- Lorenz E, Uphoff D, Reid TR, Shelton E. Modification of irradiation injury in mice and guinea pigs by bone marrow injections. J Natl Cancer Inst 1951 ; 12 : 197–201. [Google Scholar]
- Thomas ED, Lochte HL, Jr., Lu WC, Ferrebee JW. Intravenous infusion of bone marrow in patients receiving radiation and chemotherapy. N Engl J Med 1957 ; 257 : 491–6. [Google Scholar]
- Mathe G. [Problems presented to the hematologist by the treatment of subjects accidentally irradiated at high dose]. Rev Hematol 1960 ; 15 : 3–9. [Google Scholar]
- Robins MM, Noyes WD. Aplastic anemia treated with bone-marrow transfusion from an identical twin. N Engl J Med 1961 ; 265 : 974–9. [Google Scholar]
- Mathe G, Amiel JL, Schwarzenberg L, et al. Successful allogenic bone marrow transplantation in man: chimerism, induced specific tolerance and possible anti-leukemic effects. Blood 1965 ; 25 : 179–96. [Google Scholar]
- Malard F, Holler E, Sandmaier BM, et al. Acute graft-versus-host disease. Nat Rev Dis Primers 2023 ; 9 : 27. [Google Scholar]
- Degos L. Jean Dausset a scientific pioneer: intuition and creativity for the patients (1916-2009). Haematologica 2009 ; 94 : 1331–2. [Google Scholar]
- Jouet JP. La greffe de moelle osseuse, d’un siècle à l’autre. Med Sci (Paris) 2010 ; 26 : 447–8. [Google Scholar]
- Petersdorf EW. HLA structure and function in hematopoietic-cell transplantation. Best Pract Res Clin Haematol 2024 ; 37 : 101564. [Google Scholar]
- Aljurf M, Weisdorf D, Alfraih F, et al. Worldwide network for blood & marrow transplantation (WBMT) special article, challenges facing emerging alternate donor registries. Bone Marrow Transplant 2019 ; 54 : 1179–88. [Google Scholar]
- Scala S, Aiuti A. In vivo dynamics of human hematopoietic stem cells: novel concepts and future directions. Blood Adv 2019 ; 3 : 1916–24. [Google Scholar]
- Konturek-Ciesla A, Bryder D. Stem Cells, Hematopoiesis and lineage tracing: transplantation-centric views and beyond. Front Cell Dev Biol 2022 ; 10 : 903528. [Google Scholar]
- Calabria A, Spinozzi G, Cesana D, et al. Long-term lineage commitment in haematopoietic stem cell gene therapy. Nature 2024 ; 636 : 162–71. [Google Scholar]
- Spencer Chapman M, Wilk CM, Boettcher S, et al. Clonal dynamics after allogeneic haematopoietic cell transplantation. Nature 2024 ; 635 : 926–34. [Google Scholar]
- Wu C, Li B, Lu R, et al. Clonal tracking of rhesus macaque hematopoiesis highlights a distinct lineage origin for natural killer cells. Cell Stem Cell 2014 ; 14 : 486–99. [Google Scholar]
- Kim S, Kim N, Presson AP, et al. Dynamics of HSPC repopulation in nonhuman primates revealed by a decade-long clonal-tracking study. Cell Stem Cell 2014 ; 14 : 473–85. [Google Scholar]
- Koelle SJ, Espinoza DA, Wu C, et al. Quantitative stability of hematopoietic stem and progenitor cell clonal output in rhesus macaques receiving transplants. Blood 2017 ; 129 : 1448–57. [Google Scholar]
- Radtke S, Adair JE, Giese MA, et al. A distinct hematopoietic stem cell population for rapid multilineage engraftment in nonhuman primates. Sci Transl Med 2017 ; 9. [Google Scholar]
- Aiuti A, Biasco L, Scaramuzza S, et al. Lentiviral hematopoietic stem cell gene therapy in patients with Wiskott-Aldrich syndrome. Science 2013 ; 341 : 1233151. [Google Scholar]
- Hacein-Bey-Abina S, Pai SY, Gaspar HB, et al. A modified gamma-retrovirus vector for X-linked severe combined immunodeficiency. N Engl J Med 2014 ; 371 : 1407–17. [Google Scholar]
- Hacein-Bey Abina S, Gaspar HB, Blondeau J, et al. Outcomes following gene therapy in patients with severe Wiskott-Aldrich syndrome. JAMA 2015 ; 313 : 1550–63. [Google Scholar]
- Biasco L, Pellin D, Scala S, et al. In vivo tracking of human hematopoiesis reveals patterns of clonal dynamics during early and steady-state reconstitution phases. Cell Stem Cell 2016 ; 19 : 107–19. [Google Scholar]
- Scala S, Basso-Ricci L, Dionisio F, et al. Dynamics of genetically engineered hematopoietic stem and progenitor cells after autologous transplantation in humans. Nat Med 2018 ; 24 : 1683–90. [Google Scholar]
- De Ravin SS, Liu S, Sweeney CL, et al. Lentivector cryptic splicing mediates increase in CD34+ clones expressing truncated HMGA2 in human X-linked severe combined immunodeficiency. Nat Commun 2022 ; 13 : 3710. [Google Scholar]
- Biffi A, Montini E, Lorioli L, et al. Lentiviral hematopoietic stem cell gene therapy benefits metachromatic leukodystrophy. Science 2013 ; 341 : 1233158. [Google Scholar]
- Cavazzana M. Progrès de la thérapie génique dans les maladies génétiques du système hématopoïétique. Med Sci (Paris) 2022 ; 38 : 768–71. [Google Scholar]
- Chneiweiss H. 2023 : premiers succès et nouveaux enjeux de l’édition du génome en thérapeutique humaine. Med Sci (Paris) 2023 ; 39 : 589–90. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Sessa M, Lorioli L, Fumagalli F, et al. Lentiviral haemopoietic stem-cell gene therapy in early-onset metachromatic leukodystrophy: an ad-hoc analysis of a non-randomised, open-label, phase 1/2 trial. Lancet 2016 ; 388 : 476–87. [Google Scholar]
- Cartier N, Hacein-Bey-Abina S, Bartholomae CC, et al. Hematopoietic stem cell gene therapy with a lentiviral vector in X-linked adrenoleukodystrophy. Science 2009 ; 326 : 818–23. [Google Scholar]
- Fumagalli F, Calbi V, Natali Sora MG, et al. Lentiviral haematopoietic stem-cell gene therapy for early-onset metachromatic leukodystrophy: long-term results from a non-randomised, open-label, phase 1/2 trial and expanded access. Lancet 2022 ; 399 : 372–83. [Google Scholar]
- de Tocqueville S, Revy P. Sauvetage génétique somatique dans les maladies hématopoïétiques mendéliennes : du darwinisme cellulaire à la thérapie génique naturelle. Med Sci (Paris) 2025 ; 41 : 877–86. [Google Scholar]
- Mitchell E, Spencer Chapman M, Williams N, et al. Clonal dynamics of haematopoiesis across the human lifespan. Nature 2022 ; 606 : 343–50. [Google Scholar]
- Jaiswal S, Ebert BL. Clonal hematopoiesis in human aging and disease. Science 2019 ; 366. [Google Scholar]
- Oran B, Champlin RE, Wang F, et al. Donor clonal hematopoiesis increases risk of acute graft versus host disease after matched sibling transplantation. Leukemia 2022 ; 36 : 257–62. [Google Scholar]
- Gibson CJ, Kim HT, Zhao L, et al. Donor clonal hematopoiesis and recipient outcomes after transplantation. J Clin Oncol 2022 ; 40 : 189–201. [Google Scholar]
- Frick M, Chan W, Arends CM, et al. Role of donor clonal hematopoiesis in allogeneic hematopoietic stem-cell transplantation. J Clin Oncol 2019 ; 37 : 375–85. [Google Scholar]
- Oshima MU, Higgins J, Jenkins I, et al. Characterization of clonal dynamics using duplex sequencing in donor-recipient pairs decades after hematopoietic cell transplantation. Sci Transl Med 2024 ; 16 : eado5108. [Google Scholar]
La statistique bayésienne est une approche statistique fondée sur l’inférence bayésienne, dans laquelle la probabilité exprime un degré de croyance en un événement. Le degré initial de croyance peut être basé sur des connaissances a priori, comme les résultats d’expériences antérieures, ou sur des croyances personnelles concernant l’événement (ndlr).
Les progéniteurs hématopoïétiques représentent le stade ultime de différenciation des cellules-souches hématopoïétiques engagées de façon irréversible dans une lignée (ndlr).
Les sinusoïdes sont des capillaires, qui se trouvent dans les glandes surrénales, le foie, la rate et la moelle osseuse. Les artérioles sont de petits vaisseaux sanguins situées à la fin du réseau artériel, entre les artères et les capillaires (ndlr).
La myéloablation correspond à l’administration de chimiothérapies et/ou d’irradiations à haute intensité visant à éradiquer l’hématopoïèse médullaire endogène afin de permettre l’implantation de nouvelles cellules souches hématopoïétiques (ndlr).
L’accident nucléaire de Vinča s’est produit le 15 octobre 1958 à l’Institut Boris Kidrič des sciences nucléaires de Vinča en Serbie, lorsqu’une fuite de matières radioactives a eu lieu dans un réacteur nucléaire installé plusieurs mois plus tôt, le premier dans l’ex-Yougoslavie (ndlr).
Jean Dausset [1916-2009] a révolutionné le monde de l’immunologie avec sa découverte des molécules du « complexe majeur d’histocompatibilité », une contribution essentielle pour comprendre les règles de la compatibilité tissulaire entre les donneurs et les receveurs de greffe d’organes, et les mécanismes présidant au développement de la réponse immunitaire. Ses travaux lui ont permis de recevoir, en 1980, le prix Nobel de physiologie ou médecine qu’il partagea avec les Américains Baruj Benacerraf et George David Snell (ndlr).
L’aplasie médullaire est une défaillance de la moelle osseuse entraînant une diminution des cellules sanguines (globules rouges, globules blancs et/ou plaquettes), provoquant fatigue, infections et saignements, et regroupant des formes idiopathiques, toxiques ou constitutionnelles selon l’origine (ndlr).
Le terme « mobilisation » désigne le phénomène par lequel les CSPH quittent transitoirement le compartiment médullaire pour circuler dans le compartiment sanguin. Dans le cas de greffes de cellules sanguines, les CSPH médullaires sont recueillies chez le donneur, grâce à l’injection sous-cutanée pendant 4 à 5 jours d’un facteur de croissance hématopoïétique, le G-CSF (Granulocyte Colony-Stimulating Factor) qui mobilise les CSPH, les fait passer dans la circulation où elles sont recueillies par prélèvement sanguin.
Dans ce texte : une paire fait toujours référence à un ensemble « donneur-receveur ».
Le conditionnement pré-greffe correspond à l’administration de chimiothérapies et/ou d’irradiation à haute intensité visant à fortement supprimer l’hématopoïèse et le système immunitaire du receveur, afin de permettre l’implantation du greffon, de réduire la charge tumorale résiduelle et de prévenir le rejet immunologique. Un conditionnement peut être une myloablation mais une myéloablation n’est pas un conditionnement.
Les mutations driver sont des mutations somatiques acquises par les cellules souches hématopoïétiques qui confèrent un avantage sélectif, se traduisant par une augmentation de la prolifération et/ou une différenciation anormale des cellules concernées. Ces mutations sont responsables de l’expansion clonale des cellules souches hématopoïétiques et de leur descendance, un phénomène désigné sous le terme d’hématopoïèse clonale.
La coalescence désigne la réunion, normale ou pathologique, de tissus voisins. Il peut s’agir de deux organes végétaux différents comme un pétale et une étamine. Il peut aussi s’agir des deux lèvres d’une plaie simple en voie de cicatrisation (ndlr).
Liste des figures
 |
Figure 1 Suivi de l’hématopoïèse post-greffe. En haut : greffe de cellules autologues après correction génique par lentivirus et traçage des CSPH ingéniérées grâce aux sites d’insertion des vecteurs viraux. Trois maladies génétiques distinctes affectant l’hématopoïèse ont été ciblées : la leucodystrophie métachromatique, maladie métabolique neurodégénérative ; le syndrome de Wiskott-Aldrich, maladie récessive liée à l’X et la β-thalassémie, maladie génétique héréditaire qui affecte la production des chaines ß de l’hémoglobine. Cette étude révèle le rôle clé du microenvironnement pathologique pour biaiser la production hématopoïétique vers les lignages déficients dans la maladie. CSPH : cellules souches pluripotentes hématopoïétiques ; BTHAL : β-thalassémie ; WAS : syndrome de Wiskott-Aldrich ; MLD : leucodystrophie métachromatique. En bas : greffes allogéniques et suivi des CSPH greffées et résiduelles par l’analyse des mutations somatiques. La liste des mutations présentes dans les cellules hématopoïétiques du donneur est établie et sert de socle pour évaluer l’influence de la greffe sur l’accumulation de mutations post-greffe. Les profils mutationnels hématopoïétiques des donneurs et des receveurs sont suivis longitudinalement. L’influence de la greffe sur le profil mutationnel est établie ainsi que les dynamiques de reconstitution hématopoïétique post-greffe. La conclusion est que l’âge du donneur influence de façon majeure la dynamique de reconstitution hématopoïétique avec, dans le cas de donneurs âgés, une très forte réduction du nombre de CSH contribuant à l’hématopoïèse chez le receveur, accompagnée d’une accumulation plus importante de mutations par rapport aux cellules du donneur n’ayant pas subi de greffe. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




