| Issue |
Med Sci (Paris)
Volume 42, Number 3, Mars 2026
|
|
|---|---|---|
| Page(s) | 254 - 257 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026032 | |
| Published online | 20 March 2026 | |
Recâblage métabolique des cellules dendritiques pour dynamiser l’immunité antitumorale
Metabolic rewiring of dendritic cells to re-invigorate antitumor immunity
1
Institut pour l’avancée des biosciences, Équipe « Immunologie translationnelle et immunothérapie dans les maladies chroniques », Inserm U1209, CNRS UMR5309, Université Grenoble Alpes, Grenoble, France
2
Établissement français du sang Auvergne-Rhône-Alpes, Laboratoire de recherche et développement, Grenoble, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
La subversion du système immunitaire par les tumeurs cancéreuses conditionne leur développement. Malgré les innovations thérapeutiques, en particulier dans le domaine de l’immunothérapie, le contrôle de ces tumeurs à long terme reste un défi médical. Il importe donc de comprendre les mécanismes de la subversion pour concevoir de nouveaux traitements anticancéreux et accroître l’efficacité des thérapies existantes.
Subversion des cellules dendritiques par le mélanome
Les cellules dendritiques jouent un rôle crucial dans l’induction des réponses immunitaires antitumorales. Elles se répartissent en différents sous-types de cellules aux fonctions complémentaires [1]. Alors que les cellules dendritiques conventionnelles de type 1 (cDC1), BDCA3+, excellent dans la présentation des antigènes tumoraux aux lymphocytes T CD8+, les cellules dendritiques conventionnelles de type 2 (cDC2), BDCA1+, activent les lymphocytes T CD4+ et induisent des réponses Th1/Th17. Quant aux cellules dendritiques plasmocytoïdes (pDC), BDCA2/4+, elles participent au recrutement des lymphocytes T cytotoxiques et des lymphocytes natural killers (NK), exercent une cytotoxicité directe sur les cellules tumorales, et potentialisent la fonction d’autres cellules de l’immunité. La reconnaissance des motifs moléculaires associés aux microorganismes pathogènes ou aux dommages cellulaires par les récepteurs de type Toll déclenche la production d’interleukine-12, d’interférons de type I (α, β) ou III (λ1) par les cDC2, pDC et cDC1 respectivement, ainsi que la sécrétion de chimiokines qui attirent et activent les cellules effectrices, favorisant ainsi les réponses antitumorales. Outre les lymphocytes T conventionnels, les lymphocytes T γδ et les lymphocytes NK sont cruciaux pour la surveillance immunitaire des cancers grâce à leur puissante capacité cytolytique envers les cellules tumorales et à la sécrétion de cytokines qui potentialisent d’autres cellules immunitaires. Cependant, le cancer échappe fréquemment au contrôle immunitaire en détournant le fonctionnement des cellules dendritiques. Dans le contexte du mélanome, nous avons montré précédemment que les cDC1 restent fonctionnelles et sont associées à une évolution favorable, alors que les cDC2 et pDC présentent des dysfonctionnements et un dialogue perturbé avec les cellules effectrices antitumorales, conduisant à des réponses protumorales et à une évolution défavorable [2].
Les mécanismes de cette subversion des cellules dendritiques par la tumeur ne sont que partiellement élucidés. Ils incluent la sécrétion de facteurs immunosuppresseurs et des molécules immunomodulatrices, ainsi que l’exposition de glycans anormaux par les cellules tumorales, ou l’induction d’un stress métabolique interférant avec la différenciation, la maturation et le fonctionnement des cellules dendritiques [2]. En outre, les cellules tumorales ont une glycosylation atypique de leurs protéines et lipides de surface, notamment un plus grand nombre de N-glycans branchés et d’acides sialiques, et une modulation de la fucosylation. Ces glycosylations aberrantes, qui ensemble constituent un glycocode, peuvent être détectées par les récepteurs de type lectine, tels que les lectines de type C (C-type lectin receptors, CLR) ou les SIGLEC (sialic acid-binding immunoglobulin-like lectins), présents à la surface des cellules immunitaires. Les interactions entre glycans et lectines sont cruciales pour façonner l’immunité antitumorale, mais elles sont exploitées par la tumeur pour déclencher l’évasion immunitaire [3, 4]. Nous avons montré précédemment que les cellules tumorales du mélanome ont un glycocode aberrant, dont les motifs sialylés et fucosylés induisent, via les récepteurs lectine de type C, un dysfonctionnement des cellules dendritiques en influant sur leur expression de marqueurs d’activation et de points de contrôle immunitaires, et en remodelant leur profil de sécrétion de cytokines et chimiokines [5].
Contrôle métabolique du fonctionnement des cellules immunitaires
L’immunométabolisme apparaît essentiel dans le contrôle du fonctionnement des cellules immunitaires dans le cancer [6, 7]. Pour produire l’ATP nécessaire à leur fonctionnement, ces cellules utilisent deux voies principales, la phosphorylation oxydante mitochondriale (OXPHOS) et la glycolyse aérobie, principalement régies par les voies de signalisation AMPK (AMP-activated protein kinase) et mTOR (mammalian target of rapamycin), respectivement. Lors de leur activation, les cellules immunitaires subissent une « déviation métabolique » de la voie OXPHOS vers la glycolyse aérobie pour répondre aux besoins bioénergétiques nécessaires à leur prolifération et à leurs fonctions effectrices. Les transporteurs de solutés (solute carriers, SLC) assurent une absorption efficace des nutriments pendant ce changement métabolique, notamment le transporteur du glucose SLC2A1/GLUT1, le transporteur de la glutamine SLC38A1/2, SLC7A5 pour l’importation de méthionine, et les transporteurs de monocarboxylates, qui assurent le mouvement bidirectionnel du lactate et des acides cétoniques.
La flexibilité métabolique des cellules dendritiques orchestre leur activation et leur fonctionnement [8], et son ajustement par le microenvironnement favorise l’émergence de cellules dendritiques inflammatoires ou tolérogènes, et stimule subséquemment l’immunité ou la tolérance. De même, les différents stades de différenciation des lymphocytes T sont sous-tendus par des programmes métaboliques divergents : les lymphocytes T effecteurs activés augmentent rapidement leur glycolyse et le métabolisme de la glutamine afin de produire l’énergie nécessaire à leur fonctionnement, alors que les lymphocytes T mémoires centraux augmentent leur capacité respiratoire mitochondriale (OXPHOS) pour se maintenir à long terme, et que les lymphocytes T régulateurs utilisent principalement l’oxydation des acides gras pour fonctionner dans le microenvironnement tumoral.
Reprogrammation métabolique des cellules immunitaires dans le cancer
Pour soutenir leur prolifération active, les cellules tumorales opèrent elles aussi un changement métabolique caractérisé par une augmentation de leur consommation du glucose et des acides aminés. Même en présence d‘oxygène, le pyruvate issu de la glycolyse n’est pas utilisé pour alimenter la voie OXPHOS, mais il est converti en lactate par la lactate déshydrogénase, puis exporté par les transporteurs de monocarboxylates (effet Warburg). Cela crée un environnement métabolique hostile pour les cellules immunitaires infiltrantes, avec une compétition pour les nutriments, une acidification, une hypoxie et l’accumulation de métabolites toxiques dans le microenvironnement tumoral. Ce stress métabolique soutient le métabolisme des cellules immunitaires protumorales (lymphocytes T régulateurs, cellules myéloïdes suppressives) et interfère avec le recrutement, la maturation et le fonctionnement des cellules dendritiques, altérant les réponses immunitaires et favorisant l’échappement de la tumeur à la surveillance immunitaire [6–8].
Pour mieux comprendre les mécanismes de la subversion du système immunitaire par le mélanome, nous avons exploré les caractéristiques métaboliques des sous-types de cellules dendritiques (cDC1, cDC2, pDC) dans le mélanome en utilisant la méthode SCE-NITH (single-cell energetic metabolism by profiling translation inhibition) [9, 10]. Cette méthode est fondée sur la mesure de la synthèse protéique, à l’échelle d’une seule cellule, par cytométrie en flux à l’aide de la puromycine, une molécule qui inhibe la traduction des ARN messagers, mais dont l’incorporation dans la chaîne polypeptidique en cours d’élongation permet de quantifier la synthèse protéique. SCENITH révèle l’activité métabolique globale des cellules, et permet aussi de définir leur profil métabolique (capacités et dépendances glycolytique et mitochondriale) en évaluant les changements de la synthèse protéique sous l’action d’inhibiteurs spécifiques des voies de la glycolyse et OXPHOS, en combinaison avec leurs propriétés phénotypiques et fonctionnelles. Nous avons ainsi identifié des profils métaboliques distincts selon les sous-types de cellules dendritiques, indiquant que les programmes métaboliques façonnent la spécialisation immunitaire. Cette analyse a aussi révélé des perturbations métaboliques majeures des cellules dendritiques circulant dans le sang et infiltrant la tumeur, en lien avec leur état d’activation, leur profil d’expression des protéines correspondant aux points de contrôle immunitaire, et leur polarisation fonctionnelle. Ces perturbations métaboliques sont corrélées avec des altérations phénotypiques et des dysfonctionnements concernant l’activation et la polarisation des lymphocytes T naïfs, et elles affectent l’évolution du cancer chez les patients. Les cellules tumorales, par le biais de motifs glycans sialylés et fucosylés à la surface cellulaire, remodèlent le métabolisme et le fonctionnement des cellules dendritiques. Nous avons montré que la modulation expérimentale du métabolisme de ces cellules, en particulier des voies dépendantes de mTOR/AMPK, ou l’inhibition du transporteur de lactate MCT1, préserve les cellules dendritiques de l’influence négative des glycans tumoraux sur la reprogrammation métabolique, tout en rétablissant leurs fonctions et en restaurant l’orientation antitumorale des lymphocytes T (Figure 1) [9].
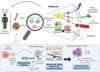 |
Figure 1 Le blocage du transporteur de lactate MCT1 stimule l’immunité antitumorale grâce au recâblage métabolique des cellules dendritiques dans le mélanome. En haut : Les cellules dendritiques jouent un rôle crucial dans le développement de l’immunité antitumorale, mais le cancer échappe au contrôle immunitaire en détournant leur fonctionnement. Afin de mieux comprendre les mécanismes de cette subversion, nous avons 1) exploré les dérèglements potentiels du profil métabolique des sous-types de cellules dendritiques (cDC2, cDC1, pDC) circulant dans le sang et infiltrant la tumeur des patients atteints de mélanome, 2) évalué le lien entre profils métaboliques et caractéristiques des cellules (état d’activation, expression des points de contrôle immunitaire, fonctionnalité, sécrétome), 3) recherché si les cellules tumorales ou les glycans dérivés de tumeurs peuvent moduler directement le métabolisme des cellules immunitaires, et 4) étudié le potentiel de réversion de la subversion des cellules immunitaires induite par la tumeur en agissant sur les voies métaboliques. Cette étude a révélé des perturbations métaboliques majeures des cellules dendritiques circulantes et infiltrant la tumeur, et mis en évidence les liens entre le profil métabolique de ces cellules et leurs caractéristiques phénotypiques (état d’activation, profil d’expression des points de contrôle immunitaire) et fonctionnelles (sécrétion de cytokines), qui influent sur l’évolution du cancer. En bas (encadré bleuté) : Les cellules tumorales, qui exposent à leur surface un glycocode aberrant, remodèlent directement le métabolisme et le fonctionnement des cellules dendritiques par le biais de motifs glycans sialylés et fucosylés. La modulation expérimentale des voies métaboliques, en particulier l’inhibition du transporteur de lactate MCT1 (par la molécule BAY-8002), permet de protéger les cellules dendritiques de l’influence négative des glycans tumoraux, tout en rétablissant leurs fonctions et leur capacité à activer une réponse antitumorale des lymphocytes T appropriée. Ces résultats éclairent le lien entre métabolisme, glycocode tumoral et évasion immunitaire dans le mélanome. Ils ouvrent la voie à une exploitation thérapeutique de la flexibilité métabolique des cellules immunitaires afin de les préserver de la subversion par les tumeurs et de restaurer des réponses antitumorales efficaces. OXPHOS : phosphorylation oxydante mitochondriale. |
Perspectives
La découverte que le mélanome manipule le métabolisme énergétique des cellules dendritiques de façon dépendante des glycans tumoraux afin de détourner leur fonctionnement et d’échapper à la surveillance immunitaire ouvre des perspectives de reprogrammation des voies métaboliques de ces cellules pour tenter de prévenir leur subversion et restaurer leur fonctionnalité. Plus généralement, la mise en évidence, pour le mélanome, de ce lien entre glycocode des cellules tumorales, reprogrammation métabolique des cellules dendritiques, et évasion immunitaire ouvre la voie à des stratégies thérapeutiques innovantes fondées sur la reprogrammation métabolique des cellules de l’immunité pour empêcher leur subversion par les tumeurs et restaurer des réponses immunitaires antitumorales efficaces [11, 12].
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article
Références
- Kvedaraite E, Ginhoux F. Human dendritic cells in cancer. Sci Immunol 2022 ; 7 : eabm9409. [CrossRef] [PubMed] [Google Scholar]
- Sosa Cuevas E, Saas P, Aspord C. Dendritic cell subsets in melanoma: Pathophysiology, clinical prognosis and therapeutic exploitation. Cancers 2023 ; 15 : 2206. [Google Scholar]
- Rodriguez E, Schetters STT, van Kooyk Y. The tumour glyco-code as a novel immune checkpoint for immunotherapy. Nat Rev Immunol 2018 ; 18 : 204–11. [Google Scholar]
- Niveau C, Sosa Cuevas E, Saas P, Aspord C. Glycans in melanoma: Drivers of tumour progression but sweet targets to exploit for immunotherapy. Immunology 2024 ; 173 : 33–52. [Google Scholar]
- Sosa Cuevas E, Roubinet B, Mouret S, et al. The melanoma tumor glyco-code impacts human dendritic cells’ functionality and dictates clinical outcomes. Front Immunol 2023 ; 14 : 1120434. [Google Scholar]
- Ricci JE. Tumor-induced metabolic immunosuppression: Mechanisms and therapeutic targets. Cell Reports 2025 ; 44 : 115206. [Google Scholar]
- Leone RD, Powell JD. Metabolism of immune cells in cancer. Nat Rev Cancer 2020 ; 20 : 516–31. [Google Scholar]
- Giovanelli P, Sandoval TA, Cubillos-Ruiz JR. Dendritic cell metabolism and function in tumors. Trends Immunol 2019 ; 40 : 699–718. [CrossRef] [PubMed] [Google Scholar]
- Niveau C, Cettour-Cave M, Mouret S, et al. MCT1 lactate transporter blockade re-invigorates anti-tumor immunity through metabolic rewiring of dendritic cells in melanoma. Nat Commun 2025 ; 16 : 1083. [Google Scholar]
- Arguello RJ, Combes AJ, Char R, et al. SCENITH: A flow cytometry-based method to functionally profile energy metabolism with single-cell resolution. Cell Metab 2020 ; 32 : 1063–75 e7. [Google Scholar]
- O’Sullivan D, Sanin DE, Pearce EJ, Pearce EL. Metabolic interventions in the immune response to cancer. Nat Rev Immunol 2019 ; 19 : 324–35. [Google Scholar]
- Shevchenko I, Bazhin AV. Metabolic checkpoints: Novel avenues for immunotherapy of cancer. Front Immunol 2018 ; 9 : 1816. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1 Le blocage du transporteur de lactate MCT1 stimule l’immunité antitumorale grâce au recâblage métabolique des cellules dendritiques dans le mélanome. En haut : Les cellules dendritiques jouent un rôle crucial dans le développement de l’immunité antitumorale, mais le cancer échappe au contrôle immunitaire en détournant leur fonctionnement. Afin de mieux comprendre les mécanismes de cette subversion, nous avons 1) exploré les dérèglements potentiels du profil métabolique des sous-types de cellules dendritiques (cDC2, cDC1, pDC) circulant dans le sang et infiltrant la tumeur des patients atteints de mélanome, 2) évalué le lien entre profils métaboliques et caractéristiques des cellules (état d’activation, expression des points de contrôle immunitaire, fonctionnalité, sécrétome), 3) recherché si les cellules tumorales ou les glycans dérivés de tumeurs peuvent moduler directement le métabolisme des cellules immunitaires, et 4) étudié le potentiel de réversion de la subversion des cellules immunitaires induite par la tumeur en agissant sur les voies métaboliques. Cette étude a révélé des perturbations métaboliques majeures des cellules dendritiques circulantes et infiltrant la tumeur, et mis en évidence les liens entre le profil métabolique de ces cellules et leurs caractéristiques phénotypiques (état d’activation, profil d’expression des points de contrôle immunitaire) et fonctionnelles (sécrétion de cytokines), qui influent sur l’évolution du cancer. En bas (encadré bleuté) : Les cellules tumorales, qui exposent à leur surface un glycocode aberrant, remodèlent directement le métabolisme et le fonctionnement des cellules dendritiques par le biais de motifs glycans sialylés et fucosylés. La modulation expérimentale des voies métaboliques, en particulier l’inhibition du transporteur de lactate MCT1 (par la molécule BAY-8002), permet de protéger les cellules dendritiques de l’influence négative des glycans tumoraux, tout en rétablissant leurs fonctions et leur capacité à activer une réponse antitumorale des lymphocytes T appropriée. Ces résultats éclairent le lien entre métabolisme, glycocode tumoral et évasion immunitaire dans le mélanome. Ils ouvrent la voie à une exploitation thérapeutique de la flexibilité métabolique des cellules immunitaires afin de les préserver de la subversion par les tumeurs et de restaurer des réponses antitumorales efficaces. OXPHOS : phosphorylation oxydante mitochondriale. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




