| Issue |
Med Sci (Paris)
Volume 31, Number 3, Mars 2015
|
|
|---|---|---|
| Page(s) | 275 - 281 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/20153103013 | |
| Published online | 8 avril 2015 | |
Le récepteur de l’apeline
Une voie originale dans la stratégie antidiabétique
The APJ receptor: a new therapeutic approach in diabetic treatment
Institut des maladies métaboliques et cardiovasculaires, Inserm U1048, université Paul Sabatier, 1, avenue Jean Poulhès, 31432
Toulouse Cedex 4, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Le gène codant pour le récepteur de l’apeline (APJ) a été cloné dès 1993, et son ligand identifié en 1998. L’expression du récepteur APJ au niveau du système nerveux central, notamment dans l’hypothalamus, ainsi que dans divers tissus (cœur, vaisseaux, estomac, etc.), en fait une cible pharmacologique de choix. En effet, les recherches sur APJ ont permis le développement de molécules essentiellement peptidiques permettant d’activer et/ou de bloquer le récepteur et, plus récemment, de découvrir un autre ligand endogène : apela. Parmi les fonctions régulées par le système APJ/apeline, le contrôle du métabolisme énergétique apparaît aujourd’hui au tout premier plan. Une meilleure connaissance de la pharmacologie du récepteur APJ devrait donc permettre d’envisager une approche thérapeutique innovante dans la lutte contre les maladies métaboliques.
Abstract
The APJ receptor cloned in 1993 found its ligand in 1998 with the discovery of apelin. The presence of APJ in the central nervous system (more particularly in the hypothalamus) and in various tissues (heart, blood vessels, stomach, etc.) makes it a potential pharmacological target. Interest in APJ has allowed the development of peptidic molecules able to stimulate and/or inhibit the receptor and, more recently, to discover another endogenous ligand: apela. Among the functions regulated by the APJ/apelin system, the control of energy metabolism appears today in the forefront. A better understanding of the pharmacology of APJ receptor should allow innovative therapeutic approaches in the treatment of metabolic diseases.
© 2015 médecine/sciences – Inserm
Le récepteur APJ : un récepteur aux multiples voies d’activation
Le gène codant le récepteur de l’apeline a été cloné en 1993 [1]. Ce récepteur, nommé APJ ou AGTRL1 (angiotensin receptor-like 1), appartient à la famille des récepteurs à sept domaines transmembranaires ou récepteurs couplés aux protéines G (RCPG) de la classe A1. Il présente une forte homologie de séquence (31 % de la séquence totale en acides aminés [aa] et 54 % dans les domaines transmembranaires) avec le récepteur de type 1 de l’angiotensine II (AT1a), sans pour autant lier l’angiotensine II. Le récepteur de l’apeline est resté orphelin jusqu’en 1998, année de la découverte de son ligand endogène nommé apeline (APJ endogenous ligand) [2]. Le gène apeline code pour une préproprotéine de 77 aa contenant un peptide signal en position amino-terminale, qui adresse le propeptide au compartiment sécrétoire, et une partie carboxy-terminale conservée entre les espèces. Ce propeptide génèrerait - par clivage protéolytique au niveau de doublets basiques - différents fragments d’apeline. Trois formes d’apeline ont principalement été caractérisées : l’apeline 36, l’apeline 17 et l’apeline 13 (Figure 1). Cette dernière forme représente l’entité minimale physiologiquement active et peut générer, par la présence d’un glutamate en position amino-terminale, une forme plus stable, l’apeline 13 pyroglutaminée.
 |
Figure 1. Les différents ligands d’APJ. A. L’apeline : après clivage du peptide signal, la pro-apeline entre dans la voie sécrétoire. La pro-apeline peut générer, après clivage, différentes formes actives d’apeline. B. Apela (aussi nommée elabela ou toddler) : comme pour l’apeline, apela possède des sites potentiels de clivage et pourrait générer différentes formes d’apela. Les séquences présentées sont les séquences murines d’apeline et d’apela. |
L’apeline et son récepteur sont exprimés dans différents tissus périphériques ainsi que dans différentes régions du cerveau et, en particulier, l’hypothalamus. Cette voie de signalisation joue un rôle physiologique majeur au niveau du système cardiovasculaire, sur le métabolisme énergétique et le contrôle de l’équilibre hydrique [3, 4].
Voies de signalisation en aval d’APJ
La voie de signalisation canonique stimulée par l’apeline implique l’activation des protéines G sensibles à la toxine pertussique, Gi/o, ce qui a pour effet une diminution du taux d’AMP cyclique (AMPc) cytoplasmique [5, 6]. Cependant, dans certains types cellulaires, APJ peut être aussi couplé aux protéines Gq [7, 8]. En aval des protéines G stimulées, l’apeline active des cascades de transduction diverses. En effet, que ce soit dans des systèmes hétérologues, des cellules endothéliales ou musculaires, des neurones, des cellules tumorales ou des ostéoblastes, l’apeline stimule la voie PI3K (phosphoinositide 3-kinase)/Akt (protéine kinase B) et/ou la voie MAPK (mitogen-activated protein kinase) [9]. De plus, APJ peut activer, de manière dépendante de la protéine G, à la fois la protéine kinase C (PKC) et la phospholipase C (PLC) [5, 7]. La stimulation de ces effecteurs clés va permettre ainsi la survie, la prolifération et/ou la migration de ces différents types cellulaires. Un autre effecteur intracellulaire plus récemment décrit comme étant activé par l’apeline dans les cellules musculaires, les adipocytes et les entérocytes est l’AMPK (AMP kinase). La stimulation de cette dernière par l’apeline induit différents effets métaboliques (inhibition de la lipolyse, transport de glucose, oxydation des lipides, etc.) [8, 10–14].
L’apeline permet le recrutement des β-arrestines cytoplasmiques au niveau du récepteur APJ, et une désensibilisation et internalisation de ce dernier [15] (Figure 2), comme c’est le cas pour la majorité des récepteurs couplés aux protéines G. Cependant, le devenir du récepteur à l’intérieur de la cellule diffère selon la forme d’apeline qui l’active. En effet, les travaux de Zhou et al. ont mis en évidence que l’apeline 13 engendre une internalisation suivie d’un recyclage du récepteur à la membrane, alors que dans le cas de l’apeline 36, APJ reste internalisé [16].
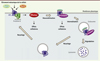 |
Figure 2. APJ, un récepteur aux multiples voies d’activation. L’activation d’APJ par l’apeline A, l’apela, ou un étirement mécanique de la cellule, engendre l’activation de différentes voies de signalisation (protéines G et recrutement des β-arrestines), conduisant aux différents effets cellulaires. Le récepteur est alors internalisé, puis recyclé à la membrane ou dégradé. |
En plus de leur fonction dans la désensibilisation et l’internalisation des RCPG, les β-arrestines ont une fonction de protéines d’échafaudage, permettant ainsi l’activation de différentes cascades de transduction en aval du récepteur, et ce de manière indépendante des protéines G. À ce jour, aucune étude n’a mis en évidence l’activation d’une voie de signalisation induite par l’apeline et dépendante des β-arrestines. Cependant, Scimia et al. ont montré chez la souris que le récepteur de l’apeline est impliqué dans l’hypertrophie cardiaque. De manière surprenante, cette activation d’APJ est indépendante de l’apeline, mais induite en réponse à l’étirement mécanique de la cellule myocardique via une signalisation dépendante des β-arrestines [17]. Ainsi, l’hypertrophie cardiaque est absente chez des souris déficientes en récepteur de l’apeline (souris APJ-/-), et réduite si les animaux sauvages sont traités avec de l’apeline qui active la voie Gi.
Depuis plusieurs années, différentes approches réalisées sur des cellules, tissus et animaux ont mis en évidence que les RCPG sont capables de former des homo- et/ou des hétérodimères, modifiant ainsi les propriétés de chacun des protomères [39]. Différents travaux récents, réalisés in vitro, ont mis en évidence que le récepteur de l’apeline peut former un hétérodimère avec différents récepteurs comme, par exemple, le récepteur de l’angiotensine [18–20]. Ces études divergent sur l’origine de l’hétérodimérisation (constitutive ou induite par l’apeline ou l’angiotensine II). Cependant, elles mettent en évidence que la signalisation apeline diminue l’affinité de l’angiotensine II pour son récepteur et modifie les voies de signalisation activées par l’angiotensine II [18–20]. Si la pertinence de cette hétérodimérisation est confirmée in vivo, il sera intéressant, d’un point de vue pharmacologique et clinique, de rechercher des molécules ciblant APJ ou AT1 présents sous la forme d’hétérodimères uniquement [39].
L’apeline et l’étirement mécanique de la cellule ne sont pas les seuls médiateurs de l’activation d’APJ. En effet, deux articles publiés très récemment ont identifié un nouveau ligand endogène d’APJ. Ce nouveau ligand, appelé elabela, toddler ou encore apela, est une préprotéine contenant dans sa partie amino-terminale un peptide signal permettant l’adressage au compartiment sécrétoire [21, 22] (Figure 1). Ce nouveau ligand d’APJ, dont la présence et la fonction ont été étudiées uniquement durant le développement embryonnaire, joue un rôle fondamental dans la migration des cellules mésendodermiques et est essentiel à la morphogenèse cardiaque. La perte d’expression d’elabela est létale chez le poisson zèbre et « phénocopie » la perte d’expression d’APJ. Il sera intéressant de savoir si ce nouveau ligand d’APJ est aussi exprimé chez l’adulte et, dans ce cas, de caractériser ses sites d’expression et sa fonction.
Agonistes ou antagonistes spécifiques d’APJ
La signalisation apeline joue un rôle important dans le système cardiovasculaire, le métabolisme énergétique, et l’angiogenèse physiologique et tumorale. Cependant, peu de molécules agissant comme agonistes ou antagonistes spécifiques d’APJ ont été décrites à ce jour.
Un des premiers antagonistes identifié ciblant APJ est l’apeline F13A [15]. Ce peptide a la même séquence que l’apeline 13, à l’exception de la substitution de la phénylalanine en position carboxy-terminale par une alanine. Cependant, cette activité antagoniste nécessite d’être caractérisée plus en détails, car différents travaux publiés mettent en évidence une activité agoniste de l’apeline F13A. Par criblage haut débit, Khan et al. ont identifié la molécule ML221, un antagoniste non peptidique d’APJ bloquant la voie Gi et le recrutement de β-arrestines [23]. Une approche de ligand bivalent a permis l’identification d’un antagoniste compétitif cyclique d’APJ, le C-14-C, ayant une demi-vie plus longue et une plus forte résistance à la dégradation [24]. Enfin, un antagoniste peptidique du récepteur CXCR4 (C-X-C chemokine receptor type 4), ALX40-4C, connu pour sa forte affinité et son activitié sur ce récepteur, reconnaît également APJ et inhibe, mais avec une efficacité moindre, la liaison d’apeline à son récepteur [16].
Le premier agoniste non peptidique identifié est le E339-3D6. Ce composé se comporte différemment selon le type de réponse cellulaire étudiée : il est agoniste partiel pour l’inhibition de l’adénylyl cyclase (i.e. l’inhibition de l’enzyme est incomplète, elle n’atteint pas 100 %) et agoniste complet pour l’internalisation d’APJ (l’internalisation atteint, elle, 100 %) [25]. L’identification de molécules stables et spécifiques de l’APJ est indispensable, afin de mieux caractériser la fonction physiologique et physiopathologique de la signalisation apeline, et pourrait représenter un intérêt pharmacologique et thérapeutique non négligeable.
Effets de l’apeline sur le métabolisme énergétique en conditions physiologiques
L’étroite relation entre apeline et insuline mise en évidence dès 2005 dans l’adipocyte par Boucher et al. a conduit différentes équipes à rechercher le rôle du couple apeline/APJ dans le métabolisme énergétique [26]. La présence d’APJ dans les cellules β d’îlots pancréatiques isolés murins et humains a ainsi été mise en évidence. Des études sur ces mêmes îlots pancréatiques ont montré que l’apeline, en fonction de la dose utilisée, est capable d’augmenter ou de diminuer la sécrétion d’insuline en réponse à une augmentation des taux circulants de glucose [27, 28]. La présence du récepteur APJ sur les cellules musculaires striées squelettiques et les adipocytes a conduit différentes équipes à étudier les rôles potentiels de l’apeline sur le métabolisme énergétique. Une injection d’apeline 13 à des concentrations physiologiques entraîne rapidement une diminution de la glycémie basale ou stimulée par une charge orale de glucose chez la souris. Lors d’un clamp euglycémique hyperinsulinémique2, la perfusion d’apeline améliore nettement l’utilisation globale de glucose en ciblant spécifiquement les tissus musculaires squelettiques et adipeux [10]. Lorsqu’elle agit au niveau du système nerveux central, l’apeline entraîne aussi une diminution la glycémie chez des souris nourries, et ce par une voie dépendante du NO (oxyde nitrique) [29]. Le rôle de l’apeline dans l’homéostasie glucidique a été également confirmé par le phénotype des souris déficientes pour l’apeline (souris knock-out), dont la perte de la sensibilité à l’insuline est exacerbée lorsqu’elles sont soumises à un régime riche en graisses et en sucrose [30]. De plus, ces souris présentent une adiposité abdominale et des taux circulants d’acides gras plus importants que les souris contrôles. Chez ces animaux déficients en apeline, la perfusion d’apeline exogène pendant deux semaines réduit l’adiposité et les concentrations d’acides gras, mais aussi de glycérol, suggérant un rôle de l’apeline dans la régulation de la lipolyse. L’apeline inhibe en effet la lipolyse induite par l’isoprénaline (agoniste β-adrénergique) sur des adipocytes isolés de tissu adipeux et de la lignée adipocytaire 3T3-L1 [8, 14]. Cependant, cette inhibition de la lipolyse ne semble pas être associée à des modifications de la masse grasse, puisque celle-ci est diminuée3. Les effets métaboliques du système apeline/APJ ont permis d’envisager de nouvelles cibles tissulaires activant le transport de glucose. Le traitement de souris et de cardiomyocytes (lignée H9C2) par de l’apeline entraîne une augmentation de la translocation de GLUT4 (glucose transporter 4) à la membrane, associée à une potentialisation du transport de glucose dans ces cellules cardiaques [31]. Au niveau intestinal, la présence du récepteur APJ au pôle apical des entérocytes permet de modifier les capacités d’absorption du glucose [13]. En réponse à un bolus de glucose, l’apeline est sécrétée dans la lumière intestinale par les entérocytes et permet le transport transépithélial de glucose, en augmentant la transcription et la translocation des transporteurs SGLT-1 (sodium glucose cotransporter-1) et GLUT2 (glucose transporter 2).
Effet de l’apeline sur le métabolisme énergétique en conditions d’obésité et de diabète
Les souris soumises à un régime riche en graisses pendant plusieurs semaines deviennent obèses, hyperglycémiques, hyperinsulinémiques et résistantes à l’action de l’insuline. Une injection intraveineuse d’apeline chez ces souris améliore la tolérance au glucose, et la perfusion d’apeline au cours d’un clamp euglycémique-hyperinsulinémique augmente la sensibilité à l’insuline [10]. Ainsi, l’efficacité de l’apeline exogène perdure chez les souris obèses et résistantes à l’insuline, malgré des concentrations plasmatiques élevées en apeline endogène. Cependant, une altération du métabolisme énergétique est aussi observée, notamment au niveau hépatique, lorsque les concentrations hypothalamiques d’apeline deviennent trop élevées [32].
Au cours d’un traitement chronique de ces souris par l’apeline, on observe une nette amélioration de la sensibilité à l’insuline et une diminution de la masse grasse [12]. Cette meilleure sensibilité à l’insuline, bien que globale à l’échelle de l’organisme, est très marquée au niveau du muscle. En effet, chez des souris obèses et résistantes à l’insuline traitées par l’apeline, l’oxydation complète des acides gras est augmentée. De plus, les taux d’acylcarnitines à longue chaîne, générés lors d’une oxydation incomplète et associés à la résistance à l’insuline, sont diminués dans les muscles de ces souris4. Ceci pourrait expliquer que le transport du glucose stimulé par l’insuline soit significativement augmenté dans les muscles des souris traitées par l’apeline [12]. Cette meilleure utilisation des lipides dans le muscle s’accompagne également d’une augmentation des capacités oxydatives mitochondriales, ainsi que de la densité des mitochondries [12].
Des résultats similaires ont été obtenus chez des souris transgéniques surexprimant l’apeline (Tg-apeline) [33]. Ces souris, soumises à un régime hyperlipidique sans que la prise alimentaire soit augmentée, ne prennent pas de poids et leur consommation d’oxygène est plus élevée. La biogenèse mitochondriale est également augmentée dans les muscles squelettiques de ces souris [33]. De façon intéressante, la résistance à l’obésité des souris Tg-apeline est corrélée à une augmentation de la formation des vaisseaux dans le muscle squelettique, en raison d’une augmentation de l’angiopoïétine-15 et de son récepteur. L’importance de l’intégrité des vaisseaux, à la fois sanguins et lymphatiques, a été récemment démontrée dans l’effet « anti-obésogène » de l’apeline [34]. En effet, les souris déficientes en apeline se caractérisent, outre par une augmentation de l’adiposité, par une perméabilité vasculaire plus importante au niveau du tissu adipeux, qui permettrait une entrée accrue d’acides gras. De plus, les fonctions vasculaires de ces souris soumises à un régime gras et traitées par un inhibiteur de la cyclooxygénase-2 (anti-inflammatoire) sont améliorées, ce qui conduirait à une diminution de la masse grasse [34]. Cette étude souligne l’importance de l’apeline qui, en bloquant l’augmentation de la perméabilité vasculaire aux acides gras, empêcherait le développement de l’obésité.
Régulation de l’expression d’APJ au cours de l’obésité et des maladies métaboliques
Dans les conditions physiologiques, APJ est présent aussi bien chez l’homme que chez la souris dans les tissus ayant une forte activité métabolique, comme les muscles et le tissu adipeux, mais pas dans le foie. En revanche, la présence et la régulation d’APJ dans les lignées établies adipocytaires et musculaires murines ou humaines sont moins claires. En cas d’obésité, l’expression d’APJ, comme celle de l’apeline, sont augmentées dans le tissu adipeux, et cette augmentation est étroitement liée aux concentrations plasmatiques d’insuline [26]. Toutefois, cette régulation par l’insuline peut être différente selon la gravité de la résistance à l’insuline. Au cours de la transition jeûne/réalimentation ou à l’état nourri, l’expression génique d’APJ est significativement augmentée dans le tissu adipeux de souris en régime gras, mais pas dans celui de souris db/db (un modèle de souris obèses et diabétiques dû à une mutation du récepteur à la leptine). Dans le muscle, l’expression génique d’APJ n’est pas modifiée au cours de cette transition, et elle diminue de façon très importante dans le muscle de souris db/db [35]. Ainsi, la régulation de l’expression d’APJ est différente dans le tissu adipeux et le muscle. Cette différence de régulation existe également chez des souris dont le régime hyperlipidique a été supplémenté (ou pas) avec un acide gras polyinsaturé : l’Epa (l’acide eicosapentaénoïque). En effet, l’EPA, associé au régime hyperlipidique, protège les souris de l’obésité et empêche le développement d’altérations métaboliques musculaires, comparativement aux souris ne recevant qu’un régime hyperlipidique. Ces effets bénéfiques s’accompagnent d’une augmentation de l’expression d’APJ dans le muscle, mais pas dans le tissu adipeux [36].
Chez l’homme, les régulations de l’expression d’APJ dans le tissu adipeux et le muscle sont similaires à celles décrites chez la souris. L’expression d’APJ augmente dans le tissu adipeux de femmes obèses et diminue en réponse à la perte de poids induite par un régime hypocalorique, soulignant la réversibilité de cette régulation [37]. Dans le tissu adipeux de patients sains et diabétiques de type II, aucune différence significative n’a été trouvée à l’état basal [35]. Cependant, l’insuline perfusée au cours d’un clamp euglycémique-hyperinsulinémique augmente l’expression d’APJ, mais uniquement dans le tissu adipeux des sujets témoins. Dans le muscle, bien qu’il n’y ait pas de différence d’expression d’APJ entre les sujets témoins et diabétiques, l’insuline administrée au cours du clamp entraîne une hausse d’APJ dans les deux groupes [35].
En revanche, dans une autre étude au cours de laquelle des sujets obèses (mais non diabétiques) ont été soumis pendant huit semaines à un programme d’entraînement physique, l’expression d’APJ reste inchangée dans les biopsies de muscle faites avant et après l’entraînement, alors que l’expression de l’apeline augmente [38].
Conclusions et perspectives thérapeutiques
L’apeline exerce un large éventail d’effets et ceux nouvellement décrits sur le métabolisme énergétique renforcent le rôle physiologique bénéfique de l’apeline (Figure 3), ainsi que son intérêt pharmacologique dans la stratégie de traitement des maladies métaboliques. APJ représente donc une cible originale pour la conception d’agents pharmacologiques. L’utilisation de ceux-ci permettra de mieux délimiter les rôles du système apeline/APJ, mais aussi de contourner les problèmes liés à la faible biodisponibilité de l’apeline. La validation, chez l’homme, des effets bénéfiques de l’apeline sur la sensibilité à l’insuline est actuellement en cours (en partenariat avec le service de diabétologie du CHU de Rangueil et le centre d’investigation clinique de Toulouse). Les premiers résultats sont très encourageants et permettent d’envisager un véritable potentiel thérapeutique de l’apeline chez le diabétique.
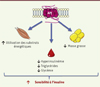 |
Figure 3. Les principaux effets métaboliques de l’apeline chez la souris obèse et résistante à l’insuline. L’activation d’APJ par l’apeline administrée pendant une période prolongée améliore l’activité métabolique du tissu adipeux, du muscle squelettique, ainsi que les paramètres plasmatiques, ce qui permet d’augmenter la sensibilité à l’insuline. |
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Les travaux réalisés dans nos équipes ont bénéficié du soutien financier de la SFD (société francophone du diabète), de la SFN (société française de nutrition) et de la région Midi-Pyrénées. Nous prions certains auteurs de bien vouloir nous excuser de ne pas avoir cité leurs travaux faute de place.
Voir le numéro thématique de m/s consacré aux « récepteurs couplés aux protéines G », n° 10, vol. 28, octobre 2012.
Le clamp hyperinsulinémique euglycémique est la méthode de choix pour mesurer l’insulinorésistance. Cette méthode consiste à perfuser de l’insuline à débit continu ainsi que du glucose pour prévenir la baisse de la glycémie. La quantité de glucose perfusé est une estimation de la quantité de glucose utilisée par les tissus en réponse à l’insuline administrée.
La baisse des acides gras circulants est due à l’effet antilipolytique de l’apeline (ils ne « sortent » plus de l’adipocyte) mais aussi à leur oxydation (qui est augmentée) dès qu’ils sont dans la circulation. Donc la baisse d’adiposité est surtout due à une utilisation des acides gras avant leur mise en réserve dans l’adipocyte (en quelque sorte les souris n’ont pas le temps de grossir).
Un des mécanismes de la résistance à l’insuline est l’incapacité du récepteur à transduire le signal intracellulaire. Ceci est en partie du à la mauvaise oxydation des lipides et à la génération de « résidus » non totalement oxydés : les acylcarnitines.
L’angiopoiétine 1 agit comme un agoniste de TIE2, un récepteur à activité tyrosine kinase des cellules endothéliales, dont l’activation agit sur la survie de ces cellules et le remodelage du système vasculaire.
Références
- O’Dowd BF, Heiber M, Chan A, et al. A human gene that shows identity with the gene encoding the angiotensin receptor is located on chromosome 11. Gene 1993 ; 136 : 355–360. [CrossRef] [PubMed] [Google Scholar]
- Tatemoto K, Hosoya M, Habata Y, et al. Isolation and characterization of a novel endogenous peptide ligand for the human APJ receptor. Biochem Biophys Res Commun 1998 ; 251 : 471–476. [CrossRef] [PubMed] [Google Scholar]
- Galanth C, Hus-Citharel A, Li B, Llorens-Cortes C. Apelin in the control of body fluid homeostasis and cardiovascular functions. Curr Pharm Des 2012 ; 18 : 789–798. [CrossRef] [PubMed] [Google Scholar]
- Llorens-Cortes C, Beaudet A. L’apéline, un inhibiteur naturel de l’effet antidiurétique de la vasopressine. Med Sci (Paris) 2005 ; 21 : 741–746. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Masri B, Lahlou H, Mazarguil H, et al. Apelin (65–77) activates extracellular signal-regulated kinases via a PTX-sensitive G protein. Biochem Biophys Res Commun 2002 ; 290 : 539–545. [CrossRef] [PubMed] [Google Scholar]
- Masri B, Morin N, Pedebernade L, et al. The apelin receptor is coupled to Gi1 or Gi2 protein and is differentially desensitized by apelin fragments. J Biol Chem 2006 ; 281 : 18317–18326. [CrossRef] [PubMed] [Google Scholar]
- Szokodi I, Tavi P, Foldes G, et al. Apelin, the novel endogenous ligand of the orphan receptor APJ, regulates cardiac contractility. Circ Res 2002 ; 91 : 434–440. [CrossRef] [PubMed] [Google Scholar]
- Yue P, Jin H, Xu S, et al. Apelin decreases lipolysis via G(q), G(i), and AMPK-dependent mechanisms. Endocrinology 2011 ; 152 : 59–68. [CrossRef] [PubMed] [Google Scholar]
- O’Carroll AM, Lolait SJ, Harris LE, Pope GR. The apelin receptor APJ: journey from an orphan to a multifaceted regulator of homeostasis. J Endocrinol 2013 ; 219 : R13–R35. [CrossRef] [PubMed] [Google Scholar]
- Dray C, Knauf C, Daviaud D, et al. Apelin stimulates glucose utilization in normal and obese insulin-resistant mice. Cell Metab 2008 ; 8 : 437–445. [CrossRef] [PubMed] [Google Scholar]
- Attane C, Daviaud D, Dray C, et al. Apelin stimulates glucose uptake but not lipolysis in human adipose tissue ex vivo. J Mol Endocrinol 2011 ; 46 : 21–28. [CrossRef] [PubMed] [Google Scholar]
- Attane C, Foussal C, Le Gonidec S, et al. Apelin treatment increases complete fatty acid oxidation, mitochondrial oxidative capacity, and biogenesis in muscle of insulin-resistant mice. Diabetes 2012 ; 61 : 310–320. [CrossRef] [PubMed] [Google Scholar]
- Dray C, Sakar Y, Vinel C, et al. The intestinal glucose-apelin cycle controls carbohydrate absorption in mice. Gastroenterology 2013 ; 144 : 771–780. [CrossRef] [PubMed] [Google Scholar]
- Than A, Cheng Y, Foh LC, et al. Apelin inhibits adipogenesis and lipolysis through distinct molecular pathways. Mol Cell Endocrinol 2012 ; 362 : 227–241. [CrossRef] [PubMed] [Google Scholar]
- Lee DK, Ferguson SS, George SR, O’Dowd BF. The fate of the internalized apelin receptor is determined by different isoforms of apelin mediating differential interaction with beta-arrestin. Biochem Biophys Res Commun 2010 ; 395 : 185–189. [CrossRef] [PubMed] [Google Scholar]
- Zhou N, Fang J, Acheampong E, et al. Binding of ALX40-4C to APJ, a CNS-based receptor, inhibits its utilization as a co-receptor by HIV-1. Virology 2003 ; 312 : 196–203. [CrossRef] [PubMed] [Google Scholar]
- Scimia MC, Hurtado C, Ray S, et al. APJ acts as a dual receptor in cardiac hypertrophy. Nature 2012 ; 488 : 394–398. [CrossRef] [PubMed] [Google Scholar]
- Siddiquee K, Hampton J, McAnally D, et al. The apelin receptor inhibits the angiotensin II type 1 receptor via allosteric trans-inhibition. Br J Pharmacol 2013 ; 168 : 1104–1117. [CrossRef] [PubMed] [Google Scholar]
- Chun HJ, Ali ZA, Kojima Y, et al. Apelin signaling antagonizes Ang II effects in mouse models of atherosclerosis. J Clin Invest 2008 ; 118 : 3343–3354. [PubMed] [Google Scholar]
- Sun X, Iida S, Yoshikawa A, et al. Non-activated APJ suppresses the angiotensin II type 1 receptor, whereas apelin-activated APJ acts conversely. Hypertens Res 2011 ; 34 : 701–706. [CrossRef] [PubMed] [Google Scholar]
- Cheng SC, Ho L, Tian J, Reversade B. ELABELA: a hormone essential for heart development signals via the apelin receptor. Dev Cell 2013 ; 27 : 672–680. [CrossRef] [PubMed] [Google Scholar]
- Pauli A, Norris ML, Valen E, et al. Toddler: an embryonic signal that promotes cell movement via apelin receptors. Science 2014 ; 343 : 1248636. [CrossRef] [PubMed] [Google Scholar]
- Khan P, Maloney PR, Hedrick M, et al. Functional agonists of the apelin (APJ) receptor. Probe Reports from the NIH Molecular Libraries Program, Bethesda (MD), 2010. [Google Scholar]
- Macaluso NJ, Pitkin SL, Maguire JJ, et al. Discovery of a competitive apelin receptor (APJ) antagonist. Chem Med Chem 2011 ; 6 : 1017–1023. [CrossRef] [Google Scholar]
- Iturrioz X, Alvear-Perez R, De Mota N, et al. Identification and pharmacological properties of E339–3D6, the first nonpeptidic apelin receptor agonist. FASEB J 2010 ; 24 : 1506–1517. [CrossRef] [PubMed] [Google Scholar]
- Boucher J, Masri B, Daviaud D, et al. Apelin, a newly identified adipokine up-regulated by insulin and obesity. Endocrinology 2005 ; 146 : 1764–1771. [CrossRef] [PubMed] [Google Scholar]
- Sorhede Winzell M, Magnusson C, Ahren B. The apj receptor is expressed in pancreatic islets and its ligand, apelin, inhibits insulin secretion in mice. Regul Pept 2005; 131 : 12–17. [CrossRef] [PubMed] [Google Scholar]
- Ringstrom C, Nitert MD, Bennet H, et al. Apelin is a novel islet peptide. Regul Pept 2010 ; 162 : 44–51. [CrossRef] [PubMed] [Google Scholar]
- Duparc T, Colom A, Cani PD, et al. Central apelin controls glucose homeostasis via a nitric oxide-dependent pathway in mice. Antioxid Redox Signal 2011 ; 15 : 1477–1496. [CrossRef] [PubMed] [Google Scholar]
- Yue P, Jin H, Aillaud M, et al. Apelin is necessary for the maintenance of insulin sensitivity. Am J Physiol Endocrinol Metab 2010 ; 298 : E59–E67. [CrossRef] [PubMed] [Google Scholar]
- Xu S, Han P, Huang M, et al. In vivo, ex vivo, and in vitro studies on apelin’s effect on myocardial glucose uptake. Peptides 2012 ; 37 : 320–326. [CrossRef] [PubMed] [Google Scholar]
- Drougard A, Duparc T, Brenachot X, et al. Hypothalamic apelin/reactive oxygen species signaling controls hepatic glucose metabolism in the onset of diabetes. Antioxid Redox Signal 2014 ; 20 : 557–573. [CrossRef] [PubMed] [Google Scholar]
- Yamamoto T, Habata Y, Matsumoto Y, et al. Apelin-transgenic mice exhibit a resistance against diet-induced obesity by increasing vascular mass and mitochondrial biogenesis in skeletal muscle. Biochim Biophys Acta 2011 ; 1810 : 853–862. [CrossRef] [PubMed] [Google Scholar]
- Sawane M, Kajiya K, Kidoya H, et al. Apelin inhibits diet-induced obesity by enhancing lymphatic and blood vessel integrity. Diabetes 2013 ; 62 : 1970–1980. [CrossRef] [PubMed] [Google Scholar]
- Dray C, Debard C, Jager J, et al. Apelin and APJ regulation in adipose tissue and skeletal muscle of type 2 diabetic mice and humans. Am J Physiol Endocrinol Metab 2010 ; 298 : E1161–E1169. [CrossRef] [PubMed] [Google Scholar]
- Bertrand C, Pignalosa A, Wanecq E, et al. Effects of dietary eicosapentaenoic acid (EPA) supplementation in high-fat fed mice on lipid metabolism and apelin/APJ system in skeletal muscle. PLoS One 2013 ; 8 : e78874. [CrossRef] [PubMed] [Google Scholar]
- Castan-Laurell I, Vitkova M, Daviaud D, et al. Effect of hypocaloric diet-induced weight loss in obese women on plasma apelin and adipose tissue expression of apelin and APJ. Eur J Endocrinol 2008 ; 158 : 905–910. [CrossRef] [PubMed] [Google Scholar]
- Besse-Patin A, Montastier E, Vinel C, et al. Effect of endurance training on skeletal muscle myokine expression in obese men: identification of apelin as a novel myokine. Int J Obes (Lond) 2014 ; 38 : 707–713. [CrossRef] [PubMed] [Google Scholar]
- Kniazeff J, Pin JP. Des dimères et des oligomères de récepteurs couplés aux protéines G, oui mais pourquoi ?. Med sci (Paris) 2012 ; 10 : 858–864. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. Les différents ligands d’APJ. A. L’apeline : après clivage du peptide signal, la pro-apeline entre dans la voie sécrétoire. La pro-apeline peut générer, après clivage, différentes formes actives d’apeline. B. Apela (aussi nommée elabela ou toddler) : comme pour l’apeline, apela possède des sites potentiels de clivage et pourrait générer différentes formes d’apela. Les séquences présentées sont les séquences murines d’apeline et d’apela. |
| Dans le texte | |
 |
Figure 2. APJ, un récepteur aux multiples voies d’activation. L’activation d’APJ par l’apeline A, l’apela, ou un étirement mécanique de la cellule, engendre l’activation de différentes voies de signalisation (protéines G et recrutement des β-arrestines), conduisant aux différents effets cellulaires. Le récepteur est alors internalisé, puis recyclé à la membrane ou dégradé. |
| Dans le texte | |
 |
Figure 3. Les principaux effets métaboliques de l’apeline chez la souris obèse et résistante à l’insuline. L’activation d’APJ par l’apeline administrée pendant une période prolongée améliore l’activité métabolique du tissu adipeux, du muscle squelettique, ainsi que les paramètres plasmatiques, ce qui permet d’augmenter la sensibilité à l’insuline. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




