| Issue |
Med Sci (Paris)
Volume 26, Number 8-9, Août-Septembre 2010
|
|
|---|---|---|
| Page(s) | 740 - 746 | |
| Section | M/S revues | |
| DOI | https://doi.org/10.1051/medsci/2010268-9740 | |
| Published online | 15 août 2010 | |
Radiothérapie et athérome
Données et questions actuelles
Radiotherapy and atherosclerosis: current data and issues
1
IRSN DRPH SRBE, BP n° 17, 92262 Fontenay-aux-Roses, France
2
Inserm U892, Centre de recherche en cancérologie Nantes-Angers, Institut de recherche thérapeutique de l’Université de Nantes, 8, quai Moncousu, BP 70721, 44007 Nantes Cedex 1, France
3
CHU Nantes, Centre René Gauducheau, service de radiothérapie, Saint-Herblain, France
4
CHU de Nantes, clinique d’endocrinologie, Hôpital Laennec, boulevard Monod, Saint-Herblain, France
5
Institut de recherche thérapeutique de l’Université de Nantes, Institut du thorax, 8, quai Moncousu BP 70721, Nantes, France
* Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
L’optimisation constante des traitements du cancer par radiothérapie pose le problème du devenir à long terme des patients traités et guéris par les rayonnements ionisants, et de la survenue éventuelle de seconds cancers ou de complications non cancéreuses. Parmi ces dernières, les pathologies cardiovasculaires sont prédominantes et peuvent concerner jusqu’à 40 % des patients selon la localisation de l’irradiation. Les dernières études épidémiologiques montrent que ce problème est sous-estimé et n’a pas fait l’objet de réelles études prospectives. La prise en charge thérapeutique de ces patients à risque vasculaire, voire à très haut risque s’ils présentent des facteurs de risque cardiovasculaires traditionnels préexistants, reste à déterminer. Les mécanismes physiopathologiques de l’athérome radio-induit ne sont pas encore clarifiés. La surveillance vasculaire prolongée des patients à distance de leur traitement par radiothérapie doit désormais être intégrée dans les schémas de soins, d’autant plus que la mise en place d’un plateau technique de radiothérapie de plus en plus sophistiqué ne résoudra pas forcément le problème du risque cardiovasculaire après traitement.
Abstract
The continuous optimization of cancer treatment with radiotherapy raises the problem of long-term issue of patients treated and cured by ionizing radiation, with the possible occurrence of second cancers or nonmalignant complications. Among these, cardiovascular diseases are prevalent and may affect up to 40 % of patients depending on the location of the irradiation. Recent epidemiological studies show that this problem is underestimated and with no real prospective studies. The management of these patients with vascular risk, or with very high vascular risk for those with pre-existing traditional cardiovascular risk factors, remains to be determined. The pathophysiological mechanisms of radiation-induced atherosclerosis have not yet been clarified. Many efforts are still needed to identify patients at risk and to find or to propose an appropriate treatment. Prolonged vascular follow-up of patients after their radiotherapy should now be integrated into patterns of care, especially because the setting up of sophisticated technical platforms of radiotherapy do not necessarily solve the issue of cardiovascular risk after treatment.
© 2010 médecine/sciences - Inserm / SRMS
La radiothérapie reste, en 2010, une arme essentielle de l’oncologue. En France, chaque année, sur les 320 000 patients chez lesquels un cancer est diagnostiqué, 60 % bénéficient d’une radiothérapie. Cette technique entraîne nécessairement des dommages aux tissus sains péritumoraux inclus dans les marges de sécurité des volumes à irradier, avec comme conséquence d’éventuelles complications radio-induites à long terme. Parmi les complications cardiovasculaires, on peut distinguer celles qui résultent d’une atteinte des petits vaisseaux de celles qui résultent de dommages aux plus gros vaisseaux. Les premières sont responsables d’une fibrose tardive du tissu cardiaque pouvant toucher le péricarde, le myocarde et l’endocarde [1, 2]. Cette toxicité cardiaque ne sera pas développée dans cette revue qui porte sur les pathologies cardiovasculaires liées à l’atteinte des moyens et gros vaisseaux et consécutives à l’athérosclérose, processus en partie inflammatoire entraînant des remaniements de la paroi artérielle et aboutissant à des événements cliniques ischémiques (infarctus du myocarde, cardiopathie ischémique, accident vasculaire cérébral, etc.). Le Tableau I résume l’incidence des pathologies cardiovasculaires induites par la radiothérapie en fonction des cancers concernés. Le risque relatif d’événements cardiovasculaires est entre 133 et 560 % supérieur à celui de la population générale. Ces chiffres impressionnants devraient motiver une recherche mécanistique, préclinique et clinique dédiée à la prévention ainsi qu’au traitement de I ‘athérome radio-induit. Aujourd’hui, on ne sait pas s’il résulte d’une accélération d’un processus athéromateux classique et/ou de réponses cellulaires et moléculaires propres à l’irradiation. Jusqu’à très récemment, les recherches analysant ou explorant la réponse vasculaire à l’irradiation étaient focalisées sur les cellules endothéliales des petits vaisseaux. Les mécanismes identifiés ne sont pas forcément extrapolables puisque l’athérosclérose se développe sur les artères de moyen et gros calibres. À terme, l’objectif est de pouvoir sélectionner des marqueurs permettant l’identification de patients à risque et de définir des stratégies thérapeutiques adaptées. Cette revue présente une synthése des données épidémiologiques récentes, puis, à partir des quelques données cliniques, les caractéristiques morphologiques et anatomopathologiques de l’athérome radio-induit. Enfin, les mécanismes physiopathologiques vasculaires après irradiation seront abordés.
Risque relatif des évènements cardiovasculaires après radiothérapie selon les cancers. Incidence du cancer : nombre de nouveaux diagnostics du cancer par an en France (ici en 2006). RR : risque relatif. Le risque relatif mesure le risque de survenue d’un évènement dans un groupe par rapport à un autre. Le risque relatif est ici le rapport de l’incidence de l’événement cardiovasculaire chez les patients après radiothérapie sur l’incidence de cet évènement dans la population témoin. IC : intervalle de confiance ; AVC : accident vasculaire cérébral ; AIT : accident ischémique transitoire. * (revue dans [3]).
Le risque cardiovasculaire augmente avec le nombre d’années suivant la radiothérapie
Quel que soit le cancer concernè, le temps de latence entre l’irradiation et l’apparition des complications est de quelques années. Ensuite, plus la période de suivi aprés le traitement augmente et plus le risque cardiovasculaire est élevé. Une étude américaine portant sur plus de 100 000 patientes issues de la cohorte SEER (surveillance epidemiology and end results) traitées par radiothérapie postchirurgicale entre 1973 et 2001 pour un cancer du sein compare la mortalité cardiaque (principalement ischémique) des patientes ayant un cancer du sein gauche à celle des patientes ayant un cancer du sein droit. Le risque relatif (RR) passe de 1,10 (IC 95 % 0,97-1,25) avant 10 ans à 1,53 (IC 95 % 1,25-1,86) aprés 15 ans [4, 5].
Pour les lymphomes de Hodgkin traités entre 1967 et 2000 par une radiothérapie supradiaphragmatique, le risque relatif d’infarctus du myocarde par rapport à la population générale est multiplié par 2,4 (IC 95 % 1,8-3,2) durant les 10 premières années et atteint 4,3 au-delà de 20 ans (IC 95 % 2,3-7,4) [6].
Dans la cohorte SEER, pour les 1 983 patients de plus de 65 ans ayant un cancer de la tête et du cou traité par radiothérapie entre 1992 et 2002, l’incidence des accidents vasculaires cérébraux (AVC) passe de 19 % à 5 ans a 34 % a 10 ans [7]. L’étude de Dorresteijn et al. [8] montre que, pour les 367 patients traités avant l’âge de 60 ans entre 1977 et 1998, moins de 10 ans après l’irradiation, le risque absolu d’AVC est de 1,9 cas pour 1 000 personnes par année et le risque relatif est de 3,7 (IC 95 % 1,3-8). Au-delà de 10 ans, ce risque passe a 14 cas pour 1 000 personnes par année avec un risque relatif de 10,1 (IC 95 % 4,4-20).
Pour les cancers du testicule de stades I-II traités entre 1951 et 1999 par une irradiation ganglionnaire prophylactique systématique après ablation chirurgicale du testicule (orchidectomie), le risque relatif de mortalité cardiaque (ischémique et insuffisance cardiaque) comparè à la population générale masculine n’est significativement augmenté qu’au-delà de 15 ans aprés les traitements et uniquement pour les patients ayant reçu une irradiation infradiaphragmatique (RR = 1,8, IC 95 % 1,01-2,98) ou médiastinale (RR = 2,33, IC 95 % 1,01-4,59) [9].
Le risque cardiovasculaire dépend du champ d’irradiation
La pathologie coronaire est particulièrement élevée dans la cohorte historique des patients atteints d’un cancer du testicule et traités dans les années 1970-1980, après orchidectomie, par une radiothérapie ganglionnaire prophylactique étendue couvrant le médiastin. Parmi ces patients, 15,7 % sont décédés de cause cardiaque (ischémique et insuffisance cardiaque) et le risque relatif est multiplié par 2,33 (IC 95 % 1,01-4,59) comparè à la population générale masculine [9]. Deux études montrent que, même pour les patients traités par une radiothérapie prophylactique limitée aux aires ganglionnaires infradiaphragmatiques, un risque de décès dû a une cause cardiaque (ischémique et insuffisance cardiaque) existe (RR = 1,8, IC 95 % 1,01-2,98 et RR = 2,4, IC 95 % 1,23-6,08) et touche 9,4 % des patients [9, 10]. Les raisons évoquées pour expliquer l’augmentation de la morbimortalité cardiovasculaire dans ces situations seraient l’irradiation d’un petit volume du cœur dans le sommet du champ lombo-aortique ainsi que d’une partie des reins et/ou des artéres rénales [9].
Pour le cancer du sein, le risque cardiovasculaire dépend du sein traité et les patientes ayant un cancer du sein gauche sont les plus exposées. Vingt ans après le traitement, les coronaropathies touchent 25 % des patientes traitées pour un cancer du sein gauche contre 10 % de celles traitées pour un cancer du sein droit (p < 0,001) [11]. Une réduction de la taille des champs d’irradiation ainsi que du volume cardiaque irradié explique la diminution des décès dus à une cause cardiaque entre les années 1970-1980 (RR = 1,42, IC 95 % 1,111-1,82) et les années 1980-1990 (RR = 1,27, IC 95 % 0,99-1,63) [5].
Une étude rétrospective d’une cohorte de 3 590 patients traités entre 1967 et 2000 pour un lymphome de Hodgkin montre que 3 % d’entre eux décèdent d’infarctus du myocarde. Le risque relatif comparé à la population générale est maximum lorsque les champs d’irradiation touchent toutes les aires ganglionnaires (RR = 9, IC 95 % 5,4-14,1). Ce risque passe à 3 pour l’irradiation en mantelet (IC 95 % 2,3-4,3) et il n’est pas significatif pour une radiothérapie infradiaphragmatique [6]. Une étude très récente réalisée sur 2 014 patients traités entre 1965 et 1995 pour un lymphome de Hodgkin montre que l’irradiation en mantelet augmente le risque relatif d’AVC et d’accident ischémique transitoire (AIT) comparativement à une radiothérapie infradiaphragmatique (RR = 2,5, IC 95 % 1,1-5,6) [12].
Le risque cardiovasculaire est majoré chez les patients jeunes au moment du traitement
Dans l’étude rétrospective de Fossa et al. [13] réalisée sur près de 39 000 patients traités pour un cancer du testicule entre 1943 et 2001, le risque relatif de mortalité cardiaque comparé à la population générale n’est significativement plus élevé que pour les patients âgés de moins de 35 ans au moment de la radiothérapie (RR = 1,7, IC 95 % 1,21-2,31).
Pour les 3 462 patients traités par une radiothérapie supradiaphragmatique pour un lymphome de Hodgkin, le risque relatif d’infarctus du myocarde comparé à la population générale est de 10,1 (IC 95 % 7-14,1) si les patients ont moins de 35 ans au moment du traitement. Ce risque passe à 2,9 pour la catégorie 35-54 ans (IC 2,1-3,9) et à 1,8 au-dela de 55 ans (IC 95 % 1,2-2,4) [6].
Pour les cancers de la tête et du cou traités entre 1977 et 1998, les patients âgés de moins de 50 ans ont un risque relatif d’AVC de 9,8 (IC 95 % 3,2-22,9) comparativement à la population générale. Ce risque diminue à 4,5 au-dela de 50 ans (IC 95 % 2,1-8,6) [8].
Le risque cardiovasculaire est majoré en présence d’autres facteurs de risque cardiovasculaire
Le risque cardiovasculaire apparaît d’autant plus élevé que les patients irradiés ont des facteurs de risque traditionnels préexistants : tabagisme, hypertension, diabète, hypercholestérolémie, antécédents de cardiopathies ischémiques. Le Tableau II illustre l’interaction entre le tabac et la radiothérapie sur l’évaluation du risque cardiovasculaire chez les patientes traitées pour un cancer du sein. De plus, pour ce cancer, les antécédents de cardiopathies ischémiques, l’hypertension et l’hypercholestérolémie majorent respectivement d’un facteur 1,5, 1,7 et 2,9 le risque relatif d’infarctus du myocarde chez les patientes traitées [14]. Pour les cancers de la tête et du cou, le diabète et l’hypertension majorent respectivement d’un facteur 2,1 et 2,9 le risque relatif d’AVC chez les patients traités [8]. Pour ces cancers, la consommation de tabac augmente significativement (p < 0,029) le nombre de patients irradiés ayant un degré de sténose carotidienne supérieur à 70 % [15].
Interaction entre le tabac et la radiothérapie sur le risque relatif d’infarctus du myocarde chez les patientes traitées pour un cancer du sein. On parle d’interaction entre un facteur de risque traditionnel (ici le tabac) et le risque lié à la radiothérapie si le risque relatif observé chez les fumeuses exposées à la radiothérapie (ici 3,04) est supérieur à celui obtenu en multipliant le risque relatif pour le tabac et le risque lié à la radiothérapie (ici 1,82 = 1,36 × 1,34). RR : risque relatif, IC : intervalle de confiance.
Athérome radio-induit
Données d’imagerie
Actuellement, il est admis que l’athérome radio-induit résulte d’une accélération d’un processus athéromateux classique. Or, des données de la littèrature montrent que celui-ci présente des spécificités.
Les clichés d’artériographie carotidienne réalisés chez des patients traités par radiothérapie pour un cancer de la sphère cervico-faciale révèlent une apparition des lésions chez des patients plus jeunes [16], et la I ongueur des sténoses est plus importante [17] que dans une population contrôle. Les lésions carotidiennes radio-induites sont confinées au site irradié contrairement aux lésions carotidiennes classiques qui sont souvent associées à des atteintes diffuses et disséminées sur l’arbre vasculaire. Lors d’irradiations cervicales, ces lésions postradiques sont localisées préférentiellement et de façon atypique dans l’artère carotide commune alors que les lésions classiques ont une localisation privilégiée dans l’artère carotide interne. Lorsque les lésions postradiques sont localisées dans l’artère carotide interne, il n’y a pas d’atteinte du bulbe carotidien, contrairement aux lésions classiques [18]. Enfin, une fibrose radio-induite se développe au niveau péri-artériel et des tissus sains environnant l’artère carotide irradiée : on parle alors de « cou radique » [17, 19].
L’écho-doppler d’artères carotides irradiées dont le degré de sténose est supérieur à 50 % révèle une augmentation de l’épaisseur intima-média et une lumière intimale plus rétrécie comparativement à des artères carotides contrôles non irradiées ayant un degré de sténose identique [20]. Les sténoses carotidiennes postradiques symptomatiques sont associées à une plaque plus hypoéchogène et un degré de sténose supérieur (91 % ± 8) à celui des sténoses carotidiennes postradiques asymptomatiques (67 % ± 17, p < 0,001) [20]. L’angiographie coronaire montre que les sténoses coronariennes radiques sont plus souvent proximales et ostiales1 plutôt que distales [21].
Données histologiques chez l’homme
Les études anatomopathologiques postmortem comparant des lésions d’artères coronaires de patients traités pour un lymphome de Hodgkin et de patients non irradiés montrent que l’irradiation induit une fibrose plus étendue et plus sévère de l’intima, un amincissement voire une destruction focalisée de la média, une fibrose et un épaississement plus sévères de l’adventice (Figure 1) [2, 21, 22].
 |
Figure 1 Exemple de coronaropathie chez un patient de 26 ans, 5 ans après une radiothérapie pour un lymphome de Hodgkin. A. Fibrose intimale sévère (I, double flèche) et destruction focalisée de la média (flèches), lumière intimale (L). B. Fibrose intimale (I, double flèche), occlusion thrombotique (T), média (M, double flèche) et adventice (A, double flèche) (observations à un grossissement × 36, coloration de Van Gieson) (d’après [21]). |
Physiopathologie de la paroi artérielle après irradiation : des mécanismes mal connus
Les dommages induits après irradiation des vaisseaux sanguins sont reconnus depuis plus d’une centaine d’années. Dans les petits vaisseaux, ils sont décrits comme plus sévères et plus fréquents que ceux retrouvés au niveau de vaisseaux plus gros, et par ailleurs, ils sont différents sur le plan histopathologique [23]. L’élément-clé responsable de cette radiosensibilité préférentielle des petits vaisseaux est la cellule endothéliale qui en est le constituant principal [23]. De très nombreux travaux expérimentaux réalisés sur l’endothélium des petits vaisseaux montrent que l’irradiation induit une dysfonction endothéliale à la fois aiguë et chronique, entraînant un phénotype pro-inflammatoire, prothrombotique, procoagulant et antifibrinolytique [24]. Les rôles, d’une part, des molécules d’adhésion, des cytokines pro-inflammatoires, des chémoattractants, des facteurs de croissance et des facteurs impliqués dans la coagulation et la fibrinolyse et, d’autre part, des cellules circulantes (leucocytes, plaquettes) sont bien identifiés [24–26]. L’efficacité des statines pour limiter et/ou restaurer les dommages endothéliaux radio-induits a été démontrée in vitro et in vivo et peut s’expliquer par leur action anti-inflammatoire, complémentaire de leurs propriétés hypolipé miantes [27, 28]. Les lésions vasculaires radio-induites étant différentes selon la taille des vaisseaux irradiés [23], les mécanismes physiopathologiques moléculaires et cellulaires identifiés au sein des petits vaisseaux ne peuvent pas être extrapolés aux vaisseaux plus gros. Actuellement, ces mécanismes restent encore très mal connus.
Physiopathologie vasculaire après irradiation : modèles précliniques
Un nombre anecdotique d’études précliniques montrent une accélération des lésions d’athérome après irradiation localisée d’artères d’animaux hypercholestérolémiques ou soumis à un régime proathérogène [29–31], situations où les espèces radicalaires de l’oxygène générées par l’irradiation jouent un rôle important [31]. Plus récemment, l’équipe de F. Stewart a décrit [32], dans un modèle de souris déficientes en apolipoprotéine E (ApoE-/-) prédisposées à l’athérosclérose, des caractéristiques physiopathologiques des lésions spécifiques à l’irradiation (Figure 2). D’un point de vue quantitatif, les artères carotides des souris ApoE−/− irradiées ont un nombre plus important de plaques d’athérome et un noyau lipidique par plaque de plus grande taille comparé à celles des souris ApoE−/− non irradiées et d’âge équivalent. D’un point de vue qualitatif, les plaques d’athérome des artères carotides irradiées sont plus riches en macrophages et en polynucléaires, ce qui est le signe d’un processus inflammatoire plus important. La quantité de collagène dans les plaques d’athérome est diminuée après irradiation, les rendant de fait plus instables. La présence de macrophages ayant phagocyté des érythrocytes dans les plaques d’athérome reflète un processus hémorragique qui n’est présent que dans les artères carotides irradiées. Des plaques d’athérome riches en dépôts de fibrine ne sont observées que dans les artères carotides irradiées, révélant l’induction par l’irradiation de complications thrombotiques. Des cellules endothéliales de forme atypique ne sont trouvées qu’ à la périphérie des plaques d’athérome des artères carotides irradiées [32, 33]. Ce modèle préclinique, montrant un phénotype spécifique de l’athérome radio-induit, paraît donc adapté pour étudier la pathogenèse des évènements moléculaires et cellulaires induits par l’irradiation dans les artères et pour tester des approches pharmacologiques appropriées.
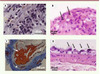 |
Figure 2 Aspect histologique de la plaque d’athérome dans les artères carotides irradiées de souris ApoE-/-. A. Présence de polynucléaires (flèches) et d’érythrocytes (pointes de flèche) (grossissement × 40, coloration hématoxyline-éosine). B. Macrophages contenant des érythrocytes (flèches), conséquence d’une hémorragie intraplaque (grossissement × 40, coloration hématoxyline-éosine). C. Dépôts de fibrine colorés en rouge (flèche) signant un phénotype thrombotique de la plaque d’athérome, média (M) et lumière intimale très rétrécie (L) (grossissement × 20, coloration au bleu de Martius Scarlet). D. Cellules endothéliales atypiques (flèches) à la périphérie de la plaque d’athérome (grossissement × 40, coloration hématoxyline-éosine) (d’après [32, 33]). |
Prise en charge des complications cardiovasculaires postradiques
Les sténoses carotidiennes sur « cou radique » sont une des indications de l’angioplastie carotidienne [19], alors que la technique de référence en France est plutôt la chirurgie carotidienne. En effet, le développement d’une fibrose péri-artérielle et des tissus environnant l’artère carotide irradiée limite l’efficacité de la chirurgie [17]. Cependant, aucune étude randomisée comparant les deux techniques n’a encore été publiée [34].
Pour les sténoses coronariennes postradiques, l’angioplastie et le pontage coronarien sont les deux options thérapeutiques utilisées, mais le pontage coronarien s’accompagne de complications plus nombreuses [35].
Amélioration de la radiothérapie : vers une diminution du risque cardiovasculaire ?
Les mesures prises il y a plusieurs années telles que l’abandon de l’irradiation en mantelet pour le lymphome de Hodgkin et médiastinale pour le cancer du testicule, la réduction des volumes irradiés, ainsi que l’amélioration de la balistique ont permis de réduire la toxicité cardiaque. Pour le risque cardiovasculaire, le recul est actuellement insuffisant pour conclure sur l’efficacité de ces mesures car le temps de latence de ces complications est long. Plus récemment, les appareils de radiothérapie de dernière génération permettent de gagner en efficacité sur la tumeur et en tolérance sur le tissu sain. Cependant, avec ces appareils, les artères coronaires ne peuvent être évitées lors de l’irradiation des chaînes mammaires internes pour un cancer du sein gauche [36], ni lors d’une irradiation ganglionnaire médiastinale pour un lymphome de Hodgkin [37]. Pour les cancers de la tête et du cou, les artères carotides servent de repères pour la définition des volumes tumoraux cibles et ne peuvent donc pas être protégées de l’irradiation [38]. Globalement, les nouvelles techniques de radiothérapie prennent en compte le risque vasculaire mais dans la limite de l’efficacité carcinologique. Dans ce contexte, le risque cardiovasculaire de l’irradiation reste toujours d’actualité.
Conclusion
À côté de son rôle bénéfique démontré, la radiothérapie pour traiter les cancers du sein, de la tête et du cou, du testicule et les lymphomes de Hodgkin peut être responsable de complications cardiovasculaires. Le risque est majoré chez les patients qui ont des facteurs de risque cardiovasculaire traditionnels et chez les patients jeunes. Actuellement, aucune donnée ne permet de dire si le pronostic de l’athérome radio-induit est différent de celui de la population générale, ni de justifier l’utilisation de traitements ayant démontré leur efficacité en prévention cardiovasculaire classique. Les résultats du seul essai clinique cité pourront apporter un élément de réponse. Il s’agit d’une étude randomisée de phase III pour des patients atteints de cancer de la tête et du cou traités avec de l’atorvastatine pendant la radiothérapie et poursuivie deux ans après la dernière séance [32, 39]. En attendant, il est primordial d’instaurer un suivi strict des patients sur le long terme avec une vigilance particulière pour la prise en charge des facteurs de risque traditionnels et le dépistage précoce des lésions vasculaires. La mise en place de stratégies spécifiques de réduction du risque cardiovasculaire après radiothérapie devra s’appuyer sur des arguments physiopathologiques justifiant le développement d’une recherche dédiée plus fondamentale.
Conflit d’intérêts
Les auteurs déclarent n’avoir aucun conflit d’intérêts concernant les données publiées dans cet article.
La sténose ostiale est localisée au niveau de l’ostium, partie anatomique à la naissance des artères coronaires. La sténose proximale est localisée au niveau des segments proximaux des artères coronaires.
Références
- Giraud P, Cosset JM. Toxicité cardiaque de la radiothérapie : physiopathologie, données cliniques. Bull Cancer 2004 ; 91 : S147-53. [Google Scholar]
- Senkus-Konefka E, Jassem J. Cardiovascular effects of breast cancer radiotherapy. Cancer Treat Rev 2007 ; 33 : 578-93. [Google Scholar]
- Guérin S, Doyon F, Hill C. La fréquence des cancers en France en 2006 et les évolutions de la mortalité depuis 1950 et de l’incidence depuis 1980. Bull Cancer 2009 ; 96 : 51-7. [Google Scholar]
- Darby SC, McGale P, Taylor CW, et al. Long term mortality from heart disease and lung cancer after radiotherapy for early breast cancer : prospective cohort study of about 300 000 women in US SEER cancer registries. Lancet Oncol 2005 ; 6 : 557-65. [Google Scholar]
- Demirci S, Nam J, Hubbs JL, et al. Radiation-induced cardiac toxicity after therapy for breast cancer: interaction between treatment and follow-up duration. Int J Radiat Oncol Biol Phys 2009 ; 73 : 980-7. [Google Scholar]
- Swerdlow AJ, Higgins CD, Smith P, et al. Myocardial infarction mortality risk after treatment for Hodgkin disease: a collaborative British cohort study. J Natl Cancer Inst 2007 ; 99 : 206-14. [Google Scholar]
- Smith GL, Smith BD, Buchholz TA, et al. Cerebrovascular disease risk in older head and neck cancer patients after radiotherapy. J Clin Oncol 2008 ; 26 : 5119-25. [Google Scholar]
- Dorresteijn DA, Kappelle AC, Boogerd W, et al. Increased risk of ischemic stroke after radiotherapy on the neck in patients younger than 60 years. J Clin Oncol 2002 ; 20 : 282-8. [Google Scholar]
- Zagars GK, Ballo MT, Lee AK, et al. Mortality after cure of testicular seminoma. J Clin Oncol 2004 ; 22 : 640-7. [Google Scholar]
- Van den Belt-Dusebout AW, de Wit R, Gietema JA, et al. Treatment-specific risks of second malignancies and cardiovascular disease in 5-year survivors of testicular cancer. J Clin Oncol 2007 ; 25 : 4370-8. [Google Scholar]
- Harris EE, Correa C, Hwang WT, et al. Late cardiac mortality and morbidity in early-stage breast cancer patients after breast-conservation treatment. J Clin Oncol 2006 ; 24 : 4100-6. [Google Scholar]
- De Bruin ML, Dorresteijn DA, van’t Veer MB, et al. Increased risk of stroke and transient ischemic attack in 5-year survivors of Hodgkin lymphoma. J Natl Cancer Inst 2009 ; 101 : 928-37. [Google Scholar]
- Fossa SD, Gilbert E, Dores GM, et al. Noncancer causes of death in survivors of testicular cancer. J Natl Cancer Inst 2007 ; 99 : 533-44. [Google Scholar]
- Hooning MJ, Botma A, Aleman BMP, et al. Long-term risk of cardiovascular disease in 10-year survivors of breast cancer. J Natl Cancer Inst 2007 ; 99 : 365-75. [Google Scholar]
- Cheng SWK, Wu LLH, Ting ACW, et al. Irradiation-induced extracranial carotid stenosis in patients with head and neck malignancies. Am J Surg 1999 ; 178 : 323-8. [Google Scholar]
- Silverberg GD, Britt RH, Goffinet DR. Radiation-induced carotid artery disease. Cancer 1978 ; 41 : 130-7. [Google Scholar]
- Houdart E, Mounayer C, Chapot R, et al. Carotid stenting for radiation-induced stenoses. A report of 7 cases. Stroke 2001 ; 32 : 118-21. [Google Scholar]
- Modrall JG, Sadjadi J. Early and late presentations of radiation arteritis. Semin Vasc Surg 2003 ; 16 : 209-14. [Google Scholar]
- Bergeron P, Piret V, Trastour JC. Angioplastie carotidienne : le point de vue du chirurgien vasculaire. e-mémoires de l’Académie nationale de chirurgie 2008 ; 7 : 36-8. [Google Scholar]
- Cheng SWK, Ting ACW, Wu LLH. Ultrasonic analysis of plaque characteristics and intimal-medial thickness in radiation-induced atherosclerotic carotid arteries. Eur J Vasc Endovasc Surg 2002 ; 24 : 499-504. [Google Scholar]
- Veinot JP, Edwards WD. Pathology of radiation-induced heart disease: a surgical and autopsy study of 27 cases. Hum Pathol 1996 ; 27 : 766-73. [Google Scholar]
- Miltenyi Z, Keresztes K, Garai I, et al. Radiation-induced coronary artery disease in Hodgkin’s disease. Cardiovasc Radiat Med 2004 ; 5 : 38-43. [Google Scholar]
- Fajardo LF. Is the pathology of radiation injury different in small versus large blood vessels? Cardiovasc Radiat Med 1999 ; 1 : 108-10. [Google Scholar]
- Gaugler MH. A unifying system: does the vascular endothelium have a role to play in multi-organ failure following radiation exposure? Br J Radiol 2005 ; S27 : 100-5. [Google Scholar]
- Gaugler MH, Squiban C, van der Meeren A, et al. Late and persistent up-regulation of intercellular adhesion molecule-1 (ICAM-1) expression by ionizing radiation in human endothelial cells in vitro. Int J Radiat Biol 1997 ; 72 : 201-9. [Google Scholar]
- Milliat F, François A, Tamarat R, et al. Rôle de l’endothélium dans les dommages radio-induits aux tissus sains. Ann Cardiol Angeiol 2008 ; 57 : 139-48. [Google Scholar]
- Gaugler MH, Vereycken-Holler V, Squiban C, et al. Pravastatin limits endothelial activation after irradiation and decreases the resulting inflammatory and thrombotic responses. Radiat Res 2005 ; 163 : 479-87. [Google Scholar]
- Holler V, Buard V, Gaugler MH, et al. Pravastatin limits radiation-induced vascular dysfunction in the skin. J Invest Dermatol 2009 ; 129 : 1280-91. [Google Scholar]
- Vos J, Aarnoudse MW, Dijk F, et al. On the cellular origin and development of atheromatous plaques. A light and electron microscopy study of combined X-ray and hypercholesterolemia-induced atheromatosis in the carotid artery of the rabbit. Virchows Arch B Cell Pathol Incl Mol Pathol 1983 ; 43 : 1-16. [Google Scholar]
- Cottin Y, Kollum M, Kolodgie FD, et al. Intravascular radiation accelerates atherosclerosis lesion formation of hypercholesteremic rabbits. Cardiovasc Radiat Med 2001 ; 2 : 231-40. [Google Scholar]
- Tribble DL, Barcellos-Hoff MH, Chu BM, et al. Ionizing radiation accelerates aortic lesion formation in fat-fed mice via SOD-inhibitable processes. Arterioscler Thromb Vasc Biol 1999 ; 19 : 1387-92. [Google Scholar]
- Stewart FA, Heeneman S, de Poele J, et al. Ionizing radiation accelerates the development of atherosclerotic lesions in ApoE−/− mice and predisposes to an inflammatory plaque phenotype prone to hemorrhage. Am J Pathol 2006 ; 168 : 649-58. [Google Scholar]
- Hoving S, Heeneman S, Gijbels MJJ, et al. Single-dose and fractionated irradiation promote initiation and progression of atherosclerosis and induce an inflammatory plaque phenotype in ApoE−/− mice. Int J Radiat Oncol Biol Phys 2008 ; 71 : 848-57. [Google Scholar]
- Favre JP, Nourissat A, Duprey A, et al. Endovascular treatment for carotid artery stenosis after neck irradiation. J Vasc Surg 2008 ; 48 : 852-8. [Google Scholar]
- Darby SC, Cutter DJ, Boerma M, et al. Radiation-related heart-disease: current knowledge and future prospects. Int J Radiat Oncol Biol Phys 2010 ; 76 : 656-65. [Google Scholar]
- Caudrelier JM, Morgan SC, Montgomery L, et al. Helical tomotherapy for locoregional irradiation including the internal mammary chain in left-side breast cancer: dosimetric evaluation. Radiother Oncol 2009 ; 90 : 99-105. [Google Scholar]
- Girinsky T, Pichenot C, Beaudre A, et al. Is intensity-modulated radiotherapy better than conventional radiation treatment and three-dimensional conformal radiotherapy for mediastinal masses in patients with Hodgkin’s disease, and is there a role for beam orientation optimization and dose constraints assigned to virtual volumes? Int J Radiat Oncol Biol Phys 2006 ; 64 : 218-26. [Google Scholar]
- Vitolo V, Millender LE, Quivey JM, et al. Assessment of carotid artery dose in the treatment of nasopharyngeal cancer with IMRT versus conventional radiotherapy. Radiother Oncol 2009 ; 90 : 213-20. [Google Scholar]
- Russell NS, Hoving S, Heeneman S, et al. Novel insights into pathological changes in muscular arteries of radiotherapy patients. Radiother Oncol 2009 ; 92 : 477-83. [Google Scholar]
Liste des tableaux
Risque relatif des évènements cardiovasculaires après radiothérapie selon les cancers. Incidence du cancer : nombre de nouveaux diagnostics du cancer par an en France (ici en 2006). RR : risque relatif. Le risque relatif mesure le risque de survenue d’un évènement dans un groupe par rapport à un autre. Le risque relatif est ici le rapport de l’incidence de l’événement cardiovasculaire chez les patients après radiothérapie sur l’incidence de cet évènement dans la population témoin. IC : intervalle de confiance ; AVC : accident vasculaire cérébral ; AIT : accident ischémique transitoire. * (revue dans [3]).
Interaction entre le tabac et la radiothérapie sur le risque relatif d’infarctus du myocarde chez les patientes traitées pour un cancer du sein. On parle d’interaction entre un facteur de risque traditionnel (ici le tabac) et le risque lié à la radiothérapie si le risque relatif observé chez les fumeuses exposées à la radiothérapie (ici 3,04) est supérieur à celui obtenu en multipliant le risque relatif pour le tabac et le risque lié à la radiothérapie (ici 1,82 = 1,36 × 1,34). RR : risque relatif, IC : intervalle de confiance.
Liste des figures
 |
Figure 1 Exemple de coronaropathie chez un patient de 26 ans, 5 ans après une radiothérapie pour un lymphome de Hodgkin. A. Fibrose intimale sévère (I, double flèche) et destruction focalisée de la média (flèches), lumière intimale (L). B. Fibrose intimale (I, double flèche), occlusion thrombotique (T), média (M, double flèche) et adventice (A, double flèche) (observations à un grossissement × 36, coloration de Van Gieson) (d’après [21]). |
| Dans le texte | |
 |
Figure 2 Aspect histologique de la plaque d’athérome dans les artères carotides irradiées de souris ApoE-/-. A. Présence de polynucléaires (flèches) et d’érythrocytes (pointes de flèche) (grossissement × 40, coloration hématoxyline-éosine). B. Macrophages contenant des érythrocytes (flèches), conséquence d’une hémorragie intraplaque (grossissement × 40, coloration hématoxyline-éosine). C. Dépôts de fibrine colorés en rouge (flèche) signant un phénotype thrombotique de la plaque d’athérome, média (M) et lumière intimale très rétrécie (L) (grossissement × 20, coloration au bleu de Martius Scarlet). D. Cellules endothéliales atypiques (flèches) à la périphérie de la plaque d’athérome (grossissement × 40, coloration hématoxyline-éosine) (d’après [32, 33]). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




