| Issue |
Med Sci (Paris)
Volume 42, Number 2, Février 2026
|
|
|---|---|---|
| Page(s) | 153 - 163 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2026014 | |
| Published online | 24 février 2026 | |
Interrégulations entre olfaction et métabolisme énergétique dans l’obésité et le diabète de type 2
Des modèles murins aux humains
Cross-regulation between olfaction and energy homeostasis in obesity and type 2 diabetes: from mouse models to humans
1
Université Paris Cité, Unité de biologie fonctionnelle et adaptative (BFA), CNRS UMR 8251, Paris, France
2
Institute of Metabolic Science-Metabolic Research Laboratories & MRC-Metabolic Diseases Unit, University of Cambridge, Cambridge, UK
3
Sorbonne Université, INSERM UMR_S-1166, NutriOmics (nutrition et obésités ; approches systémiques), Paris, France
*
Cette adresse e-mail est protégée contre les robots spammeurs. Vous devez activer le JavaScript pour la visualiser.
Résumé
Cette synthèse présente le rôle crucial de l’olfaction dans la régulation de l’homéostasie énergétique. Les neurones du système olfactif stimulent les aires cérébrales impliquées dans les émotions, la mémoire et le plaisir, et qui sont liées à l’alimentation. Ils sont modulés par le niveau du métabolisme énergétique corporel, qu’ils régulent en retour. La sensibilité olfactive diminue dans l’obésité et la chirurgie bariatrique la rétablit. Dans le diabète de type 2, l’apparition de troubles olfactifs peut prédire les troubles cognitifs. Enfin, dans un modèle murin de l’obésité, l’activation locale du système glucagon-like peptide-1 (GLP-1) dans le bulbe olfactif, première structure cérébrale codant les odeurs, induit une meilleure régulation de la glycémie et de la prise alimentaire. Le recrutement de cette nouvelle voie neurométabolique menant jusqu’au pancréas provoque une augmentation de la libération d’insuline et de la sensibilité à cette hormone.
Abstract
This review highlights the crucial role of olfaction in regulating energy homeostasis. Neurons in the olfactory system stimulate the limbic and hedonic pathways involved in food-related behaviors. These neurons are modulated by the body’s energy metabolism status, which they, in turn, help to regulate. Olfactory sensitivity is reduced in obesity, while bariatric surgery restores olfactory function. In type 2 diabetes, the onset of olfactory dysfunction is predictive of cognitive decline. Finally, in a mouse model of obesity, local activation of glucagon-like peptide 1 (GLP-1) and its receptors in the olfactory bulb -the main brain structure responsible for encoding odorsleads to improved glycemic control and regulation of food intake. Activation of this new neurometabolic pathway connecting the olfactory system to the pancreas leads to increased insulin secretion and sensitivity to this hormone.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Inserm-Annicotte, Jean-Sébastien).
Obésité, diabète de type 2 et prise alimentaire
La prévalence du surpoids et de l’obésité ne cesse d’augmenter dans tous les pays. Actuellement, dans le monde, plus d’un milliard d’individus sont en situation d’obésité, dont 878 millions d’adultes et 159 millions d’enfants [1] (Encadré 1). Depuis les années 1990, la prévalence de l’obésité a augmenté plus rapidement chez les 5-19 ans (× 4) par rapport au reste de la population (× 2). La pandémie d’obésité n’est pas qu’un problème de santé actuel, elle sera également une maladie de notre futur. Elle résulte de plusieurs facteurs d’origine alimentaire, génétique et environnementale, qui sont interdépendants et qui influencent son développement et sa progression. Notamment, l’obésité est caractérisée par une dérégulation de la balance énergétique, provoquée par une baisse de la dépense énergétique totale (due à l’augmentation de la sédentarité) et de façon concomitante, par un excès d’apport calorique (aliments palatables1, car riches en graisses, en sucres et en sel dénommés junk food ou western food). Des facteurs psychologiques et socio-économiques font également partie des causes de l’obésité. L’obésité et le diabète de type 2 (Encadré 2) sont des maladies chroniques qui ont en commun un dysfonctionnement de l’homéostasie énergétique. L’obésité est caractérisée par un excès de masse grasse, donc une accumulation excessive de triglycérides dans le tissu adipeux. Cependant, tous les patients en situation d’obésité ne présentent pas de diabète de type 2. Il a été mis en évidence que, à indice de masse corporelle identique, le stockage de l’excès lipidique dans le tissu adipeux intra-abdominal (ou viscéral) augmente le risque de diabète de type 2 par rapport au stockage lipidique dans le tissu adipeux sous-cutané et sous-ombilical. Ainsi, si l’obésité constitue un facteur de risque pour le diabète de type 2 [2], les différents tissus adipeux ne sont pas identiques quant au risque de développer une résistance à l’insuline et une hyperglycémie chronique liées au dysfonctionnement des cellules β pancréatiques. L’excès de tissu adipeux viscéral est inflammatoire, de telle sorte que le risque de complications métaboliques est important lorsque le ratio entre tissu adipeux viscéral et tissu adipeux sous-cutané est élevé (ou, en pratique clinique, lorsque le rapport tour de taille/tour de hanche est élevé). La résistance à l’insuline constitue un mécanisme physiopathologique clé, à l’origine de maladies métaboliques et cardiovasculaires, qui se manifeste aussi bien dans les organes cibles de l’insuline, comme les muscles ou le foie, qu’au niveau cérébral [3]. Elle est provoquée, en grande partie, par la lipotoxicité des acides gras, qui, n’ayant pas pu être stockés complètement dans le tissu adipeux viscéral (aux capacités d’expansion limitées), vont s’accumuler dans le foie, les muscles et le pancréas (donc hors tissu adipeux). Cette accumulation dite « ectopique » de triglycérides dans le foie et les muscles squelettiques, ainsi que la libération de cytokines pro-inflammatoires à partir du tissu adipeux, est la base de la physiopathologie de la résistance à l’insuline et de la dérégulation de l’homéostasie énergétique, puis de l’hyperglycémie chronique, qui entraîne des facteurs aggravants comme la glucotoxicité.
1. L’obésité
Selon l’Organisation mondiale de la santé, le surpoids et l’obésité sont définis comme une accumulation excessive ou anormale de masse grasse représentant un risque pour la santé. Cette accumulation, qui est due au déséquilibre de la balance énergétique (baisse de l’activité physique et augmentation d’une alimentation hypercalorique), a des causes multiples, parmi lesquelles des causes socio-économiques. Ainsi, les départements les plus pauvres en France ont les taux d’obésité les plus élevés. Les causes de cette dérégulation nutritionnelle proviennent à la fois de troubles de la perception sensorielle des signaux externes (liés à l’environnement, au mode de vie et à leur apprentissage par l’expérience), de modifications des signaux internes (hormones, microbiote intestinal) et des prédispositions d’origine génétiques et épigénétiques. Même s’il n’est pas le seul, l’indice de masse corporelle (IMC) reste un outil généralisé de mesure du poids relatif, calculé en divisant le poids (kg) par la taille au carré (m²). Un IMC entre 25 et 30 kg/m² définit le surpoids, un IMC supérieur à 30 kg/m² correspond à une obésité, et un IMC supérieur à 40 kg/m² est considéré comme une obésité sévère. L’augmentation et la transformation du tissu adipeux consécutives au stockage de triglycérides, l’accumulation ectopique de ces lipides, et l’inflammation chronique de faible intensité peuvent entraîner le dysfonctionnement du pancréas, du foie, du cœur, mais aussi, très rapidement, du cerveau. Le diabète de type 2, l’hypertension, la dyslipidémie, les maladies cardiovasculaires, les accidents vasculaires cérébraux, l’apnée du sommeil, les maladies de la vésicule biliaire, la goutte, l’arthrose ainsi que plusieurs types de cancer figurent parmi les nombreuses comorbidités associées à l’obésité. Deux milliards d’adultes sont actuellement en surpoids, dont plus d’un milliard sont considérés comme étant en situation d’obésité [1]. Depuis 1975, le nombre de cas d’obésité a presque triplé à l’échelle planétaire (source OMS : https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight). En France, la série d’enquêtes Obépi-Roche, coordonnée par l’Inserm depuis 2012, révèle une hausse de la prévalence de l’obésité, atteignant 18 % de la population adulte en 2020 [68], soit environ 12 millions de personnes.
2. Le diabète de type 2
Le diabète de type 2, qui représente près de 90 % de tous les cas de diabète, est également connu sous les noms de diabète insulinorésistant, de diabète non insulinodépendant, ou de diabète de la maturité. Le surpoids et l’obésité sont les premiers facteurs de risque du diabète de type 2. Il se caractérise généralement par l’apparition d’une résistance à l’insuline entraînant, en cascade, une défaillance de la fonction des cellules bêta pancréatiques, une sécrétion d’insuline insuffisante, une altération fluctuante de la glycémie, puis une hyperglycémie chronique permanente. Le diabète de type 2 est une cause majeure de cécité, d’insuffisance rénale, d’infarctus du myocarde, d’accident vasculaire cérébral et d’amputation des membres inférieurs. En 2022, 880 millions de personnes souffraient de diabète de type 2 dans le monde (source OMS https://www.who.int/news-room/fact-sheets/detail/diabetes). Le diabète de type 2 est le plus souvent diagnostiqué chez les adultes, mais il est de plus en plus observé chez les enfants, les adolescents et les jeunes adultes en raison de la hausse des cas d’obésité juvénile. Les conséquences du diabète de type 2 sur la santé des plus jeunes sont bien plus dévastatrices que chez les adultes [69]. En France, la prévalence du diabète de type 2 est d’environ 6,3 % avec environ 4,3 millions de personnes atteintes de la maladie en 2025 (source : https://diabetesatlas.org/data-by-location/region/europe/).
Un dysfonctionnement du dialogue bidirectionnel entre le cerveau et les autres organes du corps est aussi une caractéristique commune à l’obésité et au diabète de type 2. En effet, la régulation cérébrale de l’homéostasie énergétique repose sur un large réseau neuronal, impliquant les systèmes sensoriels, le tronc cérébral, l’hypothalamus et les structures mésocorticolimbiques2, qui surveillent constamment le milieu interne grâce à la détection des nutriments et des hormones circulantes. Ces paramètres sont intégrés par le cerveau afin de générer des réponses adaptatives pour équilibrer le bilan énergétique en termes de prise alimentaire et de régulations endocriniennes (Figure 1) [4]. De nombreuses études cliniques ont montré une association entre obésité, diabète de type 2 et troubles neurologiques, incluant une atrophie de certaines régions cérébrales, une hypoactivité vasculaire et métabolique, ainsi qu’une prévalence de maladies neuro-évolutives, comme la maladie d’Alzheimer [5]. Les personnes en situation d’obésité présentent une sensibilité intéroceptive réduite aux signaux internes de faim et de satiété [6]. L’intéroception est la capacité cérébrale à évaluer les activités physiologiques de l’organisme par la détection et la régulation des états internes vitaux, comme, par exemple, la faim. Afin d’évaluer correctement le plaisir procuré par un aliment et les conséquences métaboliques de son ingestion, un long apprentissage est nécessaire, afin d’associer les caractéristiques sensorielles des aliments à leurs propriétés nutritionnelles [7]. Par conséquent, la perception des signaux sensoriels est essentielle pour déterminer si un aliment est appétissant, plus ou moins riche en calories, et donc s’il peut être nocif en excès. L’odorat est le premier et le plus important des sens pour prédire les caractéristiques des aliments, et il joue un rôle clé dans le choix et la consommation alimentaires [8]. La relation entre olfaction et prise alimentaire a été établie dès les années 1950, notamment par les travaux de Jacques Le Magnen au Collège de France [9], mais n’a été que récemment prise en compte dans le contexte des maladies métaboliques [10]. De fait, nous connaissons encore mal les conséquences de l’obésité et du diabète de type 2 sur le fonctionnement du système olfactif. Inversement, très peu de données existent sur l’implication du système olfactif dans la régulation active du métabolisme énergétique dans ces contextes physiopathologiques.
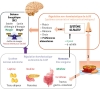 |
Figure 1 Régulation de la balance énergétique et olfaction. La balance énergétique est sous le contrôle de facteurs homéostatiques dépendant, notamment, de l’action des neurones glucosensibles de l’hypothalamus, des hormones anorexigènes comme la leptine, ou de la ghréline, l’hormone orexigène qui agit sur l’hypothalamus, et du système nerveux autonome, avec, par exemple, les afférences vagales du tractus gastro-intestinal dans le tronc cérébral. Les facteurs non homéostasiques, comme le plaisir, la mémoire et les informations sensorielles, également modulés par les hormones du métabolisme énergétique, jouent un rôle clé dans cette régulation. Les deux types de facteurs interagissent étroitement avec les préférences alimentaires et les activités olfactives induites par les odeurs alimentaires. |
La perception des odeurs
L’odorat constitue un système sensoriel vital pour l’être humain. Il permet la détection de signaux de danger, tels que les odeurs de brûlé ou les odeurs de nourriture avariée. Il renseigne également sur la qualité de la nourriture ingérée, son degré de palatabilité et participe à la flaveur, c’est-à-dire à une intégration cérébrale des informations issues des systèmes de chémodétection olfactive, gustative et trigéminale, liée à l’aliment, et qui est communément, et de façon réductrice, dénommée le goût en français. Les odeurs sont composées de petites molécules odorantes volatiles hydrophobes (à un poids moléculaire maximum de 350 g/mol), qui interagissent physiquement avec les récepteurs olfactifs, exprimés par les neurones de la muqueuse olfactive située au fond de la partie supérieure de la cavité nasale [11] (Figure 2). L’inspiration permet de capter les molécules odorantes volatiles et dissoutes dans l’air ambiant, et de les amener à la muqueuse olfactive par la voie orthonasale3, tandis que l’expiration permet aux molécules odorantes présentes dans la bouche (aussi dénommés arômes), et libérées par la mastication des aliments, d’atteindre les neurones olfactifs via la voie rétronasale, par l’arrière-bouche. On compte environ 400 types de récepteurs olfactifs (récepteurs couplés aux protéines G à sept domaines transmembranaires) différents chez l’humain, qui sont exprimés par 5 à 10 millions de neurones olfactifs. Le prix Nobel de médecine ou physiologie en 2004 a été décerné à Linda Buck et Richard Axel pour la découverte des gènes codant pour les récepteurs olfactifs chez les mammifères, qui constituent 2 à 3 % du répertoire total de gènes actifs. Chaque récepteur peut reconnaître plusieurs molécules, et chaque molécule odorante peut activer plusieurs récepteurs. Ainsi, la capacité de détection chez l’ être humain est extrêmement étendue en nombre de molécules, à quelques exceptions près, dont la plus notable est le monoxyde de carbone, qui n’est pas détecté par les êtres humains. Les projections axonales des neurones olfactifs traversent l’os crânien au niveau de la lame criblée de l’os ethmoïde4 pour atteindre le bulbe olfactif en formant le nerf olfactif (nerf crânien I). L’information olfactive est ensuite traitée par les cellules mitrales, qui sont des neurones pyramidaux du bulbe olfactif. Cette structure est la première à coder les odeurs chez les mammifères et forme en quelque sorte des cartes d’identité spatiotemporelles des molécules odorantes composant une odeur. Les cellules mitrales transmettent les informations olfactives vers les nombreuses régions cérébrales du cortex olfactif primaire. Ces régions peuvent être regroupées en systèmes : le système limbique pour la mémoire, les émotions et les connexions au corps (cortex entorhinal, hypothalamus, noyau septal médian et amygdale [12]), et le système hédonique pour la régulation du plaisir et de la récompense (tubercule olfactif, puis noyau accumbens). Le cortex piriforme est au centre du cortex olfactif primaire et contient la majorité des efférences du bulbe olfactif. Il projette à son tour massivement sur des cortex impliqués dans la perception multisensorielle, hédonique et décisionnelle (cortex insulaire, cingulaire antérieur et orbitofrontal) [13] (→).
(→) Voir m/s n° 8-9, 2011, page 687
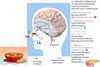 |
Figure 2 La perception olfactive. Les quatre premières étapes de la perception et de l’intégration olfactive sont similaires chez les êtres humains et les rongeurs. Quand la nourriture est en bouche (1.b.), la stimulation olfactive se fait également par la voie rétronasale, ce qui explique l’importance de l’olfaction dans le goût (flaveur). À l’étape 5, l’activation du système olfactif par les odeurs alimentaires induit une augmentation de l’insuline pancréatique chez la souris. |
Le relais thalamique, qui sert de filtre sensoriel, est présent dans toutes les modalités sensorielles, excepté le système olfactif, où le bulbe olfactif projette directement sur les structures du cortex olfactif primaire. Ainsi, les connexions anatomiques denses et directes avec le système limbique, toutes bilatérales, confèrent une organisation unique aux circuits olfactifs, expliquant pourquoi l’odorat est si fortement lié aux émotions et possède un pouvoir évocateur vivace caractérisé par une mémoire robuste et durable [14].
Plusieurs maladies peuvent altérer le sens de l’odorat, partiellement (l’hyposmie) ou totalement (l’anosmie). En France, on estime à 17 % la part de la population souffrant de troubles olfactifs causés majoritairement par des problèmes ORL (polyposes, sinusites chroniques, allergies, infections virales…) et des traumas crâniens [15]. De plus, 5 % de la population présente une olfaction très altérée. Le nombre de sujets hyposmiques augmente massivement avec l’âge (on parle alors de presbyosmie) : plus de 50 % des personnes âgées de 65 à 80 ans montrent des signes de déficience olfactive [16]. En France, l’association « Anosmie.org » regroupe des bénévoles et des patients souffrant de troubles olfactifs ainsi que des médecins ORL et des scientifiques afin d’assurer un accompagnement et une information sur les avancées biomédicales sur les troubles olfactifs. Les patients hyposmiques ou anosmiques souffrent d’un handicap sensoriel invisible et témoignent d’une altération sévère de leur qualité de vie, avec une insécurité constante (coupure des signaux de danger) et un effondrement hédonique (alimentation, libido). Ils sont fortement à risque de développer des troubles de l’humeur (dépression) [17]. Contrairement à l’Allemagne ou à la Suisse, le ministère de la Santé en France ne reconnaît pas l’anosmie comme un handicap.
Physiopathologie des interrégulations entre olfaction et prise alimentaire chez l’être humain
L’implication de l’odorat dans la prise alimentaire suit trois phases : une phase d’anticipation préprandiale qualifiée de céphalique, car uniquement dépendante du cerveau ; une phase d’exécution avec l’ingestion des aliments ; et une phase de consolidation avec la formation des préférences olfactives et alimentaires qui vont influencer la première phase (Figure 3).
 |
Figure 3 Interrégulations entre olfaction et prise alimentaire. Elles se résument en trois phases principales : préparation à jeun (phase céphalique), exécution (mastication et ingestion), et mémorisation à satiété (construction des préférences olfactives et alimentaires). Ces phases tournent en boucle au quotidien, elles s’influencent les unes avec les autres, et elles sont modulées par le contexte socio-culturel. |
Pendant ces trois phases, le système olfactif et les circuits de régulation de la prise alimentaire interagissent de façon bidirectionnelle. D’une part, les états métaboliques de l’organisme modulent la sensibilité et le traitement des informations olfactives : à jeun, la perception des odeurs est amplifiée, tandis qu’elle est réduite, en état de satiété, un mécanisme dénommé « alliesthésie », témoignant d’une forte influence de l’état interne de l’organisme sur l’acuité sensorielle [18]. Cette modulation repose sur l’action de plusieurs signaux hormonaux périphériques : la ghréline, hormone orexigène5 produite par l’estomac en période de jeûne, augmente l’activité neuronale dans la muqueuse olfactive, le bulbe olfactif et le cortex piriforme, renforçant ainsi la perception des stimuli olfactifs [19] ; la leptine, hormone anorexigène sécrétée par le tissu adipeux, exerce un effet inhibiteur sur l’activité neuronale du système olfactif, réduisant ainsi la sensibilité aux odeurs alimentaires [20]. Les neurones du système olfactif expriment des récepteurs pour l’ensemble des hormones régulant l’homéostasie énergétique [21], notamment pour le GLP-1 (glucagon-like peptide-1) (Encadré 3). D’autre part, la perception des signaux olfactifs exerce une influence directe sur le comportement alimentaire. L’exposition à des odeurs alimentaires agréables est capable d’activer les circuits neuronaux de la récompense [22], de réguler la prise alimentaire par le système des endocannabinoïdes, qui modulent l’activité du bulbe olfactif [23], et même de stimuler la phase céphalique de libération d’insuline via le bulbe olfactif [24] (une réponse préprandiale purement liée à des stimulations sensorielles du cerveau, voir détails dans la dernière partie de cet article). L’activité olfactive permet donc d’ajuster le comportement alimentaire aux besoins énergétiques de l’organisme. Toutefois, dans le contexte de l’obésité ou du diabète de type 2, ce système de régulation est altéré. Des travaux récents ont, en effet, mis en évidence une hypoacuité olfactive chez les individus obèses ou diabétiques [25], des modifications de la connectivité fonctionnelle entre les structures olfactives et les régions cérébrales impliquées dans la récompense et la motivation [26], et une augmentation de l’attrait de ces sujets pour les aliments hypercaloriques, indépendamment des signaux de satiété [27]. Ces dysfonctionnements pourraient contribuer au maintien ou à l’aggravation des troubles métaboliques en renforçant les comportements alimentaires inadaptés aux besoins énergétiques de l’individu.
3. GLP-1
Le GLP-1 (glucagon-like peptide 1) est une hormone de 30 acides aminés, découverte en 1983, qui dérive du clivage du préproglucagon (PPG), produit par le gène GCG, qui est exprimé dans le pancréas, l’intestin et le cerveau [70]. Le GLP-1 fait partie de la famille des incrétines, hormones sécrétées par les intestins dans la veine porte, en réponse à l’ingestion de nourriture et à l’absorption de glucose. Sa découverte a permis d’apporter un complément thérapeutique pour le traitement du diabète de type 2.
Les bénéfices du GLP-1 sont liés aux régulations physiologiques qu’il induit : renforcement de la sécrétion d’insuline stimulée par le glucose (GSIS pour glucose-stimulated insulin secretion), réduction de la vidange gastrique, inhibition de la prise alimentaire, protection des systèmes cardio-vasculaire et nerveux grâce à la réduction de l’inflammation et de l’apoptose. Dans le pancréas, le GLP-1 favorise la fonction et la croissance des cellules bêta en augmentant la GSIS, contribuant ainsi à abaisser la glycémie postprandiale [70]. De plus, il promeut la survie des cellules bêta et inhibe la sécrétion de glucagon par les cellules alpha du pancréas. Il est à noter qu’il n’existe pas de résistance au GLP-1 contrairement à d’autres hormones régulant l’homéostasie énergétique.
Les incrétinomimétiques sont des dérivés injectables de GLP-1, à action prolongée, qui sont résistants à l’action de la dipeptidylpeptidase-4 (DDP4), l’enzyme de dégradation sérique et tissulaire des incrétines. Plusieurs représentants de cette classe pharmacologique sont disponibles, dont les deux principaux à administration hebdomadaire sont le sémaglutide (laboratoire NovoNordisk, Ozempic®) et le dulaglutide (laboratoire Lilly, Trulicity®). Du fait d’effets digestifs parfois gênants, mais le plus souvent transitoires, ils sont administrés une fois par semaine à dose progressivement croissante, par paliers de 1 mois ou plus. L’injection hebdomadaire de ces molécules constitue une grande avancée dans le confort des patients par rapport à l’injection quotidienne de précédents incrétinomimétiques, comme le liraglutide (laboratoire NovoNordisk, Victoza®). En France, les incrétinomimétiques ne sont pris en charge par l’assurance maladie que dans le cadre de la prise en charge du diabète de type 2, et non pour celle de l’obésité sans diabète. Ces molécules sont utilisées en complément de modifications du mode de vie (régime alimentaire et activité physique), et, en seconde intention, après l’utilisation de la metformine et en association possible avec d’autres hypoglycémiants. Quelques études en vie réelle ont été récemment publiées pour le sémaglutide. L’arrêt du traitement concerne plus de la moitié des patients traités pendant la première année d’utilisation pour cause de nausées et/ou de troubles du transit [71]. Dans la même étude, il est noté que les patients qui arrêtent leur traitement au bout de deux ans ont un effet rebond avec reprise pondérale, ce qui pose la question de la nécessité d’un traitement chronique. Aux États-Unis, le traitement médicamenteux par incrétinomimétiques injectables provoque des pertes de poids qui restent inférieures à celles obtenues avec la chirurgie bariatrique [72]. Néanmoins, l’avènement des doubles agonistes GLP-1/GIP (laboratoire Lilly, Tirzepatide®) pourrait induire les mêmes réductions de poids que ce type de chirurgie, comme le montrent déjà les essais cliniques en cours [73] (→).
(→) Voir m/s n° 11, 2024, page 837
Le GLP-1 diminue l’appétit, contribuant ainsi à la régulation du poids, mais les régions cibles permettant cet effet anorexique sont mal définies, même si les structures aux populations neuronales exprimant le récepteur GLP-1R comme l’hypothalamus, le noyau du tractus solitaire, et le bulbe olfactif sont des cibles actuellement étudiées. Il a aussi un rôle de neuroprotection dans les maladies neurodégénératives [74] : il est probable que le GLP-1 agisse par des effets anti-inflammatoires et antioxydants dans le cerveau, notamment sur les vaisseaux sanguins [75], et préserve ainsi l’apprentissage et la mémoire. La synthèse intracérébrale de GLP-1 a récemment été caractérisée chez la souris, mais elle existe très probablement chez l’être humain où les transcrits PPG ont été détectés [76]. Cette synthèse neuronale locale est cruciale, puisque c’est la molécule exprimée in situ, au niveau du noyau du tractus solitaire, qui régule les circuits de la satiété et non pas l’entrée de l’hormone circulant à travers la barrière hématoencéphalique (la demi-vie dans le sang est de 2 min). Il en est de même pour les actions bénéfiques du GLP-1, produit dans le bulbe olfactif, sur le métabolisme énergétique (voir le paragraphe dans le corps du texte).
La corrélation entre l’indice de masse corporelle, la chirurgie bariatrique et l’olfaction a fait l’objet de plusieurs études. Les sujets présentant une obésité sévère sont plus susceptibles d’avoir une altération olfactive que les individus modérément obèses, et l’élévation de l’indice de masse corporelle est significativement associée à une augmentation des seuils olfactifs [28]. Dans le cas de la chirurgie bariatrique (sleeve gastrectomie [SG] et bypass gastrique, selon la méthode du Roux-en-Y [RYGBP]), il est intéressant de noter que, si les sujets en obésité sévère ont une sensibilité olfactive très réduite ou inexistante, une hypersensibilité olfactive conduisant à des aversions alimentaires a été au contraire observée en période postopératoire, notamment chez les patients ayant perdu le plus de poids. Melis et al. ont montré une amélioration de l’odorat et du goût après RYGBP et SG, avec une grande majorité d’aversions olfactives post-chirurgie [29].
Un dysfonctionnement olfactif dans le diabète de type 2 a été rapporté dès le début des années 1960 [30]. En comparaison avec une population contrôle normosmique6, les patients en situation d’obésité et atteints de diabète de type 2 sans autre complication médicale, ont des déficits olfactifs [31] qui sont, cependant, moins marqués que ceux observés chez des patients qui cumulent d’autres complications avec le diabète (rétinopathie, neuropathie, hypertension…) [32]. Le déclin cognitif lié au diabète de type 2 est 50 % plus rapide que celui lié au vieillissement cognitif normal [33], et une méta-analyse a montré que ces patients présentent une diminution de leur mémoire épisodique7 et des fonctions exécutives, comme la mémoire de travail [34]. Chez les populations âgées de 68 à 77 ans, une altération de l’olfaction chez les patients souffrant de diabète de type 2 a été associée à un déclin cognitif [35]. Plusieurs articles confirment cette bascule vers des troubles cognitifs en cas de baisse de l’acuité olfactive chez les sujets souffrant de diabète de type 2 [36, 37].
Enfin, la nature même des odeurs alimentaires influence les choix de prise alimentaire chez les sujets obèses. Stafford et Welbeck ont observé que des personnes en situation d’obésité présentent une sensibilité accrue et une préférence marquée pour les odeurs associées à des aliments plaisants et riches en énergie [38]. Il pourrait donc exister une dysrégulation de la modulation centrale de la sensibilité olfactive chez les individus en situation d’obésité, avec une plus grande sensibilité aux odeurs à forte valeur hédonique (jugées comme plaisantes), telles que l’odeur du chocolat [39]. Dans ce sens, Trellakis et al. ont montré que l’appréciation hédonique d’une odeur généralement peu appréciée était significativement plus faible chez les sujets obèses que chez les sujets non obèses (dans la tranche d’âge 20 à 45 ans) [40]. Enfin, l’attention que les sujets obèses vont porter aux aliments est régulée en partie par des signaux olfactifs traités de façon non consciente [41].
Plasticité olfactive dans les modèles précliniques de l’obésité
Bien que la majorité des connaissances sur les altérations de l’olfaction dans l’obésité et le diabète de type 2 ait été acquise chez l’être humain, des modèles animaux sont nécessaires pour en décrypter les mécanismes. Les modèles d’obésité induite par l’alimentation (DIO pour diet-induced obesity) sont considérés comme les plus pertinents pour reproduire l’aspect multidimensionnel de l’obésité humaine, car ils combinent des facteurs génétiques et environnementaux. Ils reposent sur le fait que, chez les rongeurs, comme chez l’être humain, la consommation d’aliments, enrichis en graisses et sucres à des pourcentages variables, est positivement corrélée à la prise de poids corporel et à l’augmentation des taux plasmatiques de glucose, cholestérol, triglycérides, acides gras libres et leptine.
De nombreuses altérations des performances olfactives ont été observées dans les modèles DIO chez les rongeurs. Des tests comportementaux montrent que les souris sous régime hyperlipidique présentent de moins bonnes performances olfactives que des souris témoins normopondérées [42]. Les souris dont le régime obésogène est enrichi à la fois en lipides et glucides sont affectées plus précocement que celles soumises à un régime hyperlipidique seul. Ainsi, Takase et al. montrent un impact plus fort sur les processus cognitifs lié à la sollicitation chronique du métabolisme glucidique [43]. De manière surprenante, dans la même étude, une déficience similaire a été observée chez des souris recevant exactement le même régime riche en graisses, composé d’acides gras saturés, mais en quantité ajustée chaque jour pour maintenir un poids corporel équivalent à celui du groupe témoin nourri au régime standard. Cela signifie que des souris non obèses et non-diabétiques consommant de faibles quantités de graisses saturées présentent également des déficits olfactifs.
Les observations chez le rat vont dans le même sens. Lacroix et al. ont observé une diminution du comportement d’exploration olfactive chez des rats Sprague-Dawley obèses, nourris avec un régime riche en graisses et en sucres, comparés aux rats résistants à l’obésité nourris avec un régime standard [44]. Chez les rongeurs témoins, la durée d’exploration d’une odeur alimentaire est plus longue lorsqu’ils sont à jeun que lorsqu’ils sont rassasiés. Cependant, cette différence, selon le statut métabolique, est largement diminuée chez les animaux obèses, qui passent moins de temps à explorer une odeur alimentaire lorsqu’ils sont à jeun, comparés aux témoins [44].
En résumé, ces données sont en accord avec les résultats acquis chez l’être humain montrant que les altérations métaboliques ont un impact négatif sur les performances olfactives. De plus, le choix et le type de l’odeur (alimentaire ou neutre) peuvent affecter les résultats des tests, comme cela a également été observé chez l’être humain. L’utilisation d’aliments précisément contrôlés chez les rongeurs suggère que le contenu énergétique de l’alimentation (notamment des quantités d’acides gras saturés et de sucre), qui est directement lié à la qualité alimentaire, est en soi un facteur majeur contribuant aux déficits olfactifs, indépendamment de la masse corporelle ou de l’accumulation de graisse.
Étiologie des problèmes olfactifs détectés dans l’obésité et le diabète de type 2
L’insuline
L’élévation de la glycémie et la résistance à l’insuline, observées au cours de l’obésité, peuvent induire un diabète de type 2. L’insuline et ses récepteurs (InsR), ainsi que le transporteur de glucose dépendant de l’insuline GLUT4 (glucose transporter 4), sont présents dans la muqueuse olfactive, jusqu’au cortex piriforme [45]. Les neurones du bulbe olfactif expriment GLUT4 qui est co-localisé avec les InsR [46] (à noter que les neurones du thalamus expriment et fonctionnent majoritairement avec GLUT2). Le bulbe olfactif est la région du cerveau qui contient la plus forte concentration d’insuline et le plus grand nombre en densité de ses récepteurs InsR [46] : le transport de l’insuline à travers la barrière hématoencéphalique au niveau du bulbe olfactif est deux à huit fois plus rapide que dans d’autres régions du cerveau [47]. En mesurant la concentration de glucose dans le liquide extracellulaire du bulbe olfactif de rats Zucker déficients en récepteurs à la leptine (fa/fa), Aimé et al. ont montré que le bulbe olfactif contient deux fois plus de glucose que le cortex [48]. Dans ces deux régions cérébrales, les concentrations de glucose sont deux fois plus élevées chez les rats obèses fa/fa que chez les rats témoins. Enfin, les cellules mitrales du bulbe olfactif répondent aux changements de concentration en glucose [49] et expriment des marqueurs moléculaires typiques des cellules sensibles au glucose [46], faisant d’elles des équivalents des neurones glucosensibles de l’hypothalamus, du tronc cérébral ou du thalamus. Ces données montrent clairement que le bulbe olfactif remplit une double fonction : coder des informations vitales concernant les odeurs alimentaires et détecter le statut métabolique de l’organisme [47].
Chez les rats Sprague-Dawley obèses nourris avec un régime riche en graisses et en sucre, le nombre d’InsR dans le bulbe olfactif est diminué [44]. Cependant, la résistance à l’insuline chez les souris DIO pourrait également s’expliquer par les propriétés physiologiques des cellules mitrales. Chez les souris témoins, l’application d’insuline augmente l’excitabilité des cellules mitrales, mais chez les animaux DIO, la décharge spontanée de ces cellules est altérée. Dans ce contexte, la stimulation aiguë par l’insuline diminue l’amplitude de la modulation des cellules mitrales comparativement à celle observée chez les témoins [50].
Côté clinique, chez des femmes âgées de 18-35 ans, Poessel et al. ont mesuré la sensibilité à l’insuline après un repas et ont constaté que la résistance à l’insuline était négativement corrélée à la perception des odeurs alimentaires (chocolat), indépendamment de l’indice de masse corporelle [51]. Chez les personnes âgées de plus de 50 ans, il a été montré que la résistance à l’insuline (mais pas la glycémie à jeun, l’hémoglobine glyquée ou les niveaux d’insuline sérique) est associée à un risque accru de troubles olfactifs [52]. Chez les modèles murins, une administration prolongée d’insuline par voie intranasale n’affecte pas le comportement olfactif, la dépense énergétique ou la reconnaissance d’objets [53], alors que, chez l’être humain, une administration intranasale d’insuline augmente le seuil de détection olfactive et de la perception [54].
L’inflammation
Dans l’obésité, un excès calorique chronique entraîne une accumulation de masse grasse ectopique déclenchant la sécrétion d’adipokines pro-inflammatoires qui favorisent des cascades inflammatoires. Ce type d’inflammation, dite de bas grade, entraîne des effets délétères et précoces dans le cerveau. Ainsi, la fonction olfactive est altérée chez les patients en situation d’obésité (avec ou sans diabète de type 2 [55]), chez les patients diabétiques non obèses [56], mais aussi chez des souris non obèses et non-diabétiques nourries avec de faibles quantités de graisses saturées [42]. Les mécanismes inflammatoires cérébraux sont très probablement les premiers événements pathologiques majeurs susceptibles d’altérer le système olfactif dans ces différents contextes métaboliques. Il est à noter qu’une inflammation induite rapidement par un régime riche en graisses suffit également à diminuer la sensibilité à l’insuline chez des rats non obèses et non diabétiques [57]. Une dérégulation cérébrovasculaire pourrait aussi être à l’origine d’un dysfonctionnement sensoriel dans l’obésité [58]. Nous avons étudié les profils hémodynamiques au repos et lors de stimulations sensorielles dans le bulbe olfactif de souris nourries pendant trois et huit mois avec un régime riche en graisses, par imagerie optique [59] et par ultrasons [60]. Nous avons observé que les variations relatives du flux sanguin cérébral lors de la stimulation sensorielle étaient altérées chez les souris obèses comparées aux souris témoins. Dans le bulbe olfactif, cette altération était indépendante de la densité des vaisseaux sanguins, un paramètre inchangé par le régime, mais semblait liée à l’impact de la résistance à l’insuline et à celui de l’inflammation sur le couplage neurovasculaire. Chez l’être humain, une réduction du volume du bulbe olfactif a déjà été observée dans des maladies associées à des dysfonctionnements olfactives, telles que la maladie de Parkinson, la maladie d’Alzheimer, la schizophrénie et la dépression [61]. Comme chez l’animal, une altération de la fonction olfactive périphérique peut entraîner une réduction du volume du bulbe olfactif, associée à une baisse des performances olfactives [62]. Ainsi, grâce à des mesures volumétriques par imagerie par résonance magnétique (IRM) chez l’être humain, des études ont mis en évidence une corrélation entre le volume du bulbe olfactif et les fonctions olfactives, y compris le seuil de détection, la discrimination et l’identification des odeurs [63]. Poessel et al. ont montré une corrélation négative entre la taille du bulbe olfactif et plusieurs paramètres métaboliques, tels que l’indice HOMA-IR (homeostasis model assessment for insulin resistance)8, les taux plasmatiques de leptine, et le pourcentage de masse grasse corporelle [64].
Pour résumer, les sujets obèses présentent des anomalies du traitement neuronal de l’information olfactive, qui n’informe plus correctement les systèmes limbiques, hédoniques, attentionnels et motivationnels, en lien avec la prise alimentaire.
Le rôle du GLP-1 dans le bulbe olfactif et dans la régulation d’un nouvel axe neurométabolique entre le bulbe olfactif et le pancréas
Les récepteurs du GLP-1 (GLP-1R) sont exprimés par les cellules mitrales du bulbe olfactif chez la souris, et une population spécifique d’interneurones de cette structure a été identifiée comme produisant le peptide précurseur du GLP-1, le préproglucagon (PPG) [65]. L’application de GLP-1 sur des tranches de bulbe olfactif montre une forte activation des cellules mitrales. Dans notre laboratoire, nous avons étudié, chez des souris DIO, comparées à des souris normopondérées, le rôle fonctionnel du système de signalisation du GLP-1 au sein du bulbe olfactif dans la régulation de l’ homéostasie énergétique, en postulant qu’il s’agit d’une nouvelle voie de communication avec la périphérie.
La phase céphalique est caractérisée par des mécanismes préprandiaux (augmentation de la salivation, de la sécrétion gastrique et de la motilité intestinale) qui préparent l’organisme à la surcharge énergétique liée à l’ingestion d’un repas [66]. Parmi ces réponses, la phase céphalique de libération d’insuline est définie, à jeun, comme précédant la prise alimentaire (d’environ 10 min), lorsque les récepteurs sensoriels visuels et olfactifs sont stimulés par des stimuli alimentaires. Le rôle de cette réponse insulinique sur la régulation glucidique postprandiale et les conséquences de son dysfonctionnement ne sont pas encore compris dans le contexte de l’obésité et du diabète de type 2. Nous avons soumis les souris témoins et les souris obèses à une période d’habituation à une odeur donnée, annonçant la présentation d’un cookie palatable aromatisé avec la même odeur. Nous avons ensuite stimulé par cette odeur alimentaire les souris à jeun. Dans ces conditions, une phase céphalique de libération d’insuline plasmatique a été observée chez les souris témoins, mais pas chez les souris DIO. La réduction de l’expression des ARNm de PPG dans le bulbe olfactif, par une stratégie de shRNA (short hairpin-RNA), a entraîné une diminution de l’amplitude de la phase céphalique de libération d’insuline chez les souris témoins. De plus, l’injection d’un antagoniste du GLP-1R, l’exendine-9, dans le bulbe olfactif des souris témoins a induit la suppression de la phase céphalique de libération d’insuline provoquée par une odeur alimentaire. La phase céphalique de libération d’insuline étant dépendante chez l’être humain de l’activation du système nerveux autonome parasympathique libérant de l’acétylcholine [66], nous avons injecté, par voie intrapéritonéale aux souris normopondérées, un antagoniste des récepteurs muscariniques M3 (exprimés par les cellules bêta pancréatiques murines), avant l’induction de la phase céphalique de libération d’insuline par une odeur alimentaire. Cette intervention pharmacologique a inhibé la phase céphalique de libération d’insuline, confirmant une régulation parasympathique de la libération d’insuline en aval des circuits cérébraux liés à l’olfaction. Il est important de noter que l’administration d’exendine-4, un agoniste du récepteur au GLP-1, permet de restaurer les comportements olfactifs de recherche de nourriture chez les souris obèses. Ces résultats indiquent que la signalisation GLP-1/GLP-1R dans le bulbe olfactif est essentielle pour l’induction d’une phase céphalique de libération d’insuline par les odeurs alimentaires à jeun et intervient dans la régulation de la fonction olfactive [24].
Plus récemment, nous avons démontré que l’activation du GLP-1R du bulbe olfactif augmente la sécrétion d’insuline en réponse à un test oral de tolérance au glucose, à la fois chez les souris témoins et chez les souris obèses, soit par injection dans le bulbe olfactif d’exendine-4, soit par activation chémogénétique (Gq-DREADD)9 des neurones GLP-1R+ chez les souris obèses, ou par inhibition chémogénétique (Gi-DREADD) des neurones GLP-1R+ chez les souris témoins. Notamment, l’activation des GLP-1R permet une récupération de la tolérance au glucose chez les souris obèses, et elle est associée à une réduction des niveaux de noradrénaline pancréatique. Elle est bloquée par l’administration d’un agoniste des récepteurs α2-adrénergiques, ce qui implique une inhibition du système nerveux sympathique dans cette régulation. De plus, nous avons identifié la levée d’inhibition sur les récepteurs GABA-A, dans le noyau paraventriculaire de l’hypothalamus, comme un relais critique dans cette voie issue du bulbe olfactif. L’ensemble de nos résultats révèle que la signalisation du GLP-1 dans le bulbe olfactif engage, par un relais hypothalamique dans le noyau paraventriculaire et un mécanisme de levée d’inhibition, un mécanisme neural descendant régulant la sécrétion d’insuline via le système nerveux sympathique [67] (Figure 4).
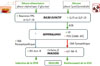 |
Figure 4 Augmentation de l’insulinémie pendant la phase CPIR (cephalic phase of insulin release) et de GSIS (glucose stimulated insulin secretion), par l’activation d’une voie neurométabolique reliant le bulbe olfactif, l’hypothalamus et le pancréas. Sigles (de haut en bas) : PPG (préproglucagon) ; AON (anterior olfactory nucleus) ; LH (lateral hypothalamus) ; PVN (paraventricular nucleus) ; SNA (système nerveux autonome) ; M3-Ach-R (récepteurs muscariniques de type 3) ; α2-NA-R (récepteurs noradrénergiques de type α2). |
Conclusion
L’ensemble de nos travaux démontre un rôle jusqu’alors méconnu de la signalisation GLP-1/GLP-1R dans le bulbe olfactif, dans le contrôle central de la perception, de la prise alimentaire et de l’homéostasie énergétique. La caractérisation d’une nouvelle voie neurométabolique reliant le bulbe olfactif au pancréas, qui permet une augmentation de la libération de l’insuline, pourrait ouvrir la voie à de nouvelles thérapeutiques innovantes pour la prise en charge de l’obésité et du diabète de type 2, par exemple par des injections intranasales de composés incrétinomimétiques10 (comme il est possible de le faire avec l’insuline intranasale [54]).
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Phelps NH, Singleton RK, Zhou B, et al. Worldwide trends in underweight and obesity from 1990 to 2022: a pooled analysis of 3663 population-representative studies with 222 million children, adolescents, and adults. Lancet 2024 ; 403 : 1027–50. [Google Scholar]
- Chatterjee S, Khunti K, Davies MJ. Type 2 diabetes. Lancet 2017 ; 389 : 2239–51. [CrossRef] [PubMed] [Google Scholar]
- Chen W, Kullmann S, Rhea EM. Expanding the understanding of insulin resistance in brain and periphery. Trends Endocrinol Metab 2025 ; 37 : 17–30. [Google Scholar]
- Berthoud H-R. Mind versus metabolism in the control of food intake and energy balance. Physiol Behav 2004 ; 81 : 781–93. [Google Scholar]
- Mattson MP. An Evolutionary perspective on why food overconsumption impairs cognition. Trends Cogn Sci 2019 ; 23 : 200–12. [Google Scholar]
- Herbert BM, Pollatos O. Attenuated interoceptive sensitivity in overweight and obese individuals. Eat Behav 2014 ; 15 : 445–8. [Google Scholar]
- Saper CB, Chou TC, Elmquist JK. The need to feed: homeostatic and hedonic control of eating. Neuron 2002 ; 36 : 199–211. [Google Scholar]
- Boesveldt S, Graaf K de. The differential role of smell and taste for eating behavior. Perception 2017 ; 46 : 307–19. [Google Scholar]
- Le Magnen J. My scientific life: 40 years at the College de France. Neurosci Biobehav Rev 2001 ; 25 : 375–94. [Google Scholar]
- Yeomans MR. Olfactory influences on appetite and satiety in humans. Physiol Behav 2006 ; 89 : 10–4. [Google Scholar]
- Firestein S. How the olfactory system makes sense of scents. Nature 2001 ; 413 : 211–8. [Google Scholar]
- Price JL. Beyond the primary olfactory cortex: Olfactory-related areas in the neocortex, thalamus and hypothalamus. Chemical Senses 1985 ; 10 : 239–58. [Google Scholar]
- Lepousez G, Gheusi G. Olfaction : quand le cortex redistribue les cartes. Med Sci (Paris) 2011 ; 27 : 687–9. [Google Scholar]
- Gottfried JA. Smell: central nervous processing. Adv Otorhinolaryngol 2006 ; 63 : 44–69. [Google Scholar]
- Manesse C, Ferdenzi C, Mantel M, et al. The prevalence of olfactory deficits and their effects on eating behavior from childhood to old age: A large-scale study in the French population. Food Quality and Preference 2021 ; 93 : 104273. [Google Scholar]
- Landis BN, Konnerth CG, Hummel T. A study on the frequency of olfactory dysfunction. Laryngoscope 2004 ; 114 : 1764–9. [Google Scholar]
- Sabiniewicz A, Hoffmann L, Haehner A, et al. Symptoms of depression change with olfactory function. Sci Rep 2022 ; 12 : 5656. [Google Scholar]
- Albrecht J, Schreder T, Kleemann AM, et al. Olfactory detection thresholds and pleasantness of a food-related and a non-food odour in hunger and satiety. Rhinology 2009 ; 47 : 160–5. [Google Scholar]
- Stark R, Dempsey H, Kleeman E, et al. Hunger signalling in the olfactory bulb primes exploration, food-seeking and peripheral metabolism. Mol Metab 2024 ; 89 : 102025. [Google Scholar]
- Julliard AK, Chaput MA, Apelbaum A, et al. Changes in rat olfactory detection performance induced by orexin and leptin mimicking fasting and satiation. Behav Brain Res 2007 ; 183 : 123–9. [Google Scholar]
- Palouzier-Paulignan B, Lacroix M-C, Aimé P, et al. Olfaction under metabolic influences. Chem Senses 2012 ; 37 : 769–97. [Google Scholar]
- Sorokowska A, Schoen K, Hummel C, et al. Food-related odors activate dopaminergic brain areas. Front Hum Neurosci 2017 ; 11 : 625. [Google Scholar]
- Soria-Gómez E, Bellocchio L, Reguero L, et al. The endocannabinoid system controls food intake via olfactory processes. Nat Neurosci 2014 ; 17 : 407–15. [Google Scholar]
- Montaner M, Denom J, Jiang W, et al. The local GLP-1 system in the olfactory bulb is required for odor-evoked cephalic phase of insulin release in mice. Mol Metab 2023 ; 73 : 101738. [Google Scholar]
- Fernandez-Garcia JC, Alcaide J, Santiago-Fernandez C, et al. An increase in visceral fat is associated with a decrease in the taste and olfactory capacity. PLOS ONE 2017 ; 12 : e0171204. [Google Scholar]
- Zhang Z, Liu Q, Wen P, et al. Activation of the dopaminergic pathway from VTA to the medial olfactory tubercle generates odor-preference and reward. Elife 2017 ; 6 : e25423. [Google Scholar]
- Martin LE, Holsen LM, Chambers RJ, et al. Neural mechanisms associated with food motivation in obese and healthy weight adults. Obesity (Silver Spring) 2010 ; 18 : 254–60. [Google Scholar]
- Peng M, Coutts D, Wang T, et al. Systematic review of olfactory shifts related to obesity. Obes Rev 2019 ; 20 : 325–338. [Google Scholar]
- Melis M, Pintus S, Mastinu M, et al. Changes of taste, smell and eating behavior in patients undergoing bariatric surgery: associations with prop phenotypes and polymorphisms in the odorant-binding protein OBPIIa and CD36 receptor genes. Nutrients 2021 ; 13 : 250. [Google Scholar]
- Jorgensen MB, Buch NH. Studies on the sense of smell and taste in diabetics. Acta Otolaryngol 1961 ; 53 : 539–45. [Google Scholar]
- Naka A, Riedl M, Luger A, et al. Clinical significance of smell and taste disorders in patients with diabetes mellitus. Eur Arch Otorhinolaryngol 2010 ; 267 : 547–50. [Google Scholar]
- Yazla S, Özmen S, Kıyıcı S, et al. Evaluation of olfaction and taste function in type 2 diabetic patients with and without peripheral neuropathy. Diabetes Metab Res Rev 2018 ; 34. [Google Scholar]
- Biessels GJ, Despa F. Cognitive decline and dementia in diabetes mellitus: mechanisms and clinical implications. Nat Rev Endocrinol 2018 ; 14 : 591–604. [Google Scholar]
- Sadanand S, Balachandar R, Bharath S. Memory and executive functions in persons with type 2 diabetes: a meta-analysis. Diabetes Metab Res Rev 2016 ; 32 : 132–42. [Google Scholar]
- Sanke H, Mita T, Yoshii H, et al. Olfactory dysfunction predicts the development of dementia in older patients with type 2 diabetes. Diabetes Res Clin Pract 2021 ; 174 : 108740. [Google Scholar]
- Zhang Z, Zhang B, Wang X, et al. Altered odor-induced brain activity as an early manifestation of cognitive decline in patients with type 2 diabetes. Diabetes 2018 ; 67 : 994–1006. [Google Scholar]
- Chen M, Wang J, Zhou S, et al. Brain structure as a correlate of odor identification and cognition in type 2 diabetes. Front Hum Neurosci 2022 ; 16 : 773309. [Google Scholar]
- Stafford LD, Welbeck K. High hunger state increases olfactory sensitivity to neutral but not food odors. Chem Senses 2011 ; 36 : 189–98. [Google Scholar]
- Stafford LD, Whittle A. Obese individuals have higher preference and sensitivity to odor of chocolate. Chem Senses 2015 ; 40 : 279–84. [Google Scholar]
- Trellakis S, Tagay S, Fischer C, et al. Ghrelin, leptin and adiponectin as possible predictors of the hedonic value of odors. Regul Pept 2011 ; 167 : 112–7. [Google Scholar]
- Mas M, Brindisi M-C, Chabanet C, et al. Implicit food odour priming effects on reactivity and inhibitory control towards foods. PLoS One 2020 ; 15 : e0228830. [Google Scholar]
- Lietzau G, Nyström T, Wang Z, et al. Western diet accelerates the impairment of odor-related learning and olfactory memory in the mouse. ACS Chem Neurosci 2020 ; 11 : 3590–602. [Google Scholar]
- Takase K, Tsuneoka Y, Oda S, et al. High-fat diet feeding alters olfactory-, social-, and reward-related behaviors of mice independent of obesity. Obesity (Silver Spring) 2016 ; 24 : 886–94. [Google Scholar]
- Lacroix M-C, Caillol M, Durieux D, et al. Long-lasting metabolic imbalance related to obesity alters olfactory tissue homeostasis and impairs olfactory-driven behaviors. Chem Senses 2015 ; 40 : 537–56. [Google Scholar]
- Al Koborssy D, Palouzier-Paulignan B, Canova V, et al. Modulation of olfactory-driven behavior by metabolic signals: role of the piriform cortex. Brain Struct Funct 2019 ; 224 : 315–36. [Google Scholar]
- Julliard A-K, Al Koborssy D, Fadool DA, et al. Nutrient sensing: another chemosensitivity of the olfactory system. Front Physiol 2017 ; 8 : 468. [Google Scholar]
- Faour M, Magnan C, Gurden H, et al. Olfaction in the context of obesity and diabetes: Insights from animal models to humans. Neuropharmacology 2022 ; 206 : 108923. [Google Scholar]
- Aimé P, Palouzier-Paulignan B, Salem R, et al. Modulation of olfactory sensitivity and glucose-sensing by the feeding state in obese Zucker rats. Front Behav Neurosci 2014 ; 8 : 326. [Google Scholar]
- Al Koborssy D, Palouzier-Paulignan B, Salem R, et al. Cellular and molecular cues of glucose sensing in the rat olfactory bulb. Front Neurosci 2014 ; 8 : 333. [Google Scholar]
- Fadool DA, Tucker K, Pedarzani P. Mitral cells of the olfactory bulb perform metabolic sensing and are disrupted by obesity at the level of the Kv1.3 ion channel. PLoS One 2011 ; 6 : e24921. [Google Scholar]
- Poessel M, Freiherr J, Wiencke K, et al. Insulin resistance is associated with reduced food odor sensitivity across a wide range of body weights. Nutrients 2020 ; 12 : 2201. [Google Scholar]
- Min J-Y, Min K-B. Insulin resistance and the increased risk for smell dysfunction in US adults. Laryngoscope 2018 ; 128 : 1992–6. [Google Scholar]
- Bell GA, Fadool DA. Awake, long-term intranasal insulin treatment does not affect object memory, odor discrimination, or reversal learning in mice. Physiol Behav 2017 ; 174 : 104–13. [Google Scholar]
- Edwin Thanarajah S, Hoffstall V, Rigoux L, et al. The role of insulin sensitivity and intranasally applied insulin on olfactory perception. Sci Rep 2019 ; 9 : 7222. [Google Scholar]
- Campolo J, Corradi E, Rizzardi A, et al. Correlates of olfactory impairment in middle-aged non-diabetic Caucasian subjects with stage I-II obesity. Eur Arch Otorhinolaryngol 2021 ; 278 : 2047–54. [Google Scholar]
- Zhang Z, Zhang B, Wang X, et al. Olfactory dysfunction mediates adiposity in cognitive impairment of type 2 diabetes: insights from clinical and functional neuroimaging studies. Diabetes Care 2019 ; 42 : 1274–83. [Google Scholar]
- Cruciani-Guglielmacci C, Vincent-Lamon M, Rouch C, et al. Early changes in insulin secretion and action induced by high-fat diet are related to a decreased sympathetic tone. Am J Physiol Endocrinol Metab 2005 ; 288 : E148–54. [Google Scholar]
- Coucha M, Abdelsaid M, Ward R, et al. Impact of metabolic diseases on cerebral circulation: structural and functional consequences. Compr Physiol 2018 ; 8 : 773–99. [Google Scholar]
- Soleimanzad H, Montaner M, Ternier G, et al. Obesity in midlife hampers resting and sensory-evoked cerebral blood flow in mice. Obesity (Silver Spring) 2021 ; 29 : 150–8. [Google Scholar]
- Soleimanzad H, Morisset C, Montaner M, et al. Western diet since adolescence impairs brain functional hyperemia at adulthood in mice: rescue by a balanced ω-3:ω-6 polyunsaturated fatty acids ratio. Int J Obes (Lond) 2025 ; 49 : 844–54. [Google Scholar]
- Negoias S, Croy I, Gerber J, et al. Reduced olfactory bulb volume and olfactory sensitivity in patients with acute major depression. Neuroscience 2010 ; 169 : 415–21. [Google Scholar]
- Gudziol V, Buschhüter D, Abolmaali N, et al. Increasing olfactory bulb volume due to treatment of chronic rhinosinusitis--a longitudinal study. Brain 2009 ; 132 : 3096–101. [Google Scholar]
- Mazal PP, Haehner A, Hummel T. Relation of the volume of the olfactory bulb to psychophysical measures of olfactory function. Eur Arch Otorhinolaryngol 2016 ; 273 : 1–7. [Google Scholar]
- Poessel M, Breuer N, Joshi A, et al. Reduced olfactory bulb volume in obesity and its relation to metabolic health status. Front Hum Neurosci 2020 ; 14 : 586998. [Google Scholar]
- Thiebaud N, Llewellyn-Smith IJ, Gribble F, et al. The incretin hormone glucagon-like peptide 1 increases mitral cell excitability by decreasing conductance of a voltage-dependent potassium channel. J Physiol 2016 ; 594 : 2607–28. [Google Scholar]
- Ahrén B, Holst JJ. The cephalic insulin response to meal ingestion in humans is dependent on both cholinergic and noncholinergic mechanisms and is important for postprandial glycemia. Diabetes 2001 ; 50 : 1030–8. [Google Scholar]
- Montaner M, Denom J, Simon V, et al. A neuronal circuit driven by GLP-1 in the olfactory bulb regulates insulin secretion. Nat Commun 2024 ; 15 : 6941. [Google Scholar]
- Fontbonne A, Currie A, Tounian P, et al. Prevalence of overweight and obesity in France: the 2020 obepi-roche study by the “Ligue contre l’obésité.” J Clin Med 2023 ; 12 : 925. [Google Scholar]
- Niechciał E, Wais P, Bajtek J, et al. Current perspectives for treating adolescents with obesity and type 2 diabetes: a review. Nutrients 2024 ; 16 : 4084. [Google Scholar]
- Holst JJ. GLP-1 physiology in obesity and development of incretin-based drugs for chronic weight management. Nat Metab 2024 ; 6 : 1866–85. [Google Scholar]
- Rodriguez PJ, Zhang V, Gratzl S, et al. Discontinuation and reinitiation of dual-labeled GLP-1 receptor agonists among US adults with overweight or obesity. JAMA Netw Open 2025 ; 8 : e2457349. [Google Scholar]
- Lah S, Hocking SL. Treatment of obesity: will incretin agonists make bariatric surgery a thing of the past? Intern Med J 2025 ; 55 : 369–75. [Google Scholar]
- Phan F, Bertrand R, Amouyal C, et al. De la découverte des hormones incrétines aux doubles et triples agonistes GIP / GLP-1 / glucagon. Med Sci (Paris) 2024 ; 40 : 837–47. [Google Scholar]
- Glotfelty EJ, Olson L, Karlsson TE, et al. Glucagon-like peptide-1 (GLP-1)-based receptor agonists as a treatment for Parkinson’s disease. Expert Opin Investig Drugs 2020 ; 29 : 595–602. [Google Scholar]
- Nyström T, Gutniak MK, Zhang Q, et al. Effects of glucagon-like peptide-1 on endothelial function in type 2 diabetes patients with stable coronary artery disease. Am J Physiol Endocrinol Metab 2004 ; 287 : E1209–15. [Google Scholar]
- Alvarez E, Martínez MD, Roncero I, et al. The expression of GLP-1 receptor mRNA and protein allows the effect of GLP-1 on glucose metabolism in the human hypothalamus and brainstem. J Neurochem 2005 ; 92 : 798–806. [Google Scholar]
Palatable : adjectif emprunté de l’anglais qui désigne ce qui est agréable au goût (ndlr).
La voie mésocorticolimbique, parfois appelée voie de la récompense, est une voie dopaminergique qui relie l’aire tegmentale ventrale au striatum ventral (nucleus accumbens) et à différentes régions du cortex (ndlr).
Les molécules odorantes, volatiles, atteignent l’épithélium olfactif situé dans la cavité nasale, soit par le nez (voie orthonasale), soit par la bouche (voie rétronasale) (ndlr).
La lame criblée de l’os ethmoïde est une structure anatomique située dans la partie antérieure de la base du crâne. Il s’agit d’une structure horizontale, percée de petits trous, qui sépare la cavité nasale de la fosse crânienne (ndlr).
Orexigène, du grec órexis, « appétit », qualifiant un stimulateur de l’appétit (ndlr).
Le terme normosmie est utilisé pour qualifier une perception olfactive normale (ndlr).
La mémoire épisodique est une forme de mémoire à long terme qui permet de se souvenir d’événements personnels vécus (autobiographiques), avec tous leurs détails contextuels comme la date, le lieu et même l’état émotionnel au moment de l’expérience (ndlr).
Il s’agit d’un indicateur biologique qui se base sur la mesure de la glycémie et de l’insulinémie à jeun.
Les DREADDs (pour designer receptor exclusively activated by designer drugs) sont des récepteurs muscariniques couplés aux protéines G (RCPG) modifiés. Ces récepteurs de synthèse sont généralement introduits dans les cellules par des vecteurs viraux et offrent une approche de type clé-serrure pour moduler sélectivement l’activité cellulaire par des moyens chimiques (ndlr).
Les incrétinomimétiques sont des agonistes du récepteur du glucagon-like peptide 1 (GLP-1). Ils sont indiqués dans le traitement du diabète de type 2 en association aux règles hygiéno-diététiques (ndlr).
Liste des figures
 |
Figure 1 Régulation de la balance énergétique et olfaction. La balance énergétique est sous le contrôle de facteurs homéostatiques dépendant, notamment, de l’action des neurones glucosensibles de l’hypothalamus, des hormones anorexigènes comme la leptine, ou de la ghréline, l’hormone orexigène qui agit sur l’hypothalamus, et du système nerveux autonome, avec, par exemple, les afférences vagales du tractus gastro-intestinal dans le tronc cérébral. Les facteurs non homéostasiques, comme le plaisir, la mémoire et les informations sensorielles, également modulés par les hormones du métabolisme énergétique, jouent un rôle clé dans cette régulation. Les deux types de facteurs interagissent étroitement avec les préférences alimentaires et les activités olfactives induites par les odeurs alimentaires. |
| Dans le texte | |
 |
Figure 2 La perception olfactive. Les quatre premières étapes de la perception et de l’intégration olfactive sont similaires chez les êtres humains et les rongeurs. Quand la nourriture est en bouche (1.b.), la stimulation olfactive se fait également par la voie rétronasale, ce qui explique l’importance de l’olfaction dans le goût (flaveur). À l’étape 5, l’activation du système olfactif par les odeurs alimentaires induit une augmentation de l’insuline pancréatique chez la souris. |
| Dans le texte | |
 |
Figure 3 Interrégulations entre olfaction et prise alimentaire. Elles se résument en trois phases principales : préparation à jeun (phase céphalique), exécution (mastication et ingestion), et mémorisation à satiété (construction des préférences olfactives et alimentaires). Ces phases tournent en boucle au quotidien, elles s’influencent les unes avec les autres, et elles sont modulées par le contexte socio-culturel. |
| Dans le texte | |
 |
Figure 4 Augmentation de l’insulinémie pendant la phase CPIR (cephalic phase of insulin release) et de GSIS (glucose stimulated insulin secretion), par l’activation d’une voie neurométabolique reliant le bulbe olfactif, l’hypothalamus et le pancréas. Sigles (de haut en bas) : PPG (préproglucagon) ; AON (anterior olfactory nucleus) ; LH (lateral hypothalamus) ; PVN (paraventricular nucleus) ; SNA (système nerveux autonome) ; M3-Ach-R (récepteurs muscariniques de type 3) ; α2-NA-R (récepteurs noradrénergiques de type α2). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




