| Issue |
Med Sci (Paris)
Volume 42, Number 4, Avril 2026
Chroniques génomiques
|
|
|---|---|---|
| Page(s) | 393 - 395 | |
| Section | Forum | |
| DOI | https://doi.org/10.1051/medsci/2026061 | |
| Published online | 24 April 2026 | |
Les TimeVaults, coffres-forts temporels des cellules
TimeVaults provide recordings of past cellular activity
Biologiste moléculaire, généticien, Président d’Aprogène (association pour la promotion de la génomique), Marseille, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Abstract
Inventive engineering of cellular organelles (Vaults) allows durable recording and later readout of the cellular transcriptional activity of living cells, at a given time point, opening up a large series of applications.
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Bertrand Jordan).
Le suivi des états transcriptionnels d’une cellule au cours du temps est indispensable pour comprendre la dynamique de son fonctionnement. Mais cette information est difficilement accessible : l’analyse du patron d’expression à un instant t est destructive (extraction et analyse des ARNm) et ne permet pas de suivre l’évolution ultérieure de la cellule. On peut certes examiner le comportement de gènes dans des cellules vivantes à travers des techniques d’imagerie, mais on est alors limité à un petit nombre d’entités. Récemment, des approches ingénieuses utilisant le système CRSPR-Cas9 ont été développées et permettent de suivre les trajectoires transcriptionnelles à plus grande échelle [1], mais elles restent incapables d’une approche large et sans a priori. Une nouvelle technique, présentée dans un récent article de la revue Science [2] constitue une véritable révolution. Son principe : emmagasiner dans une organelle cellulaire creuse (appelée Vault, ce que je traduirai par « crypte ») un échantillonnage des ARNm présents dans une cellule à un instant donné, et les garder à l’abri jusqu’à plusieurs jours au sein de la cellule vivante avant de lyser l’organelle pour analyser son contenu. Ce système, baptisé TimeVault permet ainsi de prendre un instantané de l’état transcriptionnel d’une cellule sans pour autant interrompre son développement, et de le lire ultérieurement.
Les cryptes, ubiquitaires, mais mystérieuses, et leur emploi pour le stockage des ARNm
Les Vaults ou cryptes ont été découverts il y a déjà longtemps, dans les années 1980 [3]. Il s’agit de particules ribonucléoprotéiques de grande taille (environ trois fois celle d’un ribosome) que l’on trouve dans le cytoplasme de la plupart des cellules eucaryotes à raison de quelques dizaines de milliers par cellule1. Elles se présentent sous la forme d’une sorte de petit tonneau (Figure 1) dont la paroi est formée de 78 exemplaires d’une protéine appelée MVP (major vault protein), associée à l’intérieur avec quelques exemplaires de deux autres protéines et un petit ARN. Cette organelle est essentiellement creuse et, malgré des années d’efforts de son découvreur [4], sa fonction biologique reste inconnue.
 |
Figure 1 Structure d’une crypte (Vault) de rat, obtenue par cristallographie aux rayons X [5] (licence Creative Commons). |
Comment stocker l’ARNm dans une crypte ? Le système ingénieux imaginé par les auteurs2 utilise une protéine appelée PABP (polyA binding protein) qui se fixe à la séquence polyadénylée (polyA) présente à l’extrémité 3’ de presque tous les ARNm. Cette protéine est fusionnée avec le domaine de liaison à la protéine MVP (major vault protein) d’une des protéines internes de la crypte. Si l’on ajoute à la cellule l’ARNm de cette PABP modifiée ainsi que de l’ARNm de la protéine MVP, il va y avoir formation de nouvelles cryptes qui capteront chacune un peu du mélange d’ARNm présent dans le cytoplasme. Ce mélange, reflet de l’activité de la cellule à cet instant, sera conservé à l’abri dans la crypte et pourra être lu des jours plus tard. Reste à réaliser tout cela concrètement
La mise au point du système TimeVault
Les auteurs ont d’abord vérifié qu’il était possible de provoquer l’assemblage de cryptes dans les cellules en coexprimant la protéine MVP avec la protéine GFP (Green fluorescent protein) elle-même fusionnée avec INT, le domaine de liaison à MVP d’une protéine interne minoritaire de la crypte appelée vPARP (vault polyADP-ribose polymerase) : on voit alors au microscope optique que la fluorescence est concentrée en des points lumineux (qui sont les cryptes nouvellement formées). Le système peut alors être assemblé : il comporte la protéine PABP (fixant les ARNm via leur séquence polyA) fusionnée avec le domaine de liaison INT, qui va ainsi fixer les ARNm, mais aussi être attirée à l’intérieur des cryptes en formation par son association, via son domaine INT, à la protéine MVP, l’ensemble (PABP-INT et MVP) étant coexprimé à partir d’un promoteur qui peut être, soit inductible par la doxycycline (promoteur TET-on, actif seulement en présence de doxycycline), soit réprimé par cet antibiotique (promoteur TET-off, constitutionnellement actif, mais « éteint » en présence de doxycycline). Cette construction est introduite dans les cellules par transfection d’un plasmide. Si tout cela fonctionne comme prévu, on devrait pouvoir prendre un instantané du contenu en ARNm de la cellule en induisant l’expression de ces protéines à l’instant t par l’ajout de doxycycline (promoteur TET-on), ce qui suscitera la formation de nouvelles cryptes via la synthèse de MVP et l’inclusion dans ces cryptes de complexes ARNm-PABP-INT. On arrêtera cette inclusion après quelques heures en éliminant cet antibiotique par lavage des cellules, et les ARNm contenus dans (et protégés par) les cryptes pourront être analysés plus tard : ils sont un témoin de l’activité de la cellule durant la période de l’induction.
Il faut d’abord vérifier que les ARNm sont bien protégés dans les cryptes, et évaluer la durée de cette protection. Pour cela, des cellules sont transfectées par le plasmide TimeVault, induites par la doxycycline, puis soumises à une lyse douce (qui ne détruit pas les cryptes) trois jours plus tard. Les lysats sont conservés à 37 °C pendant plusieurs jours, puis traités ou pas par la RNAse, et la quantité d’un transcrit représentatif (actine) est alors mesurée. La Figure 2 montre que l’ARNm contenu dans les cryptes (en bleu) est protégé de la dégradation jusqu’à 12 jours après la lyse des cellules alors que l’ARNm nu décroît rapidement en l’absence de RNAse (orange) et est instantanément dégradé si l’on ajoute cette enzyme (noir). Les ARNm inclus dans les cryptes sont donc bien à l’abri !
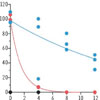 |
Figure 2 Protection des ARNm par les cryptes. En abscisse : nombre de jours après la lyse des cellules et avant le traitement par la RNAse. En ordonnée : pourcentage d’ARNm restant. En bleu : cellules traitées par le système TimeVault ; en orange : ni traitement, ni RNAse ; en noir RNAse sans TimeVault. Extrait partiel et modifié de la figure 1 de [2]. |
La suite des vérifications comporte l’estimation de la fenêtre temporelle durant laquelle la crypte capte les ARNm cellulaires : on utilise pour cela le système avec cette fois un promoteur TET-off (actif sauf en présence de doxycycline) ce qui permet d’arrêter rapidement la formation des cryptes et de réduire ainsi la fenêtre à environ un jour. Vient ensuite la vérification que le patron d’expression des cellules n’est pas modifié par l’introduction du vecteur TimeVault (sauf bien sûr pour l’expression des ARN MVP et vPARP) et donc que le fonctionnement de ces cellules n’est pas perturbé par ces traitements. Cela est attesté par le fait que le patron d’expression des ARNm extraits des cryptes produites par le système TimeVault est, comme attendu, le même que celui des ARNm extrait des cellules non traitées, pendant la même fenêtre temporelle : les cryptes ont bien capté et protégé un échantillon représentatif des ARNm cellulaires produits pendant ce laps de temps. Enfin la sensibilité du système est explorée en répertoriant par séquençage les ARNm détectés à partir d’un million, 100 000, 1 000 ou même 10 cellules : 75 % des espèces d’ARNm sont détectés à partir de seulement 1 000 cellules. Au total, le système TimeVault est donc capable de capturer un échantillon représentatif des ARNm exprimés dans une cellule durant une « fenêtre » de l’ordre d’un jour, et de le préserver au sein de la cellule vivante pour une analyse ultérieure jusqu’à plus d’une semaine après.
Une vérification : l’analyse des réponses cellulaires au stress
La réponse cellulaire au stress par choc thermique (heat shock) ou par hypoxie a été largement étudiée [6] et permet d’illustrer l’apport du système TimeVault. Pour ce faire, les auteurs utilisent sa version Tet-Off : après transfection dans les cellules, le système est actif, mais peut être stoppé par l’addition de doxycycline. Les cellules transfectées sont exposées à un choc thermique à 42 °C pendant 24 h, après quoi le système TimeVault est stoppé par l’addition de doxycycline ; les cellules sont alors ramenées à 37 °C et cultivées durant encore 48 h avant récolte. On a donc en principe emmagasiné les ARNm en condition de choc thermique dans les cryptes, puis ramené les cellules à l’état normal. Les témoins sont des cellules ayant subi le même traitement, mais sans choc thermique, et des cellules pour lesquelles le choc thermique a eu lieu après l’addition de doxycycline, donc après l’enregistrement des ARNm dans les cryptes. Pour chacune de ces trois conditions, un échantillon est lysé puis traité par la RNAse avant séquençage des ARNm protégés dans les cryptes ; et l’autre échantillon est directement séquencé, représentant l’ARNm total (y compris celui des cryptes, mais il est très minoritaire). On constate que l’ARNm contenu dans les cryptes actives lors du choc thermique montre une surexpression de la plupart des gènes connus pour être stimulés en condition de choc thermique, alors que l’ARNm cellulaire du même échantillon (rappelons que ces cellules ont récupéré deux jours à 37 °C après le choc thermique) ne montre pas de surexpression. Par contre, si le choc thermique a eu lieu après inactivation du système TimeVault par la doxycycline, l’ARNm des cryptes ne montre pas de surexpressions. Le deuxième échantillon, les cellules n’ayant pas subi de choc thermique, fournit un témoin négatif pour les différentes conditions. On constate donc que les cryptes conservent bien un échantillon représentatif des ARNm exprimés en condition de choc thermique, et qu’il n’y a pas de contamination des cryptes par les ARNm néosynthétisés si le choc thermique a lieu après inactivation de TimeVault : le système permet bien de réaliser un échantillonnage des ARNm contenus dans les cellules et de le préserver, quelle que soit leur évolution ultérieure. Une étude similaire dans un système simulant des conditions d’hypoxie grâce à l’emploi de dimethyloxalylglycine (DMOG)3 [7] confirme la capacité de TimeVault à préserver une image fidèle d’un état transcriptionnel passé, sans contamination par les évolutions ultérieures de la cellule.
Une première application en cancérologie
Le système TimeVault a permis d’analyser en détail l’origine de cellules résistantes qui apparaissent (sans modification génétique, et de manière réversible) au cours du traitement de tumeurs par chimiothérapie. Il s’est agi là de cellules d’adénocarcinome du poumon (lignée PC9) et de leur traitement par un inhibiteur de la tyrosine kinase (osimertinib). L’emploi du système TimeVault, grâce à un ensemble assez complexe d’expériences que je ne détaillerai pas ici, a permis d’identifier, via leur profil d’expression, les cellules destinées à devenir résistantes, et ce avant tout traitement. C’est un résultat important, tant du point de vue fondamental que pour la clinique, et il va susciter de nombreuses études
Quelques limites, mais aussi de très nombreuses possibilités
Le système TimeVault est donc capable de préserver, de manière très large et non biaisée, l’état transcriptionnel d’une cellule vivante en vue de son analyse ultérieure, jusqu’à une dizaine de jours plus tard. Il est en cela très supérieur aux systèmes existants qui sont limités à l’examen de quelques dizaines de gènes définis a priori [1]. Idéalement, on aimerait pouvoir étendre le délai entre « enregistrement » et analyse, afin de suivre (par exemple) les évènements liés au développement embryonnaire. On aimerait aussi pouvoir prendre plus d’un instantané et conserver la trace de l’état d’une cellule à deux ou trois moments de son évolution. Et, dans l’idéal, tout cela pourrait se faire à l’échelle d’une seule cellule Science-fiction peut-être, mais cette approche novatrice est si puissante que beaucoup d’équipes vont s’attacher à l’étendre et à la perfectionner. C’est en tout cas un triomphe d’ingénuité, un superbe travail ayant réagencé une organelle (toujours mystérieuse) pour en faire un puissant outil d’analyse biologique.
Conflits d’intérêt
L’auteur déclare qu’il n’a aucun conflit d’intérêt.
Références
- Choi J, Chen W, Minkina A, et al. A time-resolved, multi-symbol molecular recorder via sequential genome editing. Nature 2022 ; 608 : 98–107. [Google Scholar]
- Chao YK, Wu M, Gong Q, Chen F. A genetically encoded device for transcriptome storage in mammalian cells. Science 2026 Jan 15:eadz9353 [Google Scholar]
- Kedersha NL, Rome LH. Isolation and characterization of a novel ribonucleoprotein particle: Large structures contain a single species of small RNA. J Cell Biol 1986 ; 103 : 699–709. [Google Scholar]
- Travis J. The vault guy. Science. 2024 ; 384 : 1058–62. [Google Scholar]
- Tanaka H, Kato K, Yamashita E, et al. “The structure of rat liver vault at 3.5 angstrom resolution”. Science 2009 ; 323 : 384–8. [Google Scholar]
- Hästbacka HSE, Da Silva AJ, Sistonen L, Henriksson E. A guide to heat shock factors as multifunctional transcriptional regulators. FEBS J 2025 ; 292 : 4133–55. [Google Scholar]
- Barton, A., Jaśkiewicz, M., Więch-Walów, A. et al. Challenges in mimicking hypoxia: insights into HIF-regulated MiRNA expression induced by DMOG and CoCl2. Cell Commun Signal 2025 ; 23 : 454. [Google Scholar]
Qui sont seulement quatre, ce qui change agréablement des « papiers » affichant trente ou quarante auteurs…
Le DMOG induit un état d’hypoxie en bloquant l’activité des enzymes PHD (prolyl hydroxylases), qui bloquent l’activité du facteur de transcription HIF-1α (hypoxiainducible factor 1 alpha), nécessaire pour l’activation des gènes d’hypoxie.
Liste des figures
 |
Figure 1 Structure d’une crypte (Vault) de rat, obtenue par cristallographie aux rayons X [5] (licence Creative Commons). |
| Dans le texte | |
 |
Figure 2 Protection des ARNm par les cryptes. En abscisse : nombre de jours après la lyse des cellules et avant le traitement par la RNAse. En ordonnée : pourcentage d’ARNm restant. En bleu : cellules traitées par le système TimeVault ; en orange : ni traitement, ni RNAse ; en noir RNAse sans TimeVault. Extrait partiel et modifié de la figure 1 de [2]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




