| Issue |
Med Sci (Paris)
Volume 42, Number 2, Février 2026
|
|
|---|---|---|
| Page(s) | 137 - 140 | |
| Section | Nouvelles | |
| DOI | https://doi.org/10.1051/medsci/2026009 | |
| Published online | 24 February 2026 | |
Déméthyler l’ADN contre le cancer
Vers de nouvelles stratégies épigénétiques sans dommage à l’ADN
Demethylating DNA against cancer : towards new epigenetic therapeutic strategies without DNA damage
UMR7216, Épigénétique et destin cellulaire, Université Paris Cité, CNRS, Paris, France
a
This email address is being protected from spambots. You need JavaScript enabled to view it.
b
This email address is being protected from spambots. You need JavaScript enabled to view it.
c
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les marques épigénétiques sont dérégulées dans le cancer
Le cancer est une maladie complexe résultant de l’accumulation d’altérations génétiques, de perturbations des mécanismes de régulation cellulaire, mais également d’altérations épigénétiques [1]. Ces dernières possèdent un rôle clé, car elles modulent l’expression des gènes sans mutation de la séquence d’ADN.
Contrairement aux mutations, elles sont potentiellement réversibles, ce qui en fait des cibles thérapeutiques attrayantes. La méthylation de l’ADN est une des marques épigénétiques les plus étudiées, et parmi les plus prometteuses en termes d’applications thérapeutiques.
La méthylation de l’ADN : rôle, mécanismes et acteurs
La méthylation de l’ADN, une marque épigénétique essentielle chez les mammifères, consiste en l’ajout covalent d’un groupe méthyle (CH3) sur une cytosine, principalement dans un contexte de dinucléotides CpG. C’est une marque très abondante, puisqu’environ 80 % des CpG du génome humain sont méthylés. Cette méthylation de l’ADN participe au contrôle fin de l’expression génique et à la stabilité du génome [2].
Dans de nombreux cancers, la répartition de cette marque est déréglée : des promoteurs de gènes suppresseurs de tumeur sont hyperméthylés et donc réprimés, tandis que des régions intergéniques sont déméthylées, aboutissant à l’expression aberrante d’éléments répétés et augmentant l’instabilité du génome [3, 4] (→).
(→) Voir m/s n° 12, 2024, page 925
La méthylation de l’ADN est catalysée par une famille d’enzymes, les ADN méthyltransférases (DNA methyl transferase, DNMT). Il en existe trois dans l’espèce humaine : DNMT3A et DNMT3B sont des ADN méthyltransférases « de novo », qui établissent la méthylation de l’ADN au cours du développement précoce, tandis que DNMT1 est exprimée dans toutes les cellules qui se divisent. Lors de la réplication de l’ADN, les brins nouvellement synthétisés ne portent aucune méthylation des cytosines, ce qui conduit à un ADN hémiméthylé (Figure 1A). Le retour à un état entièrement méthylé nécessite l’activité enzymatique de DNMT1, qui se lie aux sites hémiméthylés et méthyle la cytosine nouvellement incorporée [5]. Un autre acteur indispensable de cette maintenance est le cofacteur UHRF1 (ubiquitin-like PHD and RING finger domain-containing protein 1), une ubiquitine ligase E3 nécessaire au recrutement de DNMT1 [6]. UHRF1 est un oncogène avéré, surabondant dans de nombreux types de cancers, où il favorise la méthylation des promoteurs de gènes suppresseurs de tumeur [7, 8]. Les rôles reconnus de la méthylation de l’ADN dans les cancers font de ses effecteurs des cibles d’intérêt pour les thérapies épigénétiques anticancéreuses, consistant principalement en des agents déméthylants de l’ADN.
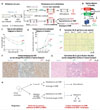 |
Figure 1. La déméthylation de l’ADN dans des cellules cancéreuses induit la sénescence. A. Mécanismes et acteurs de la méthylation de l’ADN. B. Principe du dégron à l’auxine. AID : auxin-inducible degron ; OsTIR1 : ubiquitine-ligase E3 de plante. C. Quantification du pourcentage global de dinucléotides CpG méthylés par WGBS (whole genome bisulfite sequencing) dans les lignées cellulaires témoin et « dégrons » dans les conditions indiquées. D. Courbes de prolifération cellulaire. **** p < 0,0001. E. Coloration SA-β-gal (senescense-associated β-galactosidase) des lignées traitées à l’auxine. Les cellules sénescentes sont en bleu. F. Marquage immunohistochimique de coupes de tumeurs pour le marqueur de prolifération cellulaire Ki67 (en brun), avec contre coloration par hématoxyline. G. Coloration SA-β-gal (en bleu) et nuclear fast red (en rose) de coupes de tumeurs. H. Schéma comparant les perspectives thérapeutiques apportées par ces études. SASP : senescence-associated secretory phenotype. Figure adaptée de [10] et de [11]. |
Cibler la méthylation de l’ADN dans les cancers
Sur le plan thérapeutique, la recherche clinique a longtemps exploité la vulnérabilité épigénétique, avec des analogues nucléosidiques tels que la décitabine (5-aza-déoxycytidine), notamment contre des leucémies [9]. Ces molécules, incorporées dans l’ADN durant sa réplication, forment des liens covalents avec DNMT1, laquelle est alors dégradée par la machinerie de réparation de l’ADN ; il en résulte une perte progressive de la méthylation de l’ADN, mais également de nombreux dommages à l’ADN. Ainsi, l’effet de ces molécules repose d’une part sur une reprogrammation épigénétique, et d’autre part sur un effet génotoxique, ce qui limite la tolérance clinique et complique l’interprétation des rôles respectifs de la déméthylation de l’ADN et du dommage à l’ADN dans l’activité anticancéreuse des traitements déméthylants (Figure 1A).
La méthylation de l’ADN protège les cellules cancéreuses de la sénescence
La capacité de distinguer l’effet de la déméthylation de l’ADN elle-même de celui des dommages à l’ADN est ainsi cruciale pour comprendre le rôle antitumoral propre des analogues de nucléosides. Nous avons donc cherché à identifier les conséquences de la perte de méthylation de l’ADN en elle-même sur les cellules cancéreuses, en utilisant un système dégron à l’auxine (auxine-inducible degron, AID). Cet outil repose sur l’ajout d’une « étiquette AID » à une protéine d’intérêt qui, en présence d’une ubiquitine ligase de plante (OsTIR1) et d’auxine, permet la dégradation rapide de cette protéine par le protéasome. Nous avons ainsi produit dans les cellules HCT116 [10], un modèle de cancer colorectal, une « lignée dégron » pour UHRF1 et une pour DNMT1 (Figure 1B). Comme attendu, la déplétion de UHRF1 ou de DNMT1 induit une déméthylation globale de l’ADN (Figure 1C), sans signe de génotoxicité ou de dommage à l’ADN, accompagnée d’une profonde dérégulation de l’expression de nombreux gènes [11]. Étonnamment, cette déméthylation provoque un défaut de la division cellulaire (Figure 1D), et un phénotype de sénescence cellulaire (Figure 1E). Ces constats ont également pu être faits in vivo dans un modèle de xénogreffes (Figures 1F, 1G).
La sénescence cellulaire, une conséquence de la déméthylation de l’ADN auparavant inconnue
La sénescence correspond à un état d’arrêt permanent du cycle cellulaire, généralement orchestré par le gène suppresseur de tumeur P53, et impliquant l’activation de la protéine p21, un inhibiteur de cycline-kinase qui bloque la progression du cycle cellulaire. Cet état s’accompagne également de l’émission d’un sécrétome associé à la sénescence, composé de cytokines, chimiokines, protéases et facteurs de croissance [12]. Dans les cellules HCT116 déplétées de DNMT1 ou de UHRF1, ralentissement du cycle cellulaire et sécrétome sénescent coexistent de manière indépendante de p53, ce qui témoigne d’un processus « non canonique » de sénescence. Bien que la sénescence soit le plus souvent considérée comme la conséquence de dommages à l’ADN [13], nous avons constaté que la sénescence induite par déméthylation de l’ADN apparaît sans aucun signe de génotoxicité. De plus, elle n’est pas limitée aux cellules HCT116 : elle se produit non seulement dans d’autres lignées de cancer colorectal, mais également dans d’autre types de tumeurs [11]. Le lien entre déméthylation de l’ADN et sénescence des cellules cancéreuses est donc désormais établi, mais les mécanismes sous-jacents devront faire l’objet de futurs travaux de recherche. Incidemment, la découverte tardive de ce phénotype de sénescence consécutif à la déméthylation de l’ADN s’explique peut-être par le fait que les agents hypométhylants classiques induisent de multiples dommages à l’ADN et donc une réponse pro-apoptotique plutôt que pro-sénescence (Figure 1H).
UHRF1, une cible thérapeutique prometteuse contre le cancer
Les résultats de nos travaux de recherche ont également permis d’étendre les connaissances sur UHRF1 : au-delà de son rôle de cofacteur de DNMT1, UHRF1 assure des fonctions « non canoniques » essentielles à la stabilité du méthylome [10]. Il interagit avec DNMT3A/3B et antagonise les TET (ten eleven translocation), une famille d’enzymes catalysant la déméthylation de l’ADN. Ces autres rôles de UHRF1 pourraient expliquer que la déplétion de UHRF1 est plus efficace que la déplétion de DNMT1 pour déméthyler l’ADN, et qu’elle induit la sénescence plus profondément et plus rapidement.
Dans une perspective thérapeutique anti-cancéreuse, cibler UHRF1 présente donc plusieurs avantages théoriques (Figure 1H) :
- 1)
induire une sénescence des cellules tumorales durable sans provoquer de détérioration de l’ADN génomique, ce qui pourrait réduire la toxicité systémique ;
- 2)
induire cette sénescence indépendamment de la voie p53, et donc être applicable aux très nombreuses tumeurs dans lesquelles cette voie est inactivée ;
- 3)
cibler un point clé du réseau épigénétique, intervenant à la fois dans l’établissement de nouveaux profils de méthylation de l’ADN (dynamique de novo) et dans la conservation de ces profils lors de la division cellulaire (maintenance).
Certes, des approches alternatives comme l’utilisation des inhibiteurs sélectifs de DNMT1 cherchent déjà à dissocier déméthylation de l’ADN et incorporation génotoxique [14], mais la déplétion ciblée de UHRF1 semble, d’après les résultats expérimentaux, produire un effet plus rapide et plus complet sur le méthylome.
Cependant, si le sécrétome associé à la sénescence peut favoriser l’élimination des cellules sénescentes par le système immunitaire, il peut aussi entretenir une inflammation chronique et des effets pro-tumoraux à long terme [12, 13]. Il est donc pertinent d’envisager des stratégies combinatoires associant induction de sénescence par déméthylation de l’ADN et élimination ciblée des cellules sénescentes par des médicaments sénolytiques ou par renforcement du système immunitaire (immunothérapies). Mais avant d’envisager une utilisation thérapeutique d’inhibiteurs de UHRF1, il conviendra notamment de déterminer comment les cellules non transformées réagissent à cette inhibition, et de prouver l’absence de toxicité ou la faible toxicité de tels inhibiteurs pour les tissus non tumoraux.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Hanahan D. Hallmarks of cancer: New dimensions. Cancer Discov 2022 ; 12 : 31–46. [CrossRef] [PubMed] [Google Scholar]
- Smith ZD, Hetzel S, Meissner A. DNA methylation in mammalian development and disease. Nat Rev Genet 2025 ; 26 : 7–30. [Google Scholar]
- Nishiyama A, Nakanishi M. Navigating the DNA methylation landscape of cancer. Trends Genet 2021 ; 37 : 1012–27. [Google Scholar]
- Gorse M, Bianchi C, Proudhon C. Épigénétique et cancer : la méthylation dans tous ses états. Med Sci (Paris) 2024 ; 40 : 925–34. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Petryk N, Bultmann S, Bartke T, et al. Staying true to yourself: mechanisms of DNA methylation maintenance in mammals. Nucleic Acids Res 2021 ; 49 : 3020–32. [Google Scholar]
- Ferry L, Fournier A, Tsusaka T, et al. Methylation of DNA ligase 1 by G9a/GLP recruits UHRF1 to replicating DNA and regulates DNA methylation. Mol Cell 2017 ; 67 : 550–65.e5. [Google Scholar]
- Mudbhary R, Hoshida Y, Chernyavskaya Y, et al. UHRF1 overexpression drives DNA hypomethylation and hepatocellular carcinoma. Cancer Cell 2014 ; 25 : 196–209. [Google Scholar]
- Kong X, Chen J, Xie W, et al. Defining UHRF1 domains that support maintenance of human colon cancer DNA methylation and oncogenic properties. Cancer Cell 2019 ; 35 : 633–48.e7. [Google Scholar]
- Stomper J, Rotondo JC, Greve G, et al. Hypomethylating agents (HMA) for the treatment of acute myeloid leukemia and myelodysplastic syndromes: mechanisms of resistance and novel HMA-based therapies. Leukemia 2021 ; 35 : 1873–89. [Google Scholar]
- Yamaguchi K, Chen X, Rodgers B, et al. Non-canonical functions of UHRF1 maintain DNA methylation homeostasis in cancer cells. Nat Commun 2024 ; 15 : 2960. [Google Scholar]
- Chen X, Yamaguchi K, Rodgers B, et al. DNA methylation protects cancer cells against senescence. Nat Commun 2025 ; 16 : 5901. [Google Scholar]
- Gorgoulis V, Adams PD, Alimonti A, et al. Cellular senescence: Defining a path forward. Cell 2019 ; 179 : 813–27. [CrossRef] [PubMed] [Google Scholar]
- Wang L, Lankhorst L, Bernards R. Exploiting senescence for the treatment of cancer. Nat Rev Cancer 2022 ; 22 : 340–55. [Google Scholar]
- Pappalardi MB, Keenan K, Cockerill M, et al. Discovery of a first-in-class reversible DNMT1-selective inhibitor with improved tolerability and efficacy in acute myeloid leukemia. Nat Cancer 2021 ; 2 : 1002–17. [Google Scholar]
© 2026 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l’utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. La déméthylation de l’ADN dans des cellules cancéreuses induit la sénescence. A. Mécanismes et acteurs de la méthylation de l’ADN. B. Principe du dégron à l’auxine. AID : auxin-inducible degron ; OsTIR1 : ubiquitine-ligase E3 de plante. C. Quantification du pourcentage global de dinucléotides CpG méthylés par WGBS (whole genome bisulfite sequencing) dans les lignées cellulaires témoin et « dégrons » dans les conditions indiquées. D. Courbes de prolifération cellulaire. **** p < 0,0001. E. Coloration SA-β-gal (senescense-associated β-galactosidase) des lignées traitées à l’auxine. Les cellules sénescentes sont en bleu. F. Marquage immunohistochimique de coupes de tumeurs pour le marqueur de prolifération cellulaire Ki67 (en brun), avec contre coloration par hématoxyline. G. Coloration SA-β-gal (en bleu) et nuclear fast red (en rose) de coupes de tumeurs. H. Schéma comparant les perspectives thérapeutiques apportées par ces études. SASP : senescence-associated secretory phenotype. Figure adaptée de [10] et de [11]. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




