| Issue |
Med Sci (Paris)
Volume 38, Number 12, Décembre 2022
Un monde de virus
|
|
|---|---|---|
| Page(s) | 1043 - 1051 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2022169 | |
| Published online | 13 December 2022 | |
Les virus au service de la santé : les bactériophages
Viruses for health: Bacteriophages
1
Hospices civils de Lyon, France
2
Université Claude Bernard Lyon 1, France
3
Tumor Escape Resistance and Immunity Department, Cancer Research Center of Lyon (CRCL), Inserm U1052, CNRS UMR 5286, Lyon, France
4
Centre international de recherche en infectiologie (CIRI), Inserm U1111, CNRS UMR5308, ENS de Lyon, UCBL1, Lyon, France
5
Centre de références des IOA complexes de Lyon, CRIOAc Lyon, France
6
Laboratoire de recherche et développement de pharmacie galénique industrielle, plateforme FRIPHARM, faculté de pharmacie, laboratoire de biologie tissulaire et ingénierie thérapeutique – UMR 5305, université Claude Bernard Lyon 1, Lyon, France
** This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
Les bactériophages sont des virus naturels très répandus dans l’environnement qui ciblent spécifiquement les bactéries. Leur utilisation en médecine, connue sous le terme phagothérapie, consiste à les isoler, les caractériser, les cultiver, puis les purifier pour traiter des infections bactériennes. Il existe actuellement un renouveau pour la thérapie phagique, et sa mise en œuvre présuppose de disposer de phages actifs de qualité pharmaceutique. D’un point de vue réglementaire, le statut des phages n’est pas encore clairement défini par les autorités, mais la mise à disposition de phages produits par l’industrie pharmaceutique et les programmes de développement académiques, comme le programme PHAGEinLYON, constituent un tournant dans le déploiement de la phagothérapie.
Abstract
Bacteriophages are naturally occurring viruses that specifically target bacteria. They are widely distributed in the environment. The concept of phage therapy is to isolate phages, characterize them, cultivate them and then purify them to treat bacterial infections. There is currently a revival of phage therapy, and its implementation presupposes the availability of active phages of pharmaceutical quality. From a regulatory point of view, the status of phages is not yet clearly defined by the authorities. The availability of phages produced by the pharmaceutical industry and through academic development programs such as the PHAGEinLYON program represents a breakthrough in the development of phage therapy. Prosthetic joint infections and digestive diseases seem to be relevant indications, but preclinical studies and randomized clinical trials are now needed to be done.
sous l’égide du programme PHAGEinLYON
© 2022 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Vignette (© Philippe Roingeard).
Les phages à visée thérapeutique
Les bactériophages (nommés également phages) sont des virus naturels qui infectent les bactéries. Ils sont très répandus dans l’environnement, en particulier dans les environnements telluriques et surtout aqueux, tels que l’eau salée ou douce, ou les égouts. Les phages coévoluent avec les bactéries qu’ils infectent probablement depuis quelques milliards d’années. Le plus souvent, chaque phage est spécifique d’une seule espèce bactérienne, voire d’une population clonale. Il existe une grande diversité virale, mais la grande majorité des espèces décrites appartiennent à l’ordre des Caudovirales, et en particulier aux familles Myoviridae (phages ayant une queue contractile), Podoviridae (queue courte et non contractile) et Siphoviridae (queue longue filamenteuse et non contractile), avec des protéines structurales conservées qui forment ces différentes particules virales. Les phages ont un rôle majeur dans l’équilibre écologique du monde bactérien. En fonction de leur activité sur leur bactérie hôte, deux types de phages existent : les phages tempérés, qui accomplissent un cycle lytique et lysogénique, et les phages virulents, qui n’accomplissent qu’un cycle lytique (Figure 1). Au cours du cycle lysogénique, le génome des phages s’intègre dans le génome bactérien sous la forme d’un prophage. Ils peuvent ainsi contribuer à enrichir le patrimoine génétique de la bactérie, en intégrant des gènes codant des facteurs de virulence, comme des toxines, ou des facteurs facilitant l’échappement à l’immunité, ou des gènes de résistance aux antibiotiques. Sous certaines conditions, le prophage peut s’exciser et infecter une autre bactérie environnante de la même espèce en reprenant un cycle lytique. Lors d’un cycle lytique, les phages détournent la machinerie cellulaire bactérienne pour produire des centaines de nouveaux virions. Les bactériophages provoquent ensuite la lyse de la bactérie hôte par la production de protéines virales, telles que l’endolysine qui dégrade le peptidoglycane1, ou la holine qui forme des pores dans la membrane plasmique. Cette lyse aboutit à la libération de nouveaux virions qui vont pouvoir à leur tour infecter les bactéries environnantes, selon un processus potentiellement auto-entretenu (en théorie), jusqu’à la disparition complète de la communauté bactérienne [1, 2]. La phagothérapie (ou thérapie virale par les phages) consiste donc à isoler des phages naturels virulents (dans l’environnement humain), les cultiver puis les purifier pour traiter diverses infections bactériennes (Figure 2).
 |
Figure 1. Mécanisme d’action des phages. Le cycle lysogénique peut apporter des avantages à la bactérie, et le cycle lytique peut aboutir à l’éradication de la population bactérienne (adapté de [38]). |
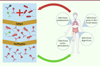 |
Figure 2. Isolement de phages dans l’environnement humain, sélection, amplification et production de phages purifiés pour traiter différentes infections bactériennes. |
Les phages en thérapeutique
La mise en œuvre de la phagothérapie dans une indication dédiée présuppose de disposer de phages actifs et d’une expertise clinique pour évaluer l’effet bénéfique potentiel de la phagothérapie.
Histoire de la phagothérapie
Historiquement, la phagothérapie a existé avant la découverte des antibiotiques. Le concept repose sur les travaux du microbiologiste Félix d’Hérelle (1873-1949), à l’Institut Pasteur de Paris, qui, dans les années 1920, isola des phages à partir des selles de patients ayant guéri de shigellose (une diarrhée infectieuse due à Shigella spp.), avec lesquels il traita, par voie orale, des patients souffrant de cette infection bactérienne digestive. Il avait alors décrit le bactériophage comme un agent « d’immunité », infectant la bactérie et permettant la guérison de l’infection. Un de ses disciples, le microbiologiste soviétique George Eliava (1892-1937), de retour en Géorgie, fonda à Tbilissi l’institut du bactériophage qui portera son nom (Institut George Eliava) ; la phagothérapie se développera ensuite particulièrement en Union soviétique (URSS) et en Pologne. En France, après avoir été développée à l’Institut Pasteur de Lyon dans les années 1960-1970, la phagothérapie fut abandonnée, en raison de la mise à disposition de divers antibiotiques à large spectre, administrables par voie intraveineuse ou par voie orale [3, 4].
Obtenir des phages de qualité pharmaceutique
La recherche de phages naturels dans l’environnement (ou phage discovery) nécessite la collecte d’eaux usées, riches en bactéries, mais également en phages lytiques ciblant différentes bactéries d’intérêt. Après des étapes de filtration, les eaux contenant les phages sont mises en culture avec la bactérie contre laquelle un ou des phages sont recherchés. En l’infectant, les phages lytiques spécifiques, s’ils sont présents, s’amplifient. Afin d’identifier chaque phage lytique d’intérêt et de le purifier, la procédure d’amplification et la culture sont réalisées plusieurs fois. Chaque phage sera finalement conservé dans une collection biologique (par exemple des staphylocoques pour les phages ciblant Staphylococcus aureus).
Le spectre d’activité de chaque phage lytique d’intérêt est évalué sur des collections de souches cliniques afin de sélectionner les plus pertinents. Mais avant d’envisager une utilisation chez l’homme, le processus final de purification est complexe : il nécessite une réamplification de la population de phages à partir d’une souche bactérienne dédiée à la production pharmaceutique, et nécessite d’éliminer les débris bactériens, les solvants et les polluants potentiellement présents dans le produit obtenu.
Les phages actuellement produits en Géorgie ou dans la Fédération de Russie ne répondent pas aux exigences de qualité pharmaceutique de l’Agence européenne du médicament (EMA). Quelques établissements pharmaceutiques français, européens ou américains cherchent à produire des phages répondant à ces exigences de qualité pharmaceutique. C’est également le cas de certaines structures publiques, comme l’hôpital Reine Astrid (Bruxelles, Belgique), ou les Hospices Civils de Lyon, avec notamment le programme PHAGEinLYON [5, 6]. Certains groupes de recherche ou établissements pharmaceutiques développent par ailleurs des phages génétiquement modifiés afin qu’ils résistent au système CRISPR-Cas mis en œuvre par les bactéries pour limiter l’infection virale, ou pour améliorer leurs propriétés antibactériennes ou élargir leur spectre d’hôtes [7].
Classification des phages
Le statut des phages n’est pas encore clairement défini par l’EMA. S’agissant de virus naturels, ils peuvent être considérés comme des allergènes, mais également comme des principes actifs (en anglais, API pour Active Pharmaceutical Ingredients), ou des médicaments, notamment des médicaments de thérapie innovante. Pour chacune de ces catégories, les processus de développement et les contrôles qualité seront différents [8].
En Belgique, les phages sont considérés comme des API. On retrouve ainsi, au sein de la pharmacopée2 belge, une monographie détaillant le processus de production et les contrôles qualité relatifs aux phages utilisés en thérapeutique [5]. Plus généralement, la phagothérapie correspond aujourd’hui au statut de préparation magistrale3 (compounding pharmacy) à base de phages naturels purifiés « sur mesure », permettant une phagothérapie dite personnalisée, pleinement adaptable à la souche infectante du patient. Ce statut de préparation magistrale existe en France comme en Europe, où la préparation répond aux exigences des bonnes pratiques de préparation (BPP). Cette phagothérapie personnalisée se distingue des cocktails de phages « fixes » développés par les industriels selon un processus similaire à celui appliqué pour la fabrication d’un médicament. Ces préparations répondent alors aux exigences des bonnes pratiques de fabrication (BPF), plus contraignantes en termes de processus de production, plus exigeantes en termes de qualité du produit final, mais permettant de produire des lots de phages plus importants [9].
Clarifier les exigences de qualité et de sécurité des phages, ainsi que la faisabilité de la phagothérapie, reste nécessaire car le statut du médicament n’est pas compatible avec une approche personnalisée, une approche qui semble indispensable compte-tenu de la spécificité du couple phage-bactérie et de leur dynamique de « coévolution ». La prise en compte de la personnalisation du traitement et de la biologie évolutive, essentielle pour le développement de la phagothérapie, nécessite donc de la définir avec le statut de préparation magistrale.
Les contrôles de qualité
En utilisant des phages « naturels » (qui ne sont donc pas génétiquement modifiés), et en fonction du statut du traitement (phagothérapie personnalisée ou recours à des cocktails « fixes »), les contrôles qualité peuvent varier. Au minimum, les phages d’intérêt préalablement mis en collection sont purifiés par des étapes successives d’amplification, de centrifugation et de filtration. Ils doivent ensuite être caractérisés avant une éventuelle utilisation en médecine humaine (comme c’est le cas pour, par exemple, les principes actifs chimiques). Cette caractérisation correspond, tout d’abord, à l’identification des phages (séquençage, microscopie électronique, absence de phages tempérés) et reprend les données concernant le processus de bioproduction (souche bactérienne utilisée pour l’amplification, techniques de purification). Des contrôles de qualité des lots préparés doivent ensuite être effectués (pureté, quantification, taux d’endotoxines, stérilité, pH, absence de débris cellulaires, cytotoxicité), et la stabilité (phages seuls sous forme de suspension ou sous forme de cocktail) doit être évaluée [5, 9]. Il est important de noter que les contraintes liées au statut BPF d’un médicament imposent une production par un laboratoire pharmaceutique avec des exigences pré-cliniques importantes (absence de toxicité cellulaire et recherche de la dose efficace grâce à des modèles in vitro et in vivo) et cliniques (essais cliniques).
Les phages disponibles en France en 2022
À ce jour, aucun phage n’a reçu d’autorisation de mise sur le marché (AMM). Les seuls phages à disposition sont des phages en cours d’évaluation dans des essais cliniques et développés par des industries pharmaceutiques. Il est cependant possible de demander un usage dit « compassionnel » si le patient ne peut être inclus dans l’essai. Des phages produits par des structures académiques peuvent également être utilisés dans ce cadre, à condition qu’ils répondent aux exigences de qualité demandées par l’Agence nationale de sécurité du médicament et des produits de santé (ANSM), exigences qui évoluent puisque le statut des phages n’est pas défini à l’échelle européenne. L’usage compassionnel n’est possible que si tous les traitements conventionnels ont échoué, chez un patient à haut risque de décès ou de perte fonctionnelle majeure, comme une amputation. Cela entre dans le cadre de la déclaration d’Helsinki élaboré par la World Medical Association (WMA), qui dicte les principes éthiques pour la recherche médicale impliquant des sujets humains ; un comité d’éthique local peut également être sollicité [10].
La phagothérapie dans les infections bactériennes
Les phages sont, en théorie, utilisables pour toutes les infections bactériennes, dès lors qu’il est possible de démontrer que le ou les phages que l’on souhaite utiliser sont actifs sur la bactérie ciblée. Il sera donc, en principe, toujours nécessaire de tester l’efficacité des phages sélectionnés sur la bactérie que l’on souhaite cibler avant d’envisager leur utilisation pour un traitement.
Avec l’augmentation des cas d’infection par des bactéries résistantes aux antibiotiques (antibiorésistance), les phages présentent un intérêt croissant pour le traitement des infections bactériennes, notamment celles dues aux bactéries à Gram négatif et aux bactéries hautement résistantes (BHRe) : les entérobactéries productrices de carbapénémase et les Pseudomonas aeruginosa multi – ou toto-résistants. Ces bactéries sont de plus en plus impliquées dans certaines situations où il n’existe, à défaut d’antibiotiques classiques, que peu de possibilités thérapeutiques : les antibiotiques efficaces disponibles étant alors coûteux et exclusivement utilisables par voie intraveineuse, comme le céfidérocol, ou les associations ceftazidime/avibactam ou ceftolozane/tazobactam récemment mises sur le marché [11]. Certains laboratoires pharmaceutiques cherchent des phages « universels » efficaces, par exemple, sur toutes les souches de Staphylococcus aureus, pour éviter la réalisation, avant le traitement, d’un phagogramme4. La réalisation du phagogramme nécessite en effet d’isoler la souche infectante ; il est coûteux en temps et n’est pas couramment réalisé, il reste « artisanal ». Ces limites rendent donc difficile le recours aux phages, notamment lorsqu’il existe une urgence thérapeutique [12].
L’existence d’une phagorésistance des bactéries, c’est-à-dire la capacité d’une bactérie à échapper à l’infection d’un bactériophage, a largement été décrite. Elle peut être présente d’emblée chez la bactérie ou se développer après que celle-ci ait été exposée aux phages. L’acquisition de telles résistances à une phagothérapie peut être prévenue en utilisant des cocktails de phages actifs. En effet la probabilité de sélectionner une population bactérienne résistante à plusieurs phages est très faible, ceux-ci utilisant des récepteurs différents sur la bactérie pour l’infecter [13].
La phagothérapie se place essentiellement comme une thérapie adjuvante, pour augmenter la probabilité de succès dans les infections bactériennes les plus sévères. Elle pourrait néanmoins également s’envisager comme une alternative à l’antibiothérapie dans les infections moins sévères afin de limiter la prescription d’antibiotiques, et in fine tenter de limiter la propagation de l’antibiorésistance. Ainsi, une phagothérapie pourrait être envisagée pour des infections mineures, urinaires ou digestives, à la place de l’antibiothérapie prescrite en médecine de ville.
Les infections de la peau et des tissus mous
Assez tôt dans l’histoire de la phagothérapie, des cocktails prêts à l’emploi, ont été produits pour cibler les streptocoques et S. aureus (les bactéries les plus fréquemment impliquées dans les infections de la peau et des tissus mous), responsables de maladies particulièrement courantes, notamment en cas de plaie traumatique. L’Union soviétique avait en effet élaboré de tels cocktails, mis à disposition de ses troupes, pour une application locale topique, préventive en cas de plaie traumatique, ou curative en cas d’infection avérée [3]. Plusieurs de ces cocktails sont toujours utilisés dans cette indication en Géorgie par le centre Eliava. En France, il n’existe aucun essai thérapeutique évaluant la phagothérapie dans les infections de la peau et des tissus mous ; de très nombreux antibiotiques ont en effet reçu une AMM et sont largement utilisés dans cette indication. En revanche, en Belgique, le recours aux phages en application locale est courant à l’hôpital Reine Astrid de Bruxelles, pour les patients brûlés nécessitant une prise en charge en réanimation, chez lesquels des surinfections par Pseudomonas aeruginosa sont fréquentes [14]. Une réduction de la charge bactérienne par les phages, certes moindre comparativement à un antibiotique de la famille des sulfamides associé à un sel d’argent antiseptique, appliqué localement, a été démontrée dans l’essai thérapeutique phagoburn de phase I/II publié en 2019 [15].
Les infections pulmonaires
Plusieurs cas d’infections pulmonaires graves traitées par phagothérapie personnalisée ont été publiés [16, 17]. La phagothérapie semble en effet pertinente dans cette indication, en thérapie adjuvante des antibiotiques, notamment chez les patients atteints de mucoviscidose, qui sont souvent colonisés et infectés par des souches de S. aureus ou de P. aeruginosa. La phagothérapie est parfois administrée par voie intraveineuse exclusive, par aérosols, ou par ces deux voies d’administration. Récemment, des infections graves à mycobactéries ont été traitées et guéries par une phagothérapie personnalisée [18].
Les infections ostéoarticulaires
Les infections ostéoarticulaires (IOA) sont des infections graves pouvant menacer le pronostic vital ou fonctionnel du patient. Toutes les IOA ne semblent pas être de bonnes indications de la phagothérapie. Les phages ont été utilisés avec succès pour traiter des IOA chroniques, comme des ostéites post-traumatiques ou les ostéomyélites [19]. Les infections associées à la pose de prothèses articulaires représentent également une bonne indication de la phagothérapie, notamment lorsqu’il s’agit d’une infection chronique chez des patients pour qui l’explantation de la prothèse aboutirait à une perte importante de fonction [20]. Chez ces patients, la principale cause d’échec de l’intervention semble liée à la persistance bactérienne à la surface de l’implant, sous la forme de biofilm. Dans différents modèles in vitro, les phages se révèlent capables de cibler ce biofilm bactérien, de manière synergique avec les antibiotiques [21].
Dans le cadre de son mandat de Centre de référence des IOA complexes (CRIOAc), les Hospices de Lyon développent des thématiques anti-infectieuses innovantes, dont la phagothérapie [22]. En effet, un centre de phagothérapie a été créé au sein du CRIOAc Lyon avec la mise en place d’une plateforme d’orientation et de validation du recours aux phages en réunion de concertation pluridisciplinaire (RCP) [6]. Depuis 2017, plus de 40 patients ont ainsi pu être traités par phagothérapie, majoritairement des patients présentant une infection de prothèses articulaires. Chez des patients présentant des infections récidivantes à S. aureus ou à P. aeruginosa (les deux seules bactéries que l’on peut actuellement traiter par phagothérapie en France), l’infection a pu être contrôlée par l’administration d’un cocktail de phages efficaces. Ce cocktail avait été administré comme thérapie adjuvante au cours d’une chirurgie dite conservatrice5, avec administration de phages localement dans la cavité articulaire, puis fermeture du site opératoire. Tous ces patients en impasse thérapeutique, avec des échecs itératifs (en dépit d’une ou plusieurs prises en charge antérieures par chirurgie et antibiothérapie), avaient reçu des antibiotiques au long cours. Aussi, l’effet précis des phages dans cette évolution favorable reste difficile à déterminer [6, 20, 23]. D’autres patients présentant une IOA pourraient potentiellement être éligibles à une phagothérapie personnalisée, notamment ceux présentant des abcédations (sur matériel ou non) dans lesquelles il serait possible d’injecter des phages.
Les infections urinaires
Les infections urinaires sont des infections courantes en médecine de ville. Elles affectent la vessie (cystite) ou les voies urinaires parenchymateuses (pyélonéphrite, prostatite). La problématique concerne cependant l’accès au site infecté, possible par voie orale avec les antibiotiques, mais a priori impossible avec les phages qui ne sont pas suffisamment absorbés au niveau du tractus digestif. Un essai thérapeutique a récemment évalué le cocktail Pyophage, élaboré par le centre Eliava en Géorgie. Ce cocktail a été administré par injection intravésicale pendant sept jours, dans des infections urinaires masculines, avant résection endoscopique urétrale de la prostate. Le taux de succès après phagothérapie ne s’est pas révélé inférieur à celui du groupe traité par antibiothérapie, mais pas supérieur à celui du groupe ayant reçu un placebo par voie intravésicale [24].
Les infections digestives
L’utilisation de bactériophages dans le traitement des infections bactériennes digestives est historique : il s’agit des premières infections bactériennes traitées par phagothérapie. Cette indication a fait l’objet de plusieurs travaux pré-cliniques aux résultats contrastés [25] (Tableau I). L’efficacité des phages pour éradiquer une cible bactérienne spécifique est en effet souvent mise en échec lorsque l’on se place dans une situation d’équilibre de l’écosystème intestinal, comme dans le cadre d’un portage asymptomatique (Salmonella Typhimurium, Escherichia coli). Une hétérogénéité spatiale existe également dans la lumière intestinale. Ainsi, dans certaines portions du tractus digestif, la présence d’une abondante couche de mucus peut protéger les bactéries cibles en réduisant leurs interactions avec les phages (Figure 3).
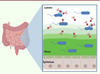 |
Figure 3. Hétérogénéité spatiale de la distribution bactérienne dans la lumière intestinale affectant les interactions phages/bactéries. |
Synthèse des principaux essais pré-cliniques de l’utilisation des phages dans le traitement des infections bactériennes intestinales (pour une revue spécifique, voir [25]).
Les résultats les plus significatifs ont cependant été observés dans des contextes d’infection symptomatique : infection par Vibrio cholerae ou par Yersinia enterocolitica. La notion de résilience du microbiote intestinal6 doit toujours être considérée, en particulier dans le cadre de la phagothérapie, et suggère la pertinence d’approches combinées ciblant plusieurs composantes de l’écosystème intestinal, comme le compartiment immunitaire, ou l’association d’un cocktail de phages avec un traitement antibiotique, par exemple.
Pour cibler des bactéries présentes dans l’intestin, la phagothérapie repose donc sur différents paradigmes : cibler directement des agents pathogènes digestifs responsables d’une infection symptomatique (diarrhées, iléo-colite) ; cibler des bactéries digestives responsables d’une colonisation avec un risque d’infection secondaire ou de diffusion dans l’environnement ; restaurer un écosystème microbien conférant une résistance accrue aux agents pathogènes « opportunistes », comme c’est le cas dans l’infection à Clostridioides difficile (anciennement Clostridium difficile) (ICD).
Pour les agents pathogènes digestifs responsables de diarrhées, plusieurs études avaient évalué l’effet de phages ciblant la bactérie Vibrio cholerae, responsable du choléra, une infection digestive hautement contagieuse et grave, afin de proposer une alternative aux antibiotiques. Les résultats se sont révélés contrastés, et aucun essai thérapeutique récent n’a pu être concluant [3, 26]. Dans les diarrhées infantiles, un essai a évalué un cocktail de phages ciblant E. coli, mais les phages n’ont pas apporté de bénéfice clinique, en raison d’une couverture insuffisante des souches bactériennes responsables des infections par les phages utilisés, mais aussi de la nécessité d’utiliser des doses de phages oraux élevées [27].
Pour les agents pathogènes à l’origine de colonisation du tractus digestif, le recours aux phages semble pertinent pour envisager l’éradication d’un portage de bactéries hautement résistantes (BHRe). Des préparations personnalisées de phages actifs, administrables par voies orale et intra-rectale, ont permis, par exemple, d’éradiquer le portage digestif de la bactérie Klebsiella pneumoniae productrice de carbapénémase, chez un patient qui présentait des infections itératives par cette bactérie [28].
Dans les infections à Clostridioides difficile (ICD), les phages pourraient être utilisés comme outil thérapeutique. C. difficile est une bactérie à Gram positif, sporulée, intestinale qui produit des toxines à l’origine d’une colite inflammatoire. Avec plus de 120 000 cas par an en Europe, l’ICD constitue un enjeu de santé publique, en particulier en raison de la fréquence des récidives pour lesquelles les possibilités thérapeutiques restent limitées. Il s’agit d’un modèle unique de maladie de l’écosystème intestinal favorisée par une rupture de l’homéostasie des relations entre l’hôte et son microbiote, notamment à la suite d’une antibiothérapie. Les bactériophages sont impliqués à différents niveaux dans la physiopathologie de cette infection. En effet, en plus du potentiel infectieux des souches de C. difficile, certains phages peuvent favoriser le transfert de matériel génétique pathogénique entre les souches bactériennes, comme des gènes codant des toxines, identifiées dans le génome de certains phages, ou promouvoir une modification du microbiote qui permettrait la survenue d’une ICD [29].
L’utilisation de phages pour le traitement de l’ICD a été surtout évaluée chez l’animal. Dans un modèle de hamster, un cocktail de bactériophages spécifiques ciblant la bactérie a ainsi permis de diminuer la charge bactérienne, in vitro et in vivo, mais sans conférer de protection durable contre l’infection, avec un taux de survie analogue chez les animaux traités et non traités infectés par une souche toxinogène de C. difficile [30]. La modification génétique de phages à l’aide, par exemple, du système CRISPR-Cas3, pour augmenter leur pouvoir lytique, pourrait toutefois améliorer l’efficacité de cette approche [31].
La modulation de la composition du microbiote que les phages induisent pourrait être à l’origine, au moins en partie, des effets thérapeutiques que l’on observe avec la transplantation de microbiote fécal (TMF), la thérapie la plus efficace aujourd’hui dans le traitement des formes multi-récidivantes d’ICD. Une étude suggère ainsi l’existence d’une corrélation entre la diversité en phages présents dans les selles du donneur et l’efficacité de la TMF [32]. Dans une étude prospective de faible effectif, l’implantation des phages de la famille des Caudovirales du donneur s’est révélée également associée à une meilleure réponse à la TMF, en corrélation avec des modifications de plusieurs familles bactériennes [33]. Enfin, l’observation que le transfert d’un filtrat sans bactérie vivante mais contenant des phages isolés de selles d’un donneur sain était associé à une guérison chez des patients présentant une ICD récidivante, renforce l’hypothèse d’un rôle thérapeutique direct des phages dans cette infection [34]. Ces différents travaux suggèrent donc que les modulations du virome pourraient constituer un outil thérapeutique d’intérêt au cours de l’ICD. Des études supplémentaires sont néanmoins nécessaires pour en préciser les modalités, l’efficacité clinique et la place dans l’arsenal thérapeutique déjà existant.
Il existe enfin un rationnel pour moduler le virome dans les maladies multi-factorielles non infectieuses dans lesquelles le microbiote a été identifié comme un acteur majeur. Le rôle du microbiote dans les maladies inflammatoires chroniques de l’intestin (MICI), telles que la maladie de Crohn ou la recto-colite hémorragique, a ainsi été particulièrement exploré. Les patients atteints de ces maladies développent une inflammation chronique intestinale liée à une réponse immunitaire inappropriée vis-à-vis des antigènes microbiens ou alimentaires. Bien que la majeure partie des travaux étudiant le rôle du microbiote dans les MICI portent sur son contingent bactérien, plusieurs études suggèrent un rôle significatif du virome. Ainsi, une augmentation de la diversité de l’ensemble du virome intestinal, avec une expansion des bactériophages de l’ordre des Caudovirales, a été observée chez les patients présentant une maladie de Crohn [35]. L’analyse de la composition et du profil fonctionnel des phages intestinaux révèle également une modification profonde de la structure du virome chez les patients atteints de MICI avec une augmentation de la proportion de phages virulents et libres [36]. Ces modifications du virome sont corrélées à des modifications du microbiote bactérien, illustrant les interconnexions entre les différents micro-organismes peuplant l’intestin et l’importance d’une approche incluant l’ensemble de ces micro-organismes dans la compréhension du rôle du microbiote dans les maladies intestinales. Notons que l’hôte n’est pas exclu de ces interactions puisque des études épidémiologiques ont montré une association entre les MICI et les polymorphismes des gènes FUT (fucosyltransférase) 2 et 3 (qui pilotent la synthèse des antigènes des groupes sanguins) et les ligands des norovirus et des rotavirus dans l’intestin [37].
Conclusion
L’ère du développement des phages à usage thérapeutique s’est ouverte il y a 100 ans, dans les années 1920. Mais ce n’est que maintenant que nous disposons des outils techniques qui permettent de mieux comprendre cette thérapie, de produire des cocktails de phages personnalisés de qualité, de les utiliser de manière sécurisée, d’évaluer leur effet potentiellement bénéfique en médecine humaine, et d’évaluer la réponse immunitaire (cellulaire et humorale) après exposition à des phages thérapeutiques. Les programmes de développement académiques de recours aux phages thérapeutiques (comme le programme PHAGEinLYON) devraient permettre une rupture dans le développement de la phagothérapie. Ils permettront en effet de mieux identifier les maladies pour lesquelles la phagothérapie apportera un bénéfice. Ils devraient ouvrir la voie à la production académique de phages de qualité pharmaceutique, complémentaires de ceux proposés par les industriels. Ils vont enfin faciliter le recours aux phages à titre compassionnel et promouvoir des essais thérapeutiques dans diverses infections bactériennes, ou d’autres maladies impliquant une dysfonction de la relation hôte-microbiote, comme les MICI. Enfin, ces programmes de développement académique se connecteront entre eux, à l’échelle européenne, dans le cadre d’un réseau qui sera promu par le groupe ESGNTA (ESCMID Study group for Non-Traditional Antibacterial therapy) de la European Society of Clinical Microbiology and Infectious Diseases (ESCMID). La phagothérapie 2.0 s’annonce ainsi comme une « innovation » médicale du xxie siècle en santé humaine.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Le programme PHAGEinLYON est soutenu par les Hospices Civils de Lyon et la fondation HCL, l’université Claude Bernard Lyon 1, le Centre international de recherche en infectiologie (CIRI) et l’Institut des sciences pharmaceutiques et biologiques (ISPB). Le programme intègre Tristan Ferry et Frédéric Laurent (respectivement coordinateurs de la partie clinique et de la partie laboratoire) ; Myrtille Le Bouar, Gilles Leboucher, Thomas Briot ; Mathieu Medina, Camille Kolenda, Floriane Laumay, Mélanie Bonhomme, Leslie Blazere, Tiphaine Legendre, Eline Terrazzoni, Fabrice Pirot, Camille Merienne, Samira Filali, Benjamine Lapras, Chloé Marchand.
Le peptidoglycane est un composant essentiel de la paroi cellulaire bactérienne. Il joue un rôle crucial dans la structure et la forme de la cellule bactérienne.
Ouvrage de référence détaillant les critères de pureté et les méthodes d’analyse de plantes médicinales et de certains principes actifs.
Un produit préparé par un pharmacien destiné à un malade déterminé lorsqu’il n’existe pas de spécialité pharmaceutique adaptée ou disponible.
Un phagogramme est un test in vitro visant à démontrer l’activité d’un ou de plusieurs phages sur la souche bactérienne responsable de l’infection, chez un patient donné.
Une arthrotomie-lavage : ouverture chirurgicale de l’articulation au cours de laquelle est réalisé un lavage pulsé.
La résilience signifie que le microbiote intestinal se renouvelle et se reconstitue.
Références
- Ackermann HW. 5500 Phages examined in the electron microscope. Arch Virol 2007 ; 152 : 227–243. [CrossRef] [PubMed] [Google Scholar]
- Bergh Ø. BØrsheim KY, Bratbak G, Heldal M. High abundance of viruses found in aquatic environments. Nature 1989 ; 340 : 467–468. [CrossRef] [PubMed] [Google Scholar]
- Summers WC. Bacteriophage therapy. Annu Rev Microbiol 2001 ; 55 : 437–451. [CrossRef] [PubMed] [Google Scholar]
- Ferry T, Kolenda C, Gustave CAet al. Phage therapy in bone and joint infection : history, scientific basis, feasibility and perspectives in France. Virologie 2018 ; 24 : 4–11. [CrossRef] [Google Scholar]
- Pirnay JP, Verbeken G, Ceyssens PJet al. The Magistral Phage. Viruses 2018 ; 10. [Google Scholar]
- Ferry T, Kolenda C, Briot T, et al. Implementation of a complex bone and joint infection phage therapy centre in France : Lessons to be learned after 4 years’ experience. Clin Microbiol Infect 2021; S1198-743X(21)00556-5. [PubMed] [Google Scholar]
- Chen Y, Batra H, Dong Jet al. Genetic Engineering of Bacteriophages against infectious diseases. Front Microbiol 2019 ; 10 : 954. [CrossRef] [PubMed] [Google Scholar]
- Fauconnier A.. Phage therapy regulation : from night to dawn. Viruses 2019 ; 11 : E352. [CrossRef] [PubMed] [Google Scholar]
- Merabishvili M, Pirnay JP, Verbeken Get al. Quality-controlled small-scale production of a well-defined bacteriophage cocktail for use in human clinical trials. PloS One 2009 ; 4 : e4944. [CrossRef] [PubMed] [Google Scholar]
- World Medical Association World medical association declaration of Helsinki : ethical principles for medical research involving human subjects. JAMA 2013 ; 310 : 2191–2194. [CrossRef] [PubMed] [Google Scholar]
- Tamma PD, Aitken SL, Bonomo RA, et al. Infectious Diseases Society of America 2022 guidance on the treatment of extended-Spectrum β-lactamase producing enterobacterales (ESBL-E), carbapenem-resistant enterobacterales (CRE), and Pseudomonas aeruginosa with difficult-to-treat resistance (DTR-P. aeruginosa). Clin Infect Dis 2022; ciac268. [Google Scholar]
- Lood C, Boeckaerts D, Stock M, et al. Digital phagograms : predicting phage infectivity through a multilayer machine learning approach. Curr Opin Virol 2022; 52 : 174–81. [CrossRef] [PubMed] [Google Scholar]
- Schooley RT, Biswas B, Gill JJet al. Development and use of personalized bacteriophage-based therapeutic cocktails to treat a patient with a disseminated resistant Acinetobacter baumannii Infection. Antimicrob Agents Chemother 2017 ; 61. [CrossRef] [PubMed] [Google Scholar]
- Djebara S, Maussen C, De Vos D, et al. Processing phage therapy requests in a Brussels military hospital : Lessons identified. Viruses 2019 17; 11(3) [Google Scholar]
- Jault P, Leclerc T, Jennes Set al. Efficacy and tolerability of a cocktail of bacteriophages to treat burn wounds infected by Pseudomonas aeruginosa (PhagoBurn): a randomised, controlled, double-blind phase 1/2 trial. Lancet Infect Dis 2019 ; 19 : 35–45. [CrossRef] [PubMed] [Google Scholar]
- Law N, Logan C, Yung Get al. Successful adjunctive use of bacteriophage therapy for treatment of multidrug-resistant Pseudomonas aeruginosa infection in a cystic fibrosis patient. Infection 2019 ; 47 : 665–668. [CrossRef] [PubMed] [Google Scholar]
- Chen P, Liu Z, Tan X, et al. Bacteriophage therapy for empyema caused by carbapenem-resistant Pseudomonas aeruginosa. Biosci Trends 2022; 16 : 158–62. [CrossRef] [PubMed] [Google Scholar]
- Dedrick RM, Guerrero-Bustamante CA, Garlena RAet al. Engineered bacteriophages for treatment of a patient with a disseminated drug-resistant Mycobacterium abscessus. Nat Med 2019 ; 25 : 730–733. [CrossRef] [PubMed] [Google Scholar]
- Ferry T, Kolenda C, Briot T, et al. Past and future of phage therapy and phage-derived proteins in patients with bone and joint infection. Viruses 2021; 13 : 2414. [CrossRef] [PubMed] [Google Scholar]
- Ferry T, Kolenda C, Batailler C, et al. Phage therapy as adjuvant to conservative surgery and antibiotics to salvage patients with relapsing S. aureus prosthetic knee infection. Front Med 2020; 7 : 570572. [CrossRef] [Google Scholar]
- Kolenda C, Josse J, Medina M, et al. Evaluation of the activity of a combination of three bacteriophages alone or in association with antibiotics on Staphylococcus aureus embedded in biofilm or internalized in osteoblasts. Antimicrob Agents Chemother 2020 21; 64. [Google Scholar]
- Ferry T, Seng P, Mainard Det al. The CRIOAc healthcare network in France : A nationwide Health Ministry program to improve the management of bone and joint infection. Orthop Traumatol Surg Res 2019 ; 105 : 185–190. [CrossRef] [PubMed] [Google Scholar]
- Ferry T, Kolenda C, Batailler C, et al. Case report : Arthroscopic “Debridement Antibiotics and Implant Retention” with local injection of personalized phage therapy to salvage a relapsing Pseudomonas aeruginosa prosthetic knee infection. Front Med 2021; 8 : 569159. [CrossRef] [Google Scholar]
- Leitner L, Ujmajuridze A, Chanishvili N, et al. Intravesical bacteriophages for treating urinary tract infections in patients undergoing transurethral resection of the prostate : a randomised, placebo-controlled, double-blind clinical trial. Lancet Infect Dis 2021; 21 : 427–36. [CrossRef] [PubMed] [Google Scholar]
- Javaudin F, Latour C, Debarbieux L, Lamy-Besnier Q. Intestinal bacteriophage therapy : Looking for optimal efficacy. Clin Microbiol Rev 2021; 34 : e0013621. [CrossRef] [PubMed] [Google Scholar]
- Marcuk LM, Nikiforov VN, Scerbak JFet al. Clinical studies of the use of bacteriophage in the treatment of cholera. Bull World Health Organ 1971 ; 45 : 77–83. [PubMed] [Google Scholar]
- Sarker SA, Sultana S, Reuteler Get al. Oral phage therapy of acute bacterial diarrhea with two coliphage preparations : A randomized trial in children From Bangladesh. EBioMedicine 2016 ; 4 : 124–137. [CrossRef] [PubMed] [Google Scholar]
- Corbellino M, Kieffer N, Kutateladze M, et al. Eradication of a multidrug-Resistant, carbapenemase-producing Klebsiella pneumoniae isolate following oral and intra-rectal therapy with a custom made, lytic bacteriophage preparation. Clin Infect Dis 2020; 70 : 1998–2001. [CrossRef] [PubMed] [Google Scholar]
- Riedel T, Wittmann J, Bunk Bet al. A Clostridioides difficile bacteriophage genome encodes functional binary toxin-associated genes. J Biotechnol 2017 ; 250 : 23–28. [CrossRef] [PubMed] [Google Scholar]
- Nale JY, Spencer J, Hargreaves KRet al. Bacteriophage combinations significantly reduce Clostridium difficile growth in vitro and proliferation in vivo. Antimicrob Agents Chemother 2016 ; 60 : 968–981. [CrossRef] [PubMed] [Google Scholar]
- Selle K, Fletcher JR, Tuson H, et al. in vivo targeting of Clostridioides difficile using phage-delivered CRISPR-Cas3 antimicrobials. mBio 2020; 11 : e00019–20. [CrossRef] [PubMed] [Google Scholar]
- Park H, Laffin MR, Jovel Jet al. The success of fecal microbial transplantation in Clostridium difficile infection correlates with bacteriophage relative abundance in the donor : a retrospective cohort study. Gut Microbes 2019 ; 10 : 676–687. [CrossRef] [PubMed] [Google Scholar]
- Zuo T, Wong SH, Lam Ket al. Bacteriophage transfer during faecal microbiota transplantation in Clostridium difficile infection is associated with treatment outcome. Gut 2018 ; 67 : 634–643. [PubMed] [Google Scholar]
- Ott SJ, Waetzig GH, Rehman Aet al. Efficacy of sterile fecal filtrate transfer for treating patients with Clostridium difficile infection. Gastroenterology 2017 ; 152 : 799–811 e7. [Google Scholar]
- Norman JM, Handley SA, Baldridge MTet al. Disease-specific alterations in the enteric virome in inflammatory bowel disease. Cell 2015 ; 160 : 447–460. [CrossRef] [PubMed] [Google Scholar]
- Clooney AG, Sutton TDS, Shkoporov ANet al. Whole-virome analysis sheds light on viral dark matter in inflammatory bowel disease. Cell Host Microbe 2019 ; 26 : 764–78.e5. [CrossRef] [PubMed] [Google Scholar]
- Tarris G, de Rougemont A, Charkaoui M, et al. Enteric Viruses and inflammatory bowel disease. Viruses 2021; 13 : 104. [CrossRef] [PubMed] [Google Scholar]
- Ferry T, Kolenda C, Gustave CA, et al. Phagothérapie pour les patients présentant une infection ostéoarticulaire : historique, fondements, faisabilité et perspectives en France. Virologie (Montrouge) 2020; 24 : 49–56. [PubMed] [Google Scholar]
Liste des tableaux
Synthèse des principaux essais pré-cliniques de l’utilisation des phages dans le traitement des infections bactériennes intestinales (pour une revue spécifique, voir [25]).
Liste des figures
 |
Figure 1. Mécanisme d’action des phages. Le cycle lysogénique peut apporter des avantages à la bactérie, et le cycle lytique peut aboutir à l’éradication de la population bactérienne (adapté de [38]). |
| Dans le texte | |
 |
Figure 2. Isolement de phages dans l’environnement humain, sélection, amplification et production de phages purifiés pour traiter différentes infections bactériennes. |
| Dans le texte | |
 |
Figure 3. Hétérogénéité spatiale de la distribution bactérienne dans la lumière intestinale affectant les interactions phages/bactéries. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




