| Issue |
Med Sci (Paris)
Volume 37, Novembre 2021
Les Cahiers de Myologie
|
|
|---|---|---|
| Page(s) | 22 - 24 | |
| Section | Mise au point | |
| DOI | https://doi.org/10.1051/medsci/2021186 | |
| Published online | 08 December 2021 | |
Extraction automatique de repères vertébraux à partir d’échographies
Automatic extraction of vertebral landmarks from ultrasound images
1
École de Technologie Supérieure, Montréal, Canada
2
CHU Sainte-Justine, Montréal, Canada
3
École Polytechnique Montréal, Canada
Certaines formes de myopathies telles que la dystrophie musculaire de Duchenne entraînent une dégénérescence progressive des muscles chez le patient. Ceci se traduit par l’apparition d’une scoliose dont la gravité augmente au cours du temps. La norme clinique pour le suivi de la scoliose consiste à réaliser un examen radiographique. Malheureusement, l’exposition répétée aux rayons X est nocive pour la santé du patient. L’échographie est une technique d’imagerie médicale non irradiante qui utilise des ondes ultrasonores (US). Cependant, l’interprétation des échographies de vertèbres est souvent difficile en raison de la qualité variable des images. En réponse à ce défi, nous présentons une méthode pour localiser automatiquement les vertèbres sur les échographies. La validation de cette approche reproductible laisse à penser qu’il serait possible, à terme, de remplacer une partie des examens radiographiques standards par l’échographie.
Abstract
Some forms of myopathies such as Duchenne muscular dystrophy cause a progressive degeneration of the patient’s muscles. This results in the development of scoliosis, which increases in severity over time. The clinical standard for monitoring scoliosis is to perform an X-ray on a regular basis. Unfortunately, repeated exposure to X-rays is harmful to the patient’s health. Ultrasound imaging is a radiation-free modality that uses ultrasound (US) waves. However, the interpretation of vertebral ultrasound images is often difficult due to the variable quality of the image. In order to tackle this challenge, we present a method to localize the vertebrae on US images automatically. The validation of this reproducible approach suggests that it would be possible, in the long term, to replace part of the X-ray exams by US imaging.
© 2021 médecine/sciences – Inserm
© DR Alysson Araujo
Introduction
La scoliose est caractérisée par une déformation en 3D de la colonne vertébrale. Cette déformation présente un risque potentiel d’aggravation au cours du temps. Par conséquent, il est nécessaire de réaliser un examen radiographique périodique afin d’évaluer la progression de la déformation. C’est notamment le cas pour les scolioses progressives causées par certaines formes de myopathies telle que la dystrophie musculaire de Duchenne [1]. Un examen radiographique tous les six mois est alors préconisé durant la période de croissance pubertaire. La fréquence des examens peut ensuite être réduite à un an, une fois la maturité squelettique atteinte. Malheureusement, ceci entraîne une exposition répétée aux radiations préjudiciable à la santé du patient [2].
L’échographie main-libre [3] représente une alternative aux rayons X. Lors d’une acquisition par échographie à main levée, une sonde US standard 2D est couplée avec un capteur de position 3D [4]. Typiquement, la surface postérieure des vertèbres est segmentée et des repères anatomiques tels que le processus épineux, les lames et les processus transverses sont utilisés pour évaluer la sévérité de la déformation scoliotique [5]. La norme clinique pour évaluer la scoliose est l’angle de Cobb, qui est mesuré à partir d’une radiographie antéro-postérieure [6]. Bien que les vertèbres apparaissent moins clairement sur les échographies que les radiographies (seule la surface postérieure est visible), différentes approches pour estimer l’angle de Cobb par proxy telles que les méthodes du centre des lames [7], de l’angle du processus épineux [8] et de l’angle des processus transverses [9] ont été proposées.
Cependant, le contraste variable des échographies durant les acquisitions US main-libre rend difficile l’interprétation de ces dernières. En particulier, la vertèbre apparaît avec une forte intensité seulement si l’axe de la sonde est positionné de façon orthogonale à la surface osseuse. Ceci rend plus difficile la localisation précise de structures osseuses, tel le processus épineux, du fait de la visibilité partielle dans le plan transverse. De ce fait, les méthodes précédemment citées pour estimer l’angle de Cobb à partir d’échographies sont manuelles ou semi-automatiques [7–9]. Il revient alors généralement au clinicien d’interpréter ces images. La pertinence de l’interprétation est donc sujette à son expertise, en plus de lui prendre un temps précieux.
Méthode
En réponse à ce défi, nous proposons d’extraire de façon automatique des repères anatomiques sur les vertèbres. La vertèbre présente une forme typique en W sur les échographies, laquelle est divisée en deux V par un axe de symétrie vertical (Figure 1). Le point de jonction entre ces deux V correspond au processus épineux (PE), tandis que la partie la plus éloignée de l’axe de symétrie de chaque V correspond respectivement aux lames gauche (LG) et droite (LD) de la vertèbre.
 |
Figure 1. La forme en W de la vertèbre (en bleu) avec trois repères anatomiques (PE : processus épineux, LG : lame gauche et LD : lame droite) en jaune (© Substance ETS). |
Ces informations sont utilisées pour extraire de façon reproductible un repère dans chacune des zones anatomiques : PE, LG, LD (Figure 2). Les sommes respectives des intensités des pixels selon les lignes (à droite) et les colonnes (en haut) sont calculées (en bleu) puis normalisées (en vert). Les repères anatomiques sont finalement identifiés en se basant sur les passages par zéro (en rouge).
 |
Figure 2. Représentation schématique de l’échographie de vertèbre avec les sommes des intensités des pixels selon les lignes (à droite) et les colonnes (en haut) avant (en bleu) et après (en vert) normalisation (© Substance ETS). |
Validation
Notre méthode a été validée par deux expériences [10]. D’une part, les vertèbres d’un cadavre de porc ont été acquises en 3D par échographie à main levée. Le volume 3D correspondant a aussi été reconstruit par tomodensitométrie (CT Scan) comme référence. La section CT correspondant à chaque échographie est ainsi obtenue à partir d’une transformation géométrique. D’autre part, les vertèbres de cinq sujets sains ont été acquises par échographie 2D avec des sondes US curvilinéaire (6C2) et linéaire (14L5). Trois observateurs expérimentés ont manuellement annoté les repères vertébraux pour chaque échographie. La position moyenne des trois annotations a été prise comme référence.
Résultats
Le Tableau I montre les sommes des distances moyennes (SDM) entre les positions des repères extraits de façon automatique (notre méthode) et les méthodes de référence (tomodensitométrie ou annotation manuelle moyenne) pour les trois repères vertébraux extraits.
Somme des distances moyennes pour les repères vertébraux extraits : processus épineux (PE), lame gauche (LG) et lame droite (LG). Sondes US curvilinéaires (6C2).
La SDM est inférieure à 2 mm lorsque l’échographie est de bonne qualité, ce qui satisfait à la précision clinique requise pour planifier des chirurgies du rachis [11]. La sonde curvilinéaire (6C2) offre une meilleure visibilité en profondeur que la sonde linéaire (14L5), expliquant ainsi que les résultats soient moins bons pour les lames dans le second cas. La Figure 3 montre les résultats obtenus avec notre méthode sur le cadavre de porc, et les sujets sains pour les sondes 6C2 et 12L5.
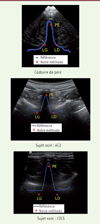 |
Figure 3. Extraction automatique des repères anatomiques (PE : processus épineux, LG : lame gauche et LD : lame droite) (© Arnaud Brignol). |
À titre de comparaison, l’annotation manuelle d’une échographie prend environ 30 secondes, tandis que l’annotation automatique par notre méthode dure moins d’une seconde. Notre méthode représente par conséquent une solution reproductible et rapide pour l’analyse des échographies de vertèbres.
Conclusion
Nos résultats sont prometteurs et indiquent qu’il serait possible de remplacer à terme une partie des examens radiographiques par un examen échographique. L’exposition du patient aux radiations s’en trouverait ainsi réduite. Des examens échographiques plus fréquents permettraient de réaliser un meilleur suivi de la scoliose, ainsi que de proposer un traitement plus adapté au cas de chaque patient.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Ce projet de recherche a été financé par le Conseil de recherches en sciences naturelles et en génie du Canada.
Références
- Apkon SD, Alman B, Birnkrant DJ, et al. Orthopedic and surgical management of the patient with Duchenne muscular dystrophy. Pediatrics 2018 ; 142 (suppl 2) : S82–S89. [CrossRef] [PubMed] [Google Scholar]
- Luo TD, Stans AA, Schueler BA, et al. Cumulative radiation exposure with EOS imaging compared with standard spine radiographs. Spine Deformity 2015 ; 3 : 144–150. [CrossRef] [PubMed] [Google Scholar]
- Zheng YP, Lee TTY, Lai KKL, et al. A reliability and validity study for Scolioscan: a radiation-free scoliosis assessment system using 3D ultrasound imaging. Scoliosis Spinal Disord 2016 ; 11 : 1–15. [CrossRef] [PubMed] [Google Scholar]
- Mozaffari MH, Lee WS. Freehand 3-D ultrasound imaging: a systematic review. Ultrasound Med Biol 2017 ; 43 : 2099–2124. [CrossRef] [PubMed] [Google Scholar]
- Young M, Hill DL, Zheng R, et al. Reliability and accuracy of ultrasound measurements with and without the aid of previous radiographs in adolescent idiopathic scoliosis (AIS). Eur Spine J 2015 ; 24 : 1427–1433. [CrossRef] [PubMed] [Google Scholar]
- Wang J, Zhang J, Xu R, et al. Measurement of scoliosis Cobb angle by end vertebra tilt angle method. J Orthopaedic Surg Res 2018 ; 13 : 1–7. [CrossRef] [Google Scholar]
- Chen W, Le LH, Lou EH. Reliability of the axial vertebral rotation measurements of adolescent idiopathic scoliosis using the center of lamina method on ultrasound images: in vitro and in vivo study. Eur Spine J 2016 ; 25 : 3265–3273. [CrossRef] [PubMed] [Google Scholar]
- Li M, Cheng J, Ying M, et al. Could clinical ultrasound improve the fitting of spinal orthosis for the patients with AIS?. Eur Spine J 2012 ; 21 : 1926–1935. [CrossRef] [PubMed] [Google Scholar]
- Ungi T, King F, Kempston M, et al. Spinal curvature measurement by tracked ultrasound snapshots. Ultrasound Med Biol 2014 ; 40 : 447–454. [CrossRef] [PubMed] [Google Scholar]
- Brignol A, Gueziri HE, Cheriet F, et al. Automatic extraction of vertebral landmarks from ultrasound images: A pilot study. Comput Biol Med 2020; 122 : 103838. [CrossRef] [PubMed] [Google Scholar]
- Cleary K.. Final report of the technical requirements for image-guided spine procedures workshop. Computer Aided Surg 2000 ; 5 : 180–215. [Google Scholar]
Liste des tableaux
Somme des distances moyennes pour les repères vertébraux extraits : processus épineux (PE), lame gauche (LG) et lame droite (LG). Sondes US curvilinéaires (6C2).
Liste des figures
 |
Figure 1. La forme en W de la vertèbre (en bleu) avec trois repères anatomiques (PE : processus épineux, LG : lame gauche et LD : lame droite) en jaune (© Substance ETS). |
| Dans le texte | |
 |
Figure 2. Représentation schématique de l’échographie de vertèbre avec les sommes des intensités des pixels selon les lignes (à droite) et les colonnes (en haut) avant (en bleu) et après (en vert) normalisation (© Substance ETS). |
| Dans le texte | |
 |
Figure 3. Extraction automatique des repères anatomiques (PE : processus épineux, LG : lame gauche et LD : lame droite) (© Arnaud Brignol). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




