| Issue |
Med Sci (Paris)
Volume 37, Number 8-9, Août–Septembre 2021
|
|
|---|---|---|
| Page(s) | 697 - 700 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/2021096 | |
| Published online | 07 September 2021 | |
La formation des vésicules intraluminales de l’endosome est contrôlée par la tension membranaire
The biogenesis of intra-lumenal vesicles is regulated by endosomal membrane tension
1
Département de biochimie, université de Genève, 30 quai Ernest Ansermet, CH-1211 Genève, Suisse.
2
Pôle de recherche national en biologie chimique, université de Genève, CH-1211 Genève, Suisse.
3
Département de chimie organique, université de Genève, CH-1211 Genève, Suisse.
a vincent.mercier@unige.ch
b aurelien.roux@unige.ch
c jean.gruenberg@unige.ch
Des récepteurs présents à la surface de la cellule déclenchent des cascades de signalisation intracellulaire après avoir lié le facteur de croissance ou l’hormone peptidique qui leur est spécifique. Cette signalisation, qui modifie le programme d’expression génique de la cellule, est régulée par l’endocytose du récepteur, suivie de sa dégradation dans les lysosomes, afin de protéger la cellule contre une surexposition de ce récepteur, qui aurait un effet oncogénique (Figure 1A). Lors de ce processus, le récepteur transmembranaire, activé par son ligand, est transporté de la membrane plasmique vers l’endosome précoce, et est modifié par ubiquitination de son domaine cytoplasmique (Figure 1A). L’ubiquitine sert alors de signal de reconnaissance pour une sous-unité du complexe protéique ESCRT-0 (endosomal sorting complex required for transport), qui va alors recruter le complexe ESCRT-I, puis le complexe ESCRT-II. Ces trois complexes vont ensuite servir de site de nucléation pour la polymérisation du complexe ESCRT-III sous forme de filaments spiralés, et ainsi permettre la déformation de la membrane vers l’intérieur de la lumière de l’endosome, et la formation de vésicules intraluminales [1]. Les vésicules intraluminales contiennent les récepteurs transmembranaires, parfois encore liés à leur ligand. L’accumulation des vésicules intraluminales dans la lumière de l’endosome conduit à la formation d’un endosome d’apparence multi-vésiculaire [1]. Alternativement, comme les complexes ESCRT-0/I/II de la voie « classique », la protéine ESCRT ALIX (ALG-2 interacting protein X) permet aussi la nucléation de filaments de ESCRT-III à la membrane de l’endosome [2]. Les vésicules intraluminales et leurs récepteurs associés sont ensuite transportés vers l’endosome tardif (ou endo-lysosome) et, finalement, vers les lysosomes pour y être dégradés. Dans certaines cellules, les vésicules intraluminales peuvent aussi être sécrétées dans le milieu extracellulaire sous la forme d’exosomes, après fusion de l’endosome avec la membrane plasmique [2].
 |
Figure 1. Voie des endosomes et lysosomes, et principe de l’expérience de choc hypertonique. A. Schéma de la voie des endosomes et lysosomes. Exemple de l’internalisation du récepteur de l’EGF (EGFR). B. Illustration de l’effet d’un choc hypertonique sur le volume de la cellule et sur celui des endosomes. C..Principe de fonctionnement de la sonde Flipper-TRTM (FliptR). En fonction de l’état de compaction des lipides au sein de la bicouche lipidique membranaire, la sonde adopte une conformation plane (en rouge) ou tordue (en vert), ce qui va se répercuter sur le temps d’émission de fluorescence de la sonde (les flèches représentent la pression latérale exercée par les lipides sur la sonde). D. Un choc hypertonique diminue la tension de la membrane des endosomes mesurée par la sonde FliptR. L’échelle de couleur varie selon les valeurs suivantes ; rouge: 5ns, bleu: 2ns, pondérées par le nombre de photons émis par pixel (tau_Av_Int = intensité du Tau moyen). Les temps d’émission de fluorescence qui ont été mesurés sont indiqués sur le graphique ; petits traits: expériences individuelles ; gros trait rouge: moyenne des expériences). *** indique une différence statistiquement significative (p < 0,001). EGF : facteur de croissance épidermique. Barre d’échelle: 10 µm. |
Les résultats d’une série de travaux montrent que la tension de la membrane plasmique contrôle certains processus tel que la migration, la signalisation et l’endocytose [3]. En revanche, le rôle de la tension des membranes intracellulaires est inconnu à ce jour. Nous nous sommes donc demandé si celle-ci jouait un rôle dans la formation des vésicules intraluminales qui accompagne la biogenèse des endosomes multivésiculaires, et plus particulièrement, si elle contrôlait la nucléation et la polymérisation des filaments de ESCRT-III, qui sont responsables du remodelage des membranes des endosomes.
Lorsqu’elles baignent dans un milieu extracellulaire hypertonique, les cellules expulsent de l’eau, ce qui conduit à une diminution du volume cytoplasmique et de la tension de la membrane plasmique (Figure 1B). Nous avons fait l’hypothèse que le volume des endosomes et la tension de leur membrane devaient aussi être affectés. En incubant dans un milieu hypertonique les cellules exprimant à un niveau endogène la sous-unité CHMP4B (charged multivesicular body protein 4B) de ESCRT-III (étiquetée avec la GFP), nous avons pu observer que CHMP4B polymérisait très rapidement (en quelques minutes seulement) sur les endosomes précoces (marqués avec la transferrine) et tardifs (marqués par le LysotrackerTM). Nous avons aussi observé que d’autres sous-unités du complexe ESCRT-III étaient recrutées conjointement, ainsi que le nucléateur ALIX, et l’ATPase VPS4 (vacuolar protein sorting-associated protein 4) nécessaire au remodelage et à la dépolymérisation des filaments de ESCRT-III. Remarquablement, la déplétion de ALIX par ARN interférent (RNAi) inhibe le recrutement de ESCRT-III à la membrane de l’endosome après un choc hypertonique (le même effet, bien que moindre, est observé après déplétion de la sous-unité TSG101 [tumor susceptibility gene 101 protein] de la voie classique). Cela démontre qu’une hypertonie du milieu extracellulaire stimule la polymérisation de ESCRT-III à la membrane de l’endosome via ses nucléateurs physiologiques.
Nous nous sommes alors demandé si, comme le modèle le prédisait (Figure 1B), le volume des endosomes et leur tension membranaire étaient diminués dans ces conditions. Pour être en mesure d’évaluer de manière fiable le volume des endosomes par microscopie confocale, nous avons surexprimé le mutant constitutivement actif de la petite GTPase RAB5, RAB5Q79L, qui stimule la fusion des endosomes, afin de produire des endosomes de grande taille. Après un choc hypertonique, le volume de ces grands endosomes était réduit d’environ 50 %, une valeur qui a été confirmée, en mesurant le volume d’endosomes normaux en l’absence de RAB5Q79L. Pour mesurer la tension de la membrane de l’endosome, nous avons utilisé la nouvelle sonde Flipper-TRTM (fluorescent lipid tension reporter) [4] et sa formule chimique modifiée pour cibler les endosomes acides (Lyso-FlipperTM) [5, 6]. Ces sondes rapportent, par le changement de leur temps d’émission de fluorescence (fluorescence lifetime imaging microscopy, FLIM), les variations de compaction lipidique qui dépendent notamment de la tension membranaire (Figure 1C). Nous avons observé, dans les endosomes, une forte diminution du temps d’émission de fluorescence de la sonde après l’incubation des cellules dans un milieu hypertonique (Figure 1D), ce qui montre que la tension de la membrane endosomale est bel et bien diminuée lorsque l’endosome est dégonflé par un choc hypertonique.
Nous avons ensuite traité les cellules avec le petit peptide LLOMe (L-leucyl-L-leucine methyl ester) qui, en perforant la membrane des endosomes, permet de réduire leur tension membranaire dans des conditions isotoniques, donc sans changement de volume. Là encore, nous avons observé un recrutement rapide de ESCRT-III dépendant de ses nucléateurs, que nous avons pu attribuer, en l’absence de réduction du volume des endosomes, à la baisse de la tension membranaire.
Nous avons alors tenté de reproduire ces observations par des expériences in vitro en n’utilisant que des composants définis chimiquement et purifiés, afin de nous assurer que l’augmentation de polymérisation de ESCRT-III est bien due à la baisse de la tension membranaire. Nous avons utilisé du CHMP4B recombinant, purifié et marqué avec le fluorochrome Alexa 488, en présence de liposomes unilamellaires géants formés de dioléoyl-phosphatidylcholine (DOPC): dioléoyl-phosphatidylsérine (DOPS) [60: 40 Mol %], car ESCRT-III se lie à la membrane par interaction électrostatique avec les lipides chargés négativement (du même type que DOPS) [7]. Remarquablement, le remplacement du tampon isotonique dans lequel baignaient ces liposomes par un tampon hypertonique a réduit leur volume de 35 % et a triplé le taux de polymérisation de CHMP4B à la membrane. Ensuite, nous avons aspiré la membrane du liposome avec une micropipette de manière à moduler la tension membranaire, à osmolarité constante. Dans ces conditions, la tension membranaire est mesurée directement en tirant un tube de membrane à partir de la surface du liposome, grâce à une bille piégée dans une pince optique : la mesure du déplacement de la bille au sein du piège reflète la tension membranaire. Nous avons ainsi montré que la vitesse de polymérisation de CHMP4B est inversement corrélée avec la tension membranaire. En fait, la vitesse de polymérisation de CHMP4B à la membrane est significativement réduite au-delà d’un seuil de tension correspondant à environ 10-4 J.m-2 (joules par m2), une valeur-seuil comparable à l’énergie de polymérisation de CHMP4B. De plus, une analyse, par cryomicroscopie électronique, a montré que l’incubation des grands liposomes de taille comparable à celle des endosomes, avec du CHMP4B en condition hypertonique, transforme ces liposomes en tubules de membrane couverts de filaments de CHMP4B. Ces observations indiquent que la polymérisation de ESCRT-III induite par la diminution de la tension membranaire est accompagnée de déformations de la bicouche lipidique.
Nous nous sommes alors demandé si la polymérisation de ESCRT-III induite par la baisse de la tension membranaire des endosomes entraînait la formation de vésicules intraluminales in vivo. Des cellules ont été analysées par microscopie optique couplée à la microscopie électronique à balayage de champ avec focalisation d’un faisceau d’ions (correlative light-focused ion beam-scanning electron microscopy, FIB-CLEM) (Figure 2A). Nous avons ainsi pu identifier les endosomes ayant massivement recruté CHMP4B-GFP, puis nous avons analysé le nombre absolu de vésicules intraluminales qu’ils contenaient (Figure 2B). Cette analyse a révélé une augmentation, de 40 % en moyenne, du nombre de vésicules intraluminales par endosome après un choc hypertonique (Figure 2B). In vivo, ces vésicules intraluminales transportent les récepteurs activés en direction des lysosomes, notamment le récepteur du facteur de croissance épidermique (epidermal growth factor, EGF). Nous avons alors incubé des cellules dont les endosomes avaient été élargis par expression du mutant RAB5Q79L (Figure 2C), en présence d’EGF fluorescent pour marquer la membrane limitante de ces endosomes élargis. Nous avons pu montrer que le choc hypertonique entraîne l’accumulation du récepteur dans la lumière des endosomes, suggérant que celui-ci s’accumule dans les vésicules intraluminales nouvellement formées (Figure 2C).
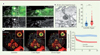 |
Figure 2. La polymérisation de ESCRT-III induite par la baisse de tension membranaire entraîne la formation de vésicules intraluminales. A. Images d’une cellule en microscopie optique couplée à la microscopie électronique (ME) à balayage de champ, avec focalisation d’un faisceau d’ions montrant des endosomes denses aux électrons et décorés par la protéine CHMP4B-GFP B. Quantification du nombre de vésicules intraluminales (VIL) par endosome avant et après choc hypertonique par microscopie électronique à balayage de champ, avec focalisation d’un faisceau d’ions. *** indique une différence statistiquement significative (p < 0,001). C. La polymérisation de ESCRT-III à la surface des endosomes volumineux obtenus par surexpression de RAB5Q79L (Q79L) entraîne l’incorporation du récepteur de l’EGF au sein de ces structures. Barres d’échelle: 5 µm. |
Enfin, nous avons évalué le rôle de la tension membranaire dans une situation physiologique en l’absence de tout choc hypertonique. Il a été montré que le facteur de croissance épidémique (EGF), en stimulant l’endocytose massive de son récepteur, entraîne l’internalisation d’une vague de membranes. Cette vague, en arrivant dans l’endosome, augmente son volume et stimule la formation de vésicules intraluminales contenant le récepteur [8]. Nous avons observé que le traitement de cellules avec l’EGF conduit en effet à un doublement du volume de l’endosome. Mais remarquablement, la tension de sa membrane mesurée avec le senseur de tension Lyso FlipperTM était alors significativement réduite, ce qui s’explique vraisemblablement par le fait que la fusion des vésicules d’endocytose avec l’endosome augmente davantage sa surface membranaire que son volume.
Nous avons donc montré que la formation des vésicules intraluminales dans les endosomes est stimulée par la diminution de la tension de leur membrane, qui favorise la polymérisation de ESCRT-III par l’intermédiaire de ses nucléateurs physiologiques, et entraîne la déformation de la membrane nécessaire à la formation des vésicules intraluminales [9]. En plus de la formation de ces vésicules, les ESCRT et ALIX sont également responsables d’autres déformations membranaires orientées vers l’extérieur du cytoplasme, par exemple dans l’abscission du pont reliant les deux cellules filles à la fin de la cytokinèse lors de la mitose, ou encore lors de la réparation de l’enveloppe nucléaire ou de la membrane plasmique. Il est donc tentant de supposer que la tension membranaire contrôle aussi ces autres rôles de ESCRT-III. Les résultats de notre étude sur les endosomes fournissent un premier exemple illustrant comment le fonctionnement d’une organelle est contrôlé par la tension de sa membrane, et l’on peut prédire que, d’une manière générale, en contrôlant le flux membranaire qui traverse les organelles, la cellule peut contrôler les fonctions de ces organelles par la tension de leurs membranes.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Les auteurs remercient la plateforme de microscopie optique et électronique de l’université de Genève ainsi que Dimitri Moreau, responsable de la plateforme ACCESS de microscopie automatisée à haut-débit, le Fonds National Suisse de la Recherche Scientifique (requête no31003A-159479), LipidX et l’initiative suisse SystemsX.ch, le Human Frontier Science Program Young Investigator (requête RGY0076/2009-C), le Fonds National Suisse de la Recherche Scientifique (requêtes no31003A-130520, -149975 et -173087), le Conseil européen de la recherche (requête Consolidator n° 311536), et le National Center for Competence in Research Chemical-Biology (NCCR Chemical-Biology).
Références
- Gruenberg J. Life in the lumen: the multivesicular endosome. Traffic 2020; 21: 76–93. [CrossRef] [PubMed] [Google Scholar]
- Larios J, Mercier V, Roux A, Gruenberg J. ALIX- and ESCRT-III-dependent sorting of tetraspanins to exosomes. J Cell Biol 2020; 219: e201904113. [CrossRef] [Google Scholar]
- Pontes B Monzo P Gauthier NC Membrane tension: a challenging but universal physical parameter in cell biology. Semin Cell Dev Biol 2017 ; 71 : 30–41. [CrossRef] [PubMed] [Google Scholar]
- Colom A Derivery E Soleimanpour S et al. A fluorescent membrane tension probe. Nat Chem 2018 ; 10 : 1118–1125. [CrossRef] [PubMed] [Google Scholar]
- Goujon A Colom A Straková K et al. Mechanosensitive fluorescent probes to image membrane tension in mitochondria, endoplasmic reticulum, and lysosomes. J Am Chem Soc 2019 ; 141 : 3380–3384. [CrossRef] [PubMed] [Google Scholar]
- Piazzolla F, Mercier V, Assies L, et al. Fluorescent membrane tension probes for early endosomes. Angew Chem Int Ed Engl 2021; doi: 10.1002/anie.202016105. [PubMed] [Google Scholar]
- Chiaruttini N Redondo-Morata L Colom A et al. Relaxation of loaded ESCRT-III spiral springs drives membrane deformation. Cell 2015 ; 163 : 866–879. [CrossRef] [PubMed] [Google Scholar]
- White IJ Bailey LM Aghakhani MR et al. EGF stimulates annexin 1-dependent inward vesiculation in a multivesicular endosome subpopulation. EMBO J 2006 ; 25 : 1–12. [CrossRef] [PubMed] [Google Scholar]
- Mercier V, Larios J, Molinard G, et al. Endosomal membrane tension regulates ESCRT-III-dependent intra-lumenal vesicle formation. Nat Cell Biol 2020; 22: 947–59. [CrossRef] [PubMed] [Google Scholar]
© 2021 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Voie des endosomes et lysosomes, et principe de l’expérience de choc hypertonique. A. Schéma de la voie des endosomes et lysosomes. Exemple de l’internalisation du récepteur de l’EGF (EGFR). B. Illustration de l’effet d’un choc hypertonique sur le volume de la cellule et sur celui des endosomes. C..Principe de fonctionnement de la sonde Flipper-TRTM (FliptR). En fonction de l’état de compaction des lipides au sein de la bicouche lipidique membranaire, la sonde adopte une conformation plane (en rouge) ou tordue (en vert), ce qui va se répercuter sur le temps d’émission de fluorescence de la sonde (les flèches représentent la pression latérale exercée par les lipides sur la sonde). D. Un choc hypertonique diminue la tension de la membrane des endosomes mesurée par la sonde FliptR. L’échelle de couleur varie selon les valeurs suivantes ; rouge: 5ns, bleu: 2ns, pondérées par le nombre de photons émis par pixel (tau_Av_Int = intensité du Tau moyen). Les temps d’émission de fluorescence qui ont été mesurés sont indiqués sur le graphique ; petits traits: expériences individuelles ; gros trait rouge: moyenne des expériences). *** indique une différence statistiquement significative (p < 0,001). EGF : facteur de croissance épidermique. Barre d’échelle: 10 µm. |
| Dans le texte | |
 |
Figure 2. La polymérisation de ESCRT-III induite par la baisse de tension membranaire entraîne la formation de vésicules intraluminales. A. Images d’une cellule en microscopie optique couplée à la microscopie électronique (ME) à balayage de champ, avec focalisation d’un faisceau d’ions montrant des endosomes denses aux électrons et décorés par la protéine CHMP4B-GFP B. Quantification du nombre de vésicules intraluminales (VIL) par endosome avant et après choc hypertonique par microscopie électronique à balayage de champ, avec focalisation d’un faisceau d’ions. *** indique une différence statistiquement significative (p < 0,001). C. La polymérisation de ESCRT-III à la surface des endosomes volumineux obtenus par surexpression de RAB5Q79L (Q79L) entraîne l’incorporation du récepteur de l’EGF au sein de ces structures. Barres d’échelle: 5 µm. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




