| Issue |
Med Sci (Paris)
Volume 37, Number 5, Mai 2021
La révolution médicale du dépistage néonatal – Une aventure médicale scientifique et sociétale
|
|
|---|---|---|
| Page(s) | 547 - 549 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/2021049 | |
| Published online | 18 May 2021 | |
Récepteur 5-HT6 et mTOR
Un couple hyperactif dans la douleur neuropathique
5-HT6 receptor-mTOR: An hyperactive couple in neuropathic pain
Université Clermont Auvergne, Inserm U1107, Neuro-Dol, 28 place Henri-Dunant, 63000 Clermont-Ferrand, France.
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Les douleurs neuropathiques constituent un groupe hétérogène de douleurs chroniques consécutives à une maladie (ou une lésion) affectant le système nerveux somato-sensoriel [1]. Elles touchent 7 à 10 % de la population générale [2, 3]. Elles sont persistantes ou récurrentes, et ne sont généralement pas améliorées par le traitement de la maladie sous-jacente, ou même par sa guérison. Elles se caractérisent par une perception aberrante de douleur spontanée ou provoquée, comme l’hyperalgie1 et l’allodynie2, et sont souvent associées à des comorbidités cognitives [4]. La prise en charge thérapeutique de ces douleurs est difficile, par manque d’efficacité des médicaments de référence et par leurs effets indésirables, qu’il s’agisse des antidépresseurs tricycliques, des antidépresseurs inhibiteurs de la recapture de la noradrénaline et de la sérotonine, ou de la gabapentine, qui inhibe spécifiquement certains canaux calciques [5]. La sérotonine est un neurotransmetteur impliqué dans la modulation de la douleur et dans de nombreuses autres fonctions, comme le contrôle de l’appétit, du sommeil, de l’humeur… La sérotonine libérée par des neurones du bulbe ventro-médian rostral projetant leurs axones sur la corne dorsale de la moelle épinière exerce un effet modulateur sur la transmission du message douloureux. Elle agit en activant des récepteurs de la sérotonine exprimés par différents types de neurones, dont le récepteur 5-HT6. Ce récepteur métabotrope (couplé aux protéines G) est exprimé par des interneurones excitateurs situés dans une région s’étendant de la couche II interne à la couche IV de la corne dorsale de la moelle épinière, correspondant à la zone de projection des mécanorécepteurs à bas seuil d’excitation (low-threshold mechanoreceptor-recipient zone) impliqués dans la perception tactile [6]. Des travaux antérieurs ont montré que le récepteur 5-HT6 interagit avec des protéines de la voie mTOR (mammalian target of rapamycin) pour modifier les fonctions cognitives dans des modèles neuro-développementaux de schizophrénie [7], et qu’il possède une activité constitutive sur la voie de signalisation de l’AMPc (adénosine monophosphate cyclique) in vitro [8]. L’activité constitutive du récepteur 5-HT6 des neurones spinaux et ses conséquences sur la voie de signalisation mTOR n’avaient cependant pas été explorées dans un contexte de douleur neuropathique.
L’activité constitutive du récepteur 5-HT6 participe à la douleur neuropathique
Pour étudier le rôle physiopathologique du récepteur 5-HT6 dans la douleur neuropathique et les comorbidités cognitives associées, nous avons utilisé des agonistes inverses et des antagonistes neutres de ce récepteur3 dans deux modèles différents de douleur neuropathique chez le rat, où elle est induite soit par la ligature de la racine L5 du nerf spinal, soit par l’injection d’un agent anticancéreux, l’oxaliplatine. Ces deux modèles permettent de mimer les neuropathies traumatiques ou iatrogènes chimio-induites, et de reproduire les symptômes douloureux qui les accompagnent. Une fois la neuropathie douloureuse installée, nous avons traité les animaux avec un agoniste inverse du récepteur 5-HT6 (SB258585) par voie intrapéritonéale. Nous avons alors observé une nette diminution des symptômes de la douleur induite par le toucher (allodynie tactile) ou le froid (allodynie thermique), ainsi qu’une diminution des déficits cognitifs (mémoire de reconnaissance sociale et mémoire épisodique). En revanche, nous n’avons observé aucun effet des antagonistes neutres du récepteur 5-HT6 (IIQ ou CPPQ) chez ces rats neuropathiques. Le ligand agoniste inverse n’avait par ailleurs aucun effet antalgique sur la nociception mécanique induite par pression de la patte chez des animaux sains [9]. L’ensemble de ces résultats indiquait l’existence d’une activité constitutive du récepteur 5-HT6, indépendante de la sérotonine endogène, dans un contexte de douleur neuropathique de cause traumatique ou toxique.
Les agonistes inverses du récepteur 5-HT6 réduisent la douleur neuropathique et les troubles cognitifs associés
Une fois démontrée l’activité spontanée du récepteur 5-HT6 in vivo, nous avons conçu et breveté un nouvel agoniste inverse (PZ-1388) bloquant cette activité. Lorsqu’elle est administrée par voie intrapéritonéale chez l’animal neuropathique, cette molécule a un effet anti-allodynique rapide et prolongé sur les symptômes d’hypersensibilité tactile et thermique. Parallèlement à l’amélioration de ces symptômes, nous avons observé une amélioration des déficits cognitifs après injection intrapéritonéale ou intrathécale de la molécule. Pour savoir si cet effet était dû à un effet pro-cognitif propre de la molécule, ou s’il était consécutif à la diminution des symptômes douloureux, nous avons utilisé des rats sains chez lesquels un déficit cognitif a été induit par la phencyclidine (un psychotrope dissociatif), et nous avons comparé les effets d’une administration intrathécale ou intrapéritonéale des agonistes inverses du récepteur 5-HT6 sur le déficit cognitif de ces rats : alors que l’injection intrapéritonéale de l’agoniste inverse améliorait les troubles cognitifs induits par la phencyclidine, l’injection intrathécale n’avait pas d’effet [9]. De l’absence d’efficacité de cette voie d’injection sur les structures cérébrales impliquées dans la cognition, nous avons conclu que l’effet de l’agoniste inverse sur les déficits cognitifs associés aux douleurs neuropathiques dépend de son effet antalgique sous-tendu par le blocage des récepteurs 5‑HT6 spinaux. En utilisant des souris transgéniques exprimant le récepteur 5-HT6 couplé à une protéine fluorescente, nous avons d’ailleurs confirmé la présence de ce récepteur dans les neurones de la moelle épinière dorsale et avons montré sa localisation dans le cil primaire de ces neurones [9].
L’activité constitutive du récepteur 5-HT6 active la voie de signalisation mTOR
L’engagement de la voie mTOR par le récepteur 5-HT6 [7] et l’implication de mTOR dans la douleur neuropathique [10] nous ont conduits à rechercher si l’activité constitutive du récepteur 5-HT6 était à l’origine d’une activation de mTOR et contribuait à la pathogénie de la douleur neuropathique. Après avoir confirmé que la neuropathie douloureuse d’origine traumatique induisait une activation de mTOR dans la moelle épinière dorsale ipsilatérale (du même côté) à la lésion, nous avons montré que l’administration intrapéritonéale d’agonistes inverses du récepteur 5-HT6 réduisait l’activité de la voie de signalisation mTOR comme le faisait la rapamycine, un inhibiteur de mTOR. L’administration de rapamycine a également amélioré l’allodynie induite par la neuropathie et les déficits de reconnaissance sociale et de discrimination d’un nouvel objet (Figure 1) [9].
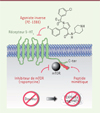 |
Figure 1. Activation de mTOR dépendante de l’activité constitutive du récepteur 5-HT6 de la sérotonine : implication dans la douleur neuropathique et les déficits cognitifs associés. Dans un contexte de neuropathie douloureuse, le récepteur 5-HT6 des neurones spinaux présente une activité constitutive se traduisant par l’activation de la protéine mTOR (mammalian target of rapamycin), avec laquelle il interagit physiquement par son extrémité carboxy-terminale (C-ter). Le blocage de cette voie de signalisation avec un agoniste inverse du récepteur 5-HT6 (PZ-1388), avec un inhibiteur de mTOR (rapamycine), ou avec un peptide mimétique supprimant l’interaction entre le récepteur 5-HT6 et mTOR, améliore la douleur et les déficits cognitifs associés. |
L’identification de la séquence C-terminale du récepteur 5-HT6 interagissant avec la protéine mTOR a permis de produire un peptide capable de supprimer l’interaction physique du récepteur avec mTOR. Cette stratégie peptido-mimétique, dont l’efficacité de découplage a été vérifiée in vitro, s’est révélée analgésique in vivo puisque l’administration intrathécale de ce peptide a considérablement réduit l’allodynie tactile et les troubles cognitifs (Figure 1) [9].
Perspectives
Ces travaux ont permis de montrer le rôle crucial de l’activité constitutive (indépendante de la sérotonine endogène) du récepteur 5-HT6 de la sérotonine dans les douleurs neuropathiques de différentes causes, et l’intérêt thérapeutique d’agonistes inverses de ce récepteur. Ils ont révélé que l’activité constitutive du récepteur 5-HT6 s’accompagne de l’activation d’une voie de signalisation non canonique, la voie mTOR, et suggèrent une nouvelle stratégie pharmacologique fondée sur la possibilité de découpler le récepteur 5-HT6 et mTOR.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Remerciements
Ce travail a été financé par l’Agence nationale de la recherche (ANR-19-CE18-0018), le programme Investissements d’avenir (16-IDEX-0001 CAP20-25) et la région Auvergne-Rhône-Alpes.
L’hyperalgie ou hyperalgésie désigne une sensibilité excessive à un stimulus nociceptif.
L’allodynie désigne une douleur déclenchée par un stimulus normalement indolore, tel qu’un effleurement de la peau, ou une petite variation de température dans un territoire cutané.
En pharmacologie, un « antagoniste neutre » d’un récepteur désigne un ligand dépourvu d’effet propre et bloquant l’effet de l’agoniste, tandis qu’un « agoniste inverse » désigne un ligand bloquant l’activité constitutive du récepteur en favorisant sa configuration inactive, effet se traduisant par une activité « négative ». La notion d’agoniste inverse repose donc sur l’idée que le récepteur et son système de transduction conduisant à un effet auraient une activité constitutive en l’absence de tout agoniste.
Références
- Treede R-D, Jensen TS, Campbell JN, et al. Neuropathic pain: redefinition and a grading system for clinical and research purposes. Neurology 2008 ; 70 : 1630–1635. [CrossRef] [PubMed] [Google Scholar]
- Bouhassira D, Lantéri-Minet M, Attal N, et al. Prevalence of chronic pain with neuropathic characteristics in the general population. Pain 2008 ; 136 : 380–387. [CrossRef] [PubMed] [Google Scholar]
- Chenaf C, Delorme J, Delage N, et al. Prevalence of chronic pain with or without neuropathic characteristics in France using the capture-recapture method: a population-based study. Pain 2018 ; 159 : 2394–2402. [CrossRef] [PubMed] [Google Scholar]
- Radat F, Margot-Duclot A, Attal N. Psychiatric co-morbidities in patients with chronic peripheral neuropathic pain: a multicentre cohort study. Eur J Pain 2013 ; 17 : 1547–1557. [Google Scholar]
- Finnerup NB, Attal N, Haroutounian S, et al. Pharmacotherapy for neuropathic pain in adults: a systematic review and meta-analysis. Lancet Neurol 2015 ; 14 : 162–173. [CrossRef] [PubMed] [Google Scholar]
- Abraira VE, Kuehn ED, Chirila AM, et al. The cellular and synaptic architecture of the mechanosensory dorsal horn. Cell 2017 ; 168 : 295–310 e19. [Google Scholar]
- Meffre J, Chaumont-Dubel S, Mannoury la Cour C, et al. 5-HT6 receptor recruitment of mTOR as a mechanism for perturbed cognition in schizophrenia. EMBO Mol Med 2012 ; 4 : 1043–1056. [CrossRef] [PubMed] [Google Scholar]
- Deraredj Nadim W, Chaumont-Dubel S, Madouri F, et al. Physical interaction between neurofibromin and serotonin 5-HT 6 receptor promotes receptor constitutive activity. Proc Natl Acad Sci USA 2016; 113 : 12310–5. [Google Scholar]
- Martin PY, Doly S, Hamieh AM, et al. mTOR activation by constitutively active serotonin6 receptors as new paradigm in neuropathic pain and its treatment. Prog Neurobiol 2020; 193 : 101846. [Google Scholar]
- Duan Z, Li J, Pang X, et al. Blocking mammalian target of rapamycin (mTOR) alleviates neuropathic pain induced by chemotherapeutic Bortezomib. Cell Physiol Biochem 2018 ; 48 : 54–62. [CrossRef] [PubMed] [Google Scholar]
© 2021 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (https://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Liste des figures
 |
Figure 1. Activation de mTOR dépendante de l’activité constitutive du récepteur 5-HT6 de la sérotonine : implication dans la douleur neuropathique et les déficits cognitifs associés. Dans un contexte de neuropathie douloureuse, le récepteur 5-HT6 des neurones spinaux présente une activité constitutive se traduisant par l’activation de la protéine mTOR (mammalian target of rapamycin), avec laquelle il interagit physiquement par son extrémité carboxy-terminale (C-ter). Le blocage de cette voie de signalisation avec un agoniste inverse du récepteur 5-HT6 (PZ-1388), avec un inhibiteur de mTOR (rapamycine), ou avec un peptide mimétique supprimant l’interaction entre le récepteur 5-HT6 et mTOR, améliore la douleur et les déficits cognitifs associés. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




