Figure 2.
Télécharger l'image originale
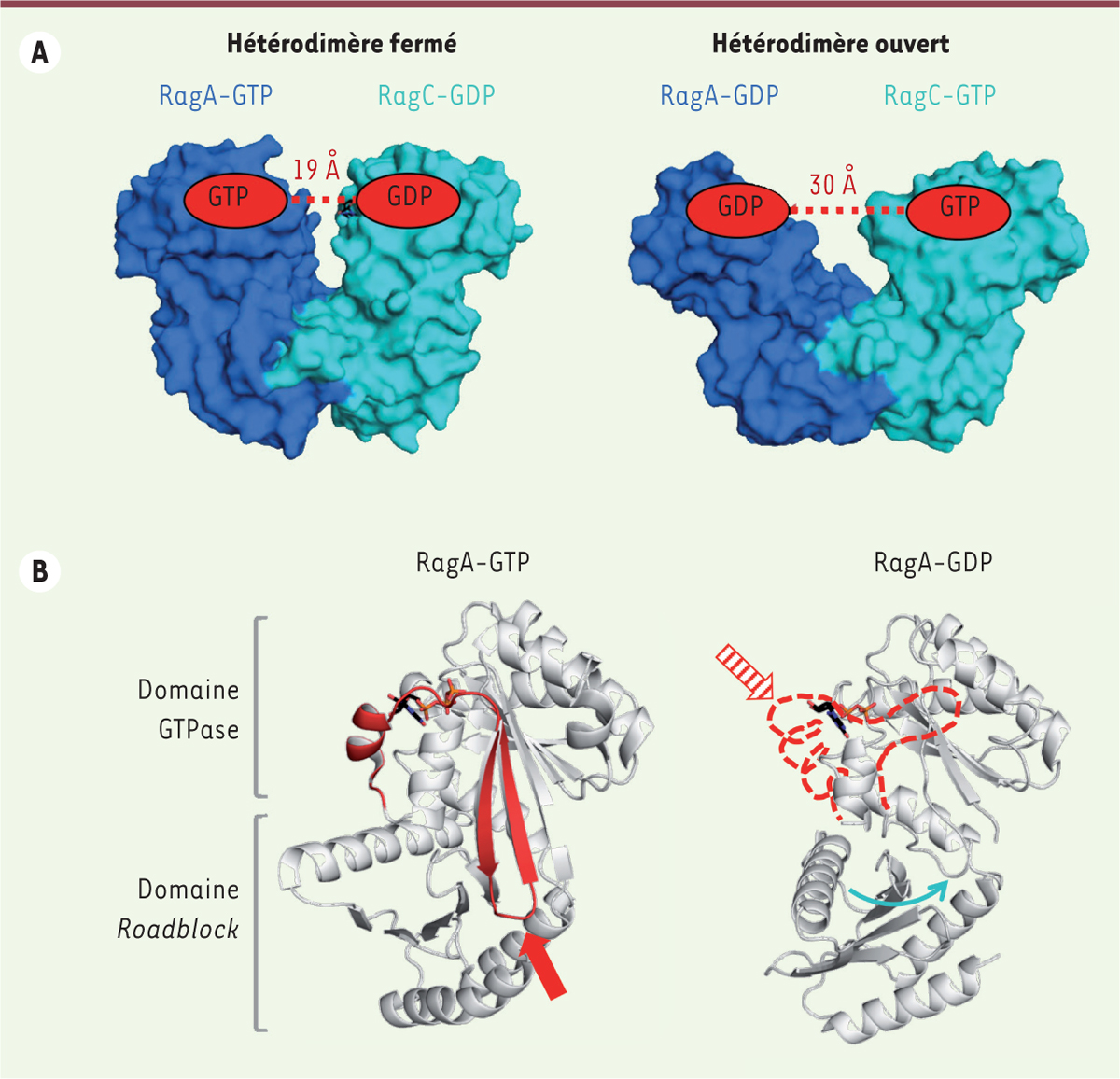
L’état nucléotidique des GTPases Rag contrôle l’assemblage du complexe mTORC1. A. La largeur de l’ouverture entre les domaines GTPases au sein de l’hétérodimère RagA/RagC dépend des nucléotides GDP et GTP. La forme la plus fermée fixe l’adaptateur RAPTOR, ce qui conduit au recrutement de mTOR à la membrane du lysosome, alors que la forme ouverte défavorise cette interaction. B. Dans la forme liée au GTP (PDB 6S6A, [14]), la région switch 1 interagit fortement avec le nucléotide et la région interswitch traverse le domaine GTPase entre le site nucléotidique et le domaine Roadblock (en rouge). Dans la forme liée au GDP (PDB 6ULG, [13]), ces deux régions sont très flexibles et désordonnées dans la structure (en pointillé rouge). Cette transition entre un état structuré, qui pousse sur le domaine Roadblock (flèche rouge pleine), et une forme flexible, qui relâche la pression (flèche rouge hachurée), explique comment le nucléotide agit à distance pour modifier la position du domaine Roadblock par rapport au domaine GTPase (flèche bleue).
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




