| Issue |
Med Sci (Paris)
Volume 35, Number 8-9, Août–Septembre 2019
|
|
|---|---|---|
| Page(s) | 682 - 688 | |
| Section | M/S Revues | |
| DOI | https://doi.org/10.1051/medsci/2019132 | |
| Published online | 18 September 2019 | |
L’imagerie élémentaire par spectroscopie LIBS
De nouvelles applications en médecine
Elemental imaging using laser-induced breakdown spectroscopy: latest medical applications
1
Institut Lumière Matière, CNRS UMR 5306, Lyon 1 University, Villeurbanne, France.
2
Institute for Advanced Biosciences (IAB), Team « Cancer Targets and Experimental Therapeutics », Inserm U1209, CNRS UMR5309, Grenoble Alpes University, allée des Alpes, 38700 Grenoble, France.
3
Clinical Cancer Laboratory, Biochemistry Department, Grenoble Alpes University Hospital, Grenoble, France.
* This email address is being protected from spambots. You need JavaScript enabled to view it.
Résumé
L’imagerie multi-élémentaire des tissus biologiques grâce à la spectroscopie LIBS (laser-induced breakdown spectroscopy) permet la visualisation directe de la distribution des éléments endogènes ou exogènes. Cette technologie est notamment utilisée pour mettre en image la cinétique des nanoparticules métalliques dans les organes d’élimination, mais également pour analyser la distribution physiologique des éléments biologiques in situ, et pour révéler la topographie des éléments chimiques, comme les métaux, dans des tissus humains qui ont été exposés à des agents extérieurs potentiellement toxiques. Fondée sur notre expérience et les travaux les plus récents dans le domaine de l’imagerie du contenu élémentaire des tissus animaux et humains, cette revue décrit les principes et les caractéristiques de l’instrumentation LIBS, présente certains aspects techniques pour mettre en place des expériences avec cet outil, montre les avantages et les limites de cette technologie, et s’intéresse aux différentes possibilités qu’offre l’imagerie LIBS pour des applications précliniques et médicales.
Abstract
Multi-elemental imaging of soft tissues using Laser-induced breakdown spectroscopy, also known as LIBS, allows for the direct visualization of the distribution of endogenous or exogenous elements within tissues. LIBS was used to image the kinetics of metal nanoparticles in elimination organs, but also the physiological distribution of biological elements in situ and the topography of chemicals or metals in exposed human tissues. Based on our experience and recent literature in the field of imaging the elemental content of animal and human specimens, this review describes the principle and characteristics of the instrument, technical considerations for setting up experiments with LIBS, its advantages, limitations and possibilities for pre-clinical and medical applications.
© 2019 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
La technique de spectrométrie sur plasma induit par laser, ou LIBS (laser-induced breakdown spectroscopy), a été développée dans les années 1960. Son principe est le suivant : un faisceau laser pulsé envoyé sur un échantillon va créer un plasma par ablation, vaporisation et excitation d’une petite quantité de matière. Les différentes espèces excitées par le laser (ions, atomes, molécules) vont retourner à des niveaux d’énergie inférieurs en émettant une lumière qui peut être collectée, puis analysée par un ou plusieurs spectromètres. Chaque élément possède des raies d’émission à des longueurs d’onde qui lui sont spécifiques. L’analyse du spectre collecté permet non seulement d’identifier les espèces élémentaires présentes dans l’échantillon, mais également d’en estimer la concentration relative (Figure 1).
 |
Figure 1. Représentation schématique des principaux composants du système LIBS. Sont présentés le laser pulsé, l’objectif du microscope, l’échantillon, la plateforme motorisée et la collection du signal transmis par fibre optique au spectromètre. Les spectres LIBS (laser-induced breakdown spectroscopy) générés ont des longueurs d’ondes caractéristiques des éléments présents dans l’échantillon. L’analyse point par point permet de reconstituer une image en deux dimensions pour chaque élément d’intérêt. Gd : gadolinium ; Na : sodium. |
La quasi-totalité des éléments chimiques répertoriés dans la classification périodique de Mendeleïev peut être détectée par cette méthode. Le couplage de l’analyse élémentaire LIBS à un microscope à champ large apporte une nouvelle dimension à cette technique. En effet, cela permet de visualiser la répartition et la concentration des composés dans l’espace, et donc de créer des images élémentaires de l’échantillon étudié.
Cette technique possède des applications dans des domaines très variés, allant du biomédical à l’exploration spatiale, en passant par la géologie ou l’industrie (Figure 2).
 |
Figure 2. Principales caractéristiques et exemples d’application du LIBS. |
Les métaux en biomédecine
Les métaux alcalins et certains alcalino-terreux, comme le sodium (Na), le potassium (K), le magnésium (Mg) et le calcium (Ca), sont des entités dynamiques qui transmettent des signaux. Les métaux de transition redox-actifs1, tels que le zinc (Zn), le cuivre (Cu) et le fer (Fe), sont des cofacteurs impliqués dans des fonctions structurales ou catalytiques. Certains d’entre eux, lorsque leur homéostasie est perturbée, peuvent déclencher un stress oxydatif et des dommages à l’ADN [1, 2]. Les métaux ont donc des fonctions biologiques pléiotropes indispensables à de très nombreuses activités cellulaires et tissulaires.
L’homéostasie des métaux résulte de l’étroite coordination entre leur absorption, leur implication dans les voies de signalisation, leur métabolisme et leur excrétion. La quantité disponible de chaque métal est étroitement régulée dans l’espace et au cours du temps [3]. En conditions normales ou pathologiques, l’analyse in situ des éléments chimiques, en particulier les métaux, présente un intérêt considérable pour objectiver des variations de répartition ou de concentration et pour permettre d’interpréter leurs effets sur les tissus et les organismes. En effet, toute carence ou surcharge en métaux affecte fortement les tissus et peut entraîner des maladies graves, voire mortelles.
Les métaux sont potentiellement incriminés dans la survenue des maladies neuro-dégénératives associées à l’âge comme la maladie d’Alzheimer ou la maladie de Parkinson. Ces pathologies peuvent être liées aux effets toxiques de métaux lourds (par exemple, le cadmium Cd, le plomb Pb, et le mercure Hg), à l’abondance des métaux biologiquement importants (par exemple, le zinc Zn et le manganèse Mn), ou des métaux non biologiques (l’aluminium Al, par exemple) [4]. L’imagerie élémentaire des métaux dans les tissus présente donc un fort intérêt pour permettre de comprendre les mécanismes pathologiques et, idéalement, pour identifier des cibles potentielles de nouveaux traitements.
Les méthodes de cartographie des composants élémentaires
Diverses techniques permettent de déterminer la composition élémentaire des échantillons, comme la spectrométrie de fluorescence des rayons X (microanalyse de rayonnement synchrotron : XRF en anglais) [5], la nano-spectrométrie de masse d’ions secondaires (nano-SIMS, pour nano-scale secondary ion mass spectrometry) [6] ou l’ablation laser couplée à la spectrométrie de masse par plasma à couplage inductif (en anglais LA-ICP-MS, pour laser ablation-inductively-coupled plasma mass spectroscopy) [7]. Ces approches offrent de hautes performances en termes de sensibilité, mais la complexité des équipements nécessaires rend difficile, voire impossible, leur utilisation en routine.
Les avantages de l’imagerie LIBS
L’analyse élémentaire LIBS est applicable sur des échantillons solides, liquides ou gazeux et se réalise à température et pression ambiantes [8]. C’est une technique simple, rapide, peu dommageable pour l’échantillon, et qui permet une analyse de l’ensemble des éléments avec une seule impulsion laser. Elle est sensible (quelques parties par million, ou ppm, sont détectables pour la plupart des éléments) et présente une large gamme dynamique de détection (de la présence de trace jusqu’à des quantités importantes). Contrainte par la limite de diffraction de la lumière et la nature de l’échantillon, la résolution spatiale peut aujourd’hui descendre jusqu’à 8 micromètres. Il n’existe en revanche aucune restriction quant à la forme des échantillons.
Les premières applications de l’imagerie LIBS
Initialement développée pour l’étude des matériaux, l’analyse élémentaire LIBS a été ensuite appliquée en biologie à des spécimens minéralisés ou calcifiés, comme les calculs biliaires, les os et les dents. L’imagerie des tissus non minéralisés est en revanche récente car il a été nécessaire de s’affranchir de l’hétérogénéité des tissus biologiques et de maîtriser tous les paramètres de l’ablation laser pour ces matériaux considérés comme « mous ».
L’utilisation possible de l’analyse élémentaire LIBS non résolue dans l’espace a été, pour la première fois, démontrée pour les applications biomédicales, après une transformation matricielle (c’est-à-dire le mixage, le séchage ou la granulation du tissu) employée pour améliorer l’efficacité de l’ablation laser et donc accroître le rapport signal sur bruit [9]. À l’aide de cette transformation, l’analyse élémentaire LIBS a permis de confirmer un diagnostic de cancer du sein [10], de cancer colorectal [11], et de mélanome [12]. Dans cette dernière étude, les auteurs ont mesuré les éléments contenus dans des tissus homogénéisés en pastilles, mais également dans les tissus cutanés directement excisés d’animaux porteurs de mélanomes. Leurs résultats indiquent que le magnésium (Mg) et le calcium (Ca) pourraient représenter des biomarqueurs pour discriminer un mélanome d’une peau saine, ce qui suggère une application clinique directe potentielle de l’analyse élémentaire LIBS pour le diagnostic des tumeurs humaines [12].
Différents instruments LIBS équipés de lasers pulsés nanoseconde ou femtoseconde [22] (→) ont été progressivement développés pour des analyses par double impulsion2, avec de nombreuses applications bio-médicales. L’analyse élémentaire LIBS peut ainsi aider à discriminer les tissus sains et pathologiques en temps réel lors d’une chirurgie laser ou pour une biopsie [13].
(→) Voir l’article Nobel de S.R. Mordon, m/s n° 2, février 2019, page 176
Dans cette revue seront présentées les avancées récentes du LIBS résolu dans l’espace, en particulier, l’apport de l’imagerie LIBS pour les tissus biologiques. Nous décrirons également certaines des applications les plus prometteuses en santé.
Principe de l’analyse élémentaire LIBS
Un laser pulsé de haute énergie est concentré à la surface de l’échantillon, induisant l’ablation de quelques nanogrammes de matière, vaporisés sous forme de plasma. Les éléments et les ions ainsi excités vont retrouver des niveaux d’énergie inférieurs en émettant des rayonnements lumineux qui leur sont propres. Fondée sur le principe de spectroscopie d’émission atomique, cette lumière sera analysée par des spectromètres équipés de détecteurs couplés à une caméra CCD (charge-coupled device). Pour chaque impulsion laser, le spectre enregistré constitue une signature unique de l’échantillon traité. Chaque élément du tableau périodique possède ses lignes d’émission caractéristiques. Sur le spectre d’émission enregistré (Figure 1), les intensités des pics correspondant à chaque ligne d’émission (par exemple 330 nm pour le sodium) sont directement corrélées à la quantité de l’élément présent dans l’échantillon analysé. Une imagerie élémentaire LIBS pourra être réalisée en balayant l’intégralité de la surface de l’échantillon par le laser afin d’obtenir une résolution spatiale. Les images élémentaires seront créées par extraction des données spectrales enregistrées pour chaque élément d’intérêt. Cette technique est aujourd’hui entièrement compatible avec la microscopie optique. Elle fournit des images élémentaires avec une sensibilité importante (de l’ordre d’une partie par million pour la plupart des métaux). Les cartographies élémentaires (ou mapping) ainsi obtenues représentent (selon l’intensité de la coloration) l’abondance relative des éléments chimiques révélés. Pour en connaître la concentration exacte, il sera indispensable de réaliser au préalable une calibration avec des standards externes de concentrations connues.
Études précliniques
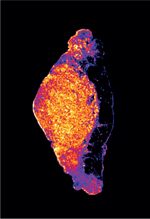
Une des applications prometteuses de l’imagerie LIBS pour les études précliniques est la détection ex vivo, à partir de tissus prélevés chez l’animal, de médicaments ou de nanocomposés (NC) contenant des métaux lourds, comme le gadolinium (Gd) ou l’or (Au) (Figure 3). La distribution dans l’espace de ces nanocomposés d’intérêt est réalisée en deux dimensions (2-D), à l’échelle d’un organe entier. La LIBS détecte directement les nanocomposés métalliques, sans qu’il soit nécessaire d’effectuer de modifications chimiques ou des marquages avec des colorants.
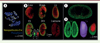 |
Figure 3. Images LIBS obtenues à partir d’échantillons biologiques. A. Tumeur pancréatique représentée par le phosphore (P, en bleu) chargée en nanocomposés d’or (Au, en jaune). B..Cinétique d’élimination rénale de nanocomposés de gadolinium (Gd-NC, en vert). Le sodium est représenté en rouge. C. Image haute résolution (600 x 410 pixels) d’un rein de souris. Le gadolinium est représenté en vert et les fortes concentrations de calcium, en rouge. D. Images en trois dimensions d’un rein de souris montrant la répartition du gadolinium (en vert), du calcium (en violet) ou du sodium (en rouge) (figure adaptée de [21]). |
Ainsi, des nanocomposés contenant de l’or (Au-NC) injectés à des souris immuno-déficientes présentant des tumeurs pancréatiques permettent de cibler les cellules cancéreuses en vue d’un traitement ultérieur par irradiation [14] (Figure 3A). De même, l’analyse de tissus biologiques murins congelés, ou inclus en paraffine, a permis de déterminer la distribution, le métabolisme, l’accumulation de nanocomposés Gd-NC (contenant du gadolinium), leur temps de résidence, mais également les cinétiques d’élimination par les reins des animaux [15]. Dès 2014, l’amélioration de la résolution spatiale à environ 35 μm a facilité le repérage de ces Gd-NC dans les structures anatomiques et donc leur localisation précise dans les organes, notamment le rein. Une cinétique d’élimination rénale des Gd-NC à différents temps après qu’ils aient été injectés à l’animal est montrée dans la Figure 3B . La résolution latérale obtenue est fortement influencée par la nature de l’échantillon : de 40 à 100 µm pour des sections congelées [16], jusqu’à 8 à 10 µm pour des échantillons durs inclus en résine époxy (Figure 3C) [17].
En plus des métaux exogènes composant les nanocomposés métalliques, les éléments endogènes qui constituent les tissus biologiques peuvent également être mis en évidence. C’est le cas du phosphore P, du fer Fe, du sodium Na, du calcium Ca et du magnésium Mg.
L’imagerie LIBS permet d’effectuer la projection en 2-D de la distribution élémentaire au sein de l’échantillon. Elle ne permet pas en revanche d’obtenir d’informations sur la composition élémentaire en profondeur.
Pour contourner cette limite, nous avons développé le concept d’imagerie élémentaire LIBS en trois dimensions (3-D) sur organes biologiques. Dérivant de la méthode d’imagerie LIBS 2-D que nous avons décrite pour étudier la cinétique rénale des Gd-NC, deux stratégies différentes, mais complémentaires, ont été appliquées pour collecter la distribution des éléments d’intérêt en profondeur dans les organes d’animaux [17].
L’analyse élémentaire LIBS a d’abord été utilisée pour réaliser des images d’éléments comme le Gd, le Ca et le Na dans une série de sections coronales adjacentes de reins murins. Les images ont ensuite été regroupées afin de reconstruire la distribution élémentaire au sein de l’organe entier, en 3-D (Figure 3D) [17].
Pour la seconde approche, la capacité du LIBS à effectuer un profilage en profondeur par ablation répétée de la même surface d’intérêt a été exploitée. Une région de plus petite taille que celle analysée avec la première approche a été cartographiée à plusieurs reprises, tout en conservant une résolution spatiale élevée (10 µm) pour obtenir un profil élémentaire 3-D complet et très résolu. La configuration utilisée pour les instruments a permis la détection simultanée de la plupart des éléments endogènes présentant un intérêt biologique : le phosphore P, l’aluminium Al, le magnésium Mg, le sodium Na, le zinc Zn, le silicium Si, le fer Fe et le cuivre Cu. L’ensemble de ces travaux réalisés sur des tissus animaux dans le cadre d’études précliniques nous a permis d’envisager de travailler sur les applications médicales de l’imagerie LIBS.
Les applications médicales de l’imagerie LIBS
La technique d’imagerie multi-élémentaire LIBS possède des applications pour la médecine très variées, allant de la visualisation d’éléments endogènes dans des conditions physiologiques ou pathologiques, à la détection in situ de métaux lourds exogènes dans les tissus après exposition professionnelle ou environnementale.
Nous avons récemment réalisé une étude de faisabilité [18], puis une étude descriptive de la distribution des éléments endogènes dans différentes biopsies de peau humaine [19]. Ces biopsies cutanées provenaient de tissus sains, mais également de carcinomes à cellules de Merkel, de carcinomes épidermoïdes, et de métastases cutanées de mélanome (Figure 4). Confrontées aux images réalisées sur des sections adjacentes par histologie (coloration par hématoxyline/éosine/safran, HES), les images élémentaires obtenues à partir de ces biopsies ont permis la visualisation et l’identification de trois différentes couches physiologiques du tissu cutané qui correspondent parfaitement à l’architecture et à l’organisation retrouvées lors de l’examen histologique. Dans le cas du mélanome métastatique, les images élémentaires de la tumeur ont révélé un gradient de concentrations en Ca, P et Mg, qui contraste avec l’apparente distribution homogène des cellules de mélanome lorsqu’observées au microscope. L’existence de larges plages dynamiques des concentrations en éléments, tels que Ca, Na, Mg et Fe, comprenant des gradients avec des zones de faibles concentrations et d’autres élevées, démontre la grande complémentarité de l’imagerie élémentaire LIBS et de l’analyse histopathologique conventionnelle. Cette étude a été réalisée sur des tissus fixés au formol tamponné puis inclus en paraffine. Les tissus paraffinés représentent la forme la plus fréquente de matériel humain archivé dans les services d’anatomo-pathologie. Ce savoir-faire permet donc d’envisager l’emploi de la technologie LIBS pour analyser au moment du diagnostic ou a posteriori, de très nombreux échantillons présentant un intérêt médical.
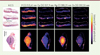 |
Figure 4. Analyse LIBS de différents éléments endogènes. Différentes biopsies humaines cutanées sont comparées à l’analyse histologique classique. HES : coloration hématoxyline/éosine/safran (figure adaptée de [21]). |
Dans une troisième étude, nous avons sélectionné des échantillons de patients pour lesquels les anatomo-pathologistes retrouvaient des anomalies lors de l’examen histo-pathologique [19]. La présence d’anomalies tissulaires (réactions granulomateuses, pigments, vacuoles, ou même corps étrangers) est fréquemment rapportée par les pathologistes lors de leurs analyses de routine, mais leur nature élémentaire est rarement examinée de façon approfondie, principalement par manque de technologies accessibles. C’est pourquoi ces anomalies demeurent souvent largement inexpliquées.
Nous avons effectué une analyse multi-élémentaire LIBS sur des lésions nodulaires sous-cutanées survenues après une vaccination. Les sels d’aluminium sont des adjuvants standard des vaccins et sont susceptibles de provoquer des effets indésirables, comme par exemple des gonflements temporaires ou persistants au niveau du site d’injection. Ces nodules parfois prurigineux ou douloureux peuvent être à l’origine d’une gêne considérable pour les patients. Un diagnostic histologique de ces nodules est généralement effectué pour permettre de distinguer sa nature qui peut être un simple granulome ou une panniculite3, ou encore un pseudo-lymphome. Nous avons analysé la distribution en LIBS de l’aluminium. Afin de recréer l’image obtenue par histologie et de visualiser l’organisation et l’architecture globale du tissu, nous avons utilisé du phosphore ou du sodium, éléments constitutifs des cellules.
Hypersensibilité aux sels d’aluminium
L’analyse LIBS de la distribution de l’aluminium a permis de révéler la présence de quantités importantes de cet élément métallique dans un granulome post-vaccinal (Figure 5A). Sa localisation réalisée par analyse du sodium correspond parfaitement aux zones granulomateuses pathognomoniques dans lesquels certains histiocytes contiennent des granules basophiles intracytoplasmiques tel que révélés après coloration à l’hématoxyline-éosine safranée.
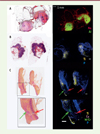 |
Figure 5. Analyse LIBS de différents éléments exogènes. A. Un granulome post-vaccinal humain est représenté par les analyses histologiques (coloration HES, panneau de gauche) et les images LIBS (panneau de droite). L’analyse LIBS met en évidence la très forte présence dans cette biopsie d’aluminium (Al, en vert). Le sodium (Na) est représenté en rouge (figure adaptée de [19]). B. Accumulation de titane dans un ganglion lymphatique « pigmenté ». Le phosphore est en bleu, le titane en jaune. C..Cicatrice de mastectomie présentant des dépôts multiples de titane, cuivre, tungstène et chrome (barre d’échelle : 1 mm). |
Ganglions lymphatiques pigmentés
Lors de l’évaluation macroscopique d’un ganglion lymphatique, la présence d’une couleur noire peut évoquer la présence de cellules de mélanome qui contiennent de la mélanine [20] (→).
(→) Voir la Synthèse de F. Gesbert et L. Larue, m/s n° 5, mai 2018, page 407
Il s’agira alors d’une métastase ganglionnaire du mélanome. La migration de particules exogènes d’encre provenant de tatouages cutanés peut cependant être également responsable de la pigmentation de certains ganglions lymphatiques. La nature des pigments de couleur sombre retrouvés par les chirurgiens ou les anatomo-pathologistes lors de biopsies ou dissections ganglionnaires doit donc impérativement être étudiée, tout particulièrement pour les patients ayant un antécédent de mélanome.
Nous avons analysé un ganglion inguinal provenant d’un patient ayant un historique de mélanome localisé au niveau de la jambe, qui avait été opéré plusieurs années auparavant. Dans un contexte de récidive locale, un curage ganglionnaire inguinal a été réalisé. Au cours de cette chirurgie, huit ganglions ont été excisés, dont un était macroscopiquement suspect (texture ferme et de couleur noire). L’examen histopathologique du ganglion pigmenté (ou « tatoué ») suspect a révélé la présence de pigments granulaires noirs formant des dépôts extracellulaires dans les sinus du ganglion, mais absents du tissu adipeux, ainsi que dans de rares histiocytes présentant de petites quantités de particules pigmentées dans leur cytoplasme ( Figure 5B , panneau de gauche). L’analyse du phosphore par LIBS a permis de visualiser l’architecture des ganglions lymphatiques, et l’étude multi-élémentaire a révélé la présence de niveaux élevés de titane (Ti) ( Figure 5B , panneau de droite) dans différentes zones du ganglion analysé, correspondant parfaitement à la topographie du pigment noir retrouvé à l’examen histopathologique. Les analyses complémentaires immuno-histochimiques, réalisées par le pathologiste, ont confirmé l’absence de cellules de mélanome. L’origine du titane responsable de la pigmentation des ganglions n’a pas été recherchée.
Particules exogènes post-chirurgicales
Chez une patiente ayant subi une ablation du sein à la suite d’un cancer, le rapport histopathologique de la cicatrice avait révélé la présence de différentes anomalies liées au processus de résorption dans le derme fibrotique : (1) des cellules géantes multinucléées entourant une substance étrangère anhistique4 ; (2) des infiltrations histiocytaires présentant un pigment basophile dans leur cytoplasme ; et (3) un petit agrégat d’histiocytes ou de granulocytes avec de petites granulations positives à l’acide periodique de Schiff5 ( Figure 5C , panneau de gauche). Une analyse LIBS a été réalisée sur les tissus cicatriciels. Les images multi-élémentaires LIBS ont révélé la présence d’un taux élevé de titane, en plus de la présence de cuivre et de particules localisées de tungstène (W) ou de chrome (Cr), confirmant la présence de débris métalliques résultant de l’acte chirurgical ( Figure C panneau de droite) pouvant expliquer les anomalies observées.
La présence de corps étrangers dans les tissus après chirurgie est largement documentée et plusieurs substances exogènes, telles que des particules ou des débris, peuvent provenir de la libération de composants d’instruments chirurgicaux, de sutures, d’agrafes, d’implants, ou d’autres sources.
Lorsqu’elle est associée à une analyse histopathologique de routine, la technologie LIBS, simple à mettre en œuvre, peut donc aider les pathologistes à établir et/ou confirmer des diagnostics dans une large gamme d’applications médicales, notamment pour identifier la nature de composés retrouvés dans un tissu qui sont potentiellement exogènes.
La combinaison de différentes techniques peut être nécessaire pour obtenir des informations complémentaires. Bonta et al. ont associé l’analyse élémentaire LIBS à une analyse par LA-ICP-MS de tissus humains de mésothéliome pleural malin [16]. L’analyse LIBS a ainsi permis d’identifier des éléments qui ne pouvaient être quantifiés par LA-ICP-MS (des éléments majoritaires, notamment le carbone, l’oxygène et l’hydrogène). La technologie ICP-MS repose, elle, sur la spectrométrie de masse. Elle permet donc la quantification absolue de tous les éléments chimiques du tableau périodique. Son excellente sensibilité rend possible le rendu en image de la distribution de certains éléments présents à des concentrations extrêmement faibles (quelques parties par milliard, ou ppb).
Conclusion
La méthode d’imagerie multi-élémentaire LIBS repose sur un système entièrement fondé sur l’optique. Elle est rapide et facilement utilisable sur différents types de matrices (tissu inclus en résine époxy ou en paraffine). Avec un laser à 10 Hz de fréquence, l’instrument LIBS permet de scanner une surface d’environ 6 cm2 en 3 heures, ce temps diminue jusqu’à 20 minutes si l’instrument est équipé d’un laser à 100 Hz [19]. L’imagerie LIBS permet une analyse avec une sensibilité de l’ordre de plusieurs dizaines d’attomoles (10-15 moles) et la distribution de nombreux éléments métalliques dans les tissus biologiques est visualisable. La préparation du tissu et la configuration du microscope LIBS répondent aux exigences de détection des éléments dans la plupart des applications biomédicales, notamment en termes de résolution et de sensibilité. Ses capacités uniques permettent d’analyser des éléments métalliques majeurs, mineurs et même à l’état de traces dans divers matériaux biologiques [8]. Les informations collectées sont directement issues de mesures réalisées au sein du tissu et analysées de façon semi-quantitative.
L’inconvénient majeur de l’imagerie LIBS est indéniablement son caractère destructeur, bien que seule une très petite quantité de matériel biologique (moins de 1 ng) soit prélevée pour la mesure. L’avantage des techniques utilisant l’ablation laser est néanmoins de permettre d’acquérir des profils de distribution en profondeur afin de créer des images en 3 dimensions avec une résolution latérale de quelques micromètres seulement.
L’analyse élémentaire LIBS des tissus biologiques donne des résultats complémentaires à ceux obtenus par des méthodes classiques utilisées en médecine, telles que la microscopie électronique à transmission et l’analyse histologique couplée à l’immunohistochimie [21]. Elle peut être associée à des techniques plus complexes offrant des performances supérieures, mais dans des conditions plus restrictives, comme l’ICP-MS, la nano-SIMS ou la µXRF. L’équipement LIBS peut également être directement couplé à des systèmes d’imagerie Raman ou de fluorescence.
L’intérêt croissant pour la distribution des éléments métalliques et organiques dans les tissus biologiques suggère que cette technologie deviendra probablement un outil d’investigation précieux pour l’imagerie multi-élémentaire directe, c’est-à-dire ne requérant aucun marquage. Cette approche est très polyvalente puisqu’une grande majorité des éléments, en particulier les métaux, peut être détectée avec une grande sensibilité. Elle peut également être aisément utilisée dans les laboratoires de recherche pour les analyses élémentaires de routine dans les domaines de la nanotechnologie et en biologie. À l’avenir, la médecine devrait pouvoir bénéficier de ces développements : découverte de nouveaux biomarqueurs pour l’identification du tissu cancéreux, recherche d’éléments exogènes et aide au diagnostic médical.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Métaux qui participent à l’oxydo-réduction.
Dans ce cas, une double impulsion laser est appliquée.
Une inflammation du pannicule, la couche de tissu adipeux et fibreux située sous l’épiderme.
Non structurée.
Cette coloration est utilisée en histologie pour mettre en évidence les polysaccharides.
Références
- Chang CJ. Searching for harmony in transition-metal signaling. Nat Chem Biol 2015 ; 11 : 744–747. [Google Scholar]
- Waldron KJ, Rutherford JC, Ford D, Robinson NJ. Metalloproteins and metal sensing. Nature 2009 ; 460 : 823–830. [CrossRef] [PubMed] [Google Scholar]
- Collingwood JF, Adams F. Chemical imaging analysis of the brain with X-ray methods. Spectrochim Acta Part B At Spectrosc 2017 ; 130 : 101–118. [Google Scholar]
- Barnham KJ, Bush AI. Biological metals and metal-targeting compounds in major neurodegenerative diseases. Chem Soc Rev 2014 ; 43 : 6727–6749. [CrossRef] [PubMed] [Google Scholar]
- Chao W, Harteneck BD, Liddle JA, et al. Soft X-ray microscopy at a spatial resolution better than 15 nm. Nature 2005 ; 435 : 1210–1213. [CrossRef] [PubMed] [Google Scholar]
- Hare DJ, New EJ, de Jonge MD, McColl G. Imaging metals in biology: balancing sensitivity, selectivity and spatial resolution. Chem Soc Rev 2015 ; 44 : 5941–5958. [CrossRef] [PubMed] [Google Scholar]
- Sussulini A, Becker JS, Becker JS. Laser ablation ICP-MS: Application in biomedical research. Mass Spectrom Rev 2017 ; 36 : 47–57. [Google Scholar]
- Gaudiuso R, Melikechi N, Abdel-Salam ZA, et al. Laser-induced breakdown spectroscopy for human and animal health: a review. Spectrochim Acta Part B At Spectros 2019 ; 152 : 123–148. [CrossRef] [Google Scholar]
- Jantzi SC, Motto-Ros V, Trichard F, et al. Sample treatment and preparation for laser-induced breakdown spectroscopy. Spectrochim Acta Part B At Spectros 2016 ; 115 : 52–63. [CrossRef] [Google Scholar]
- Ghasemi F, Parvin P, Hosseini Motlagh NS, et al. Laser induced breakdown spectroscopy and acoustic response techniques to discriminate healthy and cancerous breast tissues. Appl Opt 2016 ; 55 : 8227–8235. [CrossRef] [PubMed] [Google Scholar]
- Markushin Y, Sivakumar P, Connolly D, Melikechi N. Tag-femtosecond laser-induced breakdown spectroscopy for the sensitive detection of cancer antigen 125 in blood plasma. Anal Bioanal Chem 2015 ; 407 : 1849–1855. [CrossRef] [PubMed] [Google Scholar]
- Han JH, Moon Y, Lee JJ, et al. Differentiation of cutaneous melanoma from surrounding skin using laser-induced breakdown spectroscopy. Biomed Opt Express 2016 ; 7 : 57–66. [CrossRef] [PubMed] [Google Scholar]
- Singh VK, Rai AK. Prospects for laser-induced breakdown spectroscopy for biomedical applications: a review. Lasers Med Sci 2011 ; 26 : 673–687. [CrossRef] [PubMed] [Google Scholar]
- Kunjachan S, Detappe A, Kumar R, et al. Nanoparticle Mediated Tumor Vascular Disruption: A Novel Strategy in Radiation Therapy. Nano Letters 2015 ; 15 : 7488–7496. [CrossRef] [PubMed] [Google Scholar]
- Sancey L, Motto-Ros V, Busser B, et al. Laser spectrometry for multi-elemental imaging of biological tissues. Sci Rep 2014 ; 4 : 6065. [CrossRef] [PubMed] [Google Scholar]
- Bonta M, Gonzalez JJ, Quarles CD, et al. Elemental mapping of biological samples by the combined use of LIBS and LA-ICP-MS. J Anal At Spectrom 2016 ; 31 : 252–258. [Google Scholar]
- Gimenez Y, Busser B, Trichard F, et al. 3D Imaging of Nanoparticle Distribution in Biological Tissue by Laser-Induced Breakdown Spectroscopy. Sci Rep 2016 ; 6 : 29936. [CrossRef] [PubMed] [Google Scholar]
- Moncayo S, Trichard F, Busser B, et al. Multi-elemental imaging of paraffin-embedded human samples by laser-induced breakdown spectroscopy. Spectrochim Acta Part B At Spectros 2017 ; 133 : 40–44. [CrossRef] [Google Scholar]
- Busser B, Moncayo S, Trichard F, et al. Characterization of foreign materials in paraffin-embedded pathological specimens using in situ multi-elemental imaging with laser spectroscopy. Mod Pathol 2018 ; 31 : 378–384. [CrossRef] [PubMed] [Google Scholar]
- Gesbert F, Larue L. Le mélanome cutané: des modèles rationalisés aux soins des patients. Med Sci (Paris) 2018 ; 34 : 407–416. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Busser B, Moncayo S, Coll JL, et al. Elemental imaging using laser-induced breakdown spectroscopy: A new and promising approach for biological and medical applications. Coord Chem Rev 2018 ; 358 : 70–79. [Google Scholar]
- Mordon SR. Trois chercheurs, dont un Français, récompensés pour leurs travaux sur les lasers. Med Sci (Paris) 2019 ; 35 : 176–177. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. Représentation schématique des principaux composants du système LIBS. Sont présentés le laser pulsé, l’objectif du microscope, l’échantillon, la plateforme motorisée et la collection du signal transmis par fibre optique au spectromètre. Les spectres LIBS (laser-induced breakdown spectroscopy) générés ont des longueurs d’ondes caractéristiques des éléments présents dans l’échantillon. L’analyse point par point permet de reconstituer une image en deux dimensions pour chaque élément d’intérêt. Gd : gadolinium ; Na : sodium. |
| Dans le texte | |
 |
Figure 2. Principales caractéristiques et exemples d’application du LIBS. |
| Dans le texte | |
 |
Figure 3. Images LIBS obtenues à partir d’échantillons biologiques. A. Tumeur pancréatique représentée par le phosphore (P, en bleu) chargée en nanocomposés d’or (Au, en jaune). B..Cinétique d’élimination rénale de nanocomposés de gadolinium (Gd-NC, en vert). Le sodium est représenté en rouge. C. Image haute résolution (600 x 410 pixels) d’un rein de souris. Le gadolinium est représenté en vert et les fortes concentrations de calcium, en rouge. D. Images en trois dimensions d’un rein de souris montrant la répartition du gadolinium (en vert), du calcium (en violet) ou du sodium (en rouge) (figure adaptée de [21]). |
| Dans le texte | |
 |
Figure 4. Analyse LIBS de différents éléments endogènes. Différentes biopsies humaines cutanées sont comparées à l’analyse histologique classique. HES : coloration hématoxyline/éosine/safran (figure adaptée de [21]). |
| Dans le texte | |
 |
Figure 5. Analyse LIBS de différents éléments exogènes. A. Un granulome post-vaccinal humain est représenté par les analyses histologiques (coloration HES, panneau de gauche) et les images LIBS (panneau de droite). L’analyse LIBS met en évidence la très forte présence dans cette biopsie d’aluminium (Al, en vert). Le sodium (Na) est représenté en rouge (figure adaptée de [19]). B. Accumulation de titane dans un ganglion lymphatique « pigmenté ». Le phosphore est en bleu, le titane en jaune. C..Cicatrice de mastectomie présentant des dépôts multiples de titane, cuivre, tungstène et chrome (barre d’échelle : 1 mm). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




