| Issue |
Med Sci (Paris)
Volume 35, Number 5, Mai 2019
|
|
|---|---|---|
| Page(s) | 483 - 485 | |
| Section | Forum | |
| DOI | https://doi.org/10.1051/medsci/2019080 | |
| Published online | 22 May 2019 | |
Extension du domaine du codage : l’ADN hachimoji
Chroniques génomiques
Hachimoji DNA extends coding possibilities
UMR 7268 ADÉS, Aix-Marseille, Université/EFS/CNRS ; CoReBio PACA, case 901, Parc scientifique de Luminy, 13288 Marseille Cedex 09, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Abstract
The synthesis of four new nucleotide analogues that can form hydrogen bonds within the DNA double helix and can be incorporated without distortion of the structure extends the possibilities of synthetic biology. Although functional use of these analogues remains in the future, they already have interesting applications and represent an important step forward.
© 2019 médecine/sciences – Inserm
 Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.
Article publié sous les conditions définies par la licence Creative Commons Attribution License CC-BY (http://creativecommons.org/licenses/by/4.0), qui autorise sans restrictions l'utilisation, la diffusion, et la reproduction sur quelque support que ce soit, sous réserve de citation correcte de la publication originale.

Nous avions rapporté il y a un an le très joli travail réalisé au département de chimie du Scripps Research Institute (La Jolla, Californie), associé à l’entreprise Synthorx, qui avait réussi à synthétiser deux nouvelles bases analogues aux classiques C, T, A et G et qui pouvaient former dans l’ADN une nouvelle paire de bases. Ces chercheurs avaient même réussi à faire répliquer cet ADN par une bactérie, à assurer (grâce à diverses manipulations de haute volée) sa transcription et sa traduction et ainsi à insérer dans une protéine un acide aminé anormal (ne faisant pas partie des vingt acides aminés classiques) [1, 2] (→).
(→) Voir la Chronique génomique de B. Jordan, m/s n° 2, février 2018, page 179
Bien que très intéressant et novateur, ce travail comportait une limite : les deux bases artificielles ne forment pas de liaisons hydrogène au sein de la double hélice de l’ADN (comme le font G et C, d’une part, A et T, d’autre part) et leur association repose sur la compatibilité de leurs formes. Du coup, une paire artificielle doit être entourée de bases naturelles pour assurer la stabilité de la double hélice, ce qui limite sévèrement la gamme des séquences réalisables. Un article récemment publié dans la revue Science par un ensemble de laboratoires et d’entreprises démontre, lui, la possibilité de concevoir des bases alternatives qui peuvent s’associer par des liaisons hydrogène et respectent ainsi la structure de la double hélice [3]. Ces auteurs obtiennent ainsi un système baptisé « hachimoji » comprenant huit (« hachi » en japonais) lettres (« moji ») — les quatre habituelles plus quatre nouvelles — et montrent qu’il possède les propriétés minimales nécessaires à un système biologique capable de porter de l’information.
De nouvelles « lettres » respectant la structure en double hélice
Au terme d’un important travail de chimie, les auteurs ont obtenu quatre nouvelles bases dont la structure est assez proche (mais différente) des bases classiques : P et Z (qui peuvent s’apparier par trois liaisons hydrogène), et S et B (trois liaisons également). Elles sont représentées dans la Figure 1 sous forme de déoxynucléotides, tels qu’ils existent dans l’ADN.
 |
Figure 1. Les deux couples de bases classiques (C-G et T-A), à gauche, et les deux nouveaux couples Z-P, et S-B. Les liaisons hydrogène se forment entre atomes donneurs (H) et accepteurs (O ou N). dR désigne la chaîne de désoxyribose à laquelle est attachée chaque base. On note que le couple S-B peut former trois liaisons hydrogène au lieu de deux dans le couple T-A (extrait partiel et remanié de la figure 1 de [3]). |
A priori, compte tenu de l’encombrement de ces molécules (très proche de celui des bases classiques) et de leur capacité à former des liaisons hydrogène, on peut s’attendre à ce qu’elles s’incorporent dans la double hélice de l’ADN sans la déformer. Ce point est examiné tout d’abord en synthétisant des oligonucléotides auto-complémentaires contenant deux (par exemple GCPTAZGC) ou quatre (par exemple CSZATPBG) de ces nouveaux nucléotides. Chacun de ces oligonucléotides peut former un duplex avec lui-même1, et l’on peut alors établir une courbe de fusion et mesurer la température de fusion (Tm) qui indique le degré de stabilité de la double hélice précédemment formée. Les Tm obtenus pour une série de presque cent duplex hachimoji sont conformes à la prédiction pour une double hélice, indiquant donc que cette structure s’est bien formée et qu’elle est aussi stable qu’une double hélice « naturelle ». Pour aller plus loin et observer directement la double hélice, les auteurs ont utilisé une astuce, la possibilité de cristalliser facilement des complexes entre un segment d’ADN double brin et un fragment d’une protéine virale, complexes dans lesquels chaque extrémité du duplex est liée à un fragment protéique2, l’essentiel de l’ADN restant libre d’adopter sa structure en double hélice [4]. Ils ont pour cela synthétisé trois oligonucléotides auto-complémentaires longs de 16 bases et contenant quatre nouvelles bases. Après formation des duplex, association avec les fragments protéiques et cristallisation, la structure obtenue est bien une double hélice dont les paramètres sont conformes à ceux d’une structure naturelle. La Figure 2 montre la structure obtenue pour la double hélice formée par l’oligonucléotide CTTATPPSBZZATAAG apparié à lui-même.
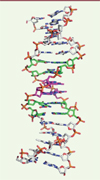 |
Figure 2. Structure tridimensionnelle par cristallographie aux rayons X du duplex formé par l’oligonucléotide auto-complémentaire CTTATPPSBZZATAAG. Cette double hélice correspond précisément à la forme B de l’ADN (extrait partiel et remanié de la figure 3 de [3]). |
On voit donc que ces quatre nouvelles bases peuvent être incorporées dans l’ADN sans perturber la structure en double hélice, respectant ainsi une propriété fondamentale de l’ADN, celle de pouvoir contenir n’importe quelle suite de bases sans que cela ne perturbe sa structure tridimensionnelle, propriété essentielle pour une molécule devant coder de l’information.
L’ADN hachimoji peut être transcrit
Pour être mise en œuvre, l’information contenue dans l’ADN doit être transcrite en ARN messager pour enfin être traduite en protéine. L’étape suivante a donc logiquement consisté à obtenir la transcription de l’ADN hachimoji. En fait, la classique ARN polymérase du bactériophage T7 s’est avérée capable de transcrire dP, dS et dZ (déoxyribonucléotides dans l’ADN) en leurs ribonucléotides complémentaires (Z, B et P), seule la transcription de dB (en S) ne fonctionnait pas. Mais il existe des variants de cette enzyme obtenus dans le cadre de projet d’amélioration menés par des entreprises de biotechnologie, et l’un d’eux, l’ARN polymérase T7 dite FAL, est capable d’effectuer cette opération. Il est donc possible grâce à ce variant de transcrire un ADN hachimoji en ARN – lui aussi hachimoji, c’est-à-dire incluant les bases anormales Z, B, P et S sous forme, bien sûr, de ribonucléotides.
L’article [3] se termine sur la synthèse d’un oligonucléotide 84-mer contenant quatre nouvelles bases et la démonstration que cet oligonucléotide conserve sa capacité à émettre de la fluorescence après liaison d’un composé dérivé de l’imidazolinone, lorsque les nouvelles bases sont situées loin du site de liaison de ce produit, et les perd lorsqu’elles sont à proximité. C’est un premier pas (encore modeste) vers des applications fonctionnelles de ce système.
Le chemin qui reste, les possibilités déjà ouvertes
Si l’on compare ce travail à celui publié il y a plus d’un an [1], il est clair qu’il va beaucoup moins loin sur le plan fonctionnel : l’ADN hachimoji peut certes être transcrit, mais on n’a pas de données précises sur la fidélité de cette transcription. La structure de cet ADN est bien en double hélice, mais sa réplication (in vitro ou in vivo) n’a pas été démontrée. Et avant d’envisager la synthèse de nouvelles protéines grâce à ce code étendu à huit lettres, il faudrait mettre en place tous les intermédiaires indispensables à la traduction : ARN de transfert reconnaissant de nouveaux codons, enzymes capables de charger ces ARN avec les acides aminés « exotiques » que l’on voudra incorporer dans les protéines… L’examen des travaux précédents [1, 2] montre l’ampleur de la tâche.
Il n’en reste pas moins que l’ADN hachimoji a déjà de nombreuses applications potentielles. Le codage par huit bases différentes augmente considérablement la quantité d’information que peut porter un segment d’ADN (un décamère hachimoji a 810 séquences possibles au lieu de 410 pour un décamère classique, soit 1 024 fois plus). Cela peut être très utile pour différents systèmes dits de barcoding ou d’étiquetage combinatoire [5], de plus en plus employés dans le secteur du diagnostic, qui utilisent la séquence de petits segments d’ADN pour caractériser différentes fractions ou pour afficher le résultat final. Pour les projets de stockage de l’information dans l’ADN déjà évoqués dans ces chroniques [6] (→), un code à huit lettres présente lui aussi des avantages évidents. Un autre domaine de recherche très actif, celui des nanostructures à base d’ADN [7], pourrait également bénéficier de ces nouvelles possibilités. Une entreprise, Firebird Biomolecular Sciences3 se charge d’ailleurs de commercialiser ces applications, et près de la moitié des auteurs du présent article sont impliqués dans cette firme.
(→) Voir la Chronique génomique de B. Jordan, m/s n° 6-7, juin-juillet 2018, page 622
Sur un plan plus philosophique, et comme déjà mentionné précédemment [2], ce travail confirme que les bases C, A, T et G utilisées par tous les organismes terrestres ne sont pas les seules possibles. Leur ubiquité dans notre monde vivant reflète simplement le fait que nous descendons tous du même organisme qui s’est trouvé fonctionner avec ces éléments : le hasard de la constitution du premier « réplicateur » s’est combiné avec la nécessité de la sélection naturelle pour aboutir aux organismes d’hier et d’aujourd’hui. Mais nous aurions bien tort, dans nos tentatives de découvrir des traces de vie sur Mars, sur le satellite Europe (une lune de Jupiter) et peut-être, plus tard, sur des planètes extrasolaires, de cibler trop précisément nos analyses sur des molécules semblables à celles que nous connaissons. Même si une vie apparue ailleurs est fondée sur la chimie du carbone, de l’oxygène et de l’azote, même si elle utilise une molécule d’ADN comme mémoire génétique, il n’y a aucune raison pour s’attendre à ce que les bases alignées le long de cette molécule soient nos habituels C, A, T ou G…
Liens d’intérêt
L’auteur déclare n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
L’oligonucléotide 5’GCPTAZGC3’ s’apparie avec lui-même, soit 3’CGZATPCG5’.
Il s’agit d’un fragment de la transcriptase inverse du virus de la leucémie murine de Moloney, comme décrit dans [4].
Références
- Zhang Y, Ptacin JL, Fischer EC, et al. A semi-synthetic organism that stores and retrieves increased genetic information. Nature. 2017 ; 551 : 644–647. [CrossRef] [PubMed] [Google Scholar]
- Jordan B.. Bases alternatives et organismes synthétiques. Med Sci (Paris). 2018 ; 34 : 179–182. [Google Scholar]
- Hoshika, Leal NA, Kim MJ, et al. Hachimoji DNA and RNA: a genetic system with eight building blocks. Science 2019; 363 : 884–7. [Google Scholar]
- Coté ML, Yohannan SJ, Georgiadis MM. Use of an N-terminal fragment from moloney murine leukemia virus reverse transcriptase to facilitate crystallization and analysis of a pseudo-16-mer DNA molecule containing G-A mispairs. Acta Crystallogr D Biol Crystallogr. 2000 ; 56 : 1120–1131. [CrossRef] [PubMed] [Google Scholar]
- Tsang HF, Xue VW, Koh SP, et al. NanoString, a novel digital color-coded barcode technology: current and future applications in molecular diagnostics. Expert Rev Mol Diagn. 2017 ; 17 : 95–103. [CrossRef] [PubMed] [Google Scholar]
- Jordan B.. L’ADN comme mémoire informatique ?. Med Sci (Paris). 2018 ; 34 : 622–625. [Google Scholar]
- Linko V, Ora A, Kostiainen MA. DNA nanostructures as smart drug-delivery vehicles and molecular devices. Trends Biotechnol. 2015 ; 33 : 586–594. [CrossRef] [PubMed] [Google Scholar]
Liste des figures
 |
Figure 1. Les deux couples de bases classiques (C-G et T-A), à gauche, et les deux nouveaux couples Z-P, et S-B. Les liaisons hydrogène se forment entre atomes donneurs (H) et accepteurs (O ou N). dR désigne la chaîne de désoxyribose à laquelle est attachée chaque base. On note que le couple S-B peut former trois liaisons hydrogène au lieu de deux dans le couple T-A (extrait partiel et remanié de la figure 1 de [3]). |
| Dans le texte | |
 |
Figure 2. Structure tridimensionnelle par cristallographie aux rayons X du duplex formé par l’oligonucléotide auto-complémentaire CTTATPPSBZZATAAG. Cette double hélice correspond précisément à la forme B de l’ADN (extrait partiel et remanié de la figure 3 de [3]). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




