| Issue |
Med Sci (Paris)
Volume 34, Number 3, Mars 2018
|
|
|---|---|---|
| Page(s) | 211 - 214 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/20183403007 | |
| Published online | 16 March 2018 | |
Nouvelle
Quand l’exposition à un perturbateur endocrinien environnemental affecte le comportement de cour chez le mâle
When exposure to an environmental endocrine disrupter reduces male courtship behavior
Sorbonne universités, Université Pierre et Marie Curie, Paris 06, Inserm, CNRS, neuroscience Paris Seine - Institut de biologie Paris Seine, 7, quai St-Bernard, Bâtiment A, 75005 Paris, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Un constat général des dernières décennies est l’augmentation de l’incidence de maladies et de dysfonctionnements du système reproducteur. La diminution de la fertilité masculine et de la qualité du sperme ou encore l’augmentation des malformations urogénitales coïncident avec l’augmentation massive de l’utilisation de molécules agissant comme des perturbateurs endocriniens [1, 2].( )
)
Ce sont des polluants environnementaux naturels ou fabriqués par l’homme capables d’interférer avec les systèmes hormonaux endogènes. Parmi ces molécules, les phtalates comme le di(2-éthylhexyle) phtalate (DEHP) sont répandus dans les produits du quotidien et figurent dans la liste des substances prioritaires1 dans le domaine de l’eau (Arrêté 7/09/2015, article R. 212-9 du code de l’environnement). Des études épidémiologiques ont rapporté une association entre les niveaux de métabolites de phtalates dans les urines et la diminution de la distance ano-génitale2, ou la réduction de jeu masculin chez les garçons [3, 4]. Des études expérimentales ont décrit des effets de l’exposition prénatale et/ou postnatale aux phtalates sur le développement et le fonctionnement de l’appareil reproducteur mâle chez les rongeurs [5, 6]. Les effets de l’exposition adulte à ces molécules sur le contrôle de la reproduction mâle au niveau du système nerveux central ne sont cependant pas documentés. Cette période reste, en effet, sous-estimée dans l’évaluation du risque sanitaire lié à l’exposition aux perturbateurs endocriniens, alors qu’il est établi que la plasticité synaptique du cerveau adulte peut être affectée à longterme. Enfin, la majorité des études portant sur les phtalates a évalué les effets de doses très élevées et donc éloignées de celles qui sont estimées pour l’exposition environnementale.
( )voir la Synthèse de C. Mauduit et al. m/s n° 1, janvier 2016, page 45
)voir la Synthèse de C. Mauduit et al. m/s n° 1, janvier 2016, page 45
La reproduction chez les rongeurs
Chez les rongeurs, l’accouplement est précédé d’une phase de cour pendant laquelle le mâle présente une préférence olfactive pour les femelles réceptives. En réponse à cette stimulation olfactive, il émet des vocalisations ultrasonores qui joueraient un rôle dans l’attraction et le maintien de la femelle réceptive à proximité du mâle, facilitant ainsi l’accouplement. Pendant la phase copulatoire, le mâle effectue des montées, d’abord sans, puis avec intromissions, et des mouvements pelviens avant d’atteindre l’éjaculation (Figure 1A). L’ensemble de ces comportements est régulé par le système nerveux central. Les informations olfactives détectées au niveau du bulbe olfactif sont transmises à l’amygdale médiane, au noyau du lit de la strie terminale et enfin au noyau préoptique hypothalamique où ces signaux sont transformés en réponse comportementale. Des projections partent également de l’hypothalamus vers des noyaux spinaux impliqués dans l’érection et l’éjaculation.
La testostérone a un rôle majeur dans la mise en place de ce circuit neural (neuronal et glial) en période périnatale et pubertaire et dans son activation à l’âge adulte. Elle peut agir directement en activant le récepteur des androgènes (AR). Elle peut également être métabolisée dans le système nerveux en œstradiol qui stimule les récepteurs des œstrogènes alpha et beta (ERa et ERß). Chez la souris, les récepteurs AR et ERa représentent les deux voies de signalisation majeures dans la régulation du comportement sexuel mâle par la testostérone [7, 8].
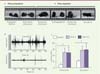 |
Figure 1. Effets de l’exposition au DEHP sur le comportement de cour. A. Séquence comportementale illustrant les phases précopulatoire et copulatoire chez la souris. B. Effets de l’exposition adulte au DEHP sur les vocalisations ultrasonores illustrées par l’onde sonore enregistrée chez un mâle contrôle et un mâle exposé au DEHP à 50 μg/kg/j (DEHP-50). C. Effets de l’exposition au DEHP aux doses 5 (DEHP-5) et 50 μg/kg/j (DEHP-50) sur la latence à la première intromission et à l’éjaculation (a : p < 0,05). Les mâles exposés au DEHP initient la première intromission et arrivent à l’éjaculation tardivement par rapport au groupe contrôle (données tirées de l’article de Dombret et al. [10]). |
Vulnérabilité sexuelle à l’exposition au DEHP
Nous avons montré précédemment que l’exposition de souris mâles adultes à de faibles doses de bisphénol A (BPA), un autre perturbateur endocrinien, altère l’expression du comportement sexuel [9]. Dans cette nouvelle étude, nous avons recherché si la vulnérabilité adulte du circuit neural impliqué dans l’expression du comportement sexuel était restreinte au BPA ou si elle pouvait être étendue à d’autres perturbateurs endocriniens comme le DEHP. Afin de répondre à cette question, des souris mâles adultes de la souche C57BL/6J ont été nourries pendant 6 semaines avec leur nourriture habituelle contenant soit le véhicule (groupe contrôle), soit le DEHP à trois faibles doses (50, 5 et 0,5 μg/kg/j). La dose la plus élevée correspond à la dose journalière tolérable3; la plus faible est celle estimée de l’exposition environnementale. L’analyse de la phase précopulatoire du comportement sexuel a montré que la préférence olfactive des mâles exposés au DEHP n’était pas affectée [10]. En revanche, les mâles exposés à la dose journalière tolérable (50 μg/kg/j de DEHP) produisaient moins de vocalisations en présence de femelles réceptives en comparaison avec le groupe contrôle (Figure 1B). Neuf types de syllabes, qui peuvent être regroupés en trois catégories, sont émis par les souris : simples, complexes et avec des sauts de fréquence. Leur analyse détaillée a révélé des modifications de distribution de chacune des catégories de syllabes dans les groupes exposés aux doses de 0,5 et 5 μg/kg/j de DEHP et les femelles réceptives ont été moins attirées par les mâles exposés aux doses 5 et 50 μg/kg/j, en comparaison avec les mâles contrôles, probablement en raison d’altération dans l’émission des vocalisations ultrasonores [10]. Cette baisse d’attractivité des femelles a été associée à un retard d’initiation de la première intromission, et par conséquent à l’arrivée à l’éjaculation (Figure 1C).
Un mécanisme neural à l’origine des effets induits par le DEHP
L’exposition adulte au DEHP, aux doses utilisées dans cette étude, ne modifie ni les niveaux circulants de testostérone, ni le système GnRH-kisspeptine4, ce qui indique que les altérations comportementales que l’on observe proviennent probablement d’atteintes du système nerveux central. Afin de vérifier cette hypothèse, nous avons isolé des noyaux préoptiques à partir de coupes de cerveaux et effectué une analyse protéomique par analyse différentielle de protéines sur gels bidimensionnels (2D-DIGE) suivie de l’identification des protéines d’intérêt par spectrométrie de masse (LC-MS-MS). Cette région joue un rôle clé dans la motivation à vocaliser et à s’accoupler. Les résultats obtenus ont identifié des protéines exprimées différentiellement entre les groupes d’animaux contrôles et exposés aux doses 5 et 50 μg/kg/j. Nous avons ainsi noté une augmentation de quantité de deux protéines du cytosquelette, la protéine acide fibrillaire gliale (GFAP) et la β-actine, suggérant des changements de structure et de morphologie des cellules gliales et/ou neuronales. La GFAP est en effet une protéine des filaments intermédiaires des astrocytes, dont l’expression est induite à la suite d’un stress cellulaire, notamment en conditions pathologiques.
L’analyse des réseaux d’interaction protéine-protéine par ingenuity pathway analysis5 a révélé une relation entre la majorité des protéines identifiées par l’approche protéomique et le récepteur des androgènes (AR) [10]. L’étude de l’expression des récepteurs AR et ERα dans le noyau préoptique par des analyses immunohistochimiques a révélé une diminution de moitié du nombre de cellules immunoréactives pour l’AR dans ce noyau, ainsi que dans les autres régions impliquées dans le comportement sexuel (amygdale médiane, noyau du lit de la strie terminale). Les niveaux des transcrits de l’AR étaient également diminués de moitié dans le noyau préoptique, suggérant que l’exposition au DEHP altérait l’expression de l’AR au niveau transcriptionnel. De manière intéressante, aucune modification du nombre de neurones immunoréactifs pour l’ERα n’a été observée, indiquant un effet sélectif de l’exposition au DEHP sur l’expression de l’AR.
Sur la base de l’ensemble de nos résultats, nous avons suggéré que l’exposition au DEHP diminue l’expression de l’AR, interférant ainsi avec l’activation par la testostérone des comportements de cour comme l’émission des vocalisations ultrasonores (Figure 2). Cette hypothèse est en accord avec les observations que les souris dépourvues d’AR dans leur système nerveux présentent une forte diminution du nombre et de la durée des vocalisations en comparaison avec leurs frères contrôles [10]. Dans une précédente étude, nous avions observé chez ces souris dépourvues d’expression d’AR, des altérations du comportement sexuel similaires à celles décrites chez les souris exposées au DEHP [7]. L’exposition au DEHP semble également induire une astrogliose6 qui pourrait être liée à la régulation négative de l’expression de l’AR. En effet, la déplétion en testostérone, pendant 5 semaines, induit une régulation négative de l’expression de l’AR et provoque une activation gliale et une neuroinflammation chez les souris mâles [11]. Le lien potentiel entre l’activation gliale et l’altération comportementale reste à préciser.
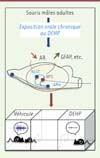 |
Figure 2. Effets comportementaux et moléculaires de l’exposition adulte au DEHP. L’exposition orale de souris mâles adultes au DEHP induit une régulation négative du récepteur des androgènes (AR) dans le circuit du comportement sexuel : amygdale médiane (AMe), noyau du lit de la strie terminale (NLST), noyau préoptique (NPO). Il en résulte des altérations du comportement de cour comme la réduction de l’émission des vocalisations ultrasonores ou de l’attraction des femelles réceptives. Au niveau cellulaire et moléculaire, l’exposition au DEHP induit, dans lenoyau préoptique, une surexpression de la protéine acide fibrillaire gliale (GFAP), marqueur de l’activation gliale. |
Conclusion
L’ensemble de ce travail illustre, pour la première fois, que le DEHP à des doses proches de celles de l’exposition environnementale altère les comportements de cour chez la souris. Ces résultats soulignent la vulnérabilité du système nerveux central adulte à l’exposition aux perturbateurs endocriniens et désignent l’AR neural comme étant l’une des principales cibles de l’exposition au DEHP. En raison de la conservation des effets de la testostérone, nous suggérons que l’exposition à ce perturbateur endocrinien pourrait également interférer avec le comportement de cour et l’accouplement chez d’autres espèces. Une étude réalisée chez l’homme a ainsi rapporté une association entre l’exposition environnementale au DEHP et un faible intérêt pour l’activité sexuelle [12]. Plusieurs questions restent cependant encore à explorer, en particulier le(s) mécanisme(s) d’action du DEHP aboutissant à la diminution de l’expression de l’AR neural. Cette étude s’inscrit dans un domaine de recherche qui représente actuellement un énorme enjeu environnemental et sanitaire. Plusieurs défis restent encore à relever pour comprendre les effets et les mécanismes des perturbateurs endocriniens, notamment dans les systèmes neuroendocrines.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Liste de substances chimiques présentes dans les eaux intérieures, souterraines et côtières et dont les concentrations relevées sont jugées dangereuses pour l’environnement.
La distance ano-génitale est une mesure utilisée pour traduire le taux de certaines hormones auquel l’individu a été exposé in utero ou dans la prime enfance. Elle augmente chez le garçon lorsque in utero le testicule embryonnaire commence à produire la testostérone. Une distance anogénitale réduite est un signe de féminisation chez les rongeurs mâles, ce qui traduit une moindre exposition foetale à la testostérone. Chez l’homme, la distance ano-génitale semble corrélable à un risque augmenté d’anomalies qui évoquent une féminisation.
Dose pouvant être ingérée quotidiennement sans danger pour l’homme, calculée à partir de la dose expérimentale sans effet nocif constaté chez l’animal, après application d’un facteur d’incertitude tenant compte de la variabilité inter-individuelle et des différences inter-espèces.
L’axe gonadotrope est sous le contrôle des neurones à GnRH (gonadotropin-releasing hormone), eux-mêmes soumis à la régulation positive exercée par les neurones kisspeptine localisés dans l’hypothalamus.
Ingenuity pathway analysis (Quiagen) est un outil bioinformatique permettant d’analyser des données protéomiques (et autres données omiques : ARN, micro-ARN, métabomome, etc.) pour établir des réseaux d’interaction.
Augmentation du nombre d’astrocytes dans le système nerveux.
Référence
- WHO (World health organization). 2012. State of the science of endocrine disrupting chemicals. http://www.who.int/ceh/publications/endocrine/en/ [accessed 24 october 2016]. [Google Scholar]
- Mauduit C, Siddeek B, Benahmed M. Origine développementale et environnementale de l’infertilité masculine. Rôle des perturbateurs hormonaux. Med Sci (Paris) 2016; 32 : 45-50. [CrossRef] [EDP Sciences] [PubMed] [Google Scholar]
- Swan SH, Main KM, Liu F, et al. Decrease in anogenital distance among male infants with prenatal phthalate exposure. Environ Health Perspect 2005; 113 : 1056-61. [CrossRef] [PubMed] [Google Scholar]
- Swan SH, Liu F, Hines M et al. Prenatal phthalate exposure and reduced masculine play in boys. Int J Androl 2010; 33 : 259-69. [Google Scholar]
- Christiansen S, Boberg J, Axelsad M et al. Low-dose perinatal exposure to di(2-ethylhexyl) phthalate induces anti-androgenic effects in male rats. Reprod Toxicol 2010; 30 : 313-21. [CrossRef] [PubMed] [Google Scholar]
- Moore RW, Rudy TA, Lin TM et al. Abnormalities of sexual development in male rats with in utero and lactational exposure to the antiandrogenic plasticizer di(2-ethylhexyl) phthalate. Environ Health Perspect 2001; 109 : 229-37. [CrossRef] [PubMed] [Google Scholar]
- Raskin K, Gendt K de, Duittoz A, et al. Conditional inactivation of androgen receptor gene in the nervous system: effects on male behavioral and neuroendocrine responses. J Neurosci 2009; 29 : 4461-70. [CrossRef] [PubMed] [Google Scholar]
- Naulé L, Marie-Luce C, Parmentier C, et al. Revisiting the role of estrogen receptor beta in male sexual behavior by conditional mutagenesis. Horm Beh 2016; 80 : 1-9. [CrossRef] [Google Scholar]
- Picot M, Naulé L, Marie-Luce C, et al. Vulnerability of the neural circuitry underlying sexual behavior to chronic adult exposure to oral bisphenol a in male mice. Endocrinology 2014; 155 : 502-12. [CrossRef] [PubMed] [Google Scholar]
- Dombret C, Capela D, Poissenot K et al. Neural mechanisms underlying disruption of male courtship behavior by adult exposure to di-(2-ethylexyl) phthalate in mice. Environ Health Perspect 2017; 125 : 097001. [CrossRef] [PubMed] [Google Scholar]
- Atallah A, Mhaouty-Kodja S, Grange-Messent V. Chronic depletion of gonadal testosterone leads to blood-brain barrier dysfunction and inflammation in male mice. J Cereb Blood Flow Metab 2017; 37 : 3161-75. [CrossRef] [PubMed] [Google Scholar]
- Barrett ES, Parlett LE, Wang C, et al. Environmental exposure to di-2-ethylhexyl phthalate is associated with low interest in sexual activity in premenopausal women. Horm Behav 2014; 66 : 787-92. [CrossRef] [PubMed] [Google Scholar]
© 2018 médecine/sciences – Inserm
Liste des figures
 |
Figure 1. Effets de l’exposition au DEHP sur le comportement de cour. A. Séquence comportementale illustrant les phases précopulatoire et copulatoire chez la souris. B. Effets de l’exposition adulte au DEHP sur les vocalisations ultrasonores illustrées par l’onde sonore enregistrée chez un mâle contrôle et un mâle exposé au DEHP à 50 μg/kg/j (DEHP-50). C. Effets de l’exposition au DEHP aux doses 5 (DEHP-5) et 50 μg/kg/j (DEHP-50) sur la latence à la première intromission et à l’éjaculation (a : p < 0,05). Les mâles exposés au DEHP initient la première intromission et arrivent à l’éjaculation tardivement par rapport au groupe contrôle (données tirées de l’article de Dombret et al. [10]). |
| Dans le texte | |
 |
Figure 2. Effets comportementaux et moléculaires de l’exposition adulte au DEHP. L’exposition orale de souris mâles adultes au DEHP induit une régulation négative du récepteur des androgènes (AR) dans le circuit du comportement sexuel : amygdale médiane (AMe), noyau du lit de la strie terminale (NLST), noyau préoptique (NPO). Il en résulte des altérations du comportement de cour comme la réduction de l’émission des vocalisations ultrasonores ou de l’attraction des femelles réceptives. Au niveau cellulaire et moléculaire, l’exposition au DEHP induit, dans lenoyau préoptique, une surexpression de la protéine acide fibrillaire gliale (GFAP), marqueur de l’activation gliale. |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




