| Issue |
Med Sci (Paris)
Volume 34, Number 2, Février 2018
|
|
|---|---|---|
| Page(s) | 125 - 128 | |
| Section | Le Magazine | |
| DOI | https://doi.org/10.1051/medsci/20183402008 | |
| Published online | 16 February 2018 | |
Nouvelle
Bio-impression assistée par laser
Une nouvelle approche pour la régénération osseuse
Laser-assisted bioprinting: a novel approach for bone regeneration applications
1
Université de Bordeaux, Bioingénierie tissulaire, 146, rue Léo Saignat, 33076 Bordeaux, France
2
Inserm U1026, Bioingénierie tissulaire, 146, rue Léo Saignat, 33076 Bordeaux, France
3
ART BioPrint, Inserm U1026, 146, rue Léo Saignat, 33076 Bordeaux, France
4
CHU Bordeaux, Services d’odontologie et de santé buccale, 146, rue Léo Saignat, 33076 Bordeaux, France
*
This email address is being protected from spambots. You need JavaScript enabled to view it.
Les technologies de bio-impression permettent de positionner précisément les cellules et ainsi de mimer avec fidélité l’architecture des tissus natifs [1, 2]. Dans cette étude nous montrons que la bio-impression assistée par laser (LAB, laser-assisted bio-printing) permet d’imprimer in situ des cellules osseuses et de les agencer afin d’améliorer et de contrôler la réparation osseuse in vivo [3] ( ).
).
( )Voir la Synthèse de J.C. Fricain, m/s n° 1, janvier 2017, page 52
)Voir la Synthèse de J.C. Fricain, m/s n° 1, janvier 2017, page 52
Le concept d’ingénierie tissulaire repose sur des constructions tridimensionnelles (3D) combinant des matériaux biocompatibles et bioactifs avec des cellules et des facteurs bioactifs. Deux stratégies majeures sont utilisées : les approches descendantes « top down » et ascendantes « bottom-up ».
Dans les approches « top down », les cellules sont souvent ensemencées de façon éparse à l’intérieur d’une matrice synthétique ou naturelle façonnée pour s’adapter à la géométrie souhaitée de la lésion à régénérer. Au cours des deux dernières décennies, cette stratégie a conduit à des progrès scientifiques et des succès précliniques, en particulier pour la régénération de tissus minces ou peu vascularisés tels que la peau, le cartilage ou les tissus conjonctifs, ou pour recréer des tissus à haute capacité de régénération et/ou de remodelage, comme l’os. Cependant, les approches « top down » reproduisent avec imprécision les caractéristiques microstructurales complexes des tissus natifs. La colonisation et la différenciation des cellules au sein des échafaudages restent difficiles à contrôler. Ces limitations expliquent que seules quelques applications cliniques aient réellement abouti à des succès.
Les approches « bottom-up », fondées sur une reconstruction brique par brique d’un tissu, offrent la possibilité de disposer chaque composant selon un patron prédéfini qui guide la maturation subséquente de la construction tissulaire vers son architecture fonctionnelle finale. La distribution des cellules peut être définie à l’échelle micrométrique. Le contrôle couche par couche de la distribution des cellules dans la matrice favorise la régénération tissulaire. Parmi les différentes techniques « bottom-up », la bio-impression est devenue, depuis ces cinq dernières années, une approche prometteuse permettant de maîtriser la géométrie des tissus imprimés. Elle bénéficie des capacités du prototypage rapide, facilité par des procédures de conception et / ou de fabrication assistées par ordinateur (respectivement CAO et FAO), qui contrôlent la géométrie de la structure interne et la forme externe des échafaudages cellulaires lors de leur impression [4].
Il existe trois techniques majeures de bio-impression : le jet d’encre, la microextrusion et l’impression laser. Leurs avantages et leurs limites respectives ont été comparés dans plusieurs revues [4, 5]. La bio-impression assistée par laser, mise au point et brevetée aux États-Unis [6], est particulièrement bien adaptée aux applications d’ingénierie tissulaire. Elle est fondée sur le LIFT (laser-induced forward transfer). Les bio-imprimantes correspondantes sont composées de trois éléments : (1) une source laser pulsée, (2) une cible, ou ruban, à partir duquel un matériel biologique est imprimé, et (3) un substrat récepteur/receveur qui recueille le matériel imprimé. Le ruban est composé d’un support transparent au laser (par exemple du verre ou du quartz) revêtu d’une mince couche métallique absorbante (composée d’or ou de titane). Le composant organique (molécules ou cellules) est préparé dans une phase liquide (par exemple un milieu de culture ou une solution de collagène) puis déposé à la surface d’un film métallique. L’impulsion laser induit la vaporisation du film métallique, entraînant la production de gouttelettes qui se déposent sur le substrat en regard [7] (Figure 1A). Cette méthode permet de déposer des gouttelettes de cellules ou de biomatériaux à une fréquence de l’ordre du mégahertz (MHz). Grâce à une résolution à l’échelle du picolitre, la bio-impression assistée par laser permet de maîtriser finement la densité cellulaire et l’organisation spatiale de l’impression en 3D. En théorie, elle permet de contrôler individuellement l’impression de chaque cellule et donc d’exercer un contrôle d’un niveau sans précédent de la répartition des cellules. Ainsi, cette technologie émergente est adaptée à la fabrication de structures qui non seulement miment l’organisation structurelle des tissus natifs, mais sont également susceptibles de développer une fonctionnalité physiologique proche de celle de leurs homologues natifs. Cette méthode présente aussi des avantages comme l’automatisation, la reproductibilité et le haut débit, qui permettent d’envisager la fabrication de constructions 3D de tailles pertinentes sur le plan physiologique.
Dans le travail publié dans la revue Scientific Reports [2], nous avons utilisé cette technologie pour réaliser des impressions de cellules directement in vivo. Un poste de travail dédié a été adapté aux expériences de bio-impression in vivo (Figure 1B) pour permettre d’imprimer des cellules pré-ostéoblastiques, in situ, à l’intérieur d’un défaut osseux de calvaria de souris. Nos objectifs étaient d’établir la preuve de concept de la capacité de cette technologie à réaliser une bio-impression in vivo, puis d’évaluer l’impact de différentes géométries d’impression des cellules sur la régénération osseuse. Des cellules D1 (des cellules stromales mésenchymateuses de souris [MSC, mesenchymal stem cells] aptes à se différencier vers la lignée ostéoblastique) ont été imprimées, suivant deux géométries distinctes, avec un nombre de cellules et une densité similaires (respectivement 700 et 800 cellules/mm2). Comme illustré sur la Figure 2 (parties B1 et B2), les deux géométries imprimées correspondaient aux modèles d’impression prédéfinis. L’impact de la géométrie d’impression sur la régénération osseuse a ensuite été évalué par micro-tomographie aux rayons X (ou μCT) après un et deux mois. La Figure 2 (C1 et C2; zone#) montre qu’une reconstruction marginale du défaut a été observée deux mois après l’impression d’une encre contrôle constituée uniquement de collagène de type I et d’hydroxyapatite (essai contrôle représenté par le symbole#). Lorsque des cellules D1 ont été ajoutées à l’encre et imprimées dans une géométrie en anneau, aucune formation osseuse majeure supplémentaire n’a été obtenue (voir la zone* sur la Figure 2, C1). En revanche, lorsqu’une géométrie de disque a été utilisée, une augmentation significative de la formation osseuse post-impression a été observée par rapport aux deux autres conditions testées (voir la zone** sur la Figure 2, C2). Ces résultats ont été confirmés par la quantification du rapport entre le volume osseux et le volume total (VO / VT), comme illustré sur la Figure 2D, ainsi que par l’analyse histologique des échantillons récupérés un mois et deux mois après l’impression [2].
Les cellules utilisées dans cette étude sont des progéniteurs multipotents (MSC) capables de se différencier en différents types cellulaires (ostéoblastes, adipocytes, chondrocytes, ténocytes et myocytes squelettiques). Ces cellules immunomodulatrices sont facilement purifiées à partir de différents tissus (moelle osseuse, tissu adipeux, cordon ombilical, etc.) et peuvent sécréter des facteurs biologiques protecteurs [8]. Conformément à nos précédents résultats [9], les cellules MSC imprimées par LAB sont viables et elles prolifèrent, in vitro et in vivo, indépendamment de la géométrie d’impression. Nous avons montré qu’en utilisant les mêmes paramètres d’impression, nous pouvions obtenir une disposition précise des cellules MSC, sans compromettre leur viabilité cellulaire, ni leur capacité à proliférer et à se différencier vers la lignée ostéoblastique, et sans induire de fragmentation de l’ADN [10]. Ces résultats confirment la capacité de la bioimpression assistée par laser à imprimer des cellules de mammifères avec un effet négligeable sur leur viabilité et leur fonction.
Ce travail fournit la première évidence de l’influence de la géométrie d’impression cellulaire par LAB, in situ, sur la régénération osseuse. Dans le modèle testé, la géométrie du disque était la plus favorable à la régénération osseuse in vivo, ce qui souligne l’importance du processus d’organisation. Nous supposons que cet effet bénéfique était fondé sur une régulation autocrine par les cellules MSC elles-mêmes. En effet, les MSC peuvent réguler leur différenciation vers la lignée ostéoblastique via un processus autocrine/paracrine, par la sécrétion d’IFNγ (interféron gamma) et de TNFα (facteur de nécrose tumorale alpha) [11]. Nous postulons que l’arrangement cellulaire en disque pourrait favoriser la régulation paracrine de la différenciation des MSC en augmentant l’homogénéité de la distribution cellulaire et leur proximité. Cependant, nous n’avons pas évalué directement I ’intégration des cellules D1 imprimées dans le tissu osseux régénéré.
L’approche LAB échappe à un problème récurrent rencontré avec les autres techniques de bio-impression : le colmatage d’une buse lors du passage de l’encre contenant des cellules. Elle permet, de plus, de contrôler la densité et la distribution à l’échelle microscopique des cellules, de préserver leur viabilité, d’atteindre des vitesses de dépôt élevées [9] et une précision d’impression de l’ordre du micron. Cette approche permet également d’utiliser, dans une même plateforme, différents rubans portant des types de cellules et de bioencres différents. Cette polyvalence pourrait permettre d’appliquer la bio-impression à d’autres tissus plus complexes, en choisissant une organisation en 3D apte à favoriser la régénération tissulaire. Cette technique permet une impression sans contact direct, nous pouvons donc envisager son application clinique sous environnement stérile. À l’intérieur du bloc opératoire, des chirurgiens pourraient diriger des imprimantes capables de réaliser des implantations cellulaires contrôlées au micron près. Néanmoins, la technologie LAB reste limitée aujourd’hui à des surfaces planes.
En conclusion, ce travail ouvre de nouvelles perspectives de contrôle de la régénération osseuse. Des développements techniques restent nécessaires pour étendre la gamme des applications à la reconstruction de tissus plus complexes et volumineux que l’os.
Liens d’intérêt
Les auteurs déclarent n’avoir aucun lien d’intérêt concernant les données publiées dans cet article.
Références
- Murphy SV, Atala A. 3D bioprinting of tissues and organs. Nat biotechnol 2014; 32 : 773-85. [Google Scholar]
- Keriquel V, Oliveira H, Remy M, et al. In situ printing of mesenchymal stromal cells, by laser-assisted bioprinting, for in vivo bone regeneration applications. Sci Rep 2017; 7 : 1778. [Google Scholar]
- Fricain JC, De Olivera H, Devillard R. Impression 3D en médecine régénératrice et ingénierie tissulaire. Med Sci (Paris) 2017; 33 : 52-9. [Google Scholar]
- Mandrycky C, Wang Z, Kim K, Kim DH. 3D bioprinting for engineering complex tissues. Biotechnol Adv 2016; 34 : 422-34. [Google Scholar]
- Gu BK, Choi DJ, Park SJ, et al. 3-dimensional bioprinting for tissue engineering applications. Biomat Res 2016; 20 : 12. [Google Scholar]
- Barron JA, Wu P, Ladouceur HD, Ringeisen BR. Biological laser printing: a novel technique for creating heterogeneous 3-dimensional cell patterns. Biomed Microdevices 2004; 6 : 139-47. [Google Scholar]
- Guillemot F, Souquet A, Catros S, Guillotin B. Laser-assisted cell printing: principle, physical parameters versus cell fate and perspectives in tissue engineering. Nanomedicine (Lond) 2010; 5 : 507-15. [Google Scholar]
- Keating A. Mesenchymal stromal cells: new directions. Cell Stem Cell 2012; 10 : 709-16. [Google Scholar]
- Guillotin B, Souquet A, Catros S, et al. Laser assisted bioprinting of engineered tissue with high cell density and microscale organization. Biomaterials 2010; 31 : 7250-6. [Google Scholar]
- Pagès E, Rémy M, Kériquel V, et al. Creation of highly defined mesenchymal stem cell patterns in three dimensions by laser-assisted bioprinting. J Nanotechnol Eng Med 2015; 6 : 021006-5. [Google Scholar]
- Li C, Li G, Liu M, et al. Paracrine effect of inflammatory cytokine-activated bone marrow mesenchymal stem cells and its role in osteoblast function. J Biosci Bioeng 2016; 121 : 213-9. [CrossRef] [PubMed] [Google Scholar]
© 2018 médecine/sciences – Inserm
Liste des figures
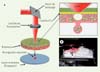 |
Figure 1 Bio-impression assistée par laser. A. Représentation schématique de la méthode de bio-impression assistée par laser (LAB). Une configuration LAB typique comprend un faisceau laser pulsé, un système de focalisation, un ruban (une lame de verre transparente, revêtue d’une couche de métal absorbant [or]), sur lequel une fine couche de bioencre (suspension cellulaire) est étalée et un substrat récepteur (biopapier) faisant face au ruban. Le principe physique de LAB est basé sur la génération d’une cavitation, dans la profondeur de la bioencre, dont l’expansion et l’effondrement induisent la formation d’un jet et, par conséquent, le transfert de microgouttes de bioencre vers le substrat. B. Le système d’impression a été adapté pour permettre l’impression in vivo et in situ dans un défaut d’os de calvaria chez la souris (figure adaptée avec permission de Keriquel et al. [2]). |
| Dans le texte | |
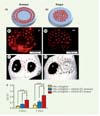 |
Figure 2 Importance de la géométrie d’impression dans une expérience de LAB in vivo. Représentation schématique des géométries bio-imprimées in vivo par LAB, à savoir un anneau (A1) de diamètre externe et interne de 3 et 2,1 mm, respectivement, et un disque (A2) de 2 mm de diamètre. Dans les deux cas, deux couches d’encre de collagène (type I) et d’hydroxyapatite (nHA) ont été imprimées en dessous et au-dessus de la couche d’encre cellulaire. Images de fluorescence représentatives des cellules D1 imprimées en anneau (B1) et en disque (B2) à l’intérieur du défaut de calvaria chez la souris, immédiatement après l’impression. Images représentatives de la reconstruction de micro-tomographie aux rayons X (μCT) de collagène et de nHA (zone#, C1, C2) et de cellules D1 imprimées en anneau (zone*, C1) ou en disque (zone**, C2), deux mois après l’impression dans le défaut de calvaria. D. Évaluation quantitative du rapport du volume osseux sur le volume total (VO / VT) par μCT, 1 mois et 2 mois après l’impression de cellules D1, en géométrie annulaire ou discale, ou celle de collagène et nHA en contrôle (moyenne du ratio, n = 9, * et *** p < 0,05 et p < 0,001, respectivement) (figure adaptée avec la permission de Keriquel et al. [2]). |
| Dans le texte | |
Current usage metrics show cumulative count of Article Views (full-text article views including HTML views, PDF and ePub downloads, according to the available data) and Abstracts Views on Vision4Press platform.
Data correspond to usage on the plateform after 2015. The current usage metrics is available 48-96 hours after online publication and is updated daily on week days.
Initial download of the metrics may take a while.




